

2. 北京中医药大学北京中医药研究院,北京 100029
2. Beijing Institute of Chinese Medicine, Beijing University of Chinese Medicine, Beijing 100029, China
丹参注射液是由丹参饮片经过水提醇沉等步骤制备而成的注射液,具有保护心脑血管、抗血小板聚集、抗菌、抗炎等药理作用[1, 2],临床上广泛用于治疗冠心病、心悸胸闷、心绞痛[3]。前期研究发现,丹参饮片中的主要药效成分水溶性酚类在注射液制备过程中易损失[4],导致不同厂家不同批次的丹参注射液质量存在差异。因此,当下亟待有综合、整体、宏观的评价方法来补充调整现行的质量控制标准。
生物活性测定法是采用恰当统计学检验方法对药物的某种生物活性进行评价,是一种涵盖药理学和药检统计分析,可定量的活性测定方法[5]。目前,美国FDA《植物药工业开发指南》,《中国药典》(2015版)都将生物活性评价方法纳入其中[6-7],表明以生物活性作为中草药、植物药的一种质量评价模式已得到越来越多的重视和认可,生物活性测定法用于中药质量控制已是一种必然的趋势。
采用生物活性测定法建立一种反映丹参注射液有效性的新质控方法,对其现有的质量标准进行补充,能更好的评价丹参注射液的品质,提高相关中药注射剂质量标准的发展速度,加快其有效性及安全性的研究与再评价的进程。
1 材料与方法 1.1 实验动物日本大耳白家兔(北京维通利华实验动物技术有限公司,二级标准),♂,体重(2.1±0.5) kg; 许可证号:SCXK(京)2006-0009。
1.2 供试药品丹参注射液由A、B、C、D四个厂家提供,其中A、B、C厂家各2批次,D厂家3批次,均为提供部颁质量标准项下检验报告合格的药品。药品批号见Tab 1。
| Manufacturer | Sample lot |
| A factory | 170203 |
| 170204 | |
| B factor | 20180601 |
| 20180701 | |
| C factory | 180725B1 |
| 180727B1 | |
| D factory | 1807241 |
| 1807242 | |
| 1807251 |
LBY-NJ4型半自动血小板聚集仪(北京瀚邦生物科技有限公司),ADVIA 2120i型血细胞分析仪(美国SIEMENS公司),0.9%氯化钠注射液(中国大冢制药有限公司,批号:0B72H2),枸橼酸钠(天津市光复精细化工研究所,批号:20101025)血小板聚集功能AA激活检测试剂盒(北京瀚邦生物科技有限公司,批号:401034)。
1.4 血浆制备家兔采取心脏取血,加入3.2%枸橼酸纳(1 :9)抗凝。抗凝血以160 g,离心10 min,得到富血小板血浆(platelet rich plasma, PRP),余下血液继续2 000 g,离心10 min,得贫血小板血浆(platelet poor plasma, PPP)。用血液分析仪测定PPP和PRP中的血小板个数,利用PPP稀释调节PRP,使PRP中的血小板数在5×1011·L-1左右。为保证结果的可靠性,PPP和PRP应在室温条件下,不可过度震荡,且确保在4 h内完成血小板聚集的测定[8]。
1.5 样品制备通过实验室综合评价,将D厂家(批号:1807242)丹参注射液为标准品,向其加入0.9%的生理盐水。以0.85的剂间比分别配制浓度为100%、85%、72.3%、61.4%、52.2%、44.4%、37.7%、32.1%、27.3%的样品各1 mL。取其他各厂家的丹参注射液,用0.9%的生理盐水作为溶剂,以0.85的剂间比分别配制浓度为100%、85%、72.3%、61.4%、52.2%、44.4%、37.7%、32.1%、27.3%的供试品各1 mL,备用。
1.6 血小板聚集率测定取PPP 300 μL加入一次性测试杯,校准调零。取PRP 274 μL,分别加入不同浓度的样品液10 μL,37 ℃孵育3 min,依次加入花生四烯酸(arachidonic acid, AA)16 μL,测定5 min内的血小板最大聚集率[9]。
1.7 统计分析各样本效价数据及方法学考察结果应用中国药典生物检定统计程序BS2000进行统计分析。
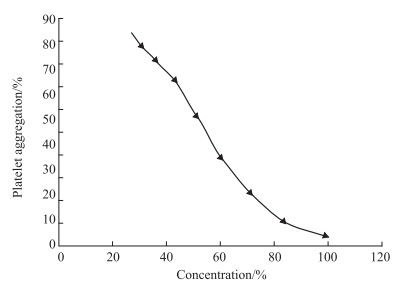
2 结果 2.1 量效学考察结果在丹参注射液标准品(S)体外对抗血小板聚集的实验中,发现血小板聚集率随丹参注射液浓度增加具备量效关系。注射液浓度在27.3%~100%范围内,量效关系显著,可得线性方程为y=-1.21x+114.30,r2 = 0.965 9。具体测定结果见Fig 1,Tab 2。丹参注射液供试品(T)量效学考察结果见Tab 3。综合丹参注射液的量效学考察结果,发现注射液浓度在37.7%~52.2%范围内,量效关系明显,线性良好。
|
| Fig 1 The dose-effect relationship of anti-platelet aggregation of standard Danshen injection |
| Concentration/% | Platelet aggregation rate/% | Average plateletaggregation rate/% | ||
| First time | Second time | Third time | ||
| 100 | 4.72 | 2.87 | 3.92 | 3.84 |
| 85 | 7.51 | 9.00 | 9.6 | 8.70 |
| 72.3 | 19.44 | 20.49 | 18.61 | 19.51 |
| 61.4 | 33.68 | 33.33 | 32.03 | 33.01 |
| 52.2 | 49.47 | 49.51 | 48.98 | 49.32 |
| 44.4 | 63.39 | 64.37 | 63.14 | 63.63 |
| 37.7 | 71.81 | 72.35 | 71.62 | 71.92 |
| 32.1 | 76.88 | 76.92 | 76.84 | 76.88 |
| 27.3 | 83.33 | 84.47 | 84.56 | 84.12 |
| Concentration/% | 170203 | 20180601 | 180727B1 | 1807241 | 170204 | 20180701 | 180725B1 | 1807251 |
| 100 | 11.11 | - | - | 10.89 | 12.57 | - | - | 6.73 |
| 85 | 17.97 | - | 14.16 | 13.86 | 18.02 | - | 18.61 | 15.55 |
| 72.3 | 29.87 | 12.30 | 15.55 | 18.02 | 31.63 | - | 26.52 | 18.61 |
| 61.4 | 42.41 | 18.61 | 24.45 | 31.96 | 41.22 | - | 31.01 | 30.93 |
| 52.2 | 55.49 | 26.06 | 30.90 | 49.26 | 51.70 | 13.86 | 36.51 | 47.34 |
| 44.4 | 66.07 | 27.34 | 46.00 | 57.17 | 64.37 | 19.44 | 47.46 | 60.86 |
| 37.7 | 74.10 | 36.68 | 54.88 | 69.29 | 73.83 | 26.06 | 53.23 | 70.25 |
| 32.1 | 83.33 | 50.51 | 65.90 | 76.70 | 82.21 | 31.01 | 66.95 | 69.59 |
| 27.3 | 90.07 | 62.61 | 72.51 | 82.20 | 87.54 | 37.04 | 71.25 | 79.01 |
| -:indicate that it isn’t detected | ||||||||
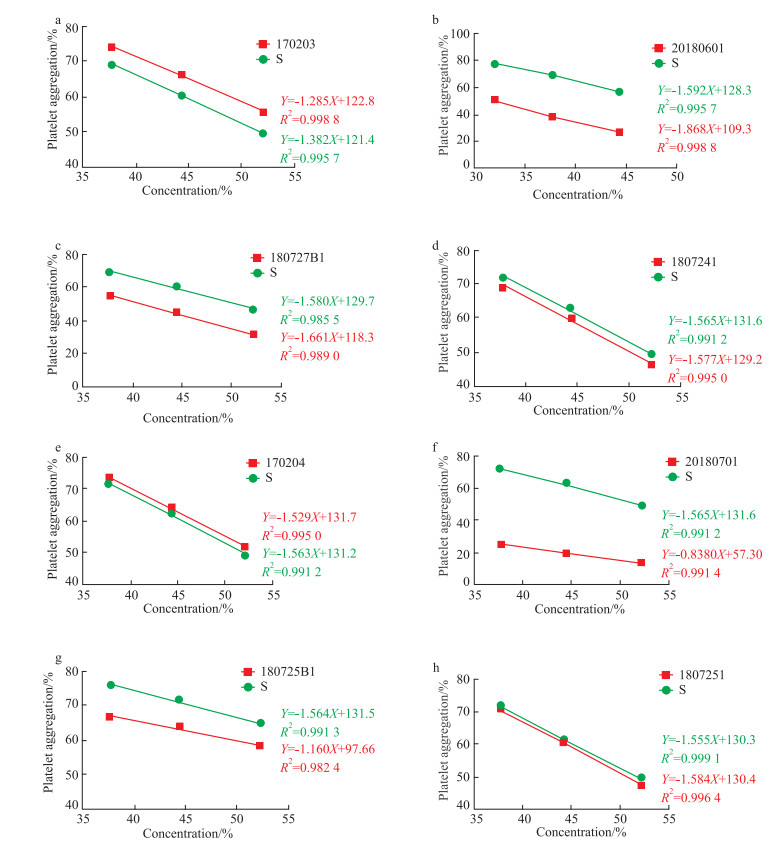
根据量效关系考察结果,发现丹参注射液对AA诱导的血小板聚集率均随浓度增加而成对数下降的趋势。可采用生物活性测定法中的量反应平行线中三三法进行实验设计,进一步筛选线性范围,各批次线性考察结果见Fig 2。由图中结果可知,丹参注射液浓度在37.7%~52.2%范围内,线性较好,相关系数均在0.9以上,从而完成线性范围筛选。
|
| Fig 2 The linear range of anti-platelet aggregation of Danshen injection |
丹参注射液标准品(S)与供试品(T)按剂间比1 :0.85各配置高、中、低3个浓度,各浓度梯度均按照S1、T1、T2、S2、S3、T3的顺序分别测定标准品组和供试品组三个含药富血小板血浆的血小板最大聚集率,平行测定3次。规定以丹参注射液标准品效价为1 000 U/L,采用中国药典生物检定统计程序BS2000计算供试品组测得效价(PT)和可信限率(FL%)并进行可靠性检验,结果见Tab 4。
| Sample lot | PT/U·L-1 | FL/% |
| 170203 | 931.2 | 3.3 |
| 20180601 | 1 584.9 | 5.5 |
| 180727B1 | 1 252.7 | 3.2 |
| 1807241 | 1 054.1 | 2.6 |
| 170204 | 990.1 | 2.8 |
| 20180701 | 2 667.9 | 4.5 |
| 180725B1 | 1 312.1 | 6.3 |
| 1807251 | 1 035.7 | 2.7 |
结果发现,不同厂家不同批次的丹参注射液效价测定结果不同,可信限率均小于10%,检定结果精密度良好。与丹参注射液标准品相比,其中A厂家抑制血小板聚集活性较弱,D厂家与标准品活性相当,B和C厂家均强于标准品,更加明确直观的反映出不同厂家的丹参注射液抑制血小板聚集作用的强弱,直关其药效。
2.2.2 可靠性检验结果对不同批次的丹参注射液依次进行可靠性检验。结果显示,变异来源中的回归项均显著,曲线、偏离平行和反向二次曲线(P>0.05),差异均无统计学意义,表明标准品(S)和供试品(T)是两条平行直线。实验结果可以通过平行线测定的相关公式计算效价和估计相应实验误差。剂间P值小于0.01,差异均有显著性,表明本次设计剂量、剂间比安排恰当,满足实验要求。证明本方法测得各批次效价可靠,可靠性通过。
2.2.3 重复性考察结果取丹参注射液(1807251),按照2.2.1项下生物活性测定方法,分别配置6份标准品及供试品,重复测定六次效价,并进行可靠性检验,结果见Tab 5。由结果可知,6次测定结果为(1 030.38±1.93) U·L-1,测得结果均通过可靠性检验,可信限率(FL)平均值2.97%,小于5%,RSD%为0.137%,小于10%,说明该方法重复性较好。
| Time | PT/U·L-1 | FL/% |
| 1 | 1 032.4 | 3.0 |
| 2 | 1 030.7 | 2.8 |
| 3 | 1 032.5 | 2.9 |
| 4 | 1 029.5 | 3.0 |
| 5 | 1 029.8 | 3.2 |
| 6 | 1 027.4 | 2.9 |
| x±s | 1 030.38±1.93 | 2.97±0.14 |
| RSD/% | 1.932 | 0.137 |
本实验基于丹参注射液的抗血小板聚集活性对其进行量效学关系考察,利用量反应平行线中三三法进行实验设计以及规定丹参注射液标准品的效价为1 000 U/L,从而测定其他丹参注射液供试品效价,测得效价可靠,重复性良好。该方法能够更好的评价不同批次丹参注射液抗血小板聚集活性,衡量其药效强弱,在综合性全面评价其质量方面具有一定参考价值。
目前,中药生物活性测定法仍在起步阶段,尤其标准品的建立尚无成熟的参考原则。该实验建立了丹参注射液体外抗血小板聚集活性的标准品,后期将组织不同实验室对其进行协作标定,可进一步为标准品的建立提供实验依据和技术支持。
近年来,中药注射剂因其剂量小、生物利用度高、疗效快、耐药率低等特点,愈加广泛的应用到临床中,已成为无可替代的中药新产品[10]。研究建立一种丹参注射液的新质量评价方法,必将极大的推进中药注射液生物活性测定法进步。该方法的建立能够为探讨生物活性测定法在中药质量控制方面提供方法学借鉴,进一步可为中药标准品的建立及生物测定方法的研究开创新思路。
| [1] |
杨锦秀, 毛威. 丹参水溶性有效成分对内皮祖细胞功能的影响[J]. 中国药理学通报, 2017, 33(9): 1203-6. Yang J X, Mao W. Effects of hydrosoluble active constituent of Salvia miltiorrhiza Bge on endothelial progenitor cell functions[J]. Chin Pharmacol Bull, 2017, 33(9): 1203-6. doi:10.3969/j.issn.1001-1978.2017.09.005 |
| [2] |
刘慧颖, 姜长涛, 冯娟, 等. 丹参酮类化合物研究进展[J]. 中国药理学通报, 2016, 32(12): 1643-7. Liu H Y, Jiang C T, Feng J, et al. Research progress of Tanshinones[J]. Chin harmacol Bull, 2016, 32(12): 1643-7. doi:10.3969/j.issn.1001-1978.2016.12.004 |
| [3] |
Zhang J, An S J, Fu J Q, et al. Mixed aqueous extract of salvia miltiorrhiza reduces blood pressure through inhibition of vascular remodelling and oxidative stress in spontaneously hypertensive rats[J]. Cell Physiol Biochem, 2016, 40(1-2): 347-60. doi:10.1159/000452550 |
| [4] |
李耿, 于长安, 李振坤, 等. 丹参煎煮化学成分溶出规律研究[J]. 中国实验方剂学杂志, 2009, 15(8): 46-9. Li G, Yu C A, Li Z K, et al. Study on the dissolution rule of the chemical constituents of Danshen[J]. Chin J Exp Tradit Med Form, 2009, 15(8): 46-9. doi:10.3969/j.issn.1005-9903.2009.08.019 |
| [5] |
Mire-Sluis A R. Setting specifications for potency assays-basic principles[J]. Dev Biol (Basel), 2002, 2(107): 107-15. |
| [6] |
U.S.Department of Health and human services food and drug administration center for drug evaluation and research.botanical drug development guidance for industry[J/OL]. U.S.2016, 12.
|
| [7] |
国家药典委员会.中国药典[M].一部.北京: 中国医药科技出版社, 2015. Chinese Pharmacopoeia Commission. Pharmacopoeia of the People's Republic of China[M]. One. Beijing: China Medical Science Press, 2015. |
| [8] |
闫文亮. 花生壳提取物对家兔血小板聚集的影响[J]. 中国药房, 2010, 21(31): 2896-7. Yan W L. Effects of extracts from peanut shell on platelet aggregation in rabbit[J]. J Chin Pharm, 2010, 21(31): 2896-7. |
| [9] |
郭玉东, 胡宇驰, 曹春然, 等. 舒血宁注射液体外抑制血小板聚集的生物活性测定法[J]. 中成药, 2014, 36(5): 1008-12. Guo Y D, Hu Y C, Cao C R, et al. Bioassay method of Shuxuening injection to inhibit platelet aggregation[J]. Chin Tradit Pat Med, 2014, 36(5): 1008-12. doi:10.3969/j.issn.1001-1528.2014.05.027 |
| [10] |
李贻奎, 张金艳. 中药注射剂的改进与提高[J]. 中国中药杂志, 2011, 36(14): 1905-9. Li Y K, Zhang J Y. Improvement and enhancement of traditional Chinese medicine injections[J]. Chin J Chin Mater Med, 2011, 36(14): 1905-9. |

