

2. 广东医科大学广东天然药物研究与开发重点实验室,广东 湛江 524023
崔燎(1962-),女,博士,教授,博士生导师,研究方向:骨质疏松的机制及防治,E-mail:cuiliao@163.com。
2. Guangdong Key Lab for Research and Development of Natural Drugs,Guangdong Medical University,Zhanjiang Guangdong 524023,China
动脉粥样硬化(atherosclerosis,AS)和骨质疏松症(osteoporosis,OP)是常见的老年性疾病,流行病学研究证明两者之间存在很强的相关性,存在共同的影响因素[1]。随着研究的深入,表明血脂代谢异常与骨质疏松有关[2-3]。作为动脉粥样硬化的主要发病机制,氧化低密度脂蛋白(oxidized low density lipoprotein,Ox-LDL)与老年心脑血管疾病关系密切。近年来的研究表明,Ox-LDL与老年性骨质疏松亦存在关联:Ox-LDL对骨髓间充质干细胞、成骨细胞、破骨细胞均有影响,少数研究表明其抑制骨髓细胞成骨分化[4],但对破骨细胞具体作用观点不一,报道未详[5-6]。目前对成骨细胞的作用多见报道。本文综述近年来Ox-LDL对成骨细胞的研究,为通过调控Ox-LDL信号途径从而寻找新作用靶点药物研究提供实验依据,也为深入探讨AS和OP关系提供理论依据。
1 动脉粥样硬化与骨质疏松的临床流行病学动脉粥样硬化与骨质疏松是老年人常见疾病。骨密度降低与心血管疾病存在着显著的负相关性[7],骨密度低的绝经妇女发生冠状动脉粥样硬化的风险更高[8]。此外,骨质疏松性骨折的风险增加与血管功能障碍和血管结构异常有关[9],骨密度与颈动脉内膜中层厚度呈负相关[10],冠状动脉微血管内皮功能障碍是绝经妇女骨质疏松症发展的独立预测因子[11]。骨质疏松人群较非骨质疏松人群更易发生动脉粥样硬化病变[12],为此尝试着去寻找它们共同的危险因素及其发病机理极其重要。
2 Ox-LDL对动脉粥样硬化的影响AS是指一组以动脉壁增厚、变硬和弹性减退为特征的动脉疾病。高脂血症被认为是其主要危险因素。载脂蛋白是低密度脂蛋白(low density lipoprotein, LDL)的一种成分,可介导与LDL受体的结合,LDL受体或APOE的缺失破坏了脂蛋白的清除,则LDL在内皮细胞外基质中积累,并通过活性氧、过氧化物酶和脂氧合酶进行氧化修饰形成Ox-LDL。Ox-LDL是一种公认的AS前体颗粒,Ox-LDL结合清除内皮细胞和巨噬细胞上的清道夫受体(scavenger receptor,SR)和Toll样受体(Toll-like receptor, TLR),刺激细胞因子的产生并激活额外的巨噬细胞和淋巴细胞,活化的巨噬细胞积聚Ox-LDL成为含脂的“泡沫”细胞,与平滑肌细胞一起,开始形成钙化的动脉粥样硬化斑块[13]。因此,Ox-LDL是引起AS的关键因素。
3 Ox-LDL对成骨细胞的影响骨质疏松症是一种以骨量低下,骨微结构破坏,导致骨脆性增加,易发生骨折为特征的全身性代谢性骨病。骨是一个活跃的不断重塑的组织,涉及由成骨细胞介导的骨形成和由破骨细胞介导的骨吸收之间的平衡。氧化脂质的生物活性在血管系统和平滑肌细胞中得到公认,近年来,有研究发现其对骨和成骨细胞亦有影响。Ox-LDL在动脉粥样硬化和骨质疏松之间起着重要作用,但究其对骨的作用机制尚极少有人阐述清楚。
3.1 过氧化物酶体增殖激活受体γ(peroxisome proliferators-activated receptors γ, PPARγ)PPARγ特异表达于脂肪组织,在脂肪形成过程中,PPARγ是脂肪细胞的必需因子。Ox-LDL为PPARγ的天然配体,Ox-LDL能够产生氧自由基,而氧自由基能破坏骨髓细胞外基质,导致骨吸收增加,骨形成减少。研究表明,不同浓度的PPARγ内源性配体Ox-LDL干预大鼠成骨细胞后,Ox-LDL呈剂量依赖性下调成骨细胞RANKL、ALP、OPG mRNA的表达水平,同时上调PPARγ、RANK、TRAP mRNA的表达水平。结果提示,Ox-LDL能激活PPARγ转录活性,抑制成骨细胞分化[4]。配体激活PPARγ转录活性对破骨细胞分化及活性的影响目前仍有争议,值得进一步研究。
|
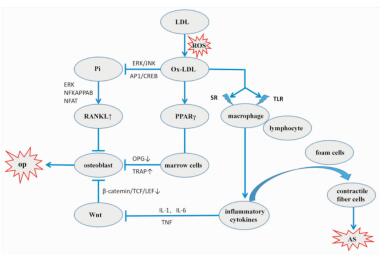
| Fig 1 Ox-LDL ascommon pathogenesis of AS and OP |
Wnt是一类分泌型糖蛋白,经相关信号通路把信号转到细胞核,阻断β-catenin降解,并经转录因子TCF/LEF介导, 促进靶细胞增殖、分化。Wnt信号通路活化,能促进骨髓干细胞形成成骨细胞,促进成骨细胞生长、增殖。氧化应激引起脂质氧化,促进IL-1、IL-6、TNF等炎症因子转录水平增加,使得Cx43、Wisp1等Wnt相关蛋白降低,成骨前Wnt配体Wnt6、Wnt10b减少,引起骨丢失[14]。Ox-LDL可能通过激活PPARγ[4],促进MSC转向脂肪细胞的分化,抑制Wnt信号,而减弱β-catenin / TCF/LEF转录。因此,脂质氧化抑制Wnt信号通路,使得MSC的成骨细胞分化减弱,成骨细胞减少,引起骨质疏松。
3.3 无机磷酸盐(Pi)信号通路Pi是骨吸收过程中释放的信号因子,通过ERK和PKC激酶诱导OPN基因的表达,促进成骨细胞矿化。氧化应激作用抑制成骨细胞的Pi信号传导和Pi诱导的矿化。Ox-LDL通过ERK/JNK和AP1/CREB损害Pi信号, 下调成骨细胞特异性基因的表达,如Cbfa1/Runx2、OPN和RANKL。因此,Ox-LDL抑制Pi信号通路,减少成骨细胞矿化,在骨中形成负面作用[15],
3.4 sirt1和runx2Sirt1(NAD-依赖性乙酰化酶sirtuin-1)是人类基因组中由Sirt1基因编码的蛋白,其功能是蛋白质上的去乙酰化。现已证明在调控成骨细胞和间充质干细胞分化中也起着关键作用。Runx2是一种早期的转录因子,附着在DNA的特定区域,启动成骨谱系的转录程序,参与了骨细胞的发育。骨髓间充质干细胞(bone marrow mesenchyml stem cell,BMSC)长期暴露于Ox-LDL可降低sirt1和runx2的表达,Ox-LDL对Apoe-/-小鼠成骨分化过程中,诱导sirt1表达成时间依赖性下降[16]。不同浓度Ox-LDL对成骨细胞的影响不一样,低浓度的Ox-LDL诱导成骨细胞的增殖[17],高浓度的Ox-LDL对细胞产生毒性作用,这可能是Ox-LDL诱导的激素样效应特征[18]。所以,Ox-LDL对成骨细胞的影响与浓度和时间有关,但具体的浓度和时间下Ox-LDL是如何降低sirt1和runx2表达的,还未见报道。
3.5 RANKL信号通路氧化应激参与RANKL诱导的破骨细胞分化[19],在小鼠中,Ox-LDL抑制Pi诱导的成骨细胞分化和矿化的同时增强RANKL诱导的ROS生成,对RANKL下游信号ERK、p38、JNK激酶和NFkappaB、NFAT转录因子传导起到抑制作用,降低RANKL诱导的破骨细胞前体分化[20]。在人成骨细胞中,Cu2+-Ox-LDL通过信号通路ERK、NFkappaB和NFAT的参与,增强人成骨细胞样细胞中RANKL的表达,其氧化脂质的部分调节成骨细胞和破骨细胞的骨重建之间的关系[21]。Ox-LDL通过RANKL信号通路对破骨细胞的作用还存在争议,有待考究。
3.6 氧化特异性表位氧化特异性表位是脂质过氧化产生高反应性降解的产物,如Ox-LDL,与蛋白质和其他脂质上的氨基反应形成物质的统称,其可与细胞上的SRs和TLRs结合,刺激细胞产生炎症因子。在成骨细胞中,破骨细胞和骨髓巨噬细胞存在SRs和TLRs,增加了氧化特异性表位的生理或病理生成,影响骨稳态的可能性[22]。E06单链抗体和IK17单链抗体可分别阻断PC-OXPL和MDA的作用,降低Ox-LDL的促炎活性,抑制骨丢失[23]。
有趣的是,众所周知,血管钙化可能是HDL在动脉壁作用的一个靶点。相关研究表明,HDL对成骨细胞的作用与Ox-LDL相反,HDL调节血管细胞的成骨细胞分化和钙化[5],阻断Ox-LDL与成骨细胞的联系,抑制Ox-LDL诱导的成骨细胞凋亡[24],逆转Ox-LDL对成骨细胞的破坏。HDL可以通过直接抑制血管细胞的成骨分化来调节血管钙化,对此机制尚未清楚。
4 动脉粥样硬化与骨质疏松的共同治疗目前心血管疾病和骨质疏松症都是广泛流行的疾病,临床上已将骨测量与动脉粥样硬化相关的测量联系起来[25],并表明他汀类药物(一种用于预防心血管疾病的降胆固醇药物)有利于改善患者骨密度水平[26],骨质疏松症和他汀类药物治疗之间的联系还有待进一步研究。丹参一直以来都是作为典型的治疗心血管疾病的药物,具有活血化瘀,疏通血管的药理作用。近年来研究发现,丹参有效成分在治疗骨质疏松上有一定的疗效, 阐述了脂溶性丹参醇通过KLF15 /PPARγ2/ FoxO3a/Wnt途径抑制脂肪形成而减轻受损的骨形成[27],水溶性丹参素、丹酚酸B可以显著减轻地塞米松处理的大鼠骨组织有害氧化变化和氧化应激[28-29],这提示我们可以通过抗脂质过氧化治疗骨质疏松和心血管疾病,这为治疗动脉粥样硬化和骨质疏松提供了统一途径。
5 总结与展望随着年龄的增长以及生活方式的改变,血脂代谢异常、相关炎症因子等因素引起的心血管疾病和老年性疾病存在密切联系。近年来,随着对老年性疾病的不断研究,发现氧化应激在老年性相关疾病中发挥主要作用[30]。因此,寻找引起动脉粥样硬化和骨质疏松症之间的转导因素,有望成为治疗动脉粥样硬化伴随骨质疏松症的新靶点。
| [1] |
Szekanecz Z, Raterman H G, Petho Z, et al. Common mechanisms and holistic care in atherosclerosis and osteoporosis[J]. Arthritis Res Ther, 2019, 21(1): 15. |
| [2] |
Yang X L, Cui Z Z, Zhang H, et al. Causal link between lipid profile and bone mineral density: A mendelian randomization study[J]. Bone, 2019, 127: 37-43. doi:10.1016/j.bone.2019.05.037 |
| [3] |
Mishra B H, Mishra P P, Mononen N, et al. Lipidomic architecture shared by subclinical markers of osteoporosis and atherosclerosis: The cardiovascular risk in young finns study[J]. Bone, 2019, 131: 115160. |
| [4] |
李丽婷. PPARγ2内源性配体对成骨细胞及骨髓细胞骨代谢相关基因表达的影响[D].太原: 山西医科大学, 2011. Li L T. Influence of endogenous ligands of PPARγ2 on mRNA expression of bone metabolism related genes of osteoblastic cells and bone marrow cells[D]. Taiyuan: Shanxi Medical University, 2011. http://cdmd.cnki.com.cn/Article/CDMD-10114-1011092528.htm |
| [5] |
Parhami F, Basseri B, Hwang J, et al. High-density lipoprotein regulates calcification of vascular cells[J]. Circ Res, 2002, 91(7): 570-6. doi:10.1161/01.RES.0000036607.05037.DA |
| [6] |
Tintut Y, Morony S, Demer L L. Hyperlipidemia promotes osteoclastic potential of bone marrow cells ex vivo[J]. Arterioscler Thromb Vasc Biol, 2004, 24(2): e6-10. |
| [7] |
Veronese N, Stubbs B, Crepaldi G, et al. Relationship between low bone mineral density and fractures with incident cardiovascular disease: A systematic review and meta-analysis[J]. J Bone Miner Res, 2017, 32(5): 1126-35. doi:10.1002/jbmr.3089 |
| [8] |
Lopes N H M. The interface between osteoporosis and atherosclerosis in postmenopausal women[J]. Arq Bras Cardiol, 2018, 110(3): 217-8. |
| [9] |
Kajikawa M, Oda N, Kishimoto S, et al. Increasing risk of osteoporotic fracture is associated with vascular dysfunction and abnormal vascular structure in both men and women[J]. Circ J, 2017, 81(6): 862-9. doi:10.1253/circj.CJ-16-1236 |
| [10] |
Mohammadi A, Shateri K, Behzadi F, et al. Relationship between intima-media thickness and bone mineral density in postmenopausal women——a cross-sectional study[J]. Int J Clin Exp Med, 2014, 7(12): 5535-40. |
| [11] |
Prasad M, Reriani M, Khosla S, et al. Coronary microvascular endothelial dysfunction is an independent predictor of development of osteoporosis in postmenopausal women[J]. Vasc Health Risk Manag, 2014, 10: 533-8. |
| [12] |
Barzilay J I, Buzkova P, Cauley J A, et al. The associations of subclinical atherosclerotic cardiovascular disease with hip fracture risk and bone mineral density in elderly adults[J]. Osteoporos Int, 2018, 29(10): 2219-30. doi:10.1007/s00198-018-4611-9 |
| [13] |
Chistiakov D A, Orekhov A N, Bobryshev Y V. LOX-1-mediated effects on vascular cells in atherosclerosis[J]. Cell Physiol Biochem, 2016, 38(5): 1851-9. doi:10.1159/000443123 |
| [14] |
Liu Y, Almeida M, Weinstein R S, et al. Skeletal inflammation and attenuation of Wnt signaling, Wnt ligand expression, and bone formation in atherosclerotic ApoE-null mice[J]. Am J Physiol Endocrinol Metab, 2016, 310(9): E762-73. doi:10.1152/ajpendo.00501.2015 |
| [15] |
Maziere C, Savitsky V, Galmiche A, et al. Oxidized low density lipoprotein inhibits phosphate signaling and phosphate-induced mineralization in osteoblasts.Involvement of oxidative stress[J]. Biochim Biophys Acta, 2010, 1802(11): 1013-9. doi:10.1016/j.bbadis.2010.07.010 |
| [16] |
Hong W, Xu X Y, Qiu Z H, et al. Sirt1 is involved in decreased bone formation in aged apolipoprotein E-deficient mice[J]. Acta Pharmacol Sin, 2015, 36(12): 1487-96. doi:10.1038/aps.2015.95 |
| [17] |
Brodeur M R, Brissette L, Falstrault L, et al. Influence of oxidized low-density lipoproteins (LDL) on the viability of osteoblastic cells[J]. Free Radic Biol Med, 2008, 44(4): 506-17. |
| [18] |
Hamel P, Abed E, Brissette L, et al. Characterization of oxidized low-density lipoprotein-induced hormesis-like effects in osteoblastic cells[J]. Am J Physiol Cell Physiol, 2008, 294(4): C1021-33. doi:10.1152/ajpcell.00361.2007 |
| [19] |
Aitken C J, Hodge J M, Nishinaka Y, et al. Regulation of human osteoclast differentiation by thioredoxin binding protein-2 and redox-sensitive signaling[J]. J Bone Miner Res, 2004, 19(12): 2057-64. doi:10.1359/jbmr.040913 |
| [20] |
Maziere C, Louvet L, Gomila C, et al. Oxidized low density lipoprotein decreases Rankl-induced differentiation of osteoclasts by inhibition of Rankl signaling[J]. J Cell Physiol, 2009, 221(3): 572-8. doi:10.1002/jcp.21886 |
| [21] |
Maziere C, Salle V, Gomila C, et al. Oxidized low density lipoprotein enhanced RANKL expression in human osteoblast-like cells.Involvement of ERK, NFkappaB and NFAT[J]. Biochim Biophys Acta, 2013, 1832(10): 1756-64. doi:10.1016/j.bbadis.2013.05.033 |
| [22] |
Martineau C, Martin-Falstrault L, Brissette L, et al. The atherogenic Scarb1 null mouse model shows a high bone mass phenotype[J]. Am J Physiol Endocrinol Metab, 2014, 306(1): E48-57. doi:10.1152/ajpendo.00421.2013 |
| [23] |
Ambrogini E, Que X, Wang S, et al. Oxidation-specific epitopes restrain bone formation[J]. Nat Commun, 2018, 9(1): 2193. doi:10.1038/s41467-018-04047-5 |
| [24] |
Brodeur M R, Brissette L, Falstrault L, et al. HDL3 reduces the association and modulates the metabolism of oxidized LDL by osteoblastic cells: a protection against cell death[J]. J Cell Biochem, 2008, 105(6): 1374-85. doi:10.1002/jcb.21938 |
| [25] |
Hamada M, Kajita E, Tamaki J, et al. Decreased bone mineral density and osteoporotic fractures are associated with the development of echogenic plaques in the carotid arteries over a 10-year follow-up period: The Japanese Population-based Osteoporosis (JPOS) Cohort Study[J]. Maturitas, 2020, 131: 40-7. doi:10.1016/j.maturitas.2019.10.010 |
| [26] |
El-Nabarawi N, El-Wakd M, Salem M. Atorvastatin, a double weapon in osteoporosis treatment: an experimental and clinical study[J]. Drug Des Devel Ther, 2017, 11: 1383-91. doi:10.2147/DDDT.S133020 |
| [27] |
Yang Y J, Zhu Z, Wang D T, et al. Tanshinol alleviates impaired bone formation by inhibiting adipogenesis via KLF15/PPARgamma2 signaling in GIO rats[J]. Acta Pharmacol Sin, 2018, 39(4): 633-41. doi:10.1038/aps.2017.134 |
| [28] |
Zhang X, Zou L, Li J, et al. Salvianolic acid B and danshensu induce osteogenic differentiation of rat bone marrow stromal stem cells by upregulating the nitric oxide pathway[J]. Exp Ther Med, 2017, 14(4): 2779-88. doi:10.3892/etm.2017.4914 |
| [29] |
Luo S Y, Chen J F, Zhong Z G, et al. Salvianolic acid B stimulates osteogenesis in dexamethasone-treated zebrafish larvae[J]. Acta Pharmacol Sin, 2016, 37(10): 1370-80. doi:10.1038/aps.2016.62 |
| [30] |
莫与琳, 杨亚军, 崔燎. TXNIP介导的氧化应激在疾病中的作用机制[J]. 中国药理学通报, 2017, 34(1): 16-9. Mo Y L, Yang Y J, Cui L. Action and mechanism of oxidative stress mediated by TXNIP in diseases[J]. Chin Pharmacol Bull, 2017, 34(1): 16-9. |
