

 ,
WU Qin,
LIU Jie,
LIU Bo,
XU Yun-yan,
WANG Li-na,
ZHANG Wei,
ZHANG Cheng-chen,
SHI Jing-shan
,
WU Qin,
LIU Jie,
LIU Bo,
XU Yun-yan,
WANG Li-na,
ZHANG Wei,
ZHANG Cheng-chen,
SHI Jing-shan

焦虑/抑郁症是当今严重危害人类身心健康的两种常见精神疾病,给家庭和社会造成沉重负担[1]。焦虑/抑郁常同时发生,目前常用的焦虑/抑郁症动物模型主要有应激诱导型焦虑/抑郁模型和药物诱导型焦虑/抑郁模型等[2-3]。但这些造模方式普遍存在着操作复杂、可重复性差等不足,使得焦虑/抑郁症的基础研究备受限制。因此,发掘一种遗传性的焦虑/抑郁动物模型无疑具有重要的意义。
Fawn-Hooded(FH/Wjd)大鼠是由Wistar大鼠近亲繁殖到第19代得到的近交系大鼠,具有饮酒量大、酒精偏爱度高、5-羟色胺(5-hydroxytryptamine,5-HT)异常、行为绝望明显等特征,其抑郁特性已得到明确,是研究抑郁症的理想的动物模型[4-6]。然而,FH/Wjd大鼠的焦虑特性及其相关生化改变的深入研究目前尚不明确。因此,本研究基于既往研究基础,以Sprague-Dawley(SD)大鼠为对照[4-8],观察FH/Wjd大鼠的焦虑特性及其机制,为FH/Wjd大鼠在神经精神领域的应用提供部分实验数据。
1 材料与方法 1.1 主要仪器与试剂Topscan旷场、高架十字迷宫行为学系统(Cleversys Inc.美国);CoulochemⅢ高效液相库伦阵列电化学仪(ESA美国);Excellence Plus天平XP型(梅特勒-托利多瑞士);Multistan Go多波长酶标仪(Thermo美国);NANO DROP 2000超微量分光光度计(Thermo美国);实时荧光定量PCR仪(Bio-Rad美国)。大鼠儿茶酚胺氧位甲基转移酶(catechol-O-methyltransferase,COMT)、单胺氧化酶(monoamine,MAO)、皮质酮(corticosterone,CORT)、促肾上腺皮质激素(adrenocorticotropic hormone,ATCH)ELISA试剂盒均购自上海江莱生物科技有限公司,批号分别为JL13490、JL12455、JL11379。3,4-二羟基苯乙酸(3, 4-dihydroxyphenylacetic acid,DOPAC)、多巴胺(dopamine,DA)、高相草酸(homovanillicacid,HVA)、5-HT、5-羟吲哚乙酸(5-hydroxyindoleacetic acid,5-HIAA)标准品均购自美国Sigma公司,批号分别为153-98-0、BCBP2642V。TRIzol、逆转录试剂盒均购自大连宝生物公司,SYBR PCR Mix(Bio-Rad美国)。
1.2 实验动物3月龄♂SPF级SD大鼠,体质量(300~350) g,购自陆军军医大学大坪医院实验动物中心[许可证号为:SCXK(渝)2017-0005]。3月龄♂ FH/Wjd大鼠,体质量(280~300) g,由北京大学药物依赖研究所梁建辉教授馈赠,并引进繁殖,饲养于遵义医科大学基础药理教育部重点实验室SPF级实验动物房(许可证号:SYXK黔2014-003),12 h光照/黑夜循环,室温(21~25) ℃,湿度50%~60%。
1.3 行为学检测 1.3.1 高架十字迷宫实验高架十字迷宫(elevated plus maze,EPM)是由一对高开臂和一对闭合臂组成。利用大鼠对新异环境的好奇、探究特性与高空畏惧回避所形成的矛盾冲突来评价其焦虑状态。将大鼠从中央区域面朝开放臂放入,仪器记录10 min内大鼠在各臂的活动情况。
1.3.2 旷场实验旷场箱是由4个长、宽、高均为40 cm的方形盒子组成,箱子底部被划分为中央区域和外周区域。旷场实验(open field test,OFT)利用大鼠的趋避性与面对开阔环境的探索驱动所形成的矛盾冲突,来评价其紧张度和焦虑行为。将大鼠从固定的一角放入,使其自主活动10 min,记录大鼠在外周及中央区域的活动情况。
1.4 DA、5-HT及其代谢产物检测 1.4.1 色谱条件QUATTRO 3 C18反相氨基酸色谱柱,150×2.1 mm(Chrom4,USA),内径5 μm。流动相为pH3.2的缓冲液[含50 mmol·L-1柠檬酸钠,90 mmol·L-1磷酸氢二钠,1.7 mmol·L-1辛烷磺酸钠,0.5 μmol·L-1乙二胺四乙酸钠]-乙腈(92:8,V/V)。0.22 μm滤膜抽滤,超声脱气15 min,HPLC仪使用前流动相平衡过夜。电化学检测器工作电极为石墨碳,检测参数ChannelⅠ-150 mV,ChannelⅡ 300 mV,guard cell 350 mV。柱温30 ℃,流速0.21 mL·min-1,进样量20 μL。
1.4.2 样本制备称取皮层组织约80 mg,按1 mg组织对应加入12.5 μL 5%的HClO4溶液,冰上匀浆,后转移置1.5 mL离心管中4 ℃ 14 000×g离心10 min去蛋白,取上清按1 : 2的体积加入流动相稀释,混匀后用0.22 μm针头滤器过滤样本,进样。
1.5 ELISA实验称取皮层组织,按1 : 9的重量体积比例,加入PBS,冰上充分研磨,将匀浆液于4 ℃ 5 000×g离心10 min,分装上清液,冻存于-80 ℃,待测。按ELISA试剂盒说明书进行操作。
1.6 实时荧光定量RT-PCR [9]取(50~100) mg组织置于1 mL TRIzol中冰上匀浆,提取组织中的总RNA,逆转录成cDNA,以cDNA为模板,荧光定量PCR检测各基因的表达。PCR引物由上海生工生物有限公司合成,GAPDH上游序列5′-CCAAGGAGTAAGACCCCTGG-3′,下游序列5′-AGGGGAGATTCAGTGGTG-3′,COMT上游序列5′-CCAGCAGCTCACACCACATC-3′,下游序列5′-ATGCCTCTGCCTCCTG GATA-3′。
1.7 mRNA-seq检测取SD、FH/Wjd大鼠海马样本,送至上海天昊生物科技有限公司进行mRNA-seq测序。
1.8 统计学分析所有数据以均数±标准差(x±s)表示,使用SPSS 18.0统计学软件进行数据分析,两组间比较采用独立样本t检验。
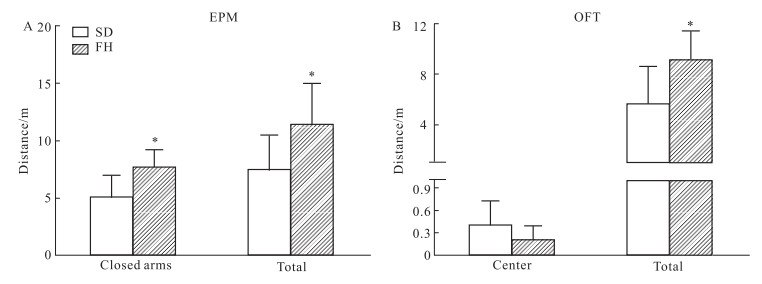
2 结果 2.1 FH/Wjd大鼠与SD大鼠焦虑行为比较Fig 1A所示,与SD大鼠比较,FH/Wjd大鼠在EPM闭合臂的活动距离及活动总路程均显著高于SD大鼠(P < 0.05;P < 0.05);Fig 1B所示,FH/Wjd大鼠在OFT中央区域活动的距离低于SD大鼠,活动总路程显著高于SD大鼠(P < 0.05)。
|
| Fig 1 Difference in anxiety behaviors between FH/Wjd rats and SD rats (x±s, n=9~10) The results of elevated plus maze test (A) and open field test (B).*P < 0.05 vs SD group. |
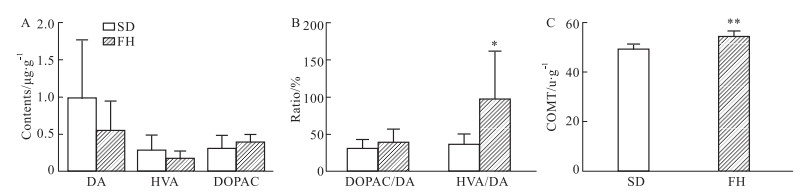
Fig 2A所示,与SD大鼠比较,FH/Wjd大鼠皮层DA、DOPAC含量较低,差异无统计学意义,HVA含量无明显差异;Fig 2B所示,FH/Wjd大鼠DOPAC/DA无明显差异,HVA/DA显著较高(P < 0.05);Fig 2C所示,FH/Wjd大鼠皮层组织中COMT活性显著较高(P < 0.01)。
|
| Fig 2 Difference in metabolism of DA between FH/Wjd rats and SD rats (x±s, n= 9~10) The contents of DA, DOPAC and HVA in rats cortex tissues detected by HPLC-ECD(A); The metabolism ratio of DA (B); The enzyme activity of COMT in rats cortex tissue detected by ELISA(C).*P < 0.05 vs SD group, **P < 0.01 vs SD group. |
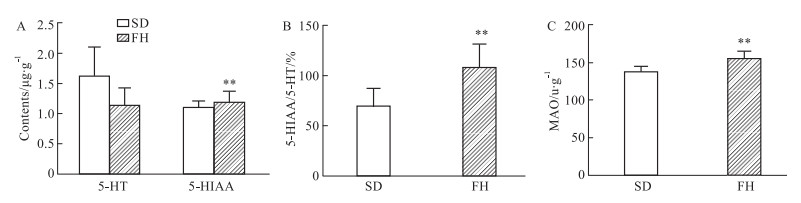
Fig 3A所示,与SD大鼠比较,FH/Wjd大鼠皮层组织中5-HT(P < 0.01)含量显著较低,5-HIAA含量无差异;Fig 3B所示,FH/Wjd大鼠5-HT代谢率显著较高(P < 0.01);皮层组织MAO活性显著较高(P < 0.01,Fig 3C)。
|
| Fig 3 Difference of 5-HT metabolism between FH/Wjd rats and SD rats (x±s, n=9~10) The contents of 5-HT and 5-HIAA in rats cortex tissues detected by HPLC-ECD (A), the metabolism ratio of 5-HT(B), the enzyme activity of MAO in rats cortex tissue detected by ELISA(C). **P < 0.01 vs SD group. |
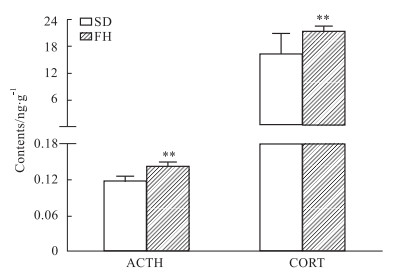
Fig 4所示,FH/Wjd大鼠皮层CORT、ACTH含量均显著高于SD大鼠(P < 0.01;P < 0.01)。
|
| Fig 4 Contents of CORT and ACTH in cortex tissues between FH/Wjd rats and SD rats detected by ELISA assay (x±s, n=9~10) **P < 0.01 vs SD group. |
Fig 5所示,FH/Wjd大鼠皮层、海马、纹状体及血清中COMT mRNA的相对表达量均高于SD大鼠(P < 0.01)。

|
| Fig 5 Expression of COMT mRNA in different tissues between FH/Wjd rats and SD rats detected by real-time PCR (x±s, n=9~10). **P < 0.01 vs SD group. |
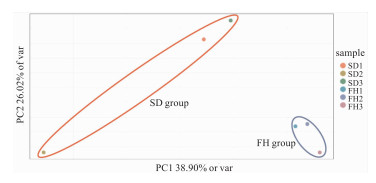
在两个主成分(PC1、PC2)的情况下,得分图中能够观察到SD大鼠与FH/Wjd大鼠的基因在不同纬度上各自聚类,SD大鼠与FH/Wjd大鼠显著区别。
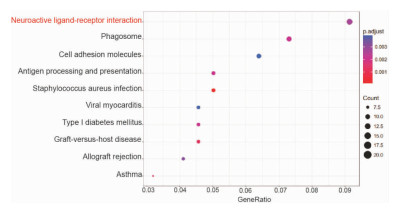
2.6.2 FH/Wjd大鼠与SD大鼠差异基因富集通路KEGG通路富集显示SD大鼠与FH/Wjd大鼠差异基因在神经活性配体受体途径富集程度最高,见Fig 7。
|
| Fig 6 PCA of transgenic contours of rat hippocampus gene at genome level (n=3) |
|
| Fig 7 KEGG analysis of differentially expressed genes between FH/Wjd rats and SD rats (n=3) |
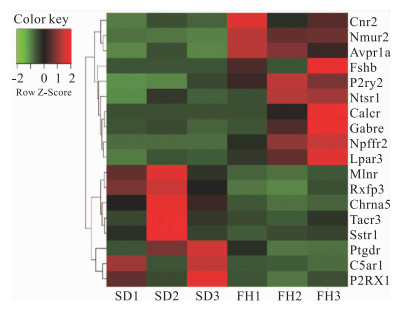
SD大鼠与FH/Wjd大鼠富集在神经活性受体配体途径的主要差异基因有18个:Cnr2、Nmur2、Avpr1a、Fshb、P2ry2、Ntsr1、Calcr、Gabre、Npffr2、Lpar3、Mlnr、Rxfp3、Chrna5、Tacr3、Sstr1、Ptgdr、C5ar1、P2rx1,其功能涉及突触传递、神经元投射、神经递质传递等方面(Fig 8)。
|
| Fig 8 Heat map analysis of rat neuroactive ligand-receptor interaction pathway genes (n=3) Red represents up-regulation, green represents down-regulation. |
既往研究表明,与SD大鼠比较,FH/Wjd大鼠在强迫游泳实验中不动时间明显较长,糖水偏爱率较低;水迷宫实验中逃避潜伏期较长,转棒实验中在棒停留时间较短,具有明显的行为绝望、快感缺失、学习记忆低、疲劳耐力差等显著抑郁特性[4, 7]。EPM、OFT是利用探索与回避形成的矛盾冲突来评价焦虑行为的经典方法[10]。本实验结果表明,FH/Wjd大鼠在EPM和OFT中自发活动性较高,EPM臂闭活动距离较多,OFT中央区域活动距离较少,因此,与SD大鼠比较,FH/Wjd大鼠同时也具有明显的焦虑行为及高活动性。
焦虑/抑郁的发生与单胺类神经递质功能紊乱密切相关,DA和5-HT是重要的单胺类神经递质[11-12]。DA主要在COMT的作用下被代谢为DOPAC和HVA,5-HT在MAO作用下生成5-HIAA。本研究结果显示,FH/Wjd大鼠DA、5-HT含量低于SD大鼠,其变化与FH/Wjd大鼠的抑郁行为相符;同时,FH/Wjd大鼠COMT、MAO活性、5-HIAA/5-HT、HVA/DA比值均显著高于SD大鼠,提示FH/Wjd大鼠DA、5-HT代谢亢进,其机制与FH/Wjd大鼠的高活动性及焦虑行为相一致。因此,FH/Wjd大鼠中枢DA、5-HT含量低下、但代谢亢进等异常表现可能与其抑郁、焦虑共病有关。
下丘脑-垂体-肾上腺(hypothalamus-pituitary-adrenal,HPA)轴功能紊乱是焦虑/抑郁症发生的重要机制,CORT、ACTH含量能够一定程度反映HPA轴的功能状态[13]。本研究结果显示FH/Wjd大鼠CORT、ACTH含量均显著高于SD大鼠,提示FH/Wjd大鼠存在HPA轴亢进,与其焦虑/抑郁的行为学表现一致。
COMT具有代谢儿茶酚胺类神经递质、儿茶酚胺类雌激素和外源性化合物的作用,COMT基因突变引起COMT表达或活性改变,进而与帕金森症、阿尔茨海默症、精神分裂症及注意缺陷障碍、重度抑郁症等疾病的产生密切相关[14]。目前,COMT被视为多种精神疾病的候选基因或诊断标志物[15]。研究报道在注意力缺陷多动症模型、精神分裂症患者中COMT含量或mRNA的表达均显著高于正常组[16]。本研究结果表明,FH/Wjd大鼠中枢、外周COMT相对表达量均较SD大鼠高,提示FH/Wjd大鼠可能存在神经精神系统的异常。同时,本实验还采用了mRNA-seq技术对SD大鼠、FH/Wjd大鼠海马组织中所有的基因进行了检测,结果表明,SD大鼠与FH/Wjd大鼠基因表达存在明显差异,其差异基因主要富集在神经活性受体配体途径,进一步提示了FH/Wjd大鼠在神经精神系统的基因表达存在差异。
综上所述,本研究通过FH/Wjd大鼠与SD大鼠比较,发现FH/Wjd大鼠具有明显的焦虑行为和高活动性,其机制可能与DA、5-HT含量低下、代谢亢进,HPA轴亢进,COMT异常,神经精神系统的异常有关。
| [1] |
Manoharan A, McMartin K, Young C, et al. Psychotherapy for major depressive disorder and generalized anxiety disorder: ahealth technology assessment[J]. Ont Health Technol Assess Ser, 2017, 17(15): 1-167. |
| [2] |
Hao Y, Ge H. Selecting an appropriate animal model of depression[J]. Int J Mol Sci, 2019, 20(19): e4827. doi:10.3390/ijms20194827 |
| [3] |
Bourin M. Animal models for screening anxiolytic-like drugs: a perspective[J]. Dialogues Clin Neurosci, 2015, 17(3): 295-303. |
| [4] |
张金娜.肠道微生物与抑郁症的关联性研究[D].昆明: 昆明医科大学, 2013. Zhang J N. Study on relationship betweeen gut microbiota and depresive disorder[D]. Kunming: Kunming Med Univ, 2013. http://cdmd.cnki.com.cn/Article/CDMD-10678-1013327495.htm |
| [5] |
张永燊, 杨长青, 段丽萍, 等. 先天抑郁大鼠内脏敏感性研究[J]. 中华消化杂志, 2011, 31(6): 377-80. Zhang Y S, Yang C Q, Duan L P, et al. Study on the visceral sensitivity of inherent depressive rats[J]. Chin J Digest, 2011, 31(6): 377-80. doi:10.3760/cma.j.issn.0254-1432.2011.06.005 |
| [6] |
刘懿萱, 张永燊, 段丽萍, 等. 先天抑郁对大鼠幼年结肠乙酸刺激致慢性内脏高敏感的影响[J]. 北京大学学报(医学版), 2015, 47(2): 289-94. Liu Y X, Zhang Y S, Duan L P, et al. Effect of inherent depression on chronic visceral hypersensitivity induced by colon acetate stimulation in neonatal rats[J]. J Peking Univ (Health Sci), 2015, 47(2): 289-94. doi:10.3969/j.issn.1671-167X.2015.02.23 |
| [7] |
熊庭旺, 贺希, 魏胜焦, 等. SD大鼠与FH/Wjd大鼠神经行为学差异比较[J]. 遵义医学院学报, 2018, 41(6): 663-8. Xiong T W, He X, Wei S J, et al. Comparison of nenrobehavioral differences between SD rats and FH/Wjd rats[J]. J Zunyi Med Univ, 2018, 41(6): 663-8. doi:10.3969/j.issn.1000-2715.2018.06.002 |
| [8] |
赵福坤, 吴芹, 李勃, 等. FH/Wjd大鼠和SD大鼠摄酒行为的比较观察[J]. 中国药理学通报, 2019, 35(3): 419-24. Zhao F K, Wu Q, Li B, et al. Comparative observation on drinking behavior of FH/Wjd rats and SD rats with different liquors[J]. Chin Pharmacol Bull, 2019, 35(3): 419-24. doi:10.3969/j.issn.1001-1978.2019.03.024 |
| [9] |
Li S, Zhou J, Xu S, et al. Induction of Nrf2 pathway by Dendrobium nobile Lindl. alkaloids protects against carbon tetrachloride induced acute liver injury[J]. Biomed Pharmacother, 2019, 117: 109073. doi:10.1016/j.biopha.2019.109073 |
| [10] |
Grubac Z, Sutulovic N, Ademovic A, et al. Short-term sleep fragmentation enhances anxiety-related behavior: the role of hormonal alterations[J]. PLoS One, 2019, 14(7): e0218920. doi:10.1371/journal.pone.0218920 |
| [11] |
王婷婷, 黄菲, 吴辉, 等. 双侧嗅球切除对小鼠行为、海马神经递质及抑郁相关基因表达的影响[J]. 中国药理学通报, 2015, 31(5): 686-91. Wang T T, Huang F, Wu H, et al. Influence of olfactory bulbectomy on mouse neurobehaviors, hippocampal neurotransmission and depression relevant gene expressions[J]. Chin Pharmacol Bull, 2015, 31(5): 686-91. doi:10.3969/j.issn.1001-1978.2015.05.019 |
| [12] |
匡胜男, 罗映, 田小燕, 等. 美洛昔康改善慢性应激大鼠抑郁行为的机制初探[J]. 中国药理学通报, 2016, 32(2): 263-8. Kang S N, Luo Y, Tian X Y, et al. Effect of meloxicam on CUMS-induced depressive-like behavior in rats and its preliminary mechanism[J]. Chin Pharmacol Bull, 2016, 32(2): 263-8. doi:10.3969/j.issn.1001-1978.2016.02.022 |
| [13] |
Ramos-Ortolaza D L, Doreste-Mendez R J, Alvarado-Torres J K, et al. Ovarian hormones modify anxiety behavior and glucocorticoid receptors after chronic social isolation stress[J]. Behav Brain Res, 2017, 328: 115-22. doi:10.1016/j.bbr.2017.04.016 |
| [14] |
金远香, 刘洁. COMT的遗传药理学研究进展[J]. 中国药理学通报, 2013, 29(8): 1041-4. Jing Y X, Liu J. Research advances in pharmacogenetics of COMT[J]. Chin Pharmacol Bull, 2013, 29(8): 1041-4. doi:10.3969/j.issn.1001-1978.2013.08.002 |
| [15] |
Halleland H, Lundervold A J, Halmoy A, et al. Association between catechol O-methyltranse (COMT) haplotypes and severity of hyperactivity symptoms in adults[J]. Am J Med Genet B Neuropsychiatr Genet, 2009, 150B(3): 403-10. doi:10.1002/ajmg.b.30831 |
| [16] |
Zai G, Robbins T W, Sahakian B J, et al. A review of molecular genetic studies of neurocognitive deficits in schizophrenia[J]. Neurosci Biobehav Rev, 2017, 72: 50-67. doi:10.1016/j.neubiorev.2016.10.024 |