

黄枚(1966-),女,硕士,教授,研究方向:心脑血管与抗炎免疫药理,通讯作者, E-mail:hmei0303@qq.com
脑卒中是一种急性脑血管疾病,据其发病机制可分为缺血性脑卒中和出血性脑卒中,其中缺血性脑卒中占脑卒中病例数的80%。缺血性脑卒中是由于脑的供血动脉狭窄或闭塞,脑供血不足导致的脑组织缺血性坏死。目前研究认为,脑缺血后的急性炎症反应是导致脑组织损伤加剧的重要因素,对脑缺血后神经元细胞死亡和神经重构具有重要影响[1]。小胶质细胞是大脑组织中固有的免疫细胞,其在脑卒中后的迅速激活是启动脑缺血炎症反应的关键[2],因此,抑制小胶质细胞的过度激活及其引起的一系列反应是缺血性脑卒中重要的治疗靶点。最新研究发现,神经元与小胶质细胞存在相互作用,小胶质细胞的活化程度受到神经元的严密调控[3]。近期的研究发现,神经元也可以释放趋化因子[4],在缺血性脑损伤发生后,受损的神经元表达的趋化因子是神经元-小胶质细胞信号传导中的重要介质。趋化因子21(chemokine ligand 21,CCL21)是神经元表达的重要趋化因子,其与小胶质细胞上表达的趋化因子受体3(chemokine receptor 3,CXCR3)结合,可激活小胶质细胞,是参与神经元-小胶质细胞信号通路的重要环节[5]。肿瘤坏死因子样弱凋亡诱导因子(tumor necrosis factor-like weak inducer of apoptosis,TWEAK)/成纤维细胞生长因子诱导型14(fibroblast growth factor-inducible immediate-early response protein 14,Fn14)信号通路可通过激活NF-κB非经典信号途径,上调神经元CCL21的表达,以此促进小胶质细胞激活,进一步加重脑损伤[6-8]。
栝楼桂枝汤(gua lou guizhi decoction,GLGZD)出自东汉末年张仲景《金匮要略》,现临床用于治疗脑卒中后肢体痉挛,疗效显著[9]。目前认为,脑卒中后肢体痉挛是脑缺血后上运动神经元损伤所致,而凋亡是脑缺血引起选择性神经元丢失的一种重要形式[10]。课题组前期研究发现,GLGZD可通过调控多条信号通路产生抗凋亡、抗炎等作用,以此来发挥神经保护作用[11-12]。但作用机制尚未完全阐明,故本研究以神经元与小胶质细胞在缺血性脑损伤中的相互作用为切入点,研究GLGZD是否通过TWEAK/Fn14/CCL21/CXCR3信号通路调控小胶质细胞的活化,以此来探索GLGZD缓解脑卒中后肢体痉挛的可能机制。
1 材料 1.1 实验动物SPF级♂SD大鼠72只,体质量(260±10)g,购自上海斯莱克实验动物责任有限公司,许可证号:SCXK(沪)2017-0005,合格证号:2015000547928。并于福建中医药大学实验动物中心饲养,合格证:SYXK(闽)2014-0001。
1.2 实验药物白芍(厦门燕来福制药有限公司,批号:180803)、天花粉(亳州市中药饮片厂,批号:1712028183)、桂枝(陇西聚善堂中药材实业有限公司,批号:20130110)、甘草(厦门燕来福制药有限公司,批号:180530)、大枣(福建承创堂药店)、生姜(福建承创堂药店)、尼莫地平(湖北百草制药有限公司,批号:170602)。
1.3 实验试剂DeadEndTM Fluorometric TUNEL System(美国Promega公司,货号:G3250);RNA isolater(南京Vazyme生物科技有限公司,货号:7E261K8);HiScript Q RT SuperMix for PCR(南京Vazyme生物科技有限公司,货号:7E281I8);ChamQTM SYBR qPCR Master Mix(南京Vazyme生物科技有限公司,货号:7E210K8);Anti-TNF alpha antibody(英国abcam公司,货号:ab6671);Anti-liver Arginase antibody(英国abcam公司,货号:ab91279);内源性过氧化物酶阻断液(武汉博士德生物工程有限公司,货号:AR1108);DAB显色试剂盒(武汉博士德生物工程有限公司,货号:AR1022);即用型SABC-POD(小鼠/兔IgG)试剂盒(武汉博士德生物工程有限公司,货号:SA1020)。
1.4 仪器尼龙线栓(广州佳灵生物技术有限公司,型号:3600AAA);小动物核磁共振成像仪(MRI,德国BRUKER公司,型号:BioSpec 70/20 USR);生物组织自动脱水机(湖北孝感宏业医用仪器有限公司,型号:TS-12D);生物组织石蜡包埋机(湖北孝感宏业医用电子技术有限公司,型号:YB-6LF);生物组织摊烤机(湖北孝感宏业医用电子技术有限公司,型号:YT-7FB);石蜡切片机(美国Thermo Fisher公司,型号:HM325);光学显微镜(德国Leica公司,型号:DM400B LED);倒置荧光显微镜(德国Leica公司,型号:DMi8);Termal circle PCR仪(美国Bio-Rad公司,型号:C1000TM);实时荧光定量PCR仪(美国Applied Biosystem公司。型号:ABI 7900)。
2 方法 2.1 制备栝楼桂枝汤GLGZD的处方:天花粉30 g、桂枝9 g、大枣9 g、白芍9 g、生姜9 g、甘草6 g。称取2个处方量的药材,放于2 000 mL圆底烧瓶中,加10倍量超纯水,浸泡30 min,于冷凝回流装置中煮沸,并保持微沸提取1.5 h,之后过滤药液,并于药渣中加入8倍量超纯水,重复以上步骤。合并两次药液,高压旋蒸浓缩至100 mL,即得栝楼桂枝汤高剂量(1.44 g·mL-1)。
2.2 MCAO模型制备用2%戊巴比妥钠(3 mL·kg-1)腹腔注射麻醉动物,仰卧位固定于鼠板上,颈正中线偏右切口,用镊子钝性分离肌肉与筋膜,分离出颈总动脉(common carotid artery,CCA)、颈外动脉(external carotid artery,ECA)、颈内动脉(internal carotid artery,ICA),结扎CCA与ICA,于ICA上挂线备用,并用动脉夹夹闭。用眼科剪在CCA近心端血管壁30°夹角剪一小口,插入线栓至线栓黑点完全进入ICA,2 h后部分抽出线栓实现再灌注,结扎缝合。待大鼠苏醒后即刻参照改良神经功能缺损评分(modified neurological severity score,mNSS)[13]对大鼠进行神经功能损伤程度的评价,评分>6分者视为造模成功,纳入实验分组。
2.3 分组与给药将造模成功的大鼠随机分为5组:MCAO模型组、GLGZD低剂量组(3.6 g·kg-1)、中剂量组(7.2 g·kg-1)、高剂量组(14.4 g·kg-1)、阳性对照组(尼莫地平,6 mg·kg-1),另设一组假手术(Sham)组,每组12只。各组大鼠均在手术当天评分后开始给药,此后于每天上午9 : 00给药,给药组灌服相应浓度药物(10 mL·kg-1·d-1),MCAO组与假手术组灌服0.9%生理盐水(10 mL·kg-1·d-1),连续7 d。
2.4 神经功能缺损评分GLGZD干预7 d后,采用mNSS[13]对各组大鼠进行神经行为学评分,该评分包括运动试验、感觉试验、平衡木试验、反射丧失和不正常运动等四项评估。运动试验包括提尾试验(含前肢屈曲、后肢屈曲、头部在30 s内偏离垂直轴>10°三个指标,每个1分,共3分)和爬行试验(正常行走计0分,不能直线行走计1分,向轻瘫侧转圈计2分,向轻瘫侧倾倒计3分),感觉试验包括放置试验(视觉和触觉任一存在障碍计1分)和本体感觉试验(将大鼠朝桌子边缘轻推,无反抗计1分),平衡木试验根据大鼠在平衡木上保持平衡的时间评分(<20 s计6分,<40 s计5分,<60 s计4分,>60 s计3分,一肢体从平衡木垂落计2分,紧抱平衡木计1分,稳定平衡姿势计0分),反射丧失和不正常运动包括耳廓反射(接触外耳道时不摇头计1分)、角膜反射(用棉丝轻触角膜时不眨眼计1分)、惊恐反射(对快弹硬纸板的噪音无运动反应计1分)和肌张力障碍(存在癫痫、肌阵挛或肌张力障碍计1分)。评价等级为0~18,0分为正常无缺陷,18分为最大缺陷。
2.5 小动物核磁共振成像(magnetic resonance imaging,MRI)检测脑梗死体积实验采用MRI对大鼠脑部进行T2WI扫描,实验参数:T2WI采用TSE序列;重复时间:4 200 ms;回声时间:35 ms;扫描层数:21层;视场:32 mm×32 mm;平均信号数:2;扫描时间:4 m 28 s 800 ms。以ImageJ图像分析软件测定大鼠T2WI脑梗死体积。
2.6 组织石蜡切片的制备大鼠末次给药2 h后用2%戊巴比妥钠(3 mL·kg-1)腹腔注射麻醉,固定,打开胸腔,用透灌针从左心室插到主动脉,将右心耳剪开。先用生理盐水推注,直至无血液流出后,再用4%多聚甲醛推注至全身僵硬,断头取完整大脑,置于4%多聚甲醛中固定24 h后,取出用超纯水清洗,再用大鼠脑模具切成均等6片,进行脱水、石蜡包埋以及切片。
2.7 TUNEL法检测细胞凋亡率取石蜡切片进行脱蜡复水,清洗后4%多聚甲醛固定10 min,清洗,使用蛋白酶K(稀释比1 : 500)处理8 min,平衡缓冲液室温孵育10 min,滴加50 μL rTdT缓冲液,盖上塑料盖玻片,放入湿盒避光并于37 ℃孵育1 h。滴加2×SSC溶液于室温避光孵育15 min,DAPI染核,抗荧光淬灭封片剂封片,使用荧光倒置显微镜于400倍镜下观察并拍摄缺血侧大脑皮层阳性细胞表达情况,实验采用ImageJ图像分析软件进行统计。
2.8 免疫组织化学法检测炎症因子TNF-α的表达水平取石蜡切片进行脱蜡复水,内源性过氧化物酶阻断液覆盖10 min,抗原修复,5% BSA封闭2 h,滴加相应一抗(稀释比1 : 100),4 ℃冰箱孵育12 h,清洗后滴加相应二抗室温孵育2 h,清洗,SABC 37 ℃孵育1 h,DAB试剂盒显影,苏木素复染,封片,使用荧光倒置显微镜于400倍镜下观察并拍摄缺血侧大脑皮层阳性细胞表达情况,实验采用ImageJ图像分析软件进行统计。
2.9 RT-qPCR检测IBA-1、TWEAK、Fn14、NIK、Rel B、CCL21、CXCR3 mRNA表达末次给药2 h后,断头取大鼠缺血侧皮层脑组织,TRIzol法提取总RNA,使用HiScript Q RT SuperMix for PCR试剂盒逆转录得到cDNA,再采用ChamQTM SYBR qPCR Master Mix试剂盒检测IBA-1、TWEAK、Fn14、NIK、Rel B、CCL21、CXCR3 mRNA表达水平,PCR引物由上海尚亚生物技术有限公司合成,本实验采用GAPDH为内参基因,各指标的基因相对表达根据2-ΔΔCt计算得到。引物序列见Tab 1。
| Gene | Forward primer(5'→3') | Reverse primer(3'→5') |
| TWEAK | ATTGGGGAATTTACGGTCATCAG | CACACCATTCACCAGCAAGT |
| Fn14 | GCTCCTCGTGTTGGGATTCG | GGACAAGAAGCGCAGTCCAT |
| NIK | CCGCTCTGTCTCAAGATTGC | ACCTCCCACTTCCTGTAACG |
| Rel B | AGACACTGATTTCTTCCCTGGTA | CAGCAGGTCCAACTAGTGAAG |
| CCL21 | GGAAGCAAGAACCGAGCCT | CCTGCAGTTTTGTTTCCCTGG |
| CXCR3 | CAGAGGCGCTTTCGAGCTAT | AGTGGATTGAGGCAGCAGTG |
| IBA-1 | TCCGAGGAGACGTTCAGTTAC | CAGTTGGCTTCTGGTGTTCTT |
结果以x±s表示,采用SPSS 20.0软件进行统计,各组间数据若符合正态分布则用采用单因素方差分析,若不符,则采用非参数检验。
3 结果 3.1 GLGZD对MCAO大鼠神经功能的影响mNSS结果显示,造模后MCAO大鼠整体神经功能评分均明显高于Sham组大鼠(P<0.01);经GLGZD干预7 d后,与MCAO组相比,GLGZD-L、GLGZD-M及GLGZD-H组整体神经功能评分均明显下降(P<0.01)。见Fig 1。

|
| Fig 1 Effects of GLGZD on neurological function in MCAO rats (x±s, n=12) **P < 0.01 vs Sham; ##P < 0.01 vs MCAO |
MRI结果显示,与Sham组相比,MCAO组大鼠缺血侧大脑出现大片明显梗死区域(P<0.01);经GLGZD干预7 d后,各剂量组大鼠缺血侧脑梗死体积明显减少,且差异具有统计学意义(P<0.05或0.01)。见Fig 2。

|
| Fig 2 Effects of GLGZD on cerebral infarction volume (Part of yellow arrow) in MCAO rats (x±s, n=12) **P < 0.01 vs Sham; #P < 0.05 vs MCAO, ##P < 0.01 vs MCAO |
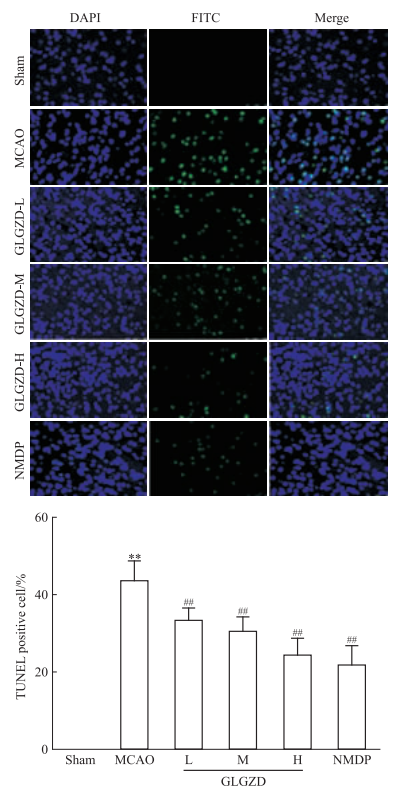
TUNEL染色结果显示,与Sham组相比,MCAO组大鼠缺血侧大脑皮层TUNEL阳性细胞表达明显升高,神经细胞凋亡率明显增高(P<0.01);经GLGZD干预7 d后,各剂量组大鼠缺血侧大脑皮层TUNEL阳性细胞数明显减少,神经细胞凋亡率均有不同程度的降低(P<0.01)。见Fig 3。
|
| Fig 3 Effects of GLGZD on apoptosis of neurons in cerebral cortex in MCAO rats (×400)(x±s, n=6) **P < 0.01 vs Sham; ##P < 0.01 vs MCAO |
免疫组织化学法结果显示,MCAO组较Sham组大鼠缺血侧皮层脑组织中TNF-α蛋白表达明显增加(P<0.01),GLGZD干预7 d后TNF-α蛋白表达明显减少(P<0.05或0.01)。见Fig 4。

|
| Fig 4 Effects of GLGZD on TNF-α positive cells in cerebral cortex in MCAO rats (×400)(x±s, n=6) **P < 0.01 vs Sham; #P < 0.05 vs MCAO, ##P < 0.01 vs MCAO |
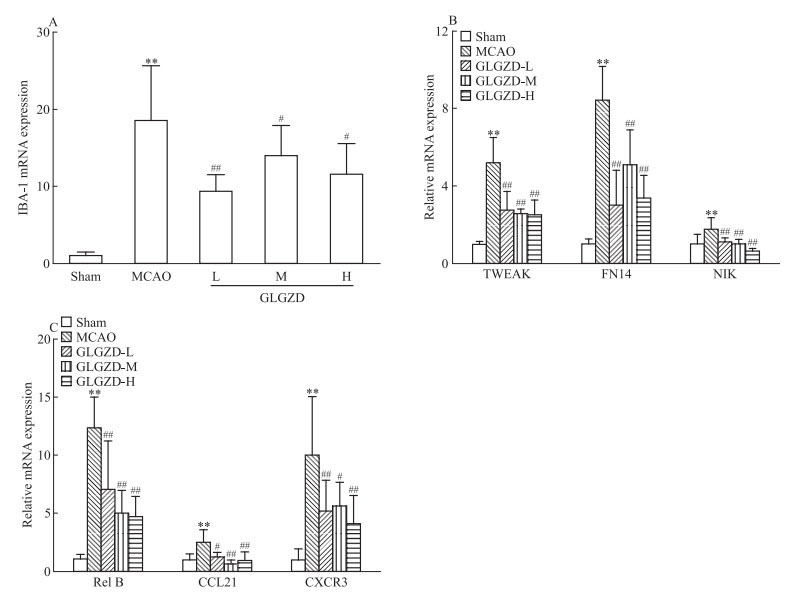
RT-qPCR法结果显示,与Sham组相比,MCAO组大鼠缺血侧大脑皮层组织IBA-1、TWEAK、Fn14、NIK、Rel B、CCL21、CXCR3 mRNA表达增加(P<0.01);经GLGZD干预7 d后,各剂量组大鼠缺血侧IBA-1、TWEAK、Fn14、NIK、Rel B、CCL21、CXCR3 mRNA表达明显减少,且差异具有统计学意义(P<0.05或0.01)。见Fig 5。
|
| Fig 5 Effects of GLGZD on IBA-1 mRNA(A) and TWEAK, Fn14, NIK mRNA(B) and Rel B, CCL21, CXCR3 mRNA(C) in MCAO rats (x±s, n=6) **P < 0.01 vs Sham; #P < 0.05, ##P < 0.01 vs MCAO |
在脑缺血/再灌注损伤的实验研究中,常采用全脑缺血或者局灶性脑缺血的动物模型,然而在临床上较为常见的是局灶性脑缺血,且MCAO造成的动物局灶性脑缺血能很好模拟临床上脑缺血疾病情况,是研究缺血性脑卒中的经典模型[14]。本实验采用线栓阻断大鼠大脑中动脉血流后,大鼠mNSS评分、脑梗死体积、神经细胞凋亡率均明显高于Sham组,提示MCAO模型大鼠制备成功。治疗7 d后,GLGZD各剂量组和阳性对照组均能明显改善模型大鼠运动、感觉、反射、平衡功能,能明显减少脑梗死体积和抑制缺血侧皮层组织中神经细胞的凋亡,且高剂量组疗效最为明显,与阳性对照组相比差异无显著性,提示GLGZD对脑缺血/再灌注损伤具有较好的保护作用,这一结果也与课题组前期研究相一致[10, 11];阳性对照药物尼莫地平对脑缺血/再灌注损伤亦具有显著的保护作用,提示本实验体系可靠,故GLGZD进一步的作用机制研究不再加入阳性对照。
缺血性脑卒中因缺血造成神经元死亡,导致原发性脑损伤,并使免疫细胞向细胞外释放促炎,这些物质可引发一系列炎症反应,进一步加剧神经细胞损伤,导致继发性脑损伤[15]。小胶质细胞对神经炎症有深远的影响,活化的小胶质细胞通常负责清除坏死的神经细胞和恢复神经功能,然而当小胶质细胞被过度激活时,会大量分泌TNF-α等多种神经炎症因子,促进周围神经细胞凋亡,导致神经元进一步受损[16]。本研究发现,与Sham组相比,MCAO大鼠缺血侧皮层脑组织中小胶质细胞活化的标志物IBA-1 mRNA和炎症因子TNF-α蛋白的表达量均明显增加,提示脑缺血/再灌注损伤后小胶质细胞大量活化,并释放大量炎症因子,诱导神经元凋亡,进一步加重脑组织损伤。干预7 d后,GLGZD各剂量组大鼠缺血侧大脑皮层脑组织中IBA-1 mRNA和TNF-α蛋白表达量均明显的减少,提示GLGZD可抑制小胶质细胞的过度活化,减少炎症因子的释放,减轻脑缺血/再灌注损伤后的炎症反应,从而发挥抗缺血后神经元的凋亡,减轻脑组织损伤的作用。
新近研究发现,神经元不仅是小胶质细胞的作用目标,而且是调节小胶质细胞活化的重要参与者,即小胶质细胞的活化程度受到神经元的严密调控[17],神经元和小胶质细胞之间存在相互作用。神经元可通过多条信号通路表达大量细胞因子,并与小胶质细胞表面的特异性受体结合介导彼此之间的信号传导,以此来调控小胶质细胞的活化。其中,TWEAK/Fn14/CCL21/CXCR3信号通路参与神经元-小胶质细胞相互作用,在小胶质细胞活化中发挥重要作用。
最新研究发现,TWEAK与Fn14的结合可增加炎症细胞的积累和神经元损伤,与脑缺血期间的细胞死亡密切相关[18]。研究指出,在中风后,Fn14在神经元上高表达,并在受TWEAK激活后可抑制细胞质中NF-κB诱导激酶(NF-κB induced kinase,NIK)的降解,而不断积累的NIK磷酸化抑制性κB激酶(inhibitory kappa B kinase,IKK),继而使核转录因子(nuclear factor kappa-B,NF-κB)p100磷酸化降解成p52,暴露其核定位序列后,与RelB组成异源二聚体转移进入细胞核内,RelB存在转录激活结构域,从而调控靶基因(如趋化因子CCL21等)的表达,进而上调神经元CCL21的表达[6, 7]。而上调的CCL21与其小胶质细胞上表达的特异性受体CXCR3结合,持续激活小胶质细胞,使其释放大量炎性介质,引发并扩大继发性脑组织损伤[8]。我们采用RT-qPCR检测结果显示,MCAO组大鼠缺血侧皮层脑组织中神经元-小胶质细胞相互作用的相关因子TWEAK、Fn14、NIK、Rel B、CCL21、CXCR3 mRNA表达量均明显增多,提示脑缺血/再灌注损伤后引起的小胶质细胞大量活化与TWEAK/Fn14/CCL21/CXCR3信号通路的激活相关,这一结果与文献报道相一致[6-8],经GLGZD干预7 d后,各剂量组均可不同程度地下调上述因子mRNA的表达,提示GLGZD可通过抑制TWEAK/Fn14/CCL21/CXCR3信号通路,调控神经元-小胶质细胞间相互作用,从而抑制小胶质细胞的过度活化,减轻炎症反应,发挥脑保护作用。
综上所述,GLGZD能显著改善大鼠脑缺血/再灌注损伤,这一作用可能与其通过影响TWEAK/Fn14/CCL21/CXCR3信号通路,抑制小胶质细胞活化,从而减轻炎症反应有关。
( 致谢: 本实验在福建中医药大学药学院生物医药研发中心完成,感谢所有老师及同学的支持与帮助!)
| [1] |
Frechou M, Beray B V, Raynaud J S, et al. Detection of vascular cell adhesion molecule-1 expression with USPIO-enhanced molecular MRI in a mouse model of cerebral ischemia[J]. Contrast Media Mol Imaging, 2013, 8(2): 157-64. |
| [2] |
Cheng Y D, Khoury L, Zivin J A. Neuroprotection for ischemic stroke: two decades of success and failure[J]. NeuroRx, 2004, 1(1): 36-45. doi:10.1602/neurorx.1.1.36 |
| [3] |
Griffiths M R, Gasque P, Neal J W. The regulation of the CNS innate immune response is vital for the restoration of tissue homeostasis(repair) after acute brain injury: A brief review[J]. Int J Inflam, 2010, 2010(1): 1-18. |
| [4] |
Vinet J, Jong E K, Boddeke H W, et al. Expression of CXCL10 in cultured cortical neurons[J]. J Neurochem, 2010, 112(3): 703-14. doi:10.1111/j.1471-4159.2009.06495.x |
| [5] |
Weering H R, Jong A P, Haas A H, et al. CCL21-induced calcium transients and proliferation in primary mouse astrocytes: CXCR3-dependent and independent responses[J]. Brain Behav Immun, 2010, 24(5): 768-75. doi:10.1016/j.bbi.2009.04.007 |
| [6] |
Green A R. Why do neuroprotective drugs that are so promising in animals fail in the clinic? An industry perspective[J]. Clin Exp Pharmacol Physiol, 2002, 29(11): 1030-4. doi:10.1046/j.1440-1681.2002.03767.x |
| [7] |
Liu Q, Xiao S, Xia Y. TWEAK/Fn14 activation participates in skin inflammation[J]. Mediators Inflamm, 2017, 2017(1): 1-12. |
| [8] |
Wang X, Xiao S, Xia Y. Tumor necrosis factor receptor mediates fibroblast growth factor-inducible 14 signaling[J]. Cell Physiol Biochem, 2017, 43(2): 579-88. |
| [9] |
陈娴雯, 李煌, 陈立典, 等. HPLC法同时测定栝楼桂枝汤中6种成分的含量[J]. 福建中医药大学学报, 2014, 24(2): 31-4. Chen X W, Li H, Chen L D, et al. Simultaneous determination of six active ingredients in gualou guizhi decoction by HPLC[J]. Fujian J Tradit Chin Med, 2014, 24(2): 31-4. |
| [10] |
李小强, 周鸿飞. 基于经筋理论中风后肢体痉挛偏瘫治疗探析[J]. 辽宁中医药大学学报, 2018, 20(12): 1-3. Li X Q, Zhou H F. Treatment of spastic hemipleyia after stroke based on the meridian sinew theory[J]. J Liaoning Univ Tradit Chin Med, 2018, 20(12): 1-3. |
| [11] |
Hu H, Zhu X, Lin R, et al. Suppressive effects of Gua Lou Gui Zhi decoction on MCAO-induced NO and PGE2 production are dependent on the MAPK and NF-kappaB signaling pathways[J]. Mol Med Rep, 2016, 14(6): 5141-7. doi:10.3892/mmr.2016.5876 |
| [12] |
陈喆鸣, 南丽红, 谢晴晴, 等. 栝楼桂枝汤对脑缺血/再灌注模型大鼠皮质内质网应激相关因子表达的影响[J]. 福建中医药大学学报, 2018, 49(1): 53-5. Chen Z M, Nan L H, Huang M, et al. Regulation effect of Gualou Guizhi decoction on ERS-associated factors expression in cerebral ischemia-reperfusion rats[J]. Fujian J Tradit Chin Med, 2018, 49(1): 53-5. |
| [13] |
Chen J, Sanberg P R, Li Y, et al. Intravenous administration of human umbilical cord blood reduces behavioral deficits after stroke in rats[J]. Stroke, 2001, 32(11): 2682-8. doi:10.1161/hs1101.098367 |
| [14] |
黄鑫, 林昱, 杨泽霖, 等. 红景天苷抑制补体成分对脑缺血/再灌注大鼠的神经保护作用[J]. 中国药理学通报, 2019, 35(7): 967-72. Huang X, Lin Y, Yang Z L, et al. Neuroprotective effects of salidroside on complement composition in cerebral ischemia-reperfusion injury rats[J]. Chin Pharmacol Bull, 2019, 35(7): 967-72. doi:10.3969/j.issn.1001-1978.2019.07.016 |
| [15] |
Wang J. Preclinical and clinical research on inflammation after intracerebral hemorrhage[J]. Prog Neurobiol, 2010, 92(4): 463-77. doi:10.1016/j.pneurobio.2010.08.001 |
| [16] |
Zhao X, Li J, Sun H. CD200-CD200R interaction: An important regulator after stroke[J]. Front Neurosci, 2019, 13(6): 840-1. |
| [17] |
Biber K, Neumann H, Inoue K, et al. Neuronar "on" and "off" signals control microglia[J]. Trends Neurosci, 2007, 30(4): 596-602. |
| [18] |
Nikolopoulos D, Fanouriakis A, Boumpas DT. Update on the pathogenesis of central nervous system lupus[J]. Curr Opin Rheumatol, 2019, 31(6): 669-77. doi:10.1097/BOR.0000000000000655 |

