

肺癌是临床上最常见的恶性肿瘤之一,其中非小细胞肺癌(non-small cell lung cancer,NSCLC))占85%。NSCLC主要包括肺腺癌和鳞癌,其5年生存率大约为15%[1]。多西他赛属于微管解聚抑制剂,是NSCLC患者的标准二线化疗药物[2]。纤维蛋白原样蛋白1(fibrinogen-like protein 1,FGL1)是肝脏分泌的一种可促进细胞有丝分裂的特异生长因子,且在正常肝组织、肿瘤细胞和组织内呈过表达状态[3-4]。生理条件下,FGL1主要以自分泌的形式促进细胞有丝分裂增殖[5]。目前,有关FGL1与多西他赛等药物敏感性的研究较少。本研究旨在探讨FGL1在人肺腺癌细胞株PC-9中的表达情况及其对肺癌细胞多西他赛敏感性的影响,为提高多西他赛的临床疗效提供理论依据。
1 材料与方法 1.1 材料 1.1.1 细胞株人正常肺上皮细胞BEAS-2B及人肺腺癌PC9细胞均购自中国科学院上海细胞库。
1.1.2 药物与试剂多西他赛购于北京索莱宝有限公司(货号ID0400),胎牛血清购自Gibco(货号10270106),RPMI培养基购自Hylcone(货号SH30022.02),CCK-8试剂盒购自北京索莱宝科技公司(货号CA12110)、二喹啉甲酸(Bicinchoninicacid,BCA)试剂盒均购自Beyotime(货号P0010S); 实时荧光定量试剂盒TBGreen购自日本TaKaRa公司(货号RR820A), β-actin抗体购自Proteintech公司(货号60008-1-lg),FGL1抗体购自Abcam公司(货号ab197357), FGL1-siRNA重组序列、随机阴性对照序列由上海吉凯基因技术有限公司设计及合成。FGL1靶点序列GAPDH序列见Tab 1。
| Gene | Primer(5′-3′) |
| FGL1-siRNA1 | Upper reaches GCCGUUAUGCACAAUAUAATT |
| Lower reaches UUAUAUUGUGCAUAACGGCT | |
| FGL1-siRNA2 | Upper reaches GCAAACCUGAAUGGUGUAUTT |
| Lower reaches AUACACCAUUCAGGUUUGCTT | |
| Negative control | Upper reaches UUCUCCGAACGUGUCACGUTT |
| Lower reaches ACGUGAVAVGUUCGGAGAATT | |
| FGL1 | Upper reaches GCTGGTGGTTTAACAGGTGTC |
| Lower reaches AGAATACCACCACCCATGCC | |
| GAPDH | Upper reaches AGAAGACTGTGGATGG |
| Lower reaches AGCTCAGGGATGACCTTG |
超净工作台(苏州净化设备厂),恒温水浴箱(北京医疗设备厂),低温高速离心机(德国Heraeus公司),普通离心机(德国Heraeus公司400e型),电泳仪(美国Bio-rad公司),酶标仪(美国Bio-rad公司), 纯水器(美国Millipore公司)。
1.2 方法 1.2.1 细胞培养人正常肺上皮BEAS-2B细胞和人肺腺癌PC-9细胞分别在含有10%胎牛血清的DMEM培养基和RPIM培养基中,置于37 ℃、5% CO2饱和湿度条件下培养。细胞为贴壁生长,取对数生长期的细胞进行实验。
1.2.2 CCK-8法检测多西他赛对细胞的抑制率将实验分为空白对照组、阴性对照组及实验组。空白对照组只加培养液,阴性对照组加细胞悬液不加药,实验组细胞培养24 h后贴壁,加入不同浓度(0、5、10、20、40、80 μmol·L-1)多西他赛分别作用于人肺腺癌PC-9细胞24 h和48 h,制备单细胞悬液,以5×104个/mL的浓度,接种于96孔培养板中,每孔200 μL(边缘孔用无菌PBS填充);终止试验前4 h在每个孔内加入CCK-8(5 g·L-1);酶标仪上测定各孔OD值(A值)。抑制率/%=[1-(药物处理组A值-空白对照组A值)/(细胞对照组A值-空白对照组A值)]×100%。计算出半数抑制浓度(half inhibitory concentration,IC50)。
1.2.3 蛋白免疫印迹法(Western blot)检测FGL1蛋白表达细胞中加入适量的裂解液,裂解完全后离心,取上清,BCA法测定蛋白浓度,蛋白液与上样缓冲液充分混匀,100 ℃加热10 min,每泳道加入40 μg样品进行8% SDS-PAGE凝胶电泳,转膜、5%脱脂牛奶封闭1 h后,FGL1和GAPDH抗体均按照1 : 1 000稀释,4 ℃孵育一抗过夜。4 ℃取出膜,吐温PBS清洗,加入按照1 : 10 000稀释二抗(HRP标记的二抗),室温孵育90 min,洗膜,化学发光法在紫外凝胶成像仪上进行拍照分析。FGL1的相对表达量通过FGL1的灰度值除以GAPDH的灰度值计算。
1.2.4 逆转录聚合酶链式反应(RT-PCR)将处于对数生长期的人肺腺癌PC-9细胞消化后接种至6孔板中,使细胞密度能够达到80%~90%。收集细胞,使用TRIzol、氯仿和异丙醇等试剂提取总RNA,根据逆转录试剂盒说明进行逆转录,FGL1和内参GAPDH的引物序列见Tab 1。以cDNA为模板用实时荧光定量PCR仪进行扩增,反应总体积20 μL,PCR反应条件:95 ℃预变性5 min,之后95 ℃、10 s,60 ℃退火40 min,共40个循环,每孔设置3个复孔。采用由公式Folds=2-△△CT计算目的基因相对表达量。1.2.5细胞转染PC-9细胞在转染前1 d消化收集,制备细胞悬液,接种细胞至6孔板中,使转染细胞密度能够达到40%~60%,实验分为空白组(Control组),阴性对照组(FGL1siNC组),FGL1siRNA实验组。空白组不经任何处理,实验组转染FGL1siRNA。严格按照lipofectamineTM2000试剂盒说明书进行siRNA转染,用Opti-MEM(Invitrogen)转染试剂进行转染,于37 ℃、5% CO2转染6 h后每组加入完全培养基,转染48 h收集细胞。采用荧光倒置显微镜观察各组转染后细胞形态观察其形态学变化,判断转染效率,通过Western-blot法验证转染效果。
1.3 统计学分析采用SPSS 22.0统计软件对实验数据分析,所有计量资料以 ±s表示。采用单因素方差分析和t检验。
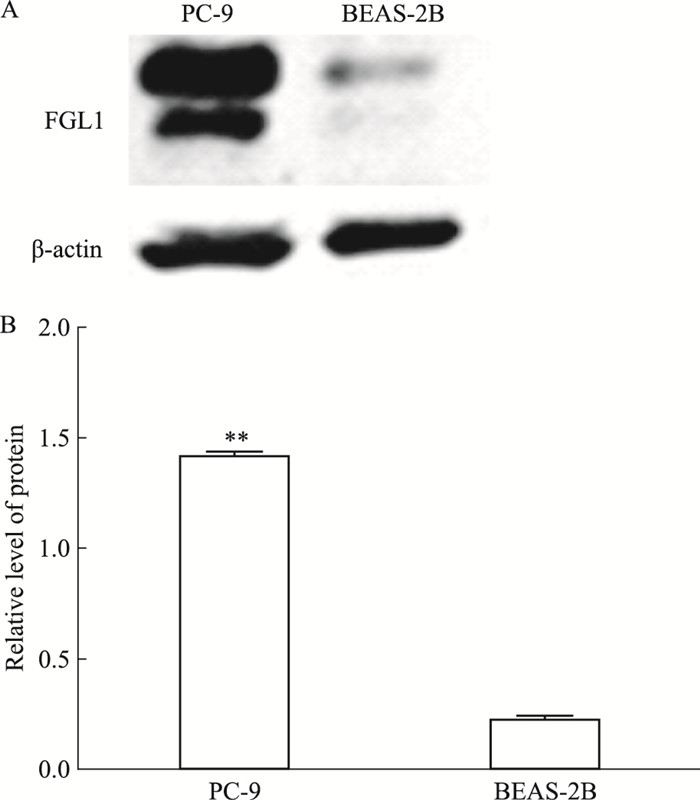
2 结果 2.1 BEAS-2B、PC-9细胞中FGL1的差异表达以人正常肺上皮BEAS-2B细胞作为对照,通过Western blot法检测FGL1蛋白在人肺腺癌PC-9细胞中的表达,见Fig 1。与BEAS-2B细胞中FGL1蛋白表达量相比,PC-9细胞FGL1相对表达量为(1.42±0.014),明显高于BEAS-2B细胞,差异具有显著性(P < 0.01)。
|
| Fig 1 Differential expression of FGL1 in BEAS-2B and PC-9 cells (x±s, n=3) A:Western blot assay was used to detect the expression difference of FGL1 protein in BEAS-2B cells and PC-9 cells; B: The relative level of FGL1 protein in BEAS-2B cells and PC-9 cells.**P < 0.01 vs BEAS-2B group |
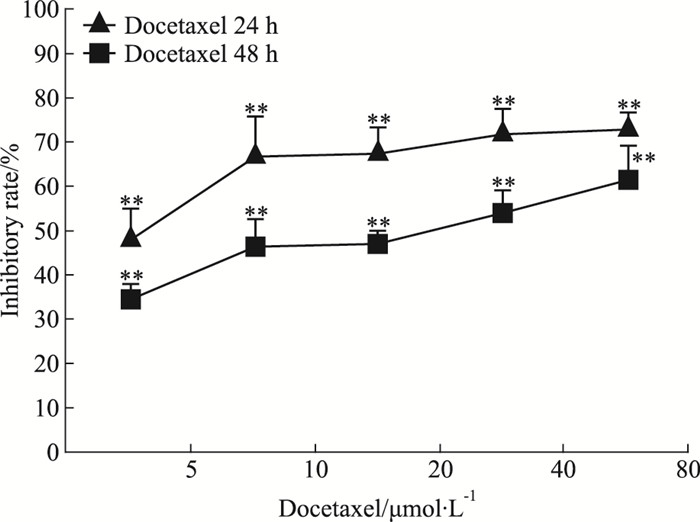
CCK-8试剂盒检测多西他赛对人肺腺癌PC-9细胞增殖抑制作用并计算IC50值,Fig 2结果发现,不同浓度多西他赛对PC-9细胞的增殖抑制作用呈现剂量依赖性。作用24 h时,药物的IC50值是29.48 μmol·L-1;而作用48 h时,药物的IC50值是5.88 μmol·L-1,提示多西他赛对PC-9细胞的增殖抑制作用可能有一定的时间依赖性。且与阴性对照组相比,差异具有显著性(P < 0.01)。
|
| Fig 2 The inhibitory effect of docetaxel at different concentrations on PC-9 cells proliferation after 24 hours and 48 hours (x±s, n=6) **P < 0.01 vs control group |
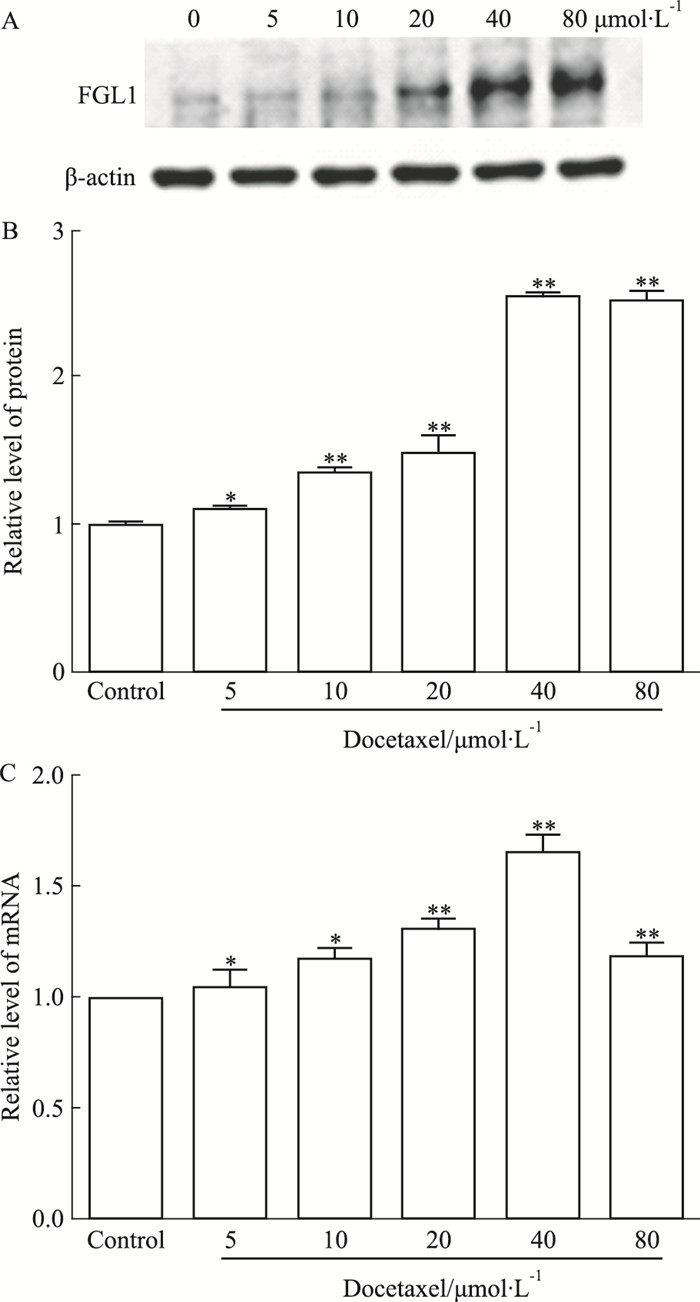
不同浓度多西他赛作用于人肺腺癌PC-9细胞24 h后,以Western blot法检测FGL1蛋白的表达情况,Fig 3A、3B发现,随着多西他赛浓度的增加,PC-9细胞中FGL1蛋白的表达水平明显上调,且各个浓度组与对照组相比,差异均具有显著性。进一步采用RT-PCR检测FGL1 mRNA的表达情况(Fig 3C)。当多西他赛浓度为5 μmol·L-1时,FGL1 mRNA相对表达量为(1.08±0.023)(P < 0.05);当多西他赛浓度为40 μmol·L-1时, FGL1 mRNA相对表达量为(1.62±0.013)(P < 0.01),与对照组相比差异均具有显著性。
|
| Fig 3 Effect of docetaxel on FGL1 expression in human lung adenocarcinoma PC-9 cells (x±s, n=3) A: The effect of docetaxel on FGL1 expression in human lung adenocarcinoma PC-9 cells by Western blot; B: The relative expression level of FGL1 protein in human lung adenocarcinoma cells PC-9 after 24 hours of docetaxel treatment; C: RT-PCR was used to detect the expression level of FGL1 mRNA in human lung adenocarcinoma PC-9 cells after docetaxel treatment.*P < 0.05, **P < 0.01 vs control group |
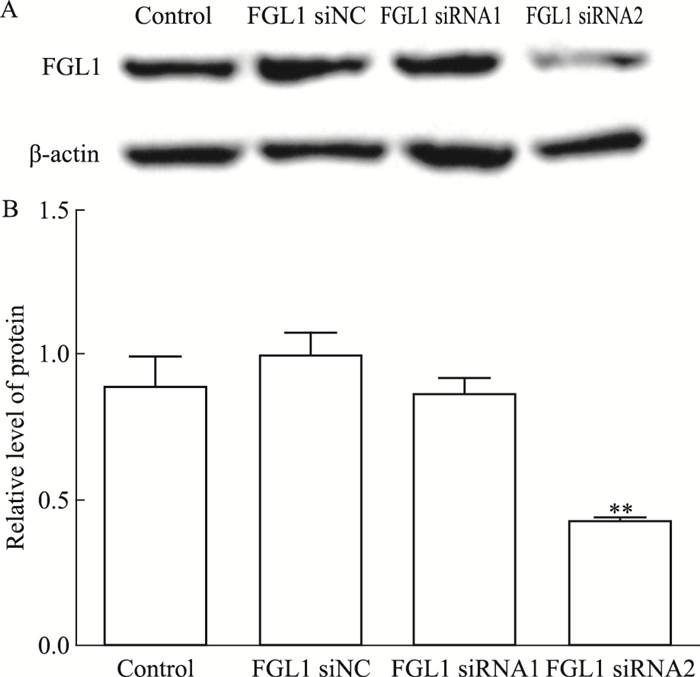
转染FGL1 siRNA 48 h后,用Western blot法检测人肺腺癌PC-9细胞中FGL1蛋白表达,见Fig 4。转染组siRNA1的FGL1相对表达量与阴性对照组相比降至(0.865±0.045)倍,差异无显著性(P>0.05);转染组siRNA2中FGL1相对表达量与阴性对照组相比降至(0.427±0.0025)倍,差异具有显著性(P < 0.01)。选取转染效果较好的FGL1siRNA-2序列用于后续实验。
|
| Fig 4 Effect of FGL1 siRNA transfection on expression of FGL1 protein in human lung adenocarcinoma PC-9 cell line (x±s, n=3) A:The transfection efficiency of FGL1 siRNA was observed with Western blot analysis in PC-9 cell line; B: The relative expression level of FGL1 protein after transfection in PC-9 cell line.**P < 0.01 vs FGL1 siNC group |
不同浓度(0、5、10、20、40、80 μmol·L-1)多西他赛作用于人肺腺癌PC-9细胞24 h后,用CCK-8试剂盒检测多西他赛对人肺腺癌PC-9细胞的增殖抑制作用,见Fig 5。FGL1 siRNA组药物IC50值为2.91 μmol·L-1, 与对照组相比差异具有显著性(P < 0.01)。而FGL1siNC组细胞IC50值为29.48 μmol·L-1,与对照组相比差异也具有显著性(P < 0.01),表明FGL1 siRNA可增加多西他赛药物的敏感性。

|
| Fig 5 Effect of FGL1 silencing on sensitivity of PC-9 cells to docetaxel (x±s, n=6) **P < 0.01 vs control group |
恶性肿瘤已经成为严重威胁中国人群健康的主要公共卫生问题之一,其中肺癌位居我国恶性肿瘤发病首位[6-7]。NSCLC的二线化疗标准方案包括多西他赛,其作用机理是加强微管蛋白聚合、抑制微管解聚作用,阻滞细胞于G2与M期,从而破坏肿瘤细胞的有丝分裂与增殖。多西他赛不仅可导致细胞分裂异常、纺锤体结构的损伤而引起细胞死亡[8-9],还可以在内皮细胞内解除对肌动蛋白调节[10],具有间接抑制血管新生功能。同时其还具有免疫调节能力,如增强肿瘤相关抗原的释放,增加细胞的抗原呈递和提高肿瘤细胞的免疫原性[11]。但由于目前多西他赛对NSCLC疗效尚不甚满意,因此寻找新的干预手段以提高肺癌细胞对其敏感性,可能是一种治疗肺癌的新策略和研究重点。
纤维蛋白原样蛋白1(FGL1),也称Hepassocin或肝细胞源性纤维蛋白原相关蛋白(HFREP-1),是Yamamoto等[12]于1993年通过差减杂交的方法在肝癌中筛选的一种过表达基因,属于纤维蛋白原家族,与羧基末端纤维蛋白β和γ亚基具有高氨基酸同源性,但它没有纤维蛋白凝块形成所必须的特征性血小板、交联区域和凝血酶敏感结合位点。目前研究发现,FGL1 mRNA在肺腺癌、前列腺癌和恶性黑色素瘤等多种肿瘤组织中表达均上调。此外,研究发现在小鼠肿瘤模型中体内沉默FGL1基因可促进T细胞的免疫而使肿瘤缩小,且通过基因芯片技术检测到人肺腺癌组织中FGL1呈过表达状态。推测FGL1是淋巴细胞活化基因3(lymphocyte-activation gene-3, LAG-3)的主要免疫抑制配体,FGL1可以通过LAG-3在体内外抑制抗原介导的T细胞应答,造成肿瘤免疫逃逸现象。此外有研究已证实FGL1在胃癌细胞和组织中高表达,且对胃癌的侵袭、迁移和增殖起促进作用[13]。Nayeb-Hashemi等[14]在肝癌研究中发现,FGL1是肝肿瘤细胞抑制因子,其丢失与分化程度低等相关[14]。但FGL1表达与化疗药物敏感性间的关系尚未见报道。本研究发现与正常肺上皮BEAS-2B细胞相比,FGL1在人肺腺癌PC-9细胞中呈高表达,通过转染FGL1siRNA沉默FGL1表达可增加不同浓度多西他赛对人肺腺癌PC-9细胞的增殖抑制作用,且与对照组相比统计学有显著性差异(P < 0.01),表明抑制人肺腺癌PC-9细胞中FGL1的表达有可能成为提高多西他赛药物敏感性的有效策略。
综上所述,FGL1在人肺腺癌PC-9细胞中呈高表达,沉默FGL1表达可增强人肺腺癌细胞PC-9对多西他赛的敏感性,抑制肿瘤细胞增殖。但FGL1对肺癌细胞凋亡、侵袭和迁移有何影响及可能的信号转导机制仍需要进一步研究。
| [1] |
Petrek H, Yu A M. MicroRNAs in non-small cell lung cancer: Gene regulation, impact on cancer cellular processes, and therapeutic potential[J]. Pharmacol Res Perspect, 2019, 7(6): 525-7. |
| [2] |
吴克伟, 杨芬, 刘俊玲, 等. Hirsutanols A通过增加活性氧选择性诱导多西他赛耐药人肺腺癌细胞PC14/TXT凋亡[J]. 中国药理学通报, 2010, 26(8): 1005-10. Wu K W, Yang F, Liu J L, et al. Hirsutanols A selectively induced apoptosisin docetaxel resistant NSCLC cells through increasing ROS production[J]. Chin Pharmacol Bull, 2010, 26(8): 1005-10. |
| [3] |
Wang J, Sanmamed M F, Datar I, et al. Fibrinogen-like Protein 1 is a major immune inhibitory ligand of LAG-3[J]. Cell, 2019, 176(1-2): 334-7. |
| [4] |
Kim M S, Pinto S M, Getnet D, et al. A draft map of the human proteome[J]. Nature, 2014, 509(7502): 575-81. |
| [5] |
Cao M M, Xu W X, Li C Y, et al. Hepassocin regulates cell proliferation of the human hepatic cells LO2 and hepatocarcioma cells through different mechanisms[J]. J Cell Biochem, 2011, 112(10): 2882-90. |
| [6] |
郑荣寿, 郑可欣, 张思维, 等. 2015年中国恶性肿瘤流行情况分析[J]. 中华肿瘤杂志, 2019, 41(1): 19-28. Zheng R S, Zheng K X, Zhang S W, et al. Report of cancer epidemiology in China, 2015[J]. Chin J Oncol, 2019, 41(1): 19-28. |
| [7] |
高雅茹, 王玮, 袁夏, 等. 地塞米松降低紫杉醇对肺癌细胞化疗作用的实验研究[J]. 中国药理学通报, 2019, 35(3): 382-7. Gao Y R, Wang W, Yuan X, et al. The experimertal research of dexamethasomereducing paclitaxel chemotherapy on lung cancer cells[J]. Chin Pharmacol Bull, 2019, 35(3): 382-7. |
| [8] |
Arnst K E, Wang Y, Hwang D J, et al. A potent, metabolically stable tubulin inhibitor targets the colchicine binding site and overcomes taxane resistance[J]. Cancer Res, 2018, 78(1): 265-77. |
| [9] |
Kanthou C, Tozer G M. The tumor vascular targeting agent combretastatin A-4-phosphate induces reorganization of the actin cytoskeleton and early membrane blebbing in human endothelial cells[J]. Blood, 2002, 99(6): 2060-9. |
| [10] |
André N, Carré M, Pasquier E. Metronomics: towards personalized chemotherapy[J]?Nat Rev Clin Oncol, 2014, 11 (7): 413-31.
|
| [11] |
Andrews P, He Y J, Xiong Y. Cytoplasmic localized ubiquitin ligase cullin 7 binds to p53 and promotes cell growth by antagonizing p53 function[J]. Oncogene, 2006, 25(33): 4534-48. |
| [12] |
Yamamoto T, Gotoh M, Sasaki H, et al. Molecular cloning and initial characterization of a novel fibrinogenrelated gene, HFREP1[J]. Biochem Biophys Res Commun, 1993, 193(2): 681-7. |
| [13] |
Zhang Y, Qiao H X, Zhou Y T, et al. Fibrinogen-like-protein 1promotes the invasion and metastasis of gastric cancer and is associated with poor prognosis[J]. Mol Med Rep, 2018, 18(2): 1465-72. |
| [14] |
Nayeb-Hashemi H, Desai A, Demchev V, et al. Targeted disruption of fibrinogen like protein1 accelerates hepatocellular carcinoma development[J]. Biochem Biophys Res Commun, 2015, 465(2): 167-73. |

