

2. 新疆维吾尔自治区维吾尔医药研究所, 新疆维吾尔医方剂学重点实验室, 新疆 乌鲁木齐 830011
2. Xinjiang Institute of Traditional Uighur Medicine, Xinjiang Lab of Uighur Medical Prescription, Urmuqi 830011, China
阿尔茨海默病(alzheimer′s disease,AD)在临床主要表现为渐进性认知衰退及痴呆,其病理特点是淀粉样斑块和神经纤维缠结,神经元细胞丢失,胶质细胞的显著激活,以及全身免疫反应。AD全身免疫反应的改变包括淋巴细胞和巨噬细胞分布和激活的变化、自身抗体的存在或异常细胞因子的产生[1]。病理学、遗传学和流行病学研究均支持免疫机制参与AD发病机制的观点[2]。另外,先天免疫细胞,特别是小胶质细胞和星形胶质细胞介导AD神经炎症的能力,也被认为是疾病发病的重要因素[3-4]。
类叶升麻苷(acteoside,AE)是苯乙醇苷类中一种天然活性成分,具有抗氧化损伤、神经保护、肝脏保护、免疫调节等多种作用。前期研究显示,类叶升麻苷有改善AD小鼠老化和抑制免疫器官萎缩的作用[5-6],但其对于免疫功能方面的作用机制仍不清楚。本实验旨在深入研究类叶升麻苷对小鼠老化及免疫细胞和免疫炎症因子的影响,探讨其对老龄小鼠免疫功能的影响。
1 材料及方法 1.1 药物与试剂类叶升麻苷(为新疆维吾尔自治区维吾尔医药研究所自制,纯度≥98%,20170827), 盐酸美金刚片(丹麦灵北药厂,694478),75%消毒酒精(新疆爱迪尔生物科技有限公司,20171225),0.9%氯化钠注射液(四川科伦药业股份有限公司,L217010304), FITC偶联小鼠CD4抗体、APC偶联抗小鼠的抗原CD3e抗体、PE-CY7偶联小鼠CD8抗体、Mouse Th1/Th2/Th17 CBA Kit(BD BIOSCIENCES PHARMINGEN,7276920、7150784、7215735、7076519)
1.2 实验仪器SQP电子天平(赛多利斯科学仪器有限公司,北京),恒温生化培养箱(博讯实业有限公司医疗设备厂,上海),LDZM-80KCS-Ⅱ型立式压力蒸汽灭菌锅(申安医疗器械厂,上海),Allegra 64R离心机(Beckman),FC500流式细胞仪(Beckman),4 ℃冰箱(海尔股份有限公司,青岛),-20 ℃冰箱(海尔股份有限公司,青岛),-80 ℃冰箱(Thermo)。
1.3 实验动物实验鼠使用健康SAMP8小鼠,以同月龄SAMR1小鼠为对照,♂,体质量(20±2)g。购于天津中医药大学第一附属医院(合格证号SCXK(津)2015-0003)。饲养于新疆维吾尔自治区维吾尔医药研究所SPF级动物房(动物使用许可证号2018-0001),温度(21~25) ℃,湿度24%~52%,12 h明暗交替饲养,自由摄食饮水。
1.4 分组及给药根据体质量及老化评分结果筛选出12只对照SAMR1小鼠和60只符合要求的SAMP8鼠,SAMP8随机分为5组,每组12只,每天灌胃给药1次,连续90 d,给药剂量如下:(1)正常对照组:(SAMR1小鼠),0.1 mL·10 g-1· d-1生理盐水灌胃。(2)模型组:0.1 mL·10 g-1· d-1生理盐水灌胃。(3)美金刚组:10 mg·kg-1· d-1灌胃。(4)类叶升麻苷-低:30mg·kg-1· d-1灌胃。(5)类叶升麻苷-中:60 mg·kg-1· d-1灌胃。(6)类叶升麻苷-高:120 mg·kg-1· d-1灌胃。
1.5 老化评分本研究评定SAM-P和SAM-R小鼠的衰老等级方法,参照日本京都大学著名的竹田俊男和细川昌则教授制定的小鼠老化度评分标准[7],根据老鼠的行为和外观,观察了11种评分项的发生情况,包括:反应性、被动性逃避反应、皮肤光泽、皮肤粗糙度、皮肤溃疡、眼部损伤、角膜溃疡,浑浊、白内障和脊柱后凸等。每项指标划分成3~5级,根据统一的评分标准评分,老化度越高体现在获得的积分更多。
1.6 免疫细胞检测在3 μL CD3、CD4和CD8中分别加入抗凝全血100 μL,充分震荡混匀,于室温避光反应15 min。取裂红素2 mL加入并混匀后,再次避光反应15 min。反应后离心5 min,转速1 000 r·min-1,弃上清。1 mL PBS,1 000 r·min-1离心5 min。200 μL PBS重悬,200目过滤。经流式细胞仪检测,Kaluza Analysis分析处理。
1.7 免疫因子检测标准品制备:取2 mL Assay Diluent稀释标准品,在避免剧烈涡旋下保证混匀,混匀后静置15 min,再用Assay Diluent倍比稀释最高浓度标准品,取每种捕获微球悬液混合,取标准品或样品每管50 μL,再依次加入50 μL捕获微球混合液及50 μL PE检测抗体孵育,孵育后以1 mL洗涤缓冲液洗涤、离心,弃上清。为重悬微球每管加入300 μL洗涤缓冲液, 并过200目筛。上机获取样品,使用FCAP软件导出和分析FCS数据文件。
1.8 统计学方法采用SPSS17.0统计学软件对实验结果进行统计学处理,数据结果用x±s表示,组间比较使用单因素方差分析和t检验。
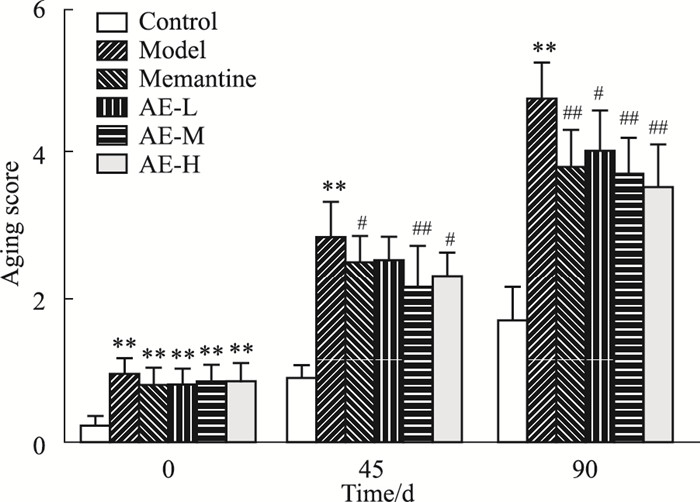
2 结果 2.1 类叶升麻苷对老化评分的影响本实验中老化评分分别于给药前,给药后45 d、90 d进行。给药前,与对照组相比,SAMP8小鼠老化评分显著增高;给药45 d,与对照组相比,模型组老化评分显著增高,与模型组比,美金刚组及类叶升麻苷中、高剂量组小鼠老化评分显著降低;给药90 d,与对照组比,模型组老化评分高于正常组,且有显著性差异,与模型组相比,美金刚组及类叶升麻苷低、中、高剂量组小鼠老化评分存在显著降低趋势(见Fig 1)。
|
| Fig 1 Effect of AE on aging score of SAMP8 mice (x±s, n=12) **P < 0.01 vs control group; #P < 0.05, ##P < 0.01 vs model group |
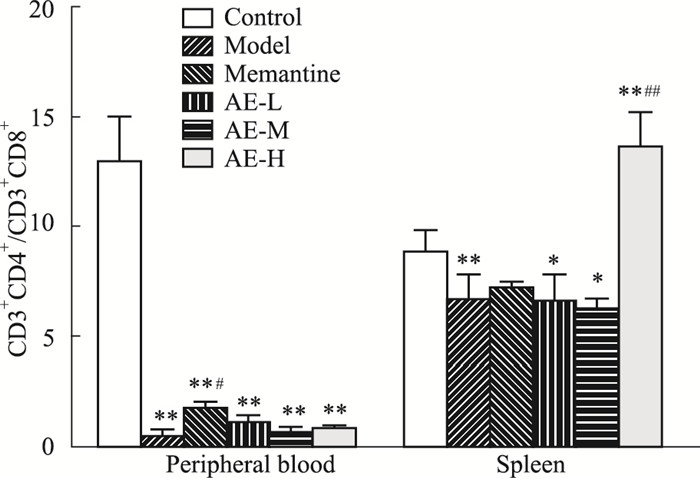
如Fig 2如示,与正常组相比,模型组SAMP8小鼠血浆中CD4+/CD8+显著低于正常组R1鼠,各给药组血浆中CD4+/CD8+均低于正常组,与模型组相比,美金刚组血浆中CD4+/CD8+显著增高;与正常组相比,模型组SAMP8小鼠脾脏中CD4+/CD8+显著低于正常组R1鼠,类叶升麻苷低、中剂量组小鼠脾脏中CD4+/CD8+也显著低于正常组,类叶升麻苷高剂量组则显著高于正常组及模型组。
|
| Fig 2 Effect of AE on T cell subsets in peripheral blood and spleen of SAMP8 model mice (x±s, n=12) *P < 0.05, **P < 0.01 vs control group; #P < 0.05, ##P < 0.01 vs model group |
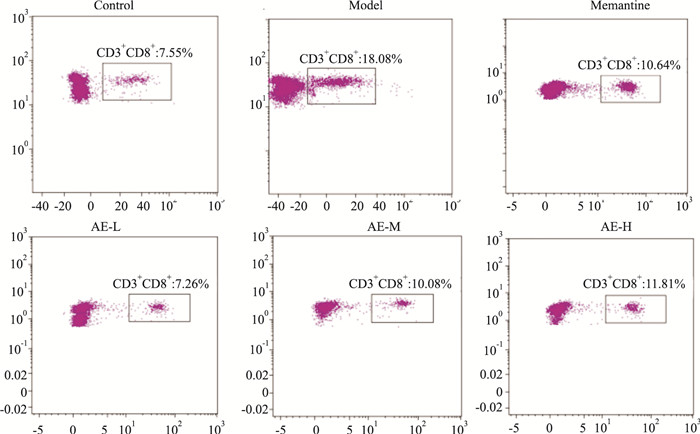
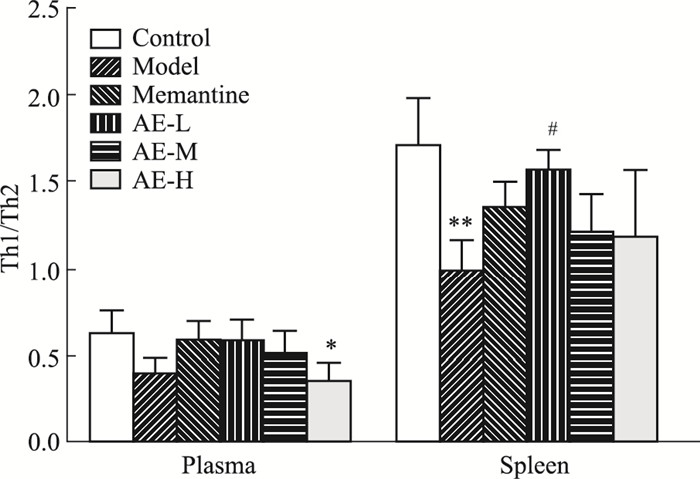
流式细胞仪检测各组小鼠血浆及脾脏中Th1型IFN-γ及Th2型IL-4免疫因子表达差异,结果显示:与正常组相比,模型组小鼠血浆及脾脏中IFN-γ的表达水平均显著性降低;与模型组相比,类叶升麻苷低、高剂量组小鼠脾脏中IFN-γ的表达水平变化明显,低剂量升高而高剂量降低。模型组小鼠血浆中IFN-γ、IL-4均显著性降低,与模型组相比,类叶升麻苷低、高剂量组小鼠血浆中IL-4降低,有显著性差异,类叶升麻苷高剂量组小鼠脾脏IFN-γ、IL-4降低,表现出显著性差异;与正常组相比,模型组小鼠脾脏Th1/Th2的偏移显著性降低,与模型组相比,类叶升麻苷低剂量组在脾脏中Th1/Th2升高,表现出显著性差异。见Fig 3, 4。

|
| Fig 3 Representative flow cytometry of CD3+ CD4+ T cell expression in peripheral blood of each group (x±s, n=12) *P < 0.05, **P < 0.01 vs control group; #P < 0.05, ##P < 0.01 vs model group |
|
| Fig 4 Representative flow cytometry of CD3+ CD4+ T cell expression in spleen of each group (x±s, n=12) *P < 0.05, **P < 0.01 vs control group; #P < 0.05, ##P < 0.01 vs model group |
|
| Fig 5 Effect of AE on Th1/Th2 change of plasma and spleen (x±s, n=12) *P < 0.05, **P < 0.01 vs control group; #P < 0.05, ##P < 0.01 vs model group |
| Group | Plasma | Spleen | |||
| IFN-γ/ ng·L-1(Th1) |
IL-4/ ng·L-1(Th2) |
IFN-γ/ ng·L-1(Th1) |
IL-4/ ng·L-1(Th2) |
||
| Control | 2.68±0.43 | 4.27±0.64 | 8.22±1.72 | 4.81±0.66 | |
| Model | 1.02±0.27** | 2.59±0.54** | 4.63±1.05** | 4.62±0.88 | |
| Memantine | 1.29±0.33** | 2.19±0.85** | 5.97±0.69** | 4.43±0.71 | |
| AE-L | 1.13±0.67** | 1.90±0.25**# | 6.89±1.60## | 4.37±1.18 | |
| AE-M | 1.35±0.60** | 2.59±0.53** | 4.78±1.95** | 3.91±0.66* | |
| AE-H | 0.61±0.37** | 1.73±0.31**## | 2.88±0.57**# | 2.40±0.82**## | |
| *P < 0.05, **P < 0.01 vs control; #P < 0.05, ##P < 0.01 vs model | |||||
免疫功能在阿尔茨海默病发病机制中的作用日益受到重视。除中枢免疫反应外,外周免疫反应还包括淋巴细胞功能与亚群分布的变化[10]。人体存在T细胞、B细胞两种免疫细胞。其中细胞免疫由T细胞负责。CD4+是辅助T细胞的一种标记。CD8+则是抑制性T细胞的一种标记。CD4+/CD8+的比值的正常,能保证机体维持正常的免疫功能状态,该值降低是机体免疫功能下降的重要标志[8-9]。
实验结果显示,SAMP8模型鼠较R1鼠CD4+/CD8+显著降低,SAMP8模型鼠是散发性阿尔茨海默病的经典动物模型[7],有研究表明,SAMP8小鼠神经内分泌免疫调节失衡[11]。说明了SAMP8鼠免疫活性普遍下降。这为研究类叶升麻苷对SAMP8小鼠机体免疫功能的影响提供了有力背景。AE高剂量组能显著提升脾脏中CD4+/CD8+的比值。提示阳性药物美金刚则相较模型组各数值均有显著的良性变化,类叶升麻苷能够促进SAMP8小鼠体内辅助性淋巴细胞的增加,有效抑制杀伤性淋巴细胞的增多,从而改善机体的免疫功能,以达到阿尔兹海默病的控制与治疗作用。
此外,已有大量文献证明细胞因子在AD的促炎和抗炎过程以及复杂的认知过程中起着关键作用[12]。机体维持正常的内环境有赖于细胞因子的动态平衡状态,其状态平衡又有赖于Th1、Th2型细胞特征因子间的相互作用和抑制,若Th1型和Th2型细胞因子失衡,机体就会处于失衡的漂移状态。Th1/Th2型偏移中Th2型细胞因子分泌较多,提示了机体免疫功能的下降,细胞因子的这种不平衡状态与认知能力下降和痴呆症有关。在本实验研究中,细胞因子的分泌是SAMP8小鼠认知障碍的潜在机制之一,许多研究报告称,衰老导致Th1和Th2细胞数量变化,Th1/Th2值失去稳态平衡[13-14],IFN-γ和IL-4作为Th1、Th2的特征细胞因子,二者之间相互拮抗又相互促进。
由实验结果可见,与正常组相比,在血浆及脾脏中,各组的IFN-γ及IL-4都呈明显降低趋势,且模型组中Th1/Th2显著偏移,提示模型鼠免疫功能的显著下降,与美金刚组药物相比,二者在延缓衰老的进程中没有明显差异,但在Th1/Th2的调节及脾脏中免疫细胞的分布上,类叶升麻苷表现出明显优势,AE低、中剂量组能够上调免疫应答模式恢复Th2/Th1的平衡稳态,使细胞免疫功能增强,达到延缓动物机体衰老的作用。提示类叶升麻苷的作用机制可能与免疫平衡相关。同时,类叶升麻苷恢复细胞因子动态平衡稳态作用以脾脏表现更为显著,这与本实验中类叶升麻苷调节免疫细胞的分布以及对模型小鼠老化程度的改善作用均一致,进一步表明了类叶升麻苷能够延缓快速老化小鼠老化进程,可能的作用机制是通过调节机体内免疫细胞及免疫因子的动态平衡、改善机体的免疫功能。这为后续的实验研究提供了一定依据,类叶升麻苷明确的作用机制有待于进一步的深入研究。
| [1] |
Pamplona F A, Pandolfo P, Duarte F S, et al. Altered ecnotiondity leads to increased pain tolerance in amyloid β(Aβ1-40)peptide-treated mice[J]. Behav Brain Res, 2010, 212(1): 96-102. doi:10.1016/j.bbr.2010.03.052 |
| [2] |
Morley J E, Farr S A, Kumar V B, et al. The SAMP8 mouse: amodel to develop therapeutic interventions for Alzheimer' s disease[J]. Curr Pharm Des, 2012, 18(8): 1123-30. doi:10.2174/138161212799315795 |
| [3] |
Pellicanò M, Larbi A, Goldeck D, et al. Immune profiling of Alzheimer patients[J]. J Neuroimmunol, 242 (1-2): 52-9
|
| [4] |
Eikelenboom P, Hoogendijk W J G, Jonker C, et al. Immunological mechanisms and the spectrum of psychiatric syndromes in Alzheimer's disease[J]. J Psychiatr Res, 2002, 36(5): 269-80. |
| [5] |
罗嘉楠, 马丁丁, 黄晏, 等. 类叶升麻苷对APP/PS1双转基因小鼠行为学和抗氧化能力的影响[J]. 中药药理与临床, 2016, 32(6): 56-60. Luo J N, Ma D D, Huang Y, et al. Effect of acteoside on behaviors and its anti-oxygenation in APP/PS1 mice[J]. Pharmacol Clin Chin Mater Med, 2016, 32(6): 56-60. |
| [6] |
高莉, 彭晓明, 霍仕霞, 等. 毛蕊花糖苷改善D-半乳糖致亚急性衰老小鼠脑损伤的作用[J]. 中草药, 2014, 45(1): 81-5. Gao L, Peng X M, Huo S X, et al. Improvement of acteoside on cerebral injury in subacute aging mice induced by D-galactose[J]. Chin Tradit Herbal Drugs, 2014, 45(1): 81-5. |
| [7] |
Hosokawa M, Kasai R, Higuchi K, et al. Grading score system: amethod for evaluation of the degree of senescence in Senescence Accelerated Mouse(SAM)[J]. Mech Ageing Dev, 1984, 26(1): 91-102. doi:10.1016/0047-6374(84)90168-4 |
| [8] |
Pellican M, Bulati M, Buffa S, et al. Systemic immune responses in Alzheimer's disease: in vitro mononuclear cell activation and cytokine production[J]. J Alzheimers Dis, 2010, 21(1): 181-92. |
| [9] |
Zhou F, Chen Y, Mok K Y, et al. Identification of genetic risk factors in the Chinese population implicates a role of immune system in Alzheimer's disease pathogenesis[J]. Proc Natl Acad Sci USA, 2018, 115(8): 1697-706. doi:10.1073/pnas.1715554115 |
| [10] |
Richartz-S E Batra A, Stransky E, et al. Altered lymphocyte distribution in Alzheimer's disease[J]. J Psychiatr Res, 2007, 41(1-2): 174-8. doi:10.1016/j.jpsychires.2006.01.010 |
| [11] |
Wang J H, Cheng X R, Zhang X R, et al. Neuroendocrine immunomodulation network dysfunction in SAMP8 mice and PrP-hAβPPswe/PS1ΔE9 mice: potential mechanism underlying cognitive impairment[J]. Oncotarget, 2014, 17(7): 22988-3005. |
| [12] |
Mcafoose J, Baune B T. Evidence for a cytokine model of cognitive function[J]. Neurosci Biobehav R, 2008, 33(3): 355-66. |
| [13] |
Huang J, Li Z, Yao X, et al. Altered Th1/Th2 commitment contributes to lung senescence in CXCR3-deficient mice[J]. Exp Gerontol, 2013, 48(8): 717-26. doi:10.1016/j.exger.2013.04.001 |
| [14] |
Watson R R, Zibadi S, Vazquez R, et al. Nutritional regulation of immunosenescence for heart health[J]. J Nutr Biochem, 2005, 16(2): 85-7. doi:10.1016/j.jnutbio.2004.10.001 |
| [15] |
谌勤, 罗洪斌, 谢文执. 板桥党参通过PP2A信号通路改善AD模型大鼠认知功能障碍[J]. 中国药理学通报, 2019, 35(9): 1232-9. Chen Q, Luo H B, Xie W Z. Banqiao Codonopisis Pilosula improves cognitive dysfunction in AD model rats by PP2 A signaling pathway[J]. Chin Pharmacol Bull, 2019, 35(9): 1232-9. doi:10.3969/j.issn.1001-1978.2019.09.010 |

