


2. 福建中医药大学药学院, 福建 福州 350122
洪桂祝(1966-),女,博士,教授,研究方向:心脑血管药理学,通讯作者, E-mail:13559102126@163.com
 ,
HUANG Xin2,
TANG Yu-heng2,
LIU Jun-jie2,
SUN Chun-xiao2,
XU A-juan2,
LAI Wen-fang2
,
HUANG Xin2,
TANG Yu-heng2,
LIU Jun-jie2,
SUN Chun-xiao2,
XU A-juan2,
LAI Wen-fang2
 ,
HONG Gui-zhu2
,
HONG Gui-zhu2

2. College of Pharmacy, Fujian University of Tranditional Chinese Medicine, Fuzhou 350122, China
脑卒中是严重威胁人类健康的常见病,同冠心病、癌症并列为威胁人类健康的三大疾病之一,其中缺血性脑卒中约占87%,严重威胁着卒中患者的生命健康和生活质量[1]。红景天(Rhodiold rosea L.)属于蔷薇目景天科,是中国传统医药学中的重要草药,具有改善心血管功能,保护肝脏,抗衰老,以及神经保护等多种药理作用[2]。红景天苷(salidroside,Sal)是从红景天中提取出来的苯乙醇类化合物,是红景天主要有效成分。课题组前期研究发现,红景天苷能够降低脑梗死体积,改善神经功能损伤,降低C3补体成分,促进Egrs家族蛋白表达,调控Bcl-xl/Bax蛋白,减少神经凋亡[3-7]。而糖原合成酶激酶3β(glycogen synthase kinase-3β,GSK-3β)是一种在进化上非常保守的丝氨酸/苏氨酸激酶,能作用于众多信号蛋白结构蛋白和转录因子,调节细胞的分化、增殖、存活和凋亡,目前越来越多的研究者选择其作为癌症、神经退行性疾病,神经精神类疾病等多种重大疾病的治疗靶点[8-9]。本研究以GSK-3β为治疗靶点,进一步探讨红景天苷脑保护的作用机制。
1 实验材料 1.1 实验动物SPF级健康♂SD大鼠86只,体质量(260~280) g,购于上海斯莱克实验动物有限公司,合格证号:2015000510392,许可证号:SCXK(沪)2017-0005,由福建中医药大学实验动物中心饲养,许可证号:SYXK(闽)2014-0005。
1.2 药品与试剂红景天苷(福建中医药大学,纯度≥98%,批号:20160928);线栓(广州佳灵技术有限公司);RIPA(碧云天生物技术有限公司),PMSF(碧云天生物技术有限公司),BCA蛋白浓度测定试剂盒,均来自碧云天生物技术有限公司。蛋白上样缓冲液(生工生物工程上海有限公司);鼠抗β-actin(北京全式金公司);caspase-9,cleaved caspase-9,GSK-3β,NMDAR1,GluR2(Cell Signaling Technology公司),pGSK-3β(Santa Cruz Biotechnology公司)。
1.3 仪器Infinite M20 Pro多功能酶标仪(瑞士TECAN公司),小型垂直电泳槽,小型转印槽(Bio-Rad),基础电泳仪电源(Bio-Rad),凝胶成像分析系统(Bio-Rad, 型号:ChemiDocXRS+),高速台式冷冻离心机(Thermo Fisher,型号:PrimoR)。
1.4 药品配制红景天苷注射液:称取红景天苷粉末1.5 g溶入0.2 L 0.9%生理盐水中,充分溶解至澄清,4 ℃保存待用。
2 方法 2.1 动物分组和给药第一批:SD大鼠造模成功后随机分为假手术组(Sham)12只、模型组(MCAO)12只、红景天苷给药组(MCAO+Sal)12只。造模2 h,再灌注1 h后,MCAO+Sal组腹腔注射红景天苷(50 mg·kg-1·d-1),其余组注射0.9%生理盐水(10 mL·kg-1·d-1),给药1 d后取材。
第二批:SD大鼠随机分为6组,即人工脑脊液+Sham组(Sham)、GSK-3β抑制剂+Sham组(SB216763+Sham)、人工脑脊液+MCAO组(MCAO)、GSK-3β抑制剂+MCAO组(SB216763+MCAO),人工脑脊液+MCAO+Sal组(MCAO+Sal),GSK-3β抑制剂+MCAO+Sal组(SB216763+MCAO+Sal),每组各10只。经侧脑室注射GSK-3β抑制剂SB216763或人工脑脊液30分钟后,除假手术组外,其余组进行MCAO造模,造模后MCAO+Sal和SB216763+MCAO+Sal组腹腔注射红景天苷(50 mg·kg-1·d-1),其余组注射0.9%生理盐水(10 mL·kg-1·d-1),给药1 d后取材。
2.2 MCAO模型制作大鼠经2%戊巴比妥钠(2 mL·kg-1)腹腔注射麻醉后,仰卧位固定,除去颈部的毛并用碘伏擦拭颈部皮肤消毒后,剪开颈部皮肤,钝性分离皮下组织,分离左侧颈总动脉(CCA),颈外动脉(ECA)、颈内动脉(ICA),结扎CCA、ECA。动脉夹夹闭ICA,使用眼科剪呈45°在CCA近心端血管壁上剪一小口,插入线栓至大脑中动脉起始端。2 h后再次麻醉大鼠,将线栓抽出并结扎开口,实现再灌注,假手术组不进行插线栓操作。参考Zea-Longa的5级4分法[10]进行神经功能评分,评分≥2分的实验动物为模型制作成功,用于后续实验。
2.3 Western blot检测cleaved caspase-9、GSK-3β、NMDAR1、GluR2的表达取新鲜大鼠左脑组织,用剪刀把组织剪切成细小碎片。称取100 mg加入1 mL蛋白裂解液(含有1%PMSF+1%蛋白磷酸酶抑制剂)进行匀浆,再4 ℃离心10 min后小心吸取上清至干净的管中,即得总蛋白。采用BCA法测定蛋白浓度。
蛋白采用SDS-PAGE凝胶电泳,湿转法将分离蛋白转至预先活化好的PVDF膜上,丽春红染色观察膜上是否有清晰条带,再用5% BSA封闭2 h后孵育一抗4 ℃过夜,一抗根据抗体说明书稀释比例制备,caspase-9(1 : 1 000)、GSK-3β(1 : 1 000)、NMDAR1(1 : 1 000)、GluR2(1 : 1 000)。次日摇床室温孵育二抗2 h,PVDF膜用TBST洗涤(10 min×3)之后加ECL显色剂,采用凝胶成像系统检测,以β-actin为内参,分析目的条带/β-actin的相对表达量。
2.4 统计学分析用SPSS20.0统计软件进行统计学处理,采用单因素方差分析(One-way ANOVA),结果用x±s表示。
3 结果 3.1 红景天苷对MCAO大鼠缺血侧脑组织cleaved caspase-9蛋白表达的影响MCAO模型大鼠给药1 d,与Sham组比较,MCAO模型大鼠缺血侧cleaved caspase-9蛋白表达增加。经红景天苷干预后,cleaved caspase-9蛋白表达降低,且具有统计学差异(P < 0.01)(Fig 1)。
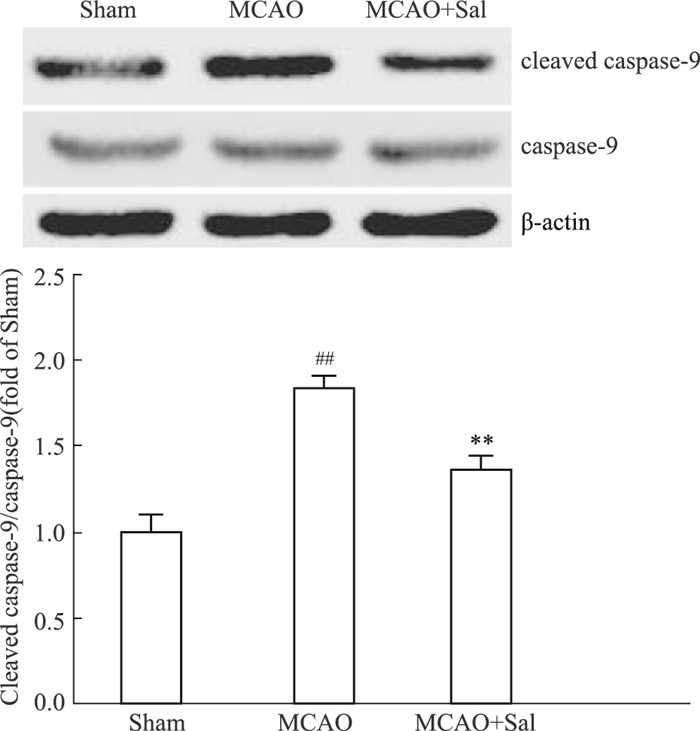
|
| Fig 1 Effects of salidroside treatment on cleaved caspase-9 protein in MCAO rats (x±s, n=6) ##P < 0.01 vs Sham, **P < 0.01 vs MCAO |
与Sham组比较,MCAO模型大鼠缺血侧pGSK-3β、NMDAR1、GluR2的蛋白表达量显著降低。经红景天苷作用后,显著促进pGSK-3β、NMDAR1、GluR2蛋白表达,具有统计学差异(P < 0.01)(Fig 2)。

|
| Fig 2 Effects of salidroside treatment on pGSK-3β, NMDAR1, GluR2 protein in MCAO rats (x±s, n=6) ##P < 0.01 vs Sham, **P < 0.01 vs MCAO |
侧脑室注射GSK-3β抑制剂和腹腔注射红景天苷后,与MCAO组比较,MCAO+Sal组可明显降低MCAO模型大鼠缺血侧脑组织中cleaved caspase-9的蛋白表达,具有统计学差异(P < 0.05);而侧脑室注射SB216763后cleaved caspase-9蛋白表达无变化(Fig 3)。

|
| Fig 3 Effects of salidroside or SB216763 treatment on caspase-9 protein in MCAO rats (x±s, n=6) ##P < 0.01 vs Sham, **P < 0.01 vs MCAO, △P < 0.05 vs SB216763+Sham, ▲▲P < 0.01 vs MCAO+Sal |
侧脑室注射GSK-3β抑制剂和腹腔注射红景天苷后,与MCAO组比较,MCAO+Sal组可明显降低MCAO模型大鼠缺血侧脑组织中pGSK-3β、NMDAR1、GluR2蛋白表达,差异有统计学意义(P < 0.05);而侧脑室注射SB216763后pGSK-3β、NMDAR1、GluR2表达均无变化(Fig 4)。
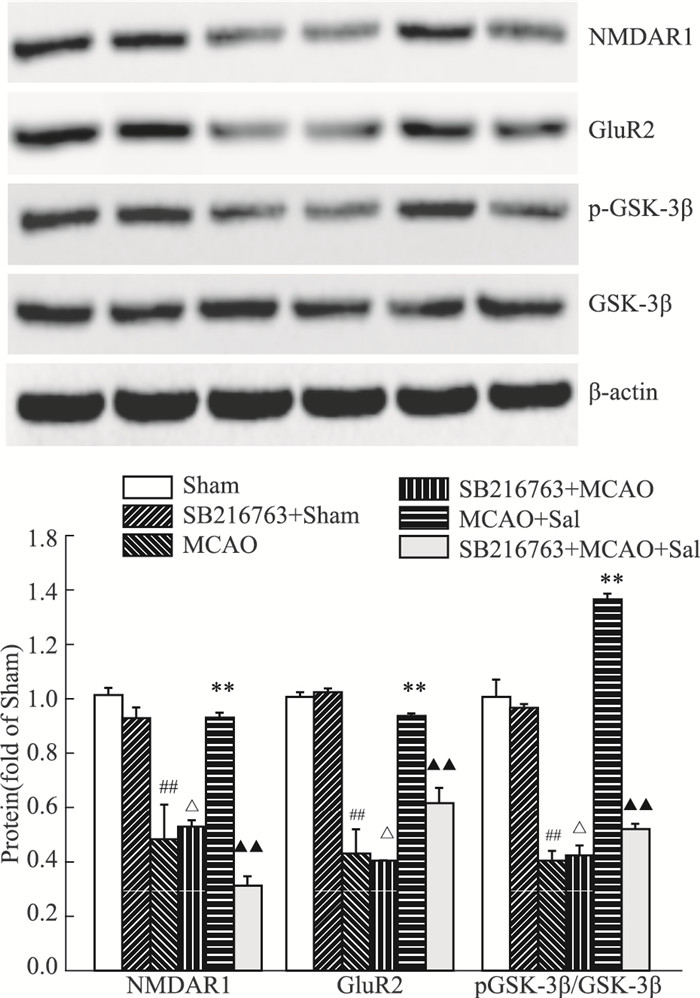
|
| Fig 4 Effects of salidroside or SB216763 treatment on pGSK-3β, NMDAR1, GluR2 protein in MCAO rats (x±s, n=6) ##P < 0.01 vs Sham, **P < 0.01 vs MCAO, △P < 0.05 vs SB216763+Sham, ▲▲P < 0.01 vs MCAO+Sal |
目前,神经元凋亡被认为是脑缺血损伤后继发性损害的重要机制,GSK-3β作为一种多功能的丝氨酸/苏氨酸激酶,其活性主要由肤链中所含丝氨酸/苏氨酸(Ser/Thr)的磷酸化水平决定,Tyr216磷酸化后GSK3β活性增强而Ser9的磷酸化则抑制GSK3β活性。在脑缺血/再灌注时,活化后的GSK可以诱导细胞凋亡,并调节线粒体mPTP开放程度,进而影响细胞色素C(Cyt-c)释放,caspase-9发生自我催化,活化的caspase-9进一步诱导caspase-3进行切割并使之激活,使级联反应进一步放大,被激活的caspase-3通过对caspase靶蛋白的水解,进一步加重凋亡损伤[11-12]。本研究结果发现caspase-9前体被大量激活,cleaved caspase-9增多,经红景天苷干预后,翻转该结果,提示红景天苷能抑制神经细胞的线粒体依赖途径凋亡。同时,实验中发现红景天苷给药组的神经功能损伤明显低于模型组,且GSK-3β磷酸化水平升高,表明红景天苷可以促进GSK-3β磷酸化,抑制其活性。
有研究表明,红景天苷可以抑制钠通道从而抑制突触的Glu释放和交感神经传递而发挥神经保护作用,减轻脑缺血/再灌注损伤[13]。在海马组织绝大部分神经元突触表面的受体含有G1uR2亚基,脑缺血继发性损伤刺激可使GluR2表达下降,导致钙离子通过AMPA受体离子通道内流增加,加重神经元损伤[14]。同时NMDA1受体(N-methyl-D-aspartate receptor)是中枢神经系统内一类重要的兴奋性氨基酸,能够参与脑缺血病理状态下的兴奋毒性机制,位于突触外的NMDAR过度激活会导致兴奋性毒性,位于突触内的NMDAR激活可以促进细胞存活。本研究表明,经红景天苷干预后,能够增加大鼠脑缺血侧脑组织中NMDA1和GluR2的蛋白表达,减少神经细胞凋亡。Patrick等[15]研究表明NMDA1受体和GluR2的分布与表达是治疗脑缺血和心肌缺血的重要机制。但是关于其上游调控机制鲜有报道。而PI3K/Akt信号通路是最主要的神经细胞存活信号通路,Akt可促使GSK-3β磷酸化增多,抑制其活性从而调节神经细胞凋亡屡有报道。为了证实红景天苷对caspase-9、NMDA1和GluR2的调节作用是通过影响GSK-3β的活性发挥作用,我们使用GSK-3β抑制剂,结果发现,注射SB216763后再给予红景天苷治疗,结果显示以上蛋白无变化。提示红景天苷是通过促进GSK-3β的磷酸化,降低caspase-9、NMDA1和GluR2的表达,减少细胞凋亡,从而发挥脑保护作用。为探究红景天苷抗细胞凋亡的脑保护作用研究奠定基础。
( 本实验在福建中医药大学药学院生物医药研发中心及省级中药学重点实验室完成,感谢所有老师及同学们的支持与帮助!)
| [1] |
Peisker T, Koznar B, StetkarovaI, et al. Acute stroke therapy:A review[J]. Trends Cardiovasc Med, 2017, 27(1): 59-66. |
| [2] |
吴秀专, 毕晓华, 王燕芳, 等. 红景天苷药理作用研究进展概述[J]. 中国药师, 2018, 21(8): 1460-2. Wu X Z, Bi X H, Wang Y F, et al. New research progress in the pharmacological function of salidroside[J]. Chin Pharm, 2018, 21(8): 1460-2. |
| [3] |
赖文芳, 张小琴, 洪海棉, 等. 红景天苷对大鼠局灶性脑缺血/再灌注损伤的神经保护作用[J]. 中国药理学通报, 2015, 31(6): 775-80. Lai W F, Zhang X Q, Hong H M, et al. Neuroprotective effects of salidroside against focal celebral ischemia/reperfusion injury in rats[J]. Chin Pharmacol Bull, 2015, 31(6): 775-80. |
| [4] |
谢秀利, 洪海棉, 赖文芳, 等. 红景天苷对大脑中动脉闭塞模型大鼠的神经保护作用[J]. 中国药理学通报, 2015, 31(10): 1452-7. Xie X L, Hong H M, Lai W F, et al. Protective effects of salidroside in MCAO rats[J]. Chin Pharmacol Bull, 2015, 31(10): 1452-7. |
| [5] |
宋百颖, 赖文芳, 苏燕青, 等. 红景天苷通过抑制补体C3的表达对MCAO大鼠缺血侧NeuN、Egr4影响的研究[J]. 中国药理学通报, 2017, 33(11): 1579-84. Song B Y, Lai W F, Su Y Q, et al. Effects of salidroside on expression of NeuN and Egr4 in ischemic side of MCAO rats by inhibiting expression of C3[J]. Chin Pharmacol Bull, 2017, 33(11): 1579-84. |
| [6] |
Lai W F, Xie X L, Zhang X Q, et al. Inhibition of complement drives increase in early growth response proteins and neuroprotection mediated by salidroside after cerebral ischemia[J]. Inflammation, 2017, 41(2): 1-15. |
| [7] |
黄鑫, 林昱, 杨泽霖, 等. 红景天苷抑制补体成分对脑缺血/再灌注大鼠的神经保护作用[J]. 中国药理学通报, 2019, 35(7): 967-72. Huang X, Lin Y, Yang Z L, et al. Neuroprotective effects of salidroside on complement composition in cerebral ischemia-reperfusion injury rats[J]. Chin Pharmacol Bull, 2019, 35(7): 967-72. |
| [8] |
李金, 唐其柱, 张文斌, 等. 糖原合成激酶-3在心血管疾病中的研究进展[J]. 中国循证心血管医学杂志, 2015, 7(6): 863-6. Li J, Tang Q Z, Zhang W B, et al. Research progress of glycogen synthase kinase-3 in cardiovascular diseases[J]. Chin J Evid Based Cardiovasc Med, 2015, 7(6): 863-6. |
| [9] |
FangG X, Zhang P L, Liu J F, et al. Inhibition of GSK-3β activity suppresses HCC malignant phenotype by inhibiting glycolysis via activating AMPK/mTOR signaling[J]. Cancer Lett, 2019, 463: 11-26. |
| [10] |
Longa E Z, Weinstein P R, Carlson S, et al. Reversible middle cerebral artery occlusion without craniectomy in rats[J]. Stroke, 1989, 20(1): 84-91. |
| [11] |
KuidaK. Caspase-9[J]. Int J Biochem Cell Biol, 2000, 32(2): 121-4. |
| [12] |
Agnès Petit-Paitel, Frédéric Brau, Cazareth J, et al. Involvment of cytosolic and mitochondrial GSK-3β in mitochondrial dysfunction and neuronal cell death of MPTP/MPP+-treated neurons[J]. PLoS One, 2009, 4(5): e5491. |
| [13] |
陈霞, 周松林, 顾晓松, 等. 红景天苷对谷氨酸损伤海马神经元的保护作用[J]. 解剖学报, 2008, 39(3): 355-9. Chen X, Zhou L S, Gu X S, et al. Protective effects of salidroside on clutamate induced neurotoxicity in cultured hippocampal neurons[J]. Acta Anat Sin, 2008, 39(3): 355-9. |
| [14] |
张小琴, 侯丽颖, 强国芳, 等. 片仔癀对局灶性脑缺血/再灌注大鼠皮质中NMDAR1和GluR2表达的影响[J]. 中国药理学通报, 2019, 35(2): 288-92. Zang X Q, Hou L Y, Qiang D F, et al. Effects of Pien-Tze-Iuang on expression of NMDAR1 and GluR2 in cortex of MCAO rats[J]. Chin Pharmacol Bull, 2019, 35(2): 288-92. |
| [15] |
Hof P R, Vissavajjhala P, Rosenthal R E, et al. Distribution of glutamate receptor subunit proteinsG1uR2(4), GluR5/6/7, and NMDAR1 in the canine and primate cerebral cortex: a comparative immunohistochemical analysis[J]. Brain Res, 1996, 723(1-2): 77-89. |