


2. 安徽医科大学临床医学院, 合肥 230032、;
3. 安徽医科大学形态学实验中心, 合肥 230032
 ,
HUANG Yan-ping1,
FANG An-ning1,
YANG Jun1,
ZHOU Wen-han2,
WANG Jia-hao2,
QU Zi-ting2,
ZHU Hao-chen2,
LI Na3,
CHEN Xiao-yu3
,
HUANG Yan-ping1,
FANG An-ning1,
YANG Jun1,
ZHOU Wen-han2,
WANG Jia-hao2,
QU Zi-ting2,
ZHU Hao-chen2,
LI Na3,
CHEN Xiao-yu3

2. Dept of Clinical Medicine, Anhui Medical University, Hefei 230032, China;
3. Morphological Experiment Center, Anhui Medical University, Hefei 230032, China
类风湿性关节炎(rheumatoid arthritis, RA)为慢性关节滑膜炎症, 其中成纤维样滑膜细胞(fibroblast-like synoviocytes, FLS)增生, 破坏局部关节结构, 是RA形成的关键因素之一[1]。同时, 关节疼痛、活动受限和长期治疗等使RA患者机体呈应激状态, 表现为氧自由基(oxygen free radical, ROS)的增加[2-3]。同时, 机体细胞中90%以上的ROS由线粒体产生, 而且慢性长期ROS的增加可能会诱导细胞突变和致瘤性, 前期研究表明, ROS的增加与FLS的异常增殖关系密切[4]。药理学研究中, 常用弗氏完全佐剂(Freund’s complete adjuvant, FCA)诱导佐剂性关节炎(adjuvant arthritis, AA), 作为筛选RA药物模型[5]。
多元酚类化合物白藜芦醇(resveratrol, Res)是从虎杖、葡萄等中提取的植物抗毒素, 有抗氧化、抗炎和免疫调节作用[6], 对肿瘤细胞有一定的抗增殖特性[7]。研究证实, RA患者机体处于氧化应激状态[2, 3]; 去乙酰化酶3(sirtuins 3, SIRT3)是位于线粒体中的去乙酰化酶, 能够抗氧化应激[8]; 金属抗氧化酶锰超氧化物歧化酶(manganese superoxide dismutase, MnSOD)在线粒体中能够将超氧阴离子自由基降解, 能够抗氧化损伤[9]。本研究探讨AA大鼠模型机体的氧化应激状态和滑膜组织中SIRT3-MnSOD蛋白表达情况, 进一步应用过氧化氢(H2O2)处理培养AA-FLS, 体外探讨H2O2对FLS细胞增殖的影响, Res对低浓度H2O2(5 μmol·L-1)处理AA-FLS增殖和凋亡作用, 以及AA-FLS线粒体SIRT3-MnSOD蛋白表达情况, 旨在探讨Res的抗氧化应激作用是否通过线粒体SIRT3-MnSOD途径实现, 为Res作用RA提供新的思路。
1 材料与方法 1.1 主要材料白藜芦醇(纯度≥99.9%, 编号501-36-1)、弗氏完全佐剂(编号5881)购于美国Sigma公司; 30% H2O2购于北京万佳科技有限公司; 培养基RPMI 1640、胎牛血清(FBS)购于美国Gibco公司; 超氧化物歧化酶(SOD)、谷胱甘肽过氧化物酶(GSH-Px)、丙二醛(MDA)检测试剂盒购于南京建成生物工程研究所; SIRT3(编号ab13533)、MnSOD(编号ab137037)、β-actin(编号ab8227)、波形蛋白(Vimentin)(编号ab92547)购于英国Abcam公司; CCK-8试剂盒(编号ck04)购于日本同仁生物有限公司; Hoechst 33258凋亡检测试剂盒(编号C1011)、蛋白预染Maker、荧光标记的二抗、ECL化学发光液购于上海碧云天生物有限公司。
1.2 实验动物20只SD大鼠, 雄性, 体质量(180~200)g, 清洁级, 购于安徽省动物实验中心(合格证号:皖医动准2019-01), 每天光照:黑暗周期(12 h :12 h), 自由进食饮水。
1.3 实验方法 1.3.1 实验动物分组、建模和标本收集20只SD大鼠随机均分成两组:正常组、模型组。模型鼠采取0.1 mL FCA注射入左后足趾皮内致炎, 建模28 d后, 戊巴比妥钠麻醉下, 腹主动脉内取血5 mL, 放置试管中, 离心后, 将血清-20 ℃贮存待测氧化应激指标, 应用分光光度计, 硫代巴比妥酸法检测MDA含量, 比色法测定GSH-Px活性, 羟胺法检测SOD活性。
1.3.2 踝关节免疫组织化学染色正常组和模型组SD大鼠致炎侧踝关节组织, 每组3只, 置于10%福尔马林溶液中固定48 h, 10%硝酸溶液脱钙2周, 自来水冲洗过夜, 梯度乙醇脱水, 二甲苯透明, 常规石蜡包埋, 厚3 μm切片, 60 ℃温箱烤片1 h, 枸橼酸钠缓冲液微波热抗原修复, 羊抗鼠SIRT3(1 :300)、羊抗鼠MnSOD(1 :200)单克隆一抗50 μL, 湿盒4 ℃冰箱孵育过夜, PBS冲洗, 加入37 ℃温箱中生物素标记的二抗50 μL, 苏木精衬染, 脱水、透明、中性树胶封片, Nikon生物显微镜观察并摄片。
1.3.3 踝关节滑膜细胞培养、鉴定按照本课题组前期建立的方法[10], 模型组大鼠FLS采取组织块培养法, 无菌超净台下, 将致炎侧踝关节附近的脂肪组织、肌腱和韧带钝性分离, 眼科手术剪小心剥离滑膜组织, 剪碎, 放置于少量含20%胎牛血清的RPMI 1640培养基的瓶中, 37 ℃、5%CO2培养, 待组织块周围长出较多细胞后, 移除组织块, 继续培养, 胰酶消化传代, 取培养第3~5代细胞, 采用免疫荧光细胞化学, 羊抗鼠Vimentin单克隆一抗(1 :200), 鉴定培养细胞是否为AA大鼠FLS。
1.3.4 H2O2对FLS细胞增殖影响采用CCK-8法试剂盒检测, 取对数生长期的FLS细胞, 接种于96孔板中, 每孔加入细胞3.0×103个/100 μL, 次日待FLS细胞贴壁后, 采取不同浓度的H2O2(0.1、0.5、1、3、5、10、20、40、80 μmol·L-1)处理24 h, 每组细胞设5个复孔, 以不含H2O2(0 μmol·L-1)的培养基为对照; 全自动酶标仪, 450 nm波长处测吸光度(absorbance, A)A450值, 观察AA大鼠FLS在H2O2处理后的增殖情况。
1.3.5 Res对低浓度H2O2处理FLS细胞增殖影响FLS细胞接种于96孔板中贴壁, CCK-8法检测。根据1.3.4实验结果, 取使FLS细胞增殖活跃的低浓度H2O2(5 μmol·L-1)预先处理24 h, 细胞贴壁生长, 加入不同浓度的Res(0、1、5、10、20、40、80、160 μmol·L-1)处理24 h后, 每孔加入10 μL的CCK-8继续培养4 h。观察波长450 nm处酶标仪测定吸光度A450值。
1.3.6 HE染色观察Res对低浓度H2O2处理FLS细胞凋亡情况取对数生长期的AA模型FLS, 1×106/孔接种于6孔板中, 低浓度H2O2(5 μmol·L-1)处理FLS细胞贴壁生长24 h后, 实验分4组:AA模型FLS组、Res给药组(终浓度为5、20、40 μmol·L-1)处理24 h, 吸弃培养基, 每孔加入少量4%多聚甲醛液固定细胞15 min, PBS清洗, Triton X-100透化10 min, 吸干后, 每孔滴加Hoechst 33258染色液50 μL, 避光染色15 min, PBS清洗, 荧光显微镜观察摄片。
1.3.7 Western blot检测Res对低浓度H2O2处理FLS细胞氧化应激相关蛋白的表达取对数生长期细胞, 6孔板中接种1×106/孔FLS, 培养24 h后, RIPA细胞裂解液提取总蛋白, 离心后取上清液, 蛋白定量后, SDS-PAGE电泳, 转膜, 脱脂奶粉室温封闭, 羊抗鼠SIRT3(1 :3 000)、羊抗鼠MnSOD(1 :2 000)、羊抗鼠β-actin(1 :2 000)单克隆一抗50 μL, 4 ℃孵育过夜后, TBST缓冲液充分洗膜, 兔抗羊二抗室温中孵育2 h, TBST洗膜, ECL化学发光, 曝光、显影、定影。
1.4 统计学处理采用SPSS 22.0统计软件, 结果采用x±s表示, 单因素方差分析(One-way ANOVA)多组间均数比较, t检验比较两组间差异。
2 结果 2.1 AA大鼠血清氧化应激指标如Tab 1所示, 与正常对照组比较, AA模型组大鼠血清MDA含量升高, GSH-Px含量降低, SOD活性下降, 两组间比较差异均有统计学意义(P < 0.01), 表明AA模型大鼠机体处于氧化应激状态。
| Group | MDA/μmol·L-1 | GSH-Px/μmol·L-1 | SOD/U·mL-1 |
| Normal | 5.16±0.52 | 186.31±9.27 | 215.27±9.04 |
| Model | 11.07±1.21** | 140.27±8.25** | 138.08±8.67** |
| **P < 0.01 vs normal | |||
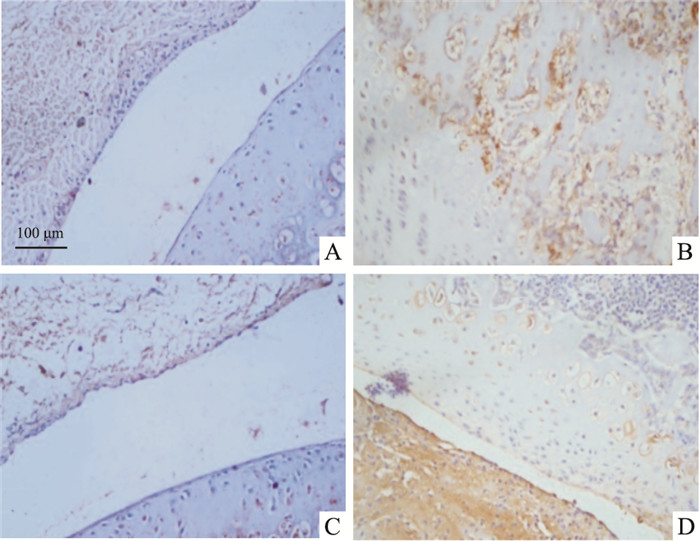
正常组大鼠踝关节SIRT3蛋白表达不明显(Fig 1A), 而模型组大鼠踝关节滑膜组织、软骨组织中SIRT3蛋白表达明显增强, 阳性染色呈黄色或棕黄色(Fig 1B)。相似的, MnSOD蛋白在正常大鼠踝关节阳性表达不明显(Fig 1C), 而模型组大鼠踝关节滑膜和软骨组织中阳性表达明显增强, 以关节表面滑膜组织及下方软骨组织最为明显(Fig 1D)。
|
| Fig 1 Results of immunohistochemical staining of ankle joint A.SIRT3 protein expression in normal rat; B. SIRT3 protein expression in model rats; C. MnSOD protein expression in normal rats; D.MnSOD protein expression in model rats |
采取组织块培养法, 待FLS长出AA大鼠踝关节组织, 移去组织块, 继续培养, 胰酶消化并传代培养, 取3~5代FLS细胞实验, 波形蛋白Vimentin是FLS的分子标记物, 采用免疫荧光细胞化学染色, 结果如Fig 2所示。

|
| Fig 2 Vimentin immunofluorescent staining in synovial cells of AA rats (×400) |
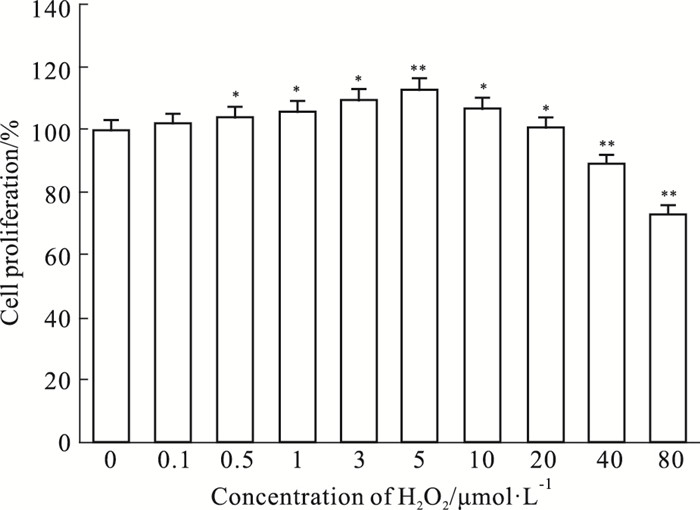
不同浓度的H2O2处理AA大鼠FLS 24 h后, 将对照组(H2O2 0 μmol·L-1)的细胞活力设为100%, 结果表明, 在H2O2浓度在0.1~5 μmol·L-1间, FLS细胞增殖活力逐渐增加, 随着H2O2浓度升高, FLS细胞活力呈下降趋势。表明在低浓度H2O2(≤5 μmol·L-1)刺激下, 可能促进AA大鼠FLS增殖。见Fig 3。
|
| Fig 3 FLS cell proliferation in AA rats treated with different concentrations of H2O2(x±s, n=5) *P < 0.05, **P < 0.01 vs H2O2 (0 μmol·L-1) |
预先在培养的FLS中加入低浓度H2O2(5 μmol·L-1)处理24 h后, 然后Res处理(终浓度1、5、10、20、40、80、160 μmol·L-1), 以未加Res(0 μmol·L-1)处理为对照组, Res作用24 h后, 结果见Fig 4, 可见加入1~160 μmol·L-1 Res后, 抑制了低浓度H2O2处理的FLS增殖, 且当Res处理终浓度超过5 μmol·L-1时, 差异有显著性(P < 0.05, P < 0.01)。

|
| Fig 4 FLS of AA rats proliferation inhibiting by different concentrations of Res with low concentrations of H2O2(x±s, n=5) *P < 0.05, **P < 0.01 vs Res (0 μmol·L-1) |
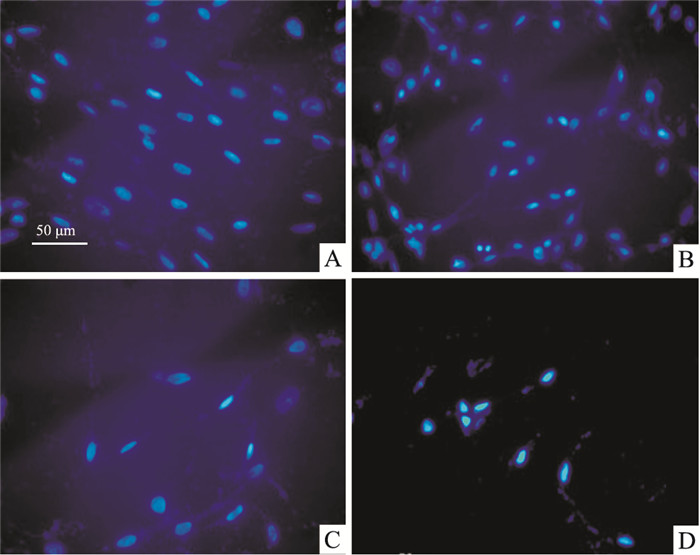
培养的FLS中加入低浓度H2O2(5 μmol·L-1)处理24 h后, Res(0、5、20、40 μmol·L-1)作用于AA大鼠FLS 24 h后, 在荧光显微镜下, Res(0 μmol·L-1)对照组细胞数目多, 细胞核呈均匀蓝色荧光, Res低浓度(5 μmol·L-1)作用后FLS有散在的核染色质聚集、碎裂, Res高浓度(20、40 μmol·L-1)作用后, 细胞凋亡现象明显, 表现为较多的FLS细胞核染色质聚集、碎裂。见Fig 5。
|
| Fig 5 Immunofluorescence staining by Hoechst 33258 A:Res(0 μmol·L-1), B:Res(5 μmol·L-1), C:Res(20 μmol·L-1), D:Res(40 μmol·L-1) |
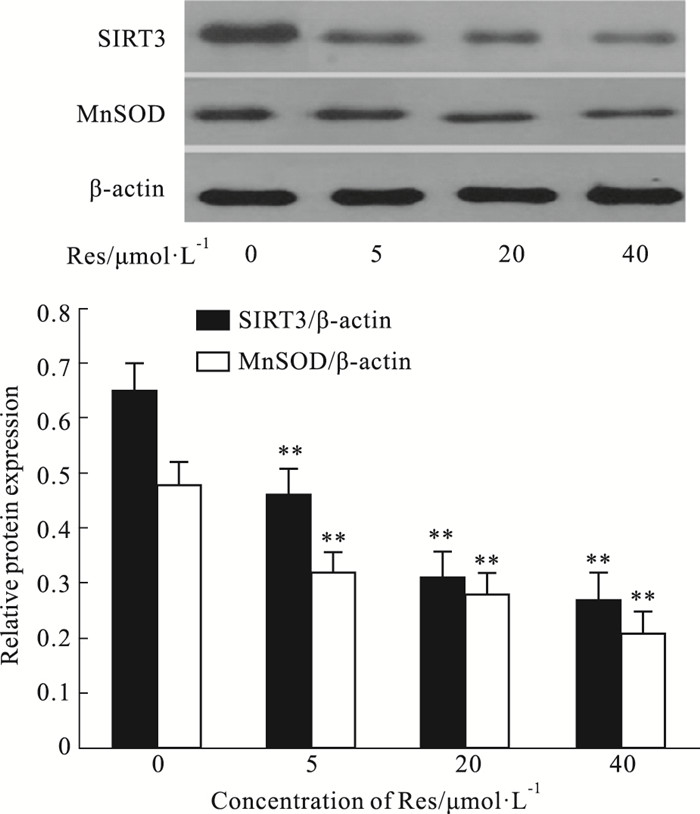
Western blot结果表明, 与低浓度H2O2处理的对照组Res(0 μmol·L-1)比较, Res不同浓度(5、20、40 μmol·L-1)作用下, SIRT3、MnSOD蛋白表达降低(Fig 6A); 统计处理表明(Fig 6B), 随着Res的浓度的增加, SIRT3、MnSOD表达量与内参照β-actin比值呈浓度依耐性的降低, 较对照组差异有显著性(P < 0.05, P < 0.01)。
|
| Fig 6 Effect of Res on the expressions of SIRT3 and MnSOD protein in FLS(x±s, n=3) A: typical Western blot; B: semi-quantitative analysis (x±s, n=3), *P < 0.05, **P < 0.01 vs Res (0 μmol·L-1) |
RA患者病变关节的主要病理特征为增生增厚的滑膜组织中血管翳形成, FLS和大量炎性细胞, 包括淋巴细胞和巨噬细胞浸润到关节组织结构中, 破坏局部关节, 故FLS在RA发病过程中至关重要[1]。过多的炎性细胞因子刺激活化巨噬细胞分泌ROS, 成为关节损伤的媒介[11]。MDA是生物膜脂质过氧化产物, 反映机体细胞ROS损伤后氧化损伤状态, GSH-Px和SOD是抗ROS损伤的重要酶类, GSH-Px可等活化还原型谷胱甘肽(GSH), 促进H2O2等过氧化物降低, 保护细胞膜结构完整性。本研究构建AA模型大鼠为动物模型, 先检测大鼠机体氧化应激状况。结果表明, 与正常组比较, AA模型大鼠血清MDA含量上升, GSH-Px含量下降和SOD活性降低, 说明AA模型组大鼠机体存在氧化应激现象。
在RA发病过程中, FLS起着关键性作用, 增生活跃的FLS激活促炎性因子, 促进ROS生成, 成为关节损伤一个重要因素[12]。本研究成功分离和培养FLS, 并经过鉴定培养细胞为FLS; 同时, 低浓度(≤5 μmol·L-1)H2O2可促进AA大鼠FLS增殖, 故本研究中, 我们应用低浓度H2O2(5 μmol·L-1)刺激FLS生长, 验证Res对AA大鼠FLS增殖和凋亡作用。Res属于多元酚类化合物, 存在于多种水果和蔬菜中, 具有广泛的抗氧化和抗衰老等功效。细胞增殖实验证实, Res能够抑制低浓度H2O2处理FLS的增殖, 且与Res浓度呈正相关; 同时, Res能够浓度依赖性的增加低浓度H2O2处理FLS的凋亡, 但Res诱导FLS凋亡的机制尚不明确。
SIRT3是位于线粒体中的SIRTs家族成员, 能够调节线粒体乙酰化蛋白脱乙酰基, 调节能量代谢; MnSOD是真核生物细胞线粒体中的金属抗氧化酶, 可清除超氧阴离子自由基, 具有抗氧化损伤作用[12]。SIRT3可以脱乙酰化MnSOD 122位的赖氨酸残基, 激活MnSOD, 降低ROS生成, 从而具有抗氧化作用[13]。本研究证实, AA大鼠关节滑膜组织中SIRT3、MnSOD高表达; 体外蛋白免疫印迹检测证实, 通过低浓度H2O2处理后, AA大鼠FLS细胞中SIRT3和MnSOD高表达, 不同浓度Res处理后, 低浓度H2O2处理的AA大鼠FLS细胞增殖明显受到抑制, FLS凋亡增加, SIRT3、MnSOD蛋白表达也降低, 表明Res可能通过降低线粒体SIRT3- MnSOD信号通路蛋白而具有抗FLS增殖作用。
( 致谢: 感谢安徽医科大学组胚教研室和形态实验中心的老师和同学们在实验过程中给予的帮助 )
| [1] |
Frey O, Hückel M, Gajda M, et al. Induction of chronic destructive arthritis in SCID mice by arthritogenic fibroblast-like synoviocytes derived from mice with antigen-induced arthritis[J]. Arthritis Res Ther, 2018, 20(1): 261. |
| [2] |
Machado C R L, Resende G G, Macedo R B V, et al. Fibroblast-like synoviocytes from fluid and synovial membrane from primary osteoarthritis demonstrate similar production of interleukin 6, and metalloproteinases 1 and 3[J]. Clin Exp Rheumatol, 2019, 37(2): 306-9. |
| [3] |
Iwamoto N, Fukui S, Takatani A, et al. Osteogenic differentiation offibroblast-like synovial cells in rheumatoid arthritis is induced by microRNA-218 through a ROBO/Slit pathway[J]. Arthritis Res Ther, 2018, 20(1): 189. |
| [4] |
Angiolilli C, Kabala P A, Grabiec A M, et al. Control of cytokine mRNA degradation by the histone deacetylase inhibitor ITF2357 in rheumatoid arthritis fibroblast-like synoviocytes: beyond transcriptional regulation[J]. Arthritis Res Ther, 2018, 20(1): 148. doi:10.1186/s13075-018-1638-4 |
| [5] |
Tu J, Hong W, Zhang P, et al. Ontology and function of fibroblast-like and macrophage-like synoviocytes: how do they talk to each other and can they be targeted for rheumatoid arthritis therapy[J]. Front Immunol, 2018, 9: 1467. doi:10.3389/fimmu.2018.01467 |
| [6] |
Ghaiad H R, Nooh M M, El-Sawalhi M M, et al. Resveratrol promotes remyelination in cuprizone model of multiple sclerosis: biochemical and histological study[J]. Mol Neurobiol, 2017, 54(5): 3219-29. doi:10.1007/s12035-016-9891-5 |
| [7] |
Dai H, Deng H B, Wang Y H, et al. Resveratrol inhibits the growth of gastric cancer via the Wnt/β-catenin pathway[J]. Oncol Lett, 2018, 16(2): 1579-83. |
| [8] |
Wang J, Li J, Cao N, et al. Resveratrol, an activator of SIRT1, induces protective autophagy in non-small-cell lung cancer via inhibiting Akt/mTOR and activating p38-MAPK[J]. Onco Targets Ther, 2018, 11: 7777-86. doi:10.2147/OTT.S159095 |
| [9] |
汪陶荣, 张晔, 曹威, 等. 白藜芦醇通过下调MnSOD诱导类风湿性关节炎成纤维样滑膜细胞凋亡[J]. 中国药理学通报, 2019, 35(4): 489-94. Wang T R, Zhang Y, Cao W, et al. Resveratrol mediates apoptosis of rheumatoid arthritis fibroblast-like synoviocytes by MnSOD regulation[J]. Chin Pharmacol Bull, 2019, 35(4): 489-94. doi:10.3969/j.issn.1001-1978.2019.04.009 |
| [10] |
Cao W, Zhang J Q, Wang G Y, et al. Reducing-autophagy derived mitochondrial dysfunction during resveratrol promotes FLS cell apoptosis[J]. Anat Rec (Hoboken), 2018, 301: 1179-88. |
| [11] |
Vaamonde-García C, Loureiro J, Valcárcel-Ares M N, et al. The mitochondrial inhibitor oligomycin induces an inflammatory response in the rat knee joint[J]. BMC Musculoskelet Disord, 2017, 18(1): 254. doi:10.1186/s12891-017-1621-2 |
| [12] |
Zhang J Q, Song X B, Cao W, et al. Autophagy and mitochondrial dysfunction in adjuvant-arthritis rats treatment with resveratrol[J]. Sci Rep, 2016, 6: 32928. doi:10.1038/srep32928 |
| [13] |
Koltai E, Bori Z, Osvath P, et al. Master athletes have higher miR-7, SIRT3 and SOD2 expression in skeletal muscle than age-matched sedentary controls[J]. Redox Biol, 2018, 19: 46-51. doi:10.1016/j.redox.2018.07.022 |