

目前, 绝大多数中药制剂质量控制主要采用理化分析方法, 但由于其成分多样、工艺复杂等因素, 现行质量标准中检验项目没有与药效学建立直接的内在联系, 存在一定局限性[1]。生物活性测定法是检验药品质量的重要检测手段之一, 特别适用于具有多种活性成分或成分复杂、有效成分不清的中药制剂。通过生物活性测定法与理化分析技术结合应用, 致力于寻找一种方便快捷的方式考察血塞注射液生物活性, 并通过血塞通注射液探索一条活血化瘀药通用的生物活性检定方法, 使现有中药质量标准的评价更全面更合理。
1 材料与方法 1.1 供试品和对照品血塞通注射液(A), 批号12EJ07, 规格2 ml:100 mg; 血塞通注射液(B), 批号20130303, 规格2 ml:100 mg; 血塞通注射液(C), 批号20130101, 规格10 ml:250 mg。三七总皂苷(panax notoginseng saponins, PNS)(批号870-200001)、人参皂苷Rb1(ginsenoside Rb1, GRb)(批号110704-201223)、人参皂苷Rd(ginsenoside Rd, GRd)(批号111818-201001), 三七皂苷R1(notoginsenoside R1, NR)(批号110745-200617)、人参皂苷Re(ginsenoside Re, GRe)(批号110754-201123)、人参皂苷Rg1(ginsenoside Rg1, GRg)(批号110703-201128)均由中国食品药品检定研究院提供。
1.2 试剂和仪器主要试剂:活化部分凝血活酶时间(activated partial thromboplastin time, APTT)测定试剂盒购自希森美康医用电子(上海)有限公司, 批号557183;氯化钠注射液由双鹤药业(沈阳)有限责任公司生产, 批号130718A01;柠檬酸钠由国药集团化学试剂有限公司生产, 批号F20090828。主要仪器:全自动血凝分析仪CA-1500型由Sysmex公司生产, 离心机Z323K型由德国HERMLE公司生产, 十六道生理仪MP100型由BIOPAC SYSTEMS INC.公司生产。
1.3 实验动物兔, 雌雄兼用, 体质量(2.5~2.9) kg, 购自沈阳药科大学, 实验动物生产许可证SCXK(辽)2014-0002, 实验动物使用许可证SYXK(辽)2013-0011。
1.4 考察血塞通注射液APTT检测量效关系应用全自动血凝仪检测不同企业血塞通注射液(A、B、C)(r=1 :0.5)不同剂量对APTT值的影响, 分别取50、25、12.5、6.25、3.125 g·L-1血塞通注射液稀释液50 μL、兔血浆50 μL、APTT试剂50 μL至血凝杯中, 预热180 s后, 各杯加入CaCl2 50 μL, 测得APTT。
1.5 考察血塞通注射液与三七总皂苷等四种标准品生物活性相关性血塞通注射液为植物三七中提取的有效部位三七总皂苷制成的灭菌水溶液, 故选取三七总皂苷标准品、人参皂苷Rb1、人参皂苷Rg1、三七皂苷R1做对照, 采用连续测样和拉丁方设计等方案检测APTT, 具体实验步骤同上。
1.6 生物活性测定方法的建立应用三七总皂苷作为对照品考察血塞通注射液对APTT的影响, 选取两批不同企业的血塞通注射液制成供试品溶液, 与相应浓度的对照品溶液分别检测APTT值, 每种浓度至少4次。测得数据照生物检定统计法(附录ⅩⅣ)中的量反应平行线测定法计算效价及试验误差。
1.7 数据处理各样本的APTT值以x±s表示, 并对数转换后进行统计分析。应用SPSS软件进行相关性分析, 当P < 0.05时, 认为两者具有显著相关性。生物活性测定方法的建立数据应用药典生物检定统计BS2000安装软件统计分析。
2 结果 2.1 考察血塞通注射液APTT检测量效关系结果显示, 血塞通注射液(50、25、12.5、6.25、3.125 g·L-1)存在显著地量效关系, 且应用不同兔血浆、不同企业供试品测得的结果接近, 较为稳定。初步判断, 选用APTT指标和该检测方法控制血塞通注射液产品质量基本可行。
2.2 考察血塞通注射液与三七总皂苷等标准品的生物活性相关性实验结果显示, 血塞通注射液与三七总皂苷存在明显的相关性; 进一步寻找哪种成分对APTT作用较强时, 我们发现, 人参皂苷Rb1、人参皂苷Rg1、三七皂苷R1三种标准品对应浓度APTT结果不满意, 且与血塞通注射液无相关性; 同时我们发现人参皂苷Rd、人参皂苷Re应用氯化钠注射液稀释极难溶解, 故无法进行APTT检测。
2.3 生物活性测定方法建立测得数据依据《中国药典》2015年版生物检定统计法中的量反应平行线测定法计算效价及试验误差[2]。经生物检定统计, 血塞通注射液(20130303)测得效价是47.0 g·L-1, 可信限率为6.91%, 可信限范围为43.8~50.3 g·L-1; 血塞通注射液(12EJ07)测得效价是37.0 g·L-1, 可信限率为8.79%, 可信限范围为33.6~40.1 g·L-1。两批血塞通注射液三七总皂苷含量在标示量的72%~98%范围内, 与理化分析含量测定结果基本一致。
| Rabbit | XST | 50 g·L-1 | 25 g·L-1 | 12.5 g·L-1 | 6.25 g·L-1 | 3.125 g·L-1 | Blank |
| 1 | A | 49.7±7.2 | 29.2±3.3 | 19.2±2.2 | 17.2±1.8 | 13.8±0.2 | 13.6±1.5 |
| B | 55.6±4.8 | 25.7±3.9 | 15.8±1.0 | 13.1±2.0 | 13.6±1.3 | 14.8±0.8 | |
| C | / | 46.6±4.6 | 25.3±2.5 | 21.2±4.0 | 22.9±3.8 | 15.9±1.5 | |
| 2 | A | 58.4±1.9 | 40.1±3.3 | 31.6±2.1 | 19.4±1.0 | 19.6±2.0 | 17.8±1.5 |
| 3 | A | 54.4±1.9 | 25.4±2.3 | 23.8±1.2 | 21.7±0.5 | 20.8±0.7 | 16.9±0.3 |
| 4 | A | 61.4±2.4 | 42.4±2.3 | 28.6±1.8 | 20.3±0.9 | 18.4±0.3 | 18.6±0.3 |
| Rabbit | Subject(lot) | 50 g·L-1 | 25 g·L-1 | 12.5 g·L-1 | 6.25 g·L-1 | 3.125 g·L-1 | Blank |
| 3 | XST(20130303) | 58.4±1.9* | 40.1±3.3* | 31.6±2.1* | 19.4±1.0* | 19.6±2.0* | 18.2±0.8 |
| PNS(870-200001) | 59.2±2.9 | 44.7±3.6 | 26.3±1.7 | 16.9±0.1 | 18.3±1.5 | ||
| *P<0.05 vs PNS | |||||||
| Rabbit | Subject(lot) | 50 g·L-1 | 25 g·L-1 | 12.5 g·L-1 | 6.25 g·L-1 | 3.125 g·L-1 | Blank |
| 3 | XST(20130303) | 40.6±4.8 | 25.4±2.3 | 23.8±1.2 | 21.7±0.5 | 20.8±0.7 | 16.9±0.3 |
| GRb(110704-201223) | 19.1±1.1 | 17.9±1.3 | 17.1±1.6 | 17.9±0.3 | / |
| Rabbit | Subject(lot) | 50 g·L-1 | 25 g·L-1 | 12.5 g·L-1 | 6.25 g·L-1 | 3.125 g·L-1 | Blank |
| 4 | XST(20130303) | 63.2±3.1** | 35.8±1.5** | 28.9±1.2** | 20.1±1.7** | 17.9±0.7** | 17.2±0.1 |
| GRg(110703-201128) | 22.0±0.7 | 18.8±0.8 | 18.0±0.4 | 16.9±0.6 | 16.1±0.2 | ||
| PNS(870-200001) | 64.6±2.8 | 41.3±1.6 | 26.9±2.4 | 17.8±1.4 | 20.9±1.0 | ||
| **P<0.01 vs PNS | |||||||
| Rabbit | Subject(lot) | 50 g·L-1 | 25 g·L-1 | 12.5 g·L-1 | 6.25 g·L-1 | 3.125 g·L-1 | Blank |
| 4 | XST(20130303) | 65.7±4.7 | 37.8±5.0 | 28.3±0.6 | 22.2±0.5 | 17.1±0.6 | 16.4±0.2 |
| NR(110745-200617) | 18.5±1.5 | 17.7±0.7 | 17.3±0.5 | 17.1±0.3 | 17.1±0.6 |

|
| Fig 1 Correlation of APTT values between Xuesaitong injection and standard substance at different concentrations |
| Rabbit | Subject(lot) | 50 g·L-1 | 25 g·L-1 | 12.5 g·L-1 | Blank |
| 4 | XST(20130303) | 63.2±3.1 | 35.8±1.5 | 28.9±1.2 | 19.3±1.6 |
| PNS(870-200001) | 64.6±2.8 | 41.3±1.6 | 26.9±2.4 | 19.3±1.6 | |
| 8 | XST(12EJ07) | 63.8±5.3 | 46.0±2.8 | 17.6±2.0 | 19.6±3.0 |
| PNS(870-200001) | 82.4±4.9 | 56.0±6.4 | 26.2±1.8 | 19.6±3.0 |
传统中药依功效可分为解表药、清热药、温里药、活血化瘀药、补虚药等。其中, 活血化瘀药是临床治疗心脑血管疾病最为常用药。研究表明, 活血化瘀类药可以改善血液粘滞性, 可通过抑制凝血因子活性而抑制内外源性凝血途径, 延长凝血酶时间、凝血活酶时间和凝血酶原时间, 具有明显抗凝血作用[3-4]。血塞通注射液就是这类药的代表, 其主要功效是活血祛瘀, 通脉活络; 主要用于中风偏瘫、瘀血阻络证等。血塞通注射液现执行标准通过理化检测手段(指纹图谱、含量测定等)对其进行质量控制, 但中药有其特殊性和复杂性, 它的活性成分不一定是有效成分。所以, 有必要在现有的中药质量控制模式基础上引入药效检测方法综合评价产品质量。
|
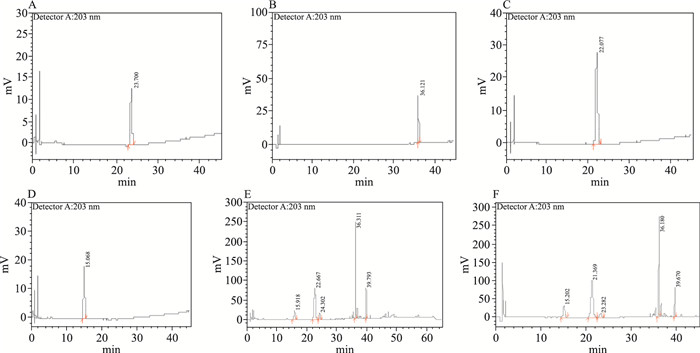
| Fig 2 HPLC determination of Xuesaitong injection A:Ginsenoside Re; B:Ginsenoside Rb1;C:Ginsenoside Rg1;D:Notoginsenoside R1;E:Panax notoginseng saponins; F:Xuesaitong injection |
近些年, 很多药品检验研究发现中药质量控制中生物活性测定引入的重要性, 并着手开展相关课题研究[4-7], 尝试将一些成熟、可推广的科学研究方法应用到药品检验领域[8-9]。已研究证实, 血塞通注射液的活血化瘀作用是通过同时影响内源性及外源性凝血系统实现的抗凝血作用[10-11]。因此, 选用检测APTT指标评价血塞通注射液活血化瘀作用的生物活性。需要说明的是, 在标准品的选择上, 依据了现行标准理化检测指标中的5种标准品进行试验方法的探索, 以期评价两者间的相关性和科学性。本文试验结果显示, 单纯的人参皂苷Rb1、人参皂苷Rg1和人参皂苷R1延长活化部分凝血活酶时间效果与血塞通注射液并没有关联性。说明三者不是血塞通注射液发挥延长APTT作用的有效成分; 而人参皂苷Re和人参皂苷Rd由于水中溶解度小, 未能检测APTT, 后两者是否为血塞通注射液药效有效成分还需进一步实验研究数据验证。
药物对生物体所引起的反应随着药物剂量的增加产生的量反应, 检定方法应选用平行线测定法[2]; 本文设计选择量反应平行线测定(3.3)法。同时, 对供试品应用法定高效液相法检测产品含量, 结果与生物活性检测方法一致。中药的有效性和活性研究注定不同于化学药品的研究理念, 单纯的成分检测远远不够, 常常是有效成分的含量检测结果与药效结果不一致。从质量控制的方向来看, 该研究考察的是产品临床实际应用效果, 与理化分析中成分检测相比, 更直接准确体现产品质量。需要注意的是, 生物检测试验结果的精确性有别于理化试验, 受多种因素(如实验动物本身、兔血制备过程、操作人员的熟练程度等)影响。在该研究生物活性检测方法中, 由于兔血的差异可能造成实验结果的误差, 建议采用颈动脉采血, 并多只兔血重复实验或混合兔血后离心使用实验3次, 减少由此带来的实验误差。对照品三七总皂苷建议选择中检院供含量测定用的。该研究以三七总皂苷为对照品, 建立血塞通注射液APTT生物活性测定方法; 符合实验动物福利, 所得数据稳定, 重复性好, 且与含量测定指标检测结果一致。建议本品新增生物活性检测方法结合理化分析严格控制产品质量:本品依血凝仪APTT生物活性测定法[2]测定, 本法的可信限率(FL%)不得大于10%, 三七总皂苷在标示量的70%~98%。
此外, 三七总皂苷具有稳定、易得、价格比较便宜等优点, 建议以三七总皂苷为对照品, 考察活血化瘀类中药相关生物活性测定方法, 以期找到一种适合我国国情、操作简单、成本较低的方法来控制中药产品质量。
| [1] |
国家药品标准: 血塞通注射液[S]. WS3-B-3590-2001(Z)-2011. National Drug Standard: Xuesaitong injection[S]. WS3-B-3590-2001(Z)-2011. |
| [2] |
国家药典委员会.《中国药典》2015年版.四部[S].北京: 中国医药科技出版社, 2015: 168, 182. Chinese Pharmacopoeia Commission.Chinese Pharmacopoeia 2015.Vol Ⅳ[S]. Beijing: Chin Med Sci Press, 2015: 168, 182. |
| [3] |
陈晨, 刘倩, 高华. 活血化瘀药药理作用研究进展[J]. 中国药事, 2011, 25(6): 603-5. Chen C, Liu Q, Gao H. Research progress on pharmacological effects of huo xue and stasis removing drugs[J]. Chin Pharm Aff, 2011, 25(6): 603-5. |
| [4] |
钟山, 崔征, 王东, 等. 水蛭注射液抗血栓与抗凝血作用[J]. 沈阳药科大学学报, 2006, 23(7): 456-8. Zhong S, Cui Z, Wang D, et al. Antithrombotic and anticoagulant effects of leech injection[J]. J Shenyang Pharm Univ, 2006, 23(7): 456-8. doi:10.3969/j.issn.1006-2858.2006.07.013 |
| [5] |
包贝华, 赵显, 曹雨诞, 等. 鸡冠花对致热复合出血模型大鼠的凉血止血效应机制研究[J]. 中国药理学通报, 2013, 29(10): 1457-61. Bao B H, Zhao X, Cao Y D, et al. Study on the mechanism of cool blood hemostatic effect of codonopsis chinensis on rat model of thermophilic compound hemorrhage[J]. Chin Pharmacol Bull, 2013, 29(10): 1457-61. doi:10.3969/j.issn.1001-1978.2013.10.030 |
| [6] |
游云, 廖福龙, 黄璐琦. 基于生物活性测定开展中药质量控制的研究进展[J]. 中国中药杂志, 2008, 43(3): 452-6. Yu Y, Liao F L, Huang L Q. Research progress on quality control of traditional Chinese medicine based on bioactivity determination[J]. Chin J Chin Mater Med, 2008, 43(3): 452-6. |
| [7] |
杨华, 李希, 高华娟, 等. 中药质量生物活性检测的发展现状及思考[J]. 中药与临床, 2014, 5(1): 50-3. Yang H, Li X, Gao H J, et al. Development status and reflection of quality biological activity detection of traditional Chinese medicine[J]. J TCM and Clinic, 2014, 5(1): 50-3. |
| [8] |
郭玉东, 王志斌, 周建平, 等. 中药生物活性测定法中标准品建立的研究[J]. 药物分析杂志, 2013, 33(4): 706-8, 15. Guo Y D, Wang Z B, Zhou J P, et al. Study on the establishment of standard products in the determination of biological activity of traditional Chinese medicine[J]. Chin J Pharm Anal, 2013, 33(4): 706-8, 15. |
| [9] |
王碧松.生物活性测定法用于活血化瘀类中药注射剂质量控制的研究[D].北京: 北京中医药大学, 2010. Wang B S. Study on the quality control of TCM injections with bioactivity assay[D].Beijing: Beijing Univ Tradit Chin Med, 2010. http://cdmd.cnki.com.cn/Article/CDMD-10026-2010144888.htm |
| [10] |
赵金明, 石玲, 商威, 等. 血塞通注射液抗凝血作用研究[J]. 辽宁中医杂志, 2006, 33(1): 106. Zhao J M, Shi L, Shang W, et al. Anticoagulant effect of xuesetong injection[J]. Liaoning J TCM, 2006, 33(1): 106. doi:10.3969/j.issn.1000-1719.2006.01.083 |
| [11] |
陈剑梅, 郭洁文. 三七总皂苷对心脑血管作用的药理研究新进展[J]. 今日药学, 2011, 21(7): 389-92. Chen J M, Guo J W. Recent advances in pharmacological studies on the effects of total saponins of panax notoginseng on cardio-cerebrovascular activity[J]. Pharm Sci, 2011, 21(7): 389-92. |

