

2. 上海市食品药品检验所药理毒理室/药物安全评价中心, 上海 201203;
3. 国家药品监督管理局化学药品制剂质量分析重点实验室, 上海 201203
唐黎明(1964-), 男, 硕士, 主任药师, 研究方向:药理毒理, 通讯作者, E-mail: tangliming@smda.sh.cn
2. Dept of Pharmacology and Toxicology / Center for Drug Safety Evaluation Shanghai Institute for Food and Drug Control, Shanghai 201203;
3. NMPA Key laboratory for Quality Analysis of Chemical Drug Preparations, Shanghai 210203
丙三醇又名甘油, 广泛用于食品、制药、化妆品和烟草等行业。丙三醇是吸入药物的辅料之一, 可作为吸入喷雾剂的助溶剂[1], 干粉吸入剂的赋形剂等[2]。电子烟在世界范围内日渐流行, 丙三醇作为电子烟中的溶剂和保湿剂, 需要进一步研究以充分评估其应用的安全性[3]。
目前, 吸入毒理学研究仍以应用实验动物进行口鼻式吸入染毒或整体暴露染毒为主[4]。相较于动物试验的周期长、成本高、种属差异等问题, 体外细胞实验方法耗时短, 实验条件可控性高。传统的浸没式条件下考察化合物对呼吸道上皮细胞的毒性, 细胞被培养基完全浸没[5]。对于吸入给药或者电子烟的抽吸而言, 浸没并不能表征实际的生理情形, 在体内化合物是以气溶胶的形式沉积在支气管和肺泡上皮细胞表面。越来越多的研究开始引入更加接近生理状态的体外毒性测试方法, 诸如VITROCELLⓇ气液界面细胞暴露云系统(air-liquid interface cell exposure-cloud, ALICE-CLOUD), 用于评价单次或重复暴露后纳米颗粒[6-8]和化学品[9]的对呼吸道细胞的毒性, 以及吸入药物的药效[10]和吸收动力学[11]等。暴露系统与气液界面培养的呼吸道上皮细胞联用, 可以将气溶胶直接递送到细胞表面, 模拟体内呼吸道上皮细胞与气溶胶的相互作用方式[12]。
本研究应用气液界面细胞暴露云系统, 将不同浓度的丙三醇溶液暴露于气液界面培养的肺腺癌细胞(A549), 模拟实际吸入丙三醇的暴露方式。用荧光素钠表征云暴露系统的递送性能, 考察丙三醇暴露后细胞存活率, 乳酸脱氢酶(lactate dehydrogenase, LDH)释放和促炎症因子白介素-6(interleukin-6, IL-6)表达的情况。通过体外细胞暴露快速评价丙三醇对呼吸道可能产生的毒性, 为丙三醇在吸入药物辅料和电子烟产品中的安全应用提供参考。
1 材料与方法 1.1 细胞株A549人肺腺癌细胞, 获赠于复旦大学药学院。
1.2 试剂与仪器丙三醇(华宝食用香精香料有限公司); 荧光素钠(Sigma, 批号BCBV8193);脂多糖(LPS, Sigma, 批号028M4094V); Triton X-100(Sigma, 批号SLBT2255);DMEM培养基(Gibco, 批号2042311);磷酸盐缓冲液(PBS, Corning, 批号26318001);胎牛血清(FBS, Hyclone, 批号DBC0520);人IL-6 ELISA试剂盒(BD, 批号9038994);CCK-8试剂盒(日本同仁化学研究所, 批号PH599)。
VITROCELL Cloud Starter Kit体外细胞暴露系统(德国Vitrocell公司); Heracell VIOS 160i CO2培养箱(德国Thermo Scientific司); BCM-1300A层流超净台(Airtech公司); Vi-cell XR细胞活力测定仪(德国Beckman counter公司); TS100-F倒置相差显微镜(日本Nikon公司); 7020全自动生化分析仪(日本Hitachi公司); SpectraMax M5多功能酶标仪(美国Molecular Devices公司); 12 mm Transwell细胞培养板(美国Corning公司)。
1.3 试验方法 1.3.1 溶液的配制丙三醇溶液:用1% PBS配制成浓度为10%、6%、4%。荧光素钠溶液:取荧光素钠粉末, 用PBS缓冲液配制成浓度为15 mg·L-1的工作溶液。将工作溶液逐级稀释成浓度为0.3, 0.15, 0.075, 0.038, 0.019 mg·L-1的系列标准溶液, 用铝箔包裹避光, 临用现配。Triton X-100溶液:用PBS稀释成0.2%的浓度。LPS溶液:取LPS粉末, 用PBS配制成浓度为1 g·L-1的LPS储备液, 分装后于-20 ℃冻存。临用前, 用DMEM培养基稀释成1 mg·L-1。
1.3.2 云暴露系统递送效率测定云暴露系统主要由暴露室、雾化头、暴露底座和温控水浴四部分组成(Fig 1), 其利用云沉降原理将液滴快速、有效和均匀地沉积到暴露室的底部。通过测定将200 μL荧光素纳溶液(15 mg·L-1)递送至12 mm Transwell小室中的量来表征云暴露系统的递送效率。暴露前, 在每个Transwell小室中加入400 μL PBS, 用于收集雾化的荧光素钠溶液。将暴露室安装在暴露底座上, 同时将雾化头装在暴露室的顶端。取200 μL荧光素钠工作溶液至雾化头中, 启动雾化器, 记录完全雾化200 μL所需的时间。雾化完成后, 关闭雾化器, 等待5 min使气溶胶沉降完全。打开暴露室, 用移液器轻轻吹打混合小室中的液体, 取混合后的液体与荧光素钠系列标准溶液, 分别加入黑色96孔板中, 50 μL/孔, n=4。采用荧光分光光度法(激发波长:483 nm; 发射波长:525 nm)测定荧光强度。以荧光素钠标准溶液的荧光强度值为Y轴, 浓度为X轴, 绘制标准曲线。根据标准曲线回归, 得到各小室中荧光素钠的浓度, 计算沉积在小室中的气溶胶体积。

|
| Fig 1 Schematic diagram of VITROCELLⓇ Cloud Starter Kit aerosol exposure system |
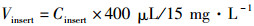
|
其中400 μL和15 mg·L-1分别代表小室中的PBS体积和雾化的荧光素钠溶液的浓度。由此可以计算沉积因子fdep。
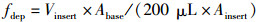
|
Abase和Ainsert分别是暴露底座的面积(92.04 cm2)和Transwell小室的底面积(1.12 cm2); 200 μL是加入雾化头中的荧光素钠溶液的体积。
1.3.3 细胞气液界面培养A549细胞采用含10% FBS的DMEM培养基, 在37 ℃、5% CO2的培养箱中培养。细胞生长至约80%时进行消化传代。将A549细胞以8×105个/mL的密度接种至12 mm Transwell小室中, 顶侧为0.5 mL细胞悬液, 底侧加1.0 mL含10% FBS的DMEM培养基, 培养24 h后, 细胞形成了致密单层。除去细胞顶侧的培养基, 同时将底侧的培养基减少至0.5 mL, 以降低培养基对细胞的压力, 防止培养基从底侧向顶侧渗漏。转换成气-液界面培养, 仅从底侧通过Transwell的膜孔向细胞提供培养基。继续孵育24 h后, 进行气液界面暴露。
1.3.4 丙三醇气液界面暴露细胞气液界面暴露条件与递送效率测定类似, 将云暴露系统放置在生物安全柜中, 并用75%乙醇灭菌, 所有步骤均在无菌条件下操作。暴露前将细胞用PBS洗2次, 放入暴露底座。将200 μL阴性对照溶液(1% PBS)和不同浓度的丙三醇溶液(4%, 6%和10%)分别加入雾化头中, 雾化约持续25 s, 等待5 min让气溶胶在暴露室中逐渐沉降至细胞表面(n=4)。取出细胞, 转移到新的预先加好0.5 mL无血清培养基的12孔板中, 37 ℃下继续孵育24 h。
1.3.5 CCK-8法测定细胞存活率使用CCK-8试剂盒测定细胞存活率。将CCK-8溶液与无血清培养基混合(1 :10), 并加入Transwell小室的顶侧, 200 μL/孔。在37 ℃孵育20 min后, 加入96孔板, 100 μL/孔, 用酶标仪测定450 nm处的吸光度, 计算细胞存活率。
1.3.6 LDH细胞毒性试验通过检测细胞培养基中LDH来评估细胞毒性, 收集培养液, 4 000 r·min-1离心10 min, 上清液用全自动生化仪测定LDH浓度。用0.2%的Triton X-100处理15 min的细胞作为LDH最大释放量的对照(100%)。LDH相对释放量代表样品的细胞毒性, 低于10%认为无细胞毒性。
1.3.7 ELISA测定培养基中的IL-6在Transwell顶侧加入200 μL 1 mg·L-1 LPS溶液, 孵育24 h, 作为阳性对照。ELISA测试前, 阴性对照组和丙三醇各剂量暴露组分别在小室顶侧加入200 μL PBS。将各组小室顶侧与底侧的液体混合后取出, 4 000 r·min-1离心10 min, 取上清液按ELISA试剂盒说明书中的步骤测定培养基中释放的促炎症细胞因子IL-6的含量, 用酶标仪在450/570 nm处测定。
1.3.8 统计学方法采用Microsoft Excel 2010和GraphPad Prism 5软件进行数据计算和作图, 结果表示为x±s。使用SPSS 19统计软件One-way ANOVA分析进行组间比较。
2 结果 2.1 云暴露系统的递送效率通过将200 μL的荧光素钠溶液雾化至Transwell小室中, 分析暴露系统递送的性能, 以下是基于3次雾化的结果。雾化头将200 μL溶液完全雾化约25 s, 输出速率为0.48 mL·min-1。在每个小室中平均沉积1.3 μL的溶液(Fig 2), 相当于厚度11.6 μm的液膜, 两个孔之间差异为5.2%。2个小室共沉积2.6 μL, 考虑到小室仅覆盖暴露室底部表面积的2.4%(=1.12 cm2×2/92.04 cm2×100%), 通过底面积换算, 沉降至暴露底座的溶液体积占所有雾化溶液体积的53.4%, 因此平均沉积因子为(0.534±14.8)%(Fig 3), 其中14.8%代表递送重复性。暴露后静置5 min沉降完全, 即释放速率为0.2 μL/cm2·min-1(=1.3 μL/1.12 cm2/5 min)(Tab 1)。

|
| Fig 2 Deposition volume in each insert(x± s, n=3) |

|
| Fig 3 Deposition factor of each insert(n=3) |
| Fluorin sodium concentration/mg·L-1 | Output rate (mL·min-1) |
Release rate (μL·cm-2 ·min-1) |
sediment yield (μL/孔) |
deposition factor |
| 15 | 0.48 | 0.2 | 1.3 | 0.534 |
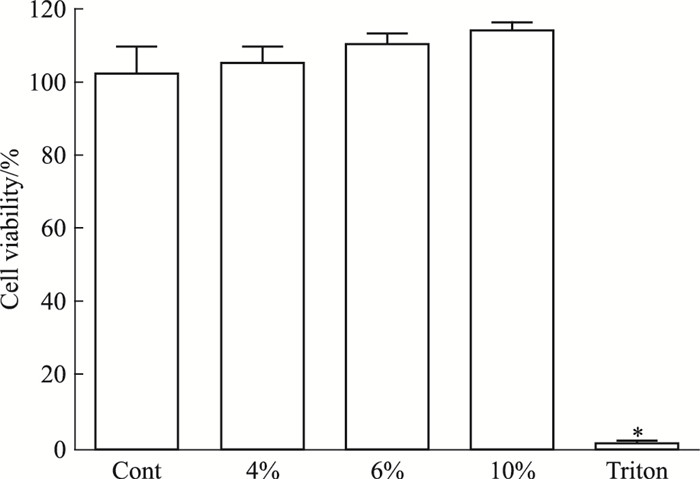
结果显示, 用0.2% Triton X-100裂解细胞作为阳性对照, 与对照组相比存活率显著降低(P < 0.05)。暴露4%、6%和10%的丙三醇后细胞存活率均高于100%, 与对照组相比差异均无显著性, 且随着剂量增加有逐渐升高的趋势(Fig 4)。在本试验条件下, 3种浓度的丙三醇气溶胶均对气液界面培养的A549的存活率无影响。
|
| Fig 4 Cell viability of A549 cells after aerosolized delivery of glycerol at ALI cultures(x±s, n=4) *P < 0.05 vs control |
用0.2% Triton X-100裂解细胞作为阳性对照, 与对照组相比LDH的释放显著增加(P < 0.05)。与对照组相比, 暴露4%, 6%和10%的丙三醇LDH释放量差异无显著性(P>0.05), 且均低于5% (Fig 5)。因此, 在本试验条件下, 3种浓度的丙三醇气溶胶均对气液界面培养的A549均无显著的细胞毒性。

|
| Fig 5 Cytotoxicity of glycerol aerosol in ALI cultures(x±s, n=4) *P < 0.05 vs control |
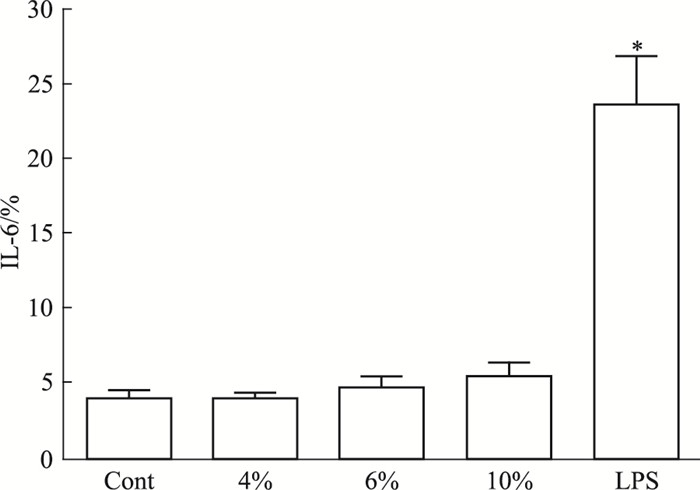
在顶侧加入LPS(1 mg·L-1)作为阳性对照。用云暴露系统分别将4%, 6%和10%的丙三醇溶液雾化至细胞表面, 培养基中的IL-6释放量有随剂量逐渐升高的趋势, 但与对照组相比差异均无显著性(P>0.05)。阳性对照组的IL-6释放量明显增加(P < 0.05)(Fig 6)。
|
| Fig 6 Effect of aerosolized glycerol on expression of IL-6 in A549 cells(x±s, n=4) *P < 0.05 vs control |
迄今为止, 大部分体外细胞毒性试验均是在传统的浸没式培养条件下开展的, 化合物以溶液或混悬液的形式直接加入培养基中, 使细胞浸没在液体环境中[5]。但对于研究可吸入物质对呼吸道的不良反应而言, 需要模拟呼吸道细胞在体内生长的微环境, 再将细胞暴露于化合物气溶胶中。而细胞气液界面培养, 进而通过暴露装置进行气液界面暴露的方式更加接近实际体内呼吸道细胞暴露于化合物气溶胶的状态[13, 14]。人肺腺癌上皮细胞株A549具有肺泡II型上皮细胞的特征, 是体外研究可吸入化合物生物效应的经典模型细胞[15]。
本研究首次应用Vitrocell云暴露系统, 将A549细胞气液界面暴露于丙三醇气溶胶中。细胞在多孔膜上生长, 仅从底侧的培养基中获得营养。试验过程中, 丙三醇溶液雾化形成的气溶胶直接与细胞表面接触, 模拟吸入药物给药或电子烟抽吸的方式, 评估丙三醇气溶胶的细胞暴露安全性。云暴露系统操作简单, 暴露剂量准确, 能够将丙三醇溶液雾化后的气溶胶有效递送至细胞表面。递送效率高(每次暴露仅5 min), 沉积率为53.4%, 重复性(14.8%)和孔间差异(5.2%)等性能良好。
在全面表征系统的递送性能后, 通过CCK-8法考察丙三醇暴露后对细胞存活率的影响, CCK-8试剂中含有WST-8, 它在电子载体的作用下被细胞线粒体中的脱氢酶还原为具有高度水溶性的黄色甲臜产物(formazan), 生成的甲臜物的数量与活细胞的数量成正比。用酶标仪在450 nm波长处测定光吸收值, 可以间接反映活细胞数量。通过暴露后24 h测定释放至底侧培养基中的LDH来评估雾化丙三醇对气液界面培养的A549细胞的毒性, 该酶从细胞质渗出是细胞膜损伤的标志。在本研究的试验条件下, 除阳性对照0.2% Triton X-100外, 所有浓度的丙三醇溶液雾化后均未引起显著的细胞毒性。炎症因子是吸入安全性评价的生物学终点之一, 介导慢性炎症性肺病的发生。其中IL-6是急性和慢性炎症重要的标志物之一, 在全身性炎症和慢阻肺(COPD)的发病机理中起着重要的作用[16]。本研究在暴露后24 h收集培养基并进行ELISA分析, 测定促炎症细胞因子IL-6的释放, LPS作为阳性对照, 来研究暴露丙三醇气溶胶后气液界面培养的A549的炎症反应。在丙三醇暴露后的细胞培养基中, IL-6随剂量的增加略有上升的趋势, 但于阴性对照相比, 差异无统计学意义。
丙三醇暴露后, A549细胞的存活率、细胞毒性、促炎症细胞因子IL-6等指标变化不显著, 可能是由于本研究的暴露时间较短, 仅考察细胞单次暴露之后24 h的毒性反应, 属于丙三醇暴露后的急性反应。因此, 后续研究将进一步开展丙三醇体外细胞重复暴露毒性研究, 以期更全面的评估丙三醇吸入暴露的安全性。
| [1] |
Lewis D A, Young P M, Buttini F, et al. Towards the bioequivalence of pressurised metered dose inhalers 1: design and characterisation of aerodynamically equivalent beclomethasone dipropionate inhalers with and without glycerol as a non-volatile excipient[J]. Eur J Pharm Biopharm, 2014, 86(1): 31-7. doi:10.1016/j.ejpb.2013.02.014 |
| [2] |
Ali M E, Lamprecht A. Spray freeze drying for dry powder inhalation of nanoparticles[J]. Eur J Pharm Biopharm, 2014, 87(3): 510-7. doi:10.1016/j.ejpb.2014.03.009 |
| [3] |
Caponnetto P, Campagna D, Papale G, et al. The emerging phenomenon of electronic cigarettes[J]. Expert Rev Respir Med, 2012, 6(1): 63-74. doi:10.1586/ers.11.92 |
| [4] |
钱伯初, 史红, 吕燕萍. 药理毒理研究的吸入给药实验方法学研究进展[J]. 中国药理学通报, 2006, 22(11): 1285-90. Qian B C, Shi H, Lu Y P. Recent development in expermient methodology for stud ies of inhaled drugs in pharmacology and toxicology[J]. Chin Pharmacol Bull, 2006, 22(11): 1285-90. doi:10.3321/j.issn:1001-1978.2006.11.002 |
| [5] |
Steimer A, Haltner E, Lehr C M. Cell culture models of the respiratory tract relevant to pulmonary drug delivery[J]. J Aerosol Med, 2005, 18(2): 137-82. doi:10.1089/jam.2005.18.137 |
| [6] |
Beyeler S, Chortarea S, Rothen-Rutishauser B, et al. Acute effects of multi-walled carbon nanotubes on primary bronchial epithelial cells from COPD patients[J]. Nanotoxicology, 2018, 12(7): 699-711. doi:10.1080/17435390.2018.1472310 |
| [7] |
Stoehr L C, Endes C, Radauer-Preiml I, et al. Assessment of a panel of interleukin-8 reporter lung epithelial cell lines to monitor the pro-inflammatory response following zinc oxide nanoparticle exposure under different cell culture conditions[J]. Part Fibre Toxicol, 2015, 12: 29. doi:10.1186/s12989-015-0104-6 |
| [8] |
Durantie E, Vanhecke D, Rodriguez-Lorenzo L, et al. Biodistribution of single and aggregated gold nanoparticles exposed to the human lung epithelial tissue barrier at the air-liquid interface[J]. Part Fibre Toxicol, 2017, 14(1): 49. doi:10.1186/s12989-017-0231-3 |
| [9] |
Wang Y, Wu Q, Muskhelishvili L, et al. Assessing the respiratory toxicity of dihydroxyacetone using an in vitro human airway epithelial tissue model[J]. Toxicol In Vitro, 2019, 59: 78-86. doi:10.1016/j.tiv.2019.04.007 |
| [10] |
Lenz A G, Stoeger T, Cei D, et al. Efficient bioactive delivery of aerosolized drugs to human pulmonary epithelial cells cultured in air-liquid interface conditions[J]. Am J Respir Cell Mol Biol, 2014, 51(4): 526-35. doi:10.1165/rcmb.2013-0479OC |
| [11] |
Schmid O, Jud C, Umehara Y, et al. Biokinetics of aerosolized liposomal ciclosporin A in human lung cells in vitro using an air-liquid cell interface exposure system[J]. J Aerosol Med Pulm Drug Deliv, 2017, 30(6): 411-24. doi:10.1089/jamp.2016.1361 |
| [12] |
Schleh C, Kreyling W G, Lehr C M. Pulmonary surfactant is indispensable in order to simulate the in vivo situation[J]. Part Fibre Toxicol, 2013, 10: 6. doi:10.1186/1743-8977-10-6 |
| [13] |
Fulcher M L, Randell S H. Human nasal and tracheo-bronchial respiratory epithelial cell culture[J]. Methods Mol Biol, 2013, 945: 109-21. |
| [14] |
Blank F, Rothen-Rutishauser B, Gehr P. Dendritic cells and macrophages form a transepithelial network against foreign particulate antigens[J]. Am J Respir Cell Mol Biol, 2007, 36(6): 669-77. doi:10.1165/rcmb.2006-0234OC |
| [15] |
黄建华, 李理, 邱娴, 等. 肺泡Ⅱ型上皮细胞A549对TNF-α和LPS的刺激效果研究[J]. 免疫学杂志, 2013, 29(3): 211-5. Huang J H, Li L, Qiu X, et al. Stimulating effects on alveolar typeⅡ epithelial A549 cells by TNF-α and LPS[J]. Immunol J, 2013, 29(3): 211-5. |
| [16] |
Wei J, Xiong X F, Lin Y H, et al. Association between serum interleukin-6 concentrations and chronic obstructive pulmonary disease: a systematic review and meta-analysis[J]. Peer J, 2015, 3: 1199. doi:10.7717/peerj.1199 |

