

2. 山东中医药大学药学院, 山东 济南 250000
代龙(1964-),硕士,教授, 研究方向:中药新制剂、新剂型及中药炮制理论,通讯作者,E-mail:druglab@sina.com
2. School of Pharmacy, Shandong University of Traditional Chinese Medicine, Jinan 250000, China
土鳖虫, 最早记载于《神农本草经》, 为鳖蠊科昆虫地鳖(Eupolyphaga sinensis Walker)及中华冀土鳖(Steleophaga Plancyi Boleny)的干燥雌虫体, 具有活血逐瘀、续筋接骨的功效[1]。现代临床主要用于高血脂、骨折、高尿酸血症等疾病的治疗[2]。土鳖虫富含蛋白质, 经文献报道土鳖虫蛋白质占到总虫体质量的60% [3]。然而, 大分子蛋白无法被人体整体吸收, 需经胃肠道蛋白消化酶的作用转变为小分子活性肽后方能被转运进入人体发挥药效作用。而土鳖虫主要以复方形式经口服给药方式发挥药效作用。因此, 本实验前期基于蛋白质消化原理和土鳖虫给药特点提出以胃蛋白酶、胰蛋白酶为酶介质的体外仿生酶解技术。并采用此技术对土鳖虫蛋白质进行处理得到了土鳖虫生物活性肽(active peptide of Eupolyphaga, APE)。
高脂血症为人体常见代谢性疾病之一, 临床表现为血清甘油三酯(triglyceride, TG)、胆固醇(cho-lesterol, TC)和低密度脂蛋白(low density lipopro-tein, LDL)异常升高; 高密度脂蛋白(high density lip-oprotein, HDL)降低[4-6]。大量临床文献研究肠道菌群的多样性可保证脂质的正常吸收与代谢。高脂血症患者肠道菌群存在不同程度的缺陷。而调整肠道菌群则可降低高脂血症患者血清内的血脂指数。这也说明肠道菌群与高脂血症之间存在紧密联系[7-10]。
土鳖虫作为"活血化瘀"药物已在临床应用千年, 但是APE是否可以调节肠道菌群来改善高脂血症状, 目前未见报道。因此本实验建立饮食性高脂血症SD大鼠模型, 利用16S rDNA方法检测SD大鼠的肠道菌群变化, 探讨APE对肠道菌群多样性以及高脂血症的改善作用。
1 材料与方法 1.1 材料 1.1.1 试剂与仪器土鳖虫经滨州医学院林莺副教授鉴定为鳖蠊科中华冀土鳖的雌虫, 购自山东省长清土元养殖场; 大鼠代谢笼; TC、TG、LDL和HDL生化试剂盒(购自南京建成生物鉴定所提供); ML104型十万分一、ME104E型万分之一天平(梅特勒上海精密仪器公司)、莱卡TD203石蜡包埋机; 美国伯乐T90组织切片机; 250 mL生理盐水(山东鲁抗医药集团)、600 mL去离子水(浙江娃哈哈纯净水公司)、10 L饮用纯净水(济南普利斯饮用水公司)、戊巴比妥钠(国药试剂有限公司)甲醛、磷酸氢二钠、磷酸二氢钠、浓盐酸、氢氧化钠、氯化钠均为分析级; 产自天津富宇化学试剂厂。
1.1.2 实验动物实验用SD大鼠, ♂; 体质量: (180 ~ 200) g, 由山东省朋悦实验动物繁育中心提供, 生产许可证号: SCXK(鲁)20140007。
1.2 实验方法 1.2.1 APE制备取土鳖虫药材500g, 粉粹过80目筛, 加入去离子水5000 mL, 加热煮沸, 保持15 min; 后放凉至40℃, 调pH至1.5;加入5.0g胃蛋白酶, 37℃酶解1 h。再调pH至8.5, 加胰蛋白酶酶解3 h; 酶解完成加热煮沸15 min, 冷却后保存12 h。离心, 取上清液, 得土鳖虫粗酶解液。采用电渗析仪器对土鳖虫粗酶解液进行脱盐实验, 得土鳖虫脱盐液。将土鳖虫脱盐液用3 000 ku超滤膜处理, 得到APE溶液。
1.2.2 肽含量测定 1.2.2.1 标准曲线建立以牛血清白蛋白为对照品, 采用文献报道的folin方法[11]进行肽标准曲线的建立。
1.2.2.2 APE含量取APE溶液50 mL, 冷冻干燥机进行干燥, 得干燥品, 加入适量去离子水溶解。采用"2.2.1"肽标准曲线方法对APE溶液进行肽含量测定。重复6次, 计算平均值。
1.2.3 高脂血症大鼠模型建立 1.2.3.1 造模方法SD大鼠, 60只; 适应性饲养7d, 然后分组, 分别为空白组、模型组、辛伐他汀组、土鳖虫活性高、中、低剂量组, 每组10只。给药剂量为; APE剂量组为1.5、0.75、0.375 g·kg -1。除空白组外, 其他各组大鼠采用特定的高脂饲料进行饲养, 高脂饲料组成为基础饲料65%、猪油15%、胆固醇5%、蛋黄10%、胆汁酸钠5%。持续造模45 d, 于d 46开始, 土鳖虫各组大鼠给予规定剂量药物, 给药15 d后取各组大鼠新鲜粪便, 肝脏, 血清等样品, 所有生物样品保存至-80℃冰箱。
1.2.3.2 检测指标采用石蜡包埋机和冷冻切片机对各组大鼠肝脏进行处理制得肝脏切片, 并结合苏木精-伊红(HE)染色方法制得各组大鼠肝脏病理切片, 在200倍电子显微镜下进行观察。同时采用TG、TC、LDL和HDL生化试剂盒对各组大鼠血清进行测定。通过肝脏病理变化和血脂四项变化判断造模情况。
1.2.3.3 大鼠菌群测定取空白组、模型组、APE高剂量组大鼠新鲜粪便, 提取肠道微生物DNA, 根据序列中的保守区域设计相应引物, 并添加样本特异性Barcode序列, 采用NEB公司的Q5高保真DNA聚合酶对rRNA基因可变区(单个或连续的多个)或特定基因片段进行PCR扩增。PCR扩增产物通过2%琼脂糖凝胶电泳进行检测, 接着采用lllumina公司的TruSeqNano DNA LT Library Prep Kit制备测序文库, 最后使用MiSeq测序仪进行2 × 300 bp的双端测序。
1.2.3.4 数据处理方法应用SMCAP15.1软件(USA; 2016)采用组学数据处理方法进行基于有效数据的OTUs聚类分析, 再对所获得的OTU进行Alpha多样性和Beta多样性计算, 结合t检验, 以P < 0.05为阈值得出代表序列的物种注释、物种信息和基于物种的丰度分布情况。
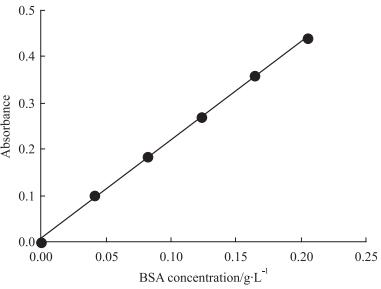
2 结果 2.1 APE含量测定结果以吸光度为纵坐标, 牛血清白蛋白含量为横坐标, 绘制标准曲线, 并计算线性回归方程。线性回归方程为Ŷ = 2.128 3X + 0.007 4, R2 = 0.999 1, 说明线性良好。结果见Fig 1。并采用此方法对APE进行测定, 得出APE溶液内总肽含量达到(71.05 ± 3.10)%, 可以作为活性部位进行下一步实验。
|
| Fig 1 Result of peptide standard curve |
各组大鼠肝脏HE染色病理切片显示:空白组大鼠肝组织结构清晰, 肝小叶结构完整, 肝细胞形态正常, 细胞核染色清晰可见, 同时未见炎细胞浸润、变性、坏死等病理变化。而模型组肝组织结构不完整, 界限不清晰, 肝小叶结构被破坏, 肝细胞排列紊乱, 肝细胞核模糊不清, 肝窦消失, 肝细胞脂滴分布密集, 部分脂滴形成大空泡, 这一结果说明造模后肝细胞出现泡沫化。与模型组比较, 阳性药组肝细胞恢复良好, 肝结构完整, 界限清晰, APE高、中、低剂量组肝脂肪变性程度均有不同程度的改善, 脂滴体积比较小, 大部分肝小叶结构清晰, 肝细胞排列相对整齐。说明APE可以改善脂肪过量摄取引起的肝脏细胞形态变化, 结果见Fig 2。

|
| Fig 2 Pathological results of HE staining A: Blank group; B: Model group; C: Simvastatin group; D: High dose group; E: Middle dose group; F: Low dose group. |
对实验各组大鼠血清中的TG、TC、LDL和HDL进行测定, 结果见Tab 1。由表可知, 长期给予高脂饲料, 模型组大鼠血液内TG、TC和LDL的含量较空白组明显上升, HDL含量则明显降低, 差异具有显著性(P < 0.05, P < 0.01), 说明模型制作成功。阳性药组、辛伐他汀可以明显降低高脂血症大鼠血液内TG、TC、LDL含量, 同时升高HDL含量。APE给药后, 大鼠TG、TC、LDL含量明显下降, 与模型组比较, 差异具有显著性(P < 0.05, P < 0.01)。说明APE可以下调高脂血症大鼠血液内TG、TC、LDL的含量。
| Groups | TG/mmol·L- 1 | TC /mmol·L- 1 | LDL/mmol·L - 1 | HDL/mmol·L- 1 | |
| Blank | 1.011 ± 0.225 | 2.053 ± 0.889 | 1.550 ± 0.412 | 0.194 ± 0.036 | |
| Model | 1.575 ± 0.674# | 5.558 ± 1.290## | 2.639 ± 0.974## | 0.797 ± 0.201## | |
| Simvastatin | 1.097 ± 0.333 ** | 2.253 ± 0.722** | 1.849 ± 0.823* | 0.275 ± 0.224* | |
| High dose | 1.263 ± 0.095 * | 3.844 ± 1.655 ** | 2.059 ± 0.676* | 0.365 ± 0.124* | |
| Middle dose | 1.345 ± 0.103 | 4.102 ± 0.943 5 * | 2.203 ± 0.348* | 0.402 ± 0.348* | |
| Low dose | 1.376 ± 0.073 | 4.509 ± 0.730 2* | 2.401 ± 0.805 * | 0.539 ± 0.738* | |
| #P < 0.05, ##P < 0.01 vs Blank group; *P < 0.05, **P < 0.01 vs Model group | |||||
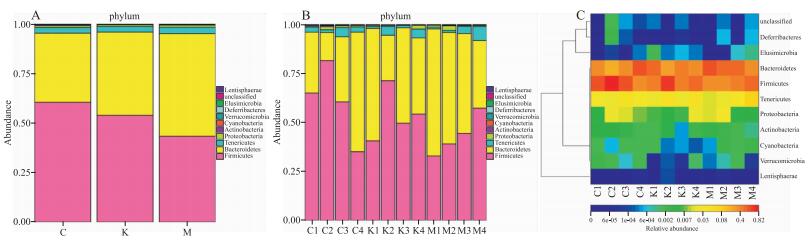
与空白组进行比较, 模型组大鼠肠道内厚壁菌门的相对丰度明显下降, 而拟杆菌门、软壁菌门的相对丰度则明显增加。而经APE干预后, 给药组大鼠肠道内厚壁菌门的相对丰度增加, 而拟杆菌门、软壁菌门的相对丰度显著下降, 见Fig 3。
|
| Fig 3 Relative abundance experimental results of Phylum A: The relative abundance mean results of Phylum; B: The relative abundance results of Phylum with all samples; C: The heatmap results of Phylum. |
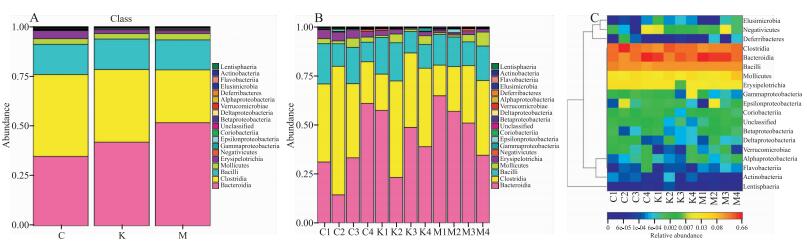
与空白组比较, 模型组大鼠肠道内拟杆菌纲相对丰度则明显上升, 而梭状芽胞杆菌相对丰度明显下降。经APE干预后, 给药组大鼠肠道内双歧杆菌、梭状芽胞杆菌丰度明显升高, 而拟杆菌纲则明显下降, 见Fig 4。
|
| Fig 4 Relative abundance experimental results of Class A: The relative abundance Mean results of Class; B: The relative abundance results of Class with all samples; C: The heatmap results of Class. |
与空白组大鼠进行比较, 模型组大鼠肠道内拟杆菌目、梭菌目相对丰度明显上升, 而乳杆菌目相对丰度明显下降。经APE干预后, 给药组大鼠肠道内乳杆菌目、杆菌目丰度明显升高。而梭菌目、拟杆菌目丰度明显下降, 见Fig 5。

|
| Fig 5 Relative abundance experimental results of Order A: The relative abundance Mean results of Order; B: The relative abundance results of Order with all samples; C: The heatmap results of Order. |
与空白组比较, 模型组大鼠肠道菌群组成发生明显变化, 芽孢杆菌、乳酸杆菌、狄氏副拟杆菌、双歧杆菌明显下降, 而马赛博斯氏菌含量乳酸菌噬菌体含量、旋毛形线虫数量则明显上升, 经APE干预后, 给药组大鼠肠道内乳酸杆菌、芽孢杆菌和双歧杆菌含量明显增加, 而拟杆菌属的产酸菌、马赛博斯氏菌含量则明显下降, 见Fig 6。

|
| Fig 6 Relative abundance experimental results of Species A: The relative abundance Mean results of Species; B: The relative abundance results of Species with all samples; C: The heatmap results of Species. |
本实验基于SD大鼠高脂血症动物研究土鳖虫生物活性肽降血脂和对肠道菌群调节作用, 结果表明, 土鳖虫生物活性肽可明显降低高脂血症大鼠血清内TC、TG、LDL的水平, 升高HDL水平, 这一现象则说明土鳖虫具有明显的降血脂功效。进一步通过16S rDNA高通量测序技术分析各组大鼠肠道菌群分布情况, 此方法可有效弥补传统的微生物体外培养导致的菌落种群丢失以及结构变化等不足。研究结果显示, 模型组大鼠肠道菌群多样性和丰度不同程度降低, 与Martinez等[12]报道一致。给予APE后, 大鼠肠道菌群丰度及多样性均有一定程度改善。Ley等[13]报道正常动物的拟杆菌门相对丰度较肥胖个体显著降低, 结果显示, APE可降低高脂血症大鼠拟杆菌门、软壁菌门丰度。说明APE可以通过降低拟杆菌门、软壁菌门丰度实现对血脂的间接干预。
高脂血症发生时, 肠道中微生物赖以生存的环境将会发生改变, 其理化性质及物质结构的改变则会直接破坏双歧杆菌、乳酸杆菌和肠球菌等有益菌的生长繁殖, 使其数量急剧减少, 而使得拟杆菌和梭菌等革兰氏阴性菌含量增加。有害菌的增加使得肠道产生过氧化炎症因子和脂质抑制因子, 例如脂多糖(LPS)和氧化三甲胺(TMAO) [14-15], 这些因子会直接抑制脂质的氧化代谢, 增加脂质在机体内的堆积。本实验表明, APE可以调节高脂血症大鼠肠道菌群变化, 也可以降低模型大鼠血液内血脂含量, 推测APE可能通过改善肠道菌群种类并抑制相关因子达到干预脂质代谢的作用。后期实验对此机制进行深入研究。
| [1] |
李洪萍.土鳖虫冻干粉对肉兔血脂的调节及SR-BI基因表达的影响[D].长春: 吉林农业大学, 2015. Li H P. Influene of eupolyphaga lyophilized powder on the regula- tion of rabbits′blood lipid and gene expression of SR-B1 [ D ]. Changchun: Jilin Agr Univ, 2015. http://cdmd.cnki.com.cn/Article/CDMD-10193-1015963403.htm |
| [2] |
张震.土鳖虫抗高胆固醇血症模型内参基因筛选及分子机制研究[D].哈尔滨: 东北农业大学, 2019. Zhang Z. Study on evaluation reference genes and molecular mech- anism of anti-hypercholesterolemia model of eupolyphaga steleoph- aga[D]. Harbin: Northeast Agr Uni, 2019. |
| [3] |
汪丽, 王俊淞, 年寅, 等. 土鳖虫的化学成分研究[J]. 昆明理工大学学报(自然科学版), 2016, 41(4): 92-9. Wang L, Wang J S, Nian Y, et al. Chemical constituents from Eupolyphaga Seu Steleophaga[J]. J Kunming Sci Tec(Natural Sci- ence), 2016, 41(4): 92-9. |
| [4] |
Adigun N S, Oladiji A T, Ajiboye T O. Hydro-ethanolic fruit ex- tract of capsicum frutescens reversed triton-X-100-induced hyper- lipidaemia in rats[J]. J D Supplements, 2020, 17(1): 53-66. doi:10.1080/19390211.2018.1482982 |
| [5] |
Magriplis E, Panagiotakos D, Mitsopoulou A V, et al. Prevalence of hyperlipidaemia in adults and its relation to the Mediterranean di- et: the hellenic national nutrition and health examination survey (HNNHS)[J]. Eur J Pre Car, 2019, 26(18): 1957-67. doi:10.1177/2047487319866023 |
| [6] |
胡娟, 汪星辉, 高杉, 等. 肠道菌群在心血管疾病中的作用及其机制研究进展[J]. 中国药理学通报, 2019, 35(11): 1496-500. Hu J, Wang X H, Gao S, et al. Research progress on role andmechanism of gut microbiota in cardiovascular diseases[J]. Chin Pharmacol Bull, 2019, 35(11): 1496-500. doi:10.3969/j.issn.1001-1978.2019.11.004 |
| [7] |
Li H, Liu B, Song J, et al. Characteristics of gut microbiota in patients with hypertension and or hyperlipidemia: A cross-sectional study on rural residents in xinxiang county[J]. Pro Mic, 2019, 7(10): 100399. |
| [8] |
Eid H M, Wright M L, Anil Kumar N V, et al. Significance of microbiota in obesity and metabolic diseases and the modulatory potential by medicinal plant and food ingredients[J]. Fro Phar- macol, 2017, 8(10): 387. |
| [9] |
Wang L, Li C, Huang Q. Polysaccharide from tratt fruit attenuates hyperglycemia and hyperlipidemia and regulates colon microbiota in diabetic mice[J]. J Agr Food Chem, 2020, 68(1): 147-59. doi:10.1021/acs.jafc.9b06247 |
| [10] |
Yuan Y, Liu Q, Zhao F, et al. Polysaccharides ameliorate hyper- lipidemia in high-fat diet-induced rats via short-chain fatty acids production and lipid metabolism regulation[J]. Int J Mol Sci, 2019, 20(19): 4738-47. doi:10.3390/ijms20194738 |
| [11] |
张玲, 石彩文, 肖凯军, 等. 双缩脲法测定罗非鱼源胶原蛋白肽含量的改良及应用评价[J]. 食品科学, 2019, 40(20): 234-40. Zhang L, Shi C W, Xiao K J, et al. Improvement and application of biuret method for determination of collagen peptide from tilapia[J]. Food Sci, 2019, 40(20): 234-40. doi:10.7506/spkx1002-6630-20181118-206 |
| [12] |
Martinez I, Wallace G, Zhang CM, et al. Diet-induced metabolic improvements in a hamster model of hypercholesterolemia are strongly linked to alterations of the gut microbiota[J]. Appl Envi- ron Microbiol, 2009, 75(12): 4175-84. doi:10.1128/AEM.00380-09 |
| [13] |
Ley R E, Turnbaugh P, Klrin S, et al. Microbial ecology Human gut microbes associated with obesity[J]. Nature, 2006, 444(7122): 1022-3. doi:10.1038/4441022a |
| [14] |
Bai C, Liu T, Xu J, et al. Effect of high calorie diet on intestinal flora in LPS-induced pneumonia rats[J]. Sci Reports, 2020, 10(1): 1701. |
| [15] |
Alexandrov P, Zhai Y, Li W. Lipopolysaccharide-stimulated, NF- kB-, miRNA-146a and miRNA-155-mediated molecular-genetic communication between the human gastrointestinal tract microbi- ome and the brain[J]. Folia neuropathologica, 2019, 57(3): 211-9. doi:10.5114/fn.2019.88449 |

