

骨骼疾病致短期或者长期身体疼痛及残疾, 治疗该疾病花费接近全球国民生产总值3% [1]。成骨细胞整个分化过程包括间充质干细胞、前成骨细胞、成熟的成骨细胞、骨细胞。骨形成和骨吸收之间的平衡被打破, 骨吸收的作用大于骨形成, 会导致骨丢失和骨缺损疾病[2, 3]。研究表明, MC3T3-E1成骨前体细胞具有活跃的生物性能, 其增殖和分化对于骨丢失和骨缺损疾病的修复至关重要。
《中国药典》记载, 淫羊藿性辛、甘, 有补肾阳, 祛风湿, 强筋骨的功效。临床主要用于治疗筋骨疲软, 腰背疼痛, 风湿麻痹, 麻木拘挛等, 有最新研究报道[4], 其对小鼠AD模型具有改善作用。Xie等[5]研究表明, 装载有淫羊藿苷(icariin, ICA)的多孔复合支架可以通过成骨诱导和抑制破骨细胞活性促进骨的重建。Gong等[6]在研究人工骨膜促进骨再生的研究中发现淫羊藿苷可以促进MC3T3-E1细胞中碱性磷酸酶(alkaline phosphatase, ALP)活性明显增强, 以及骨钙素(osteocalcin, OC)和Ⅰ型胶原蛋白酶(collagen Ⅰ, Col Ⅰ)表达增加。此外, 在负载淫羊藿苷的纤维基质上培养的MC3T3-E1细胞中钙沉积明显增多, 证明淫羊藿苷可以促进成骨。丁怀利等[7]研究表明, RNAKL/OPG比例的变化在骨质疏松发病中起到重要作用, 淫羊藿苷可以通过调节RANKL/OPG比例延缓了骨丢失随年龄增长而加剧的趋势, 从而有效的防治骨质疏松症。因此, 我们想探究淫羊藿苷对MC3T3-E1成骨细胞的增殖和分化和作用机制, 为中药单体淫羊藿苷治疗骨丢失疾病提供药理基础, 以期更好的改善骨组织受损患者的生存质量。
1 材料与方法 1.1 试剂和抗体试剂:淫羊藿苷中药对照样品购自成都德思特生物技术有限公司, HPLC级(≥ 98%); Alpha-MEM培养基、青霉素-链霉素溶液购自HyClone公司; 胎牛血清和二甲基亚砜(dimethyl sulfoxide, DMSO)购自重庆博培生物科技有限公司; CCK-8试剂盒购自Genview公司; BCA蛋白浓度测定试剂盒、Western blot凝胶试剂盒均购自碧云天公司。抗体: β-actin抗体(Bioss, 批号: bs-0061R); os- teocalcin抗体(Bioss, 批号: bs-4917R); ALP抗体(Bimake, 批号: A5111); Shh抗体(Bimake, 批号: A5115)。
1.2 细胞培养和成骨诱导MC3T3-E1小鼠胚胎成骨细胞前体细胞在含有10%胎牛血清和抗生素(1 × 102 U·L-1青霉素和100 mg·L-1链霉素)的α-MEM中生长, 每3 d更换一次成骨培养基即10 -8 mol·L-1地塞米松, 50 mg·L-1抗坏血酸和10 mmol ·L-1 β-甘油磷酸盐的培养基, 在37 ℃含有5% CO2的饱和湿度培养箱中生长。
1.3 茜素红染色α-MEM(10 -8 mol·L-1地塞米松, 50 mg·L-1抗坏血酸, 10 mmol·L-1 β-甘油磷酸)诱导成骨分化。细胞诱导14 ~ 21 d后, 4%甲醛固定细胞。40 mmol·L-1茜素红S(pH 4.4)室温染色10 min。10 mmol· L-1磷酸钠(pH 7.0), 10% cetylpyridinium chloride(sigma)处理细胞, 562 nm测量吸光度值。
1.4 ALP活性检测PBS洗涤MC3T3-E1细胞, 超声破碎。37 ℃孵育1 min, 405 nm波长检测吸光度值。碱性磷酸酶测定试剂盒购自中生北控生物科技有限公司, 批号: 160611。
1.5 CCK-8检测MC3T3-E1细胞以5 × 104个/孔细胞接种到96孔板中, 重复实验3次。然后建立对照组和药物组, 细胞随机分为6组:对照组, 2.5、5、10、20和40 μmol·L-1, CCK-8测定。培养1、3和5 d后, 加入10 μL CCK-8。37 ℃孵育3 h检测490 nm吸光度。
1.6 Western blot检测用裂解缓冲液(RIPA : PMSF = 1 000 : 1)裂解细胞, 然后置冰上30 min。4 ℃, 12 000 g离心10 min, 取上清液进行蛋白质浓度测定。通过8% ~ 10% SDS-PAGE凝胶分离等量的蛋白质, 转移至PVDF膜, 用TBST(10 mmol·L-1 Tris-HCL, 150 mmol·L-1 NaCl, 0.05% Tween-20, pH 7.6)溶解5%脱脂奶粉封闭1.5 h。分别用PBST稀释ALP、OC和Shh一抗(1 : 1 000), 4 ℃孵育过夜然后与HRP标记对应的二抗(1 : 3 000)孵育。ECL化学发光系统显色, 使用ImageJ软件分析结果。
1.7 统计学分析数据统计采用SPSS 17.0统计软件完成, 计量资料以x ± s表示, 组间比较采用t检验和单因素方差分析。
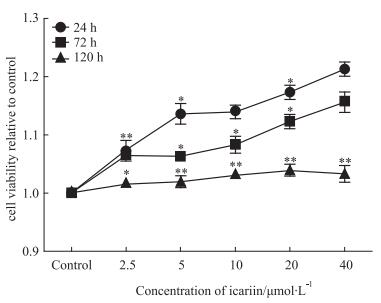
2 结果 2.1 淫羊藿苷促进MC3T3-E1细胞增殖分别用2.5、5、10、20、40 μmol·L-1 ICA处理MC3T3-E1细胞24、72、120 h, CCK-8检测细胞增殖。结果显示, 2.5 ~ 40 μmol·L-1 ICA处理组的吸光度值均较对照组高, 差异具有统计学意义(P < 0.05)。说明ICA促进细胞增殖。
|
| Fig 1 Effects of icariin on proliferation in MC3T3-E1 cells detected by CCK-8 assay(x ± s, n = 3) * P < 0.05, *P < 0.01 vs control |
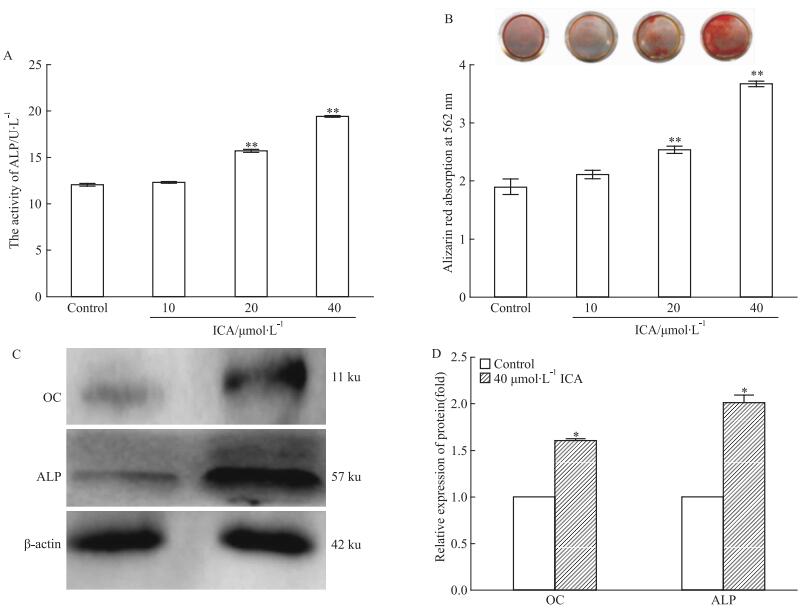
各组MC3T3-E1细胞分别用不同浓度的ICA处理后, 成骨诱导3 d检测ALP活性。结果显示, 20 μmol·L-1 ICA处理组和40 μmol·L-1 ICA处理组的ALP活性明显高于对照组(Fig 2A)。但是10 μmol·L-1 ICA处理组的ALP活性相比对照组, 差异并没有统计学意义。可能是因为低浓度的ICA处理并不能引起明显的ALP活性改变, ICA促进成骨是剂量依赖性的, 在一定范围内高浓度ICA能引起成骨分化相关指标的显著改变。所以我们后续实验选择40 μmol·L-1 ICA作为最佳实验浓度。AR-S结果表明, 20 μmol·L-1 ICA处理组和40 μmol·L-1 ICA处理组比对照组的橘红色沉积(钙结节)明显增多(P < 0.01), 说明ICA促进MC3T3-E1成骨细胞前体细胞钙结节的形成从而促进成骨分化(Fig 2B)。与对照组相比, 40 μmol·L-1 ICA作为最佳实验药物浓度处理3 d后发现OC和ALP蛋白表达也明显增高(P < 0.05), 提示ICA对成骨分化的标志基因起促进作用(Fig 2C, 2D)。这些结果表明, ICA可以加速MC3T3-E1细胞的成骨分化和矿化。同时, ALP和OC蛋白表达增加, 表明ICA可以在早期和成熟阶段促进成骨分化。
|
| Fig 2 Icariin promotes osteoblast differentiation in MC3T3-E1 cells(x ± s, n = 3) A: MC3T3-E1 cells were treated with Icariin(10, 20, or 40 μmol·L-1) or control, and further induced with osteogenic for 7 days, and then ALP activity in those cells was examined. B. MC3T3-E1 cells were treated with Icariin and further induced with osteogenic media for 21 days, and then those cells were subjected to Alizarin Red staining. Representative images were shown and quantitative mineralization levels were calculated. C. MC3T3-E1 cells were treated with 40 μmol·L-1 ICA or PBS as control, and further induced with osteogenic media for 3 days, and then cells were harvested for Western blot. D. Quantitation analysis of ALP and OC protein levels in Western blot(* P < 0.05, **P < 0.01 vs control group) |
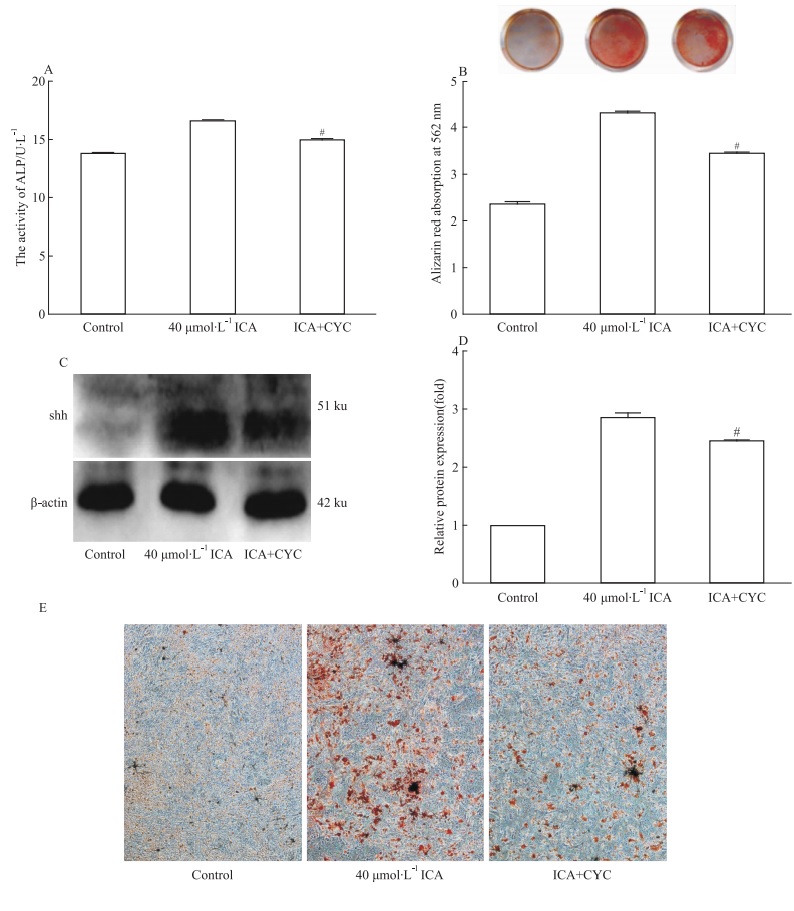
Hedgehog信号通路是参与成骨分化的关键通路。为了探究其是否参与调控淫羊藿苷促进成骨分化的进程, 加入5 μmol·L-1 Cyclopamine(CYC), (Hedgehog通路的拮抗剂)。与40 μmol·L-1 ICA处理组相比, ICA + CYC处理组ALP活性降低(P < 0.01, Fig 3A)。在成骨诱导的d 21, 进行AR-S检测钙沉积物。与40 μmol · L-1 ICA组相比, ICA + CYC处理组细胞钙沉积物数量减少(P < 0.01, Fig 3B)。这些结果表明CYC抑制ICA增强成骨分化。40 μmol·L-1 ICA组中shh蛋白表达量增加, ICA + CYC组明显降低(P < 0.01, Fig 3C, D)。这些结果说明ICA促进MC3T3-E1细胞的成骨分化, 这一过程至少部分由Hedgehog信号通路调节。与40 μmol ·L-1 ICA处理组相比, 加入CYC能够明显的降低钙结节(Fig 3E)。
|
| Fig 3 CYC inhibits osteoblast differentiation resulting from treating ICA in MC3T3-E1 cells(x ± s, n = 3) A: The MC3T3-E1 cells were treated with control, or 40 μmol·L-1 alone or the combination of 40 μmol·L-1 ICA and 5 μmol·L-1 Hedgehog pathway antagonist CYC and further induced with osteogenic media for 7 days, and then ALP activity in those cells was examined; B: The scanned images of Alizarin Red staining and quantitative mineralization levels; C: The MC3T3-E1 cells were treated with control, 40 μmol·L-1 Icariin alone or combina-tion of 40 μmol·L-1 Icariin and 5 μmol·L-1 CYC and further induced with osteogenic media for 3 days, and then those cells were harvested for West-ern blot; D: Quantitative analysis of shh protein level from Western blot; E: The images of microscopic calcium nodules by Alizarin Red staining in the MC3T3-E1 cells(100 ×). (# P < 0.05 vs 40 μmol·L-1 ICA group) |
淫羊藿苷分子量: 676.65, 化学式: C33H40O15, 是从淫羊藿中提取的植物雌激素和类黄酮化合物, 被亚洲国家广泛用于治疗骨质疏松症。之前的研究表明它可以有效预防绝经后期妇女的骨质疏松症[8-10]。MC3T3是C57BL/6乳鼠源性的成骨细胞, E1指的是它的亚属, 属于前成骨细胞系, 已成为整形外科和组织工程研究的热点。此外一些研究发现, 某些骨恶性肿瘤的发生、发展和转移也与成骨细胞密切相关[10]。成骨细胞增殖和分化对于骨重建过程中骨形成至关重要[11]。ALP是骨形成早期基因, 在骨基质矿化中起重要作用[12]。OC是一种可以与钙结合并促进矿物晶体形成从而开始矿化的糖蛋白, 在骨形成过程中由成骨细胞分泌[13]。有研究表明10 -7 ~ 10 -5 mol·L-1ICA干预在成骨细胞-破骨细胞共培养系统中可以增强成骨细胞的成骨分化作用[14]。本实验采用ICA处理MC3T3-E1细胞, 与对照组相比, 20 μmol·L-1 ICA处理组和40 μmol ·L-1 ICA处理组的ALP活性明显增加, 表明ICA可以在骨形成的早期阶段促进成骨细胞的成熟。此研究结果表明, ICA可以明显地促进成骨细胞前体细胞MC3T3-E1的增殖和成骨分化。
Hedgehog信号通路是参与动物胚胎发育最重要的信号通路之一, 并且在出生后的组织修复、组织稳态、细胞增殖等多种生理和病理过程中发挥重要作用。哺乳动物中的3个hedgehog基因, 包括Sonic hedgehog (Shh)、Indian hedgehog (Ihh)和Desert hedgehog(Dhh)。已经证明, Ihh和Shh均可以通过Runx2加速间充质祖细胞的成骨分化[16]。在我们的研究中, 与40 μmol·L-1 ICA处理组相比, ICA + CYC处理组中Hedgehog信号通路关键基因shh的蛋白表达量明显下调且ALP活性和矿化能力下降。ICA主要通过调节一些Hedgehog信号通路靶基因的转录, 从而促进成骨细胞分化。此外CYC可以显著抑制ALP活性和shh蛋白表达量。在形态学上, 我们也观察到CYC明显抑制矿化结节数量。结果表明Hedgehog信号通路介导ICA促进MC3T3-E1细胞成骨分化。
综上, 研究结果表明, ICA在成骨细胞的分化中起重要作用, 主要通过Hedgehog信号通路发挥促进成骨分化的作用, 对成骨细胞分化和增殖促进作用为骨质疏松症的治疗提供了新的思路和方向。我们还需要完善动物实验来验证这一作用, 并最终将其应用于骨丢失和骨损伤疾病的临床治疗。
| [1] |
Harvey N, Dennison E, Cooper C. Osteoporosis: impact on health and economics[J]. Nat Rev Rheumatol, 2010, 6(2): 99-105. |
| [2] |
Rodan G A. Control of bone formation and resorption: biological and clinical perspective[J]. J Cell Biochem Suppl, 1998, 30(31): 55-61. |
| [3] |
Rachner T D, Khosla S, Hofbauer L C. Osteoporosis: now and the future[J]. Lancet, 2011, 377(9773): 1276-87. doi:10.1016/S0140-6736(10)62349-5 |
| [4] |
马冬雪, 董贤慧, 贺小平, 等. 淫羊藿、黄芪、葛根有效组分复方对APPswe /PS1dE9双转基因AD模型小鼠海马CA3区hepci- din表达的影响[J]. 中国药理学通报, 2019, 35(11): 1523-7. Ma D X, Dong X H, He X P, et al. Effects of active components of Epimedium, Astragalus and Radix Puerariae on expression of hepcidin in hippocampus CA3 in APPswe /PS1dE9 double trans- genic Alzheimer's disease model mice[J]. Chin Pharmacol Bull, 2019, 35(11): 1523-7. doi:10.3969/j.issn.1001-1978.2019.11.009 |
| [5] |
Xie Y, Sun W, Yan F, et al. Icariin-loaded porous scaffolds for bone regeneration through the regulation of the coupling process of osteogenesis and osteoclastic activity[J]. Int J Nanomedicine, 2019, 14: 6019-33. doi:10.2147/IJN.S203859 |
| [6] |
Gong M, Chi C, Ye J, et al. Icariin-loaded electrospun PCL/gelatin nanofiber membrane as potential artificial periosteum[J]. Colloids SurfB Biointerf aces, 2018, 170: 201-9. doi:10.1016/j.colsurfb.2018.06.012 |
| [7] |
丁怀利, 吴银生, 林煜, 等. 鼠成骨细胞RANKL-OPG mRNA表达的增龄性变化及淫羊藿甙的干预作用[J]. 中医正骨, 2010, 22(4): 7-10. Ding H L, Wu Y S, Lin Y, et al. Changes with age and effect of Icariin on genetic expression of RANKL-OPG in rat′s osteoblasts[J]. J Tradit Chin Orthopedics Tr, 2010, 22(4): 7-10. doi:10.3969/j.issn.1001-6015.2010.04.002 |
| [8] |
Tang D, Ju C, Liu Y, et al. Therapeutic effect of icariin combined with stem cells on postmenopausal osteoporosis in rats[J]. J Bone Miner Metab, 2018, 36(2): 180-8. doi:10.1007/s00774-017-0831-x |
| [9] |
Liu Y, Zuo H, Liu X, et al. The antiosteoporosis effect of icariin in ovariectomized rats: a systematic review and meta-analysis[J]. Cell Mol Biol(Noisy-le-grand), 2017, 63(11): 124-31. doi:10.14715/cmb/2017.63.11.22 |
| [10] |
Li G W, Xu Z, Chang S X, et al. Icariin prevents ovariectomy-in- duced bone loss and lowers marrow adipogenesis[J]. Menopause, 2014, 21(9): 1007-16. doi:10.1097/GME.0000000000000201 |
| [11] |
Lamoureux F, Baud′huin M, Rodriguez Calleja L, et al. Selective inhibition of BET bromodomain epigenetic signalling interferes with the bone-associated tumour vicious cycle[J]. Nat Commun, 2014, 5: 3511. doi:10.1038/ncomms4511 |
| [12] |
Eleniste P P, Patel V, Posritong S, et al. Pyk2 and megakaryo- cytes regulate osteoblast differentiation and migration via distinct and overlapping mechanisms[J]. J Cell Biochem, 2016, 117(6): 1396-406. doi:10.1002/jcb.25430 |
| [13] |
Gauthier P, Yu Z, Tran Q T, et al. Cementogenic genes in human periodontal ligament stem cells are downregulated in response to osteogenic stimulation while upregulated by vitamin C treatment[J]. Cell Tissue Res, 2017, 368(1): 79-92. doi:10.1007/s00441-016-2513-8 |
| [14] |
Niu Y B, Kong X H, Li Y H, et al. Radix Dipsaci total saponins stimulate MC3T3-E1 cell differentiation via the bone morphogenet- ic protein-2 /MAPK/Smad-dependent Runx2 pathway[J]. Mol Med Rep, 2015, 11(6): 4468-72. doi:10.3892/mmr.2015.3249 |
| [15] |
Zhang S, Feng P, Mo G, et al. Icariin influences adipogenic dif- ferentiation of stem cells affected by osteoblast-osteoclast co-culture and clinical research adipogenic[J]. Biomed Pharmacother, 2017, 88: 436-42. doi:10.1016/j.biopha.2017.01.050 |
| [16] |
Huang C, Tang M, Yehling E, et al. Overexpressing sonic hedge- hog peptide restores periosteal bone formation in a murine bone al- lograft transplantation model[J]. Mol Ther, 2014, 22(2): 430-9. doi:10.1038/mt.2013.222 |

