


2. 中山大学药学院药理与毒理学实验室, 广东 广州
廖英勤(1993-), 女, 硕士生, 研究方向:心血管药理共同第一作者, E-mail: 13557536177@163.com。
 ,
LIAO Ying-qin1
,
LIAO Ying-qin1 ,
ZHONG Xiao-yi1,
MA Zhi-chao1,
LIU Pei-qing2,
LU Jing2,
ZANG Lin-quan1,
ZHOU Si-gui1
,
ZHONG Xiao-yi1,
MA Zhi-chao1,
LIU Pei-qing2,
LU Jing2,
ZANG Lin-quan1,
ZHOU Si-gui1

2. Dept of Pharmacology and Toxicology, School of Pharmaceutical Sciences, Sun Yat-sen University, Guangzhou 510006, China
心力衰竭是指心脏舒缩功能障碍, 无法满足机体生命活动需要时产生的疾病[1-2]。心力衰竭机制包括心肌肥厚、心肌纤维化、氧化应激、能量代谢、神经体液因素等[3-5]。得益于日益改善的心血管疾病治疗策略的运用, 心力衰竭的病死率明显下降。但心力衰竭的发病机制与年龄密切相关, 随着人口老龄化的进程, 心力衰竭的发病率正不断增长, 每年因此死亡的人数并没有明显减少。因此, 寻找新的心力衰竭治疗方法, 显得尤为重要。
短链酰基辅酶A脱氢酶(short-chain acyl-CoA dehydrogenase, SCAD)是酰基辅酶A脱氢酶家族的一员, 能特异性地分解短链酰基辅酶A底物, 是线粒体脂肪酸β氧化的第一个限速酶[6]。我们首次发现了SCAD在自发性高血压大鼠心肌肥厚中的表达明显下调[7]。进一步研究显示, 在慢性心力衰竭大鼠、心肌梗死后心力衰竭大鼠以及心肌细胞凋亡模型中, SCAD的表达均出现了显著下调[8-10]。以上研究表明, SCAD对心力衰竭具有负性调控作用。然而SCAD重组腺病毒对心力衰竭大鼠是否具有保护作用, 尚不清楚。
本研究以大鼠冠状动脉左前降支结扎术(left anterior descending coronary artery, LAD)构建大鼠心肌梗死后心力衰竭模型, 将SCAD重组腺病毒注射到心尖室壁方向, 使SCAD蛋白特异性过表达。探讨在急性病理应激情况下, SCAD重组腺病毒对心力衰竭大鼠心脏功能和线粒体能量代谢的影响。
1 材料 1.1 实验动物与试剂SD大鼠, ♂, 体质量(210 ± 20) g, 购自南方医科大学动物中心。许可证号: SCXK(粤)2017-0041。SCAD重组腺病毒、GFP空载体腺病毒(汉恒生物), SYBR (DRR420S) (大连TaKaRa, 批号: AJ12457A)、SCAD酶活性试剂盒(上海杰美生物, 批号: 1-2018412-10), 单克隆兔抗SCAD (Abcam, 批号: GR117677-4), 单克隆鼠抗GAPDH(ProteinTech, 批号: 60004-1-1g)。
1.2 仪器血压计(美国KENT), 化学发光仪(上海勤翔), 冷冻离心机(广州湘仪), - 80 ℃超低温冰箱(中科都菱), 酶标仪(Thermo), 荧光定量PCR仪(Bio-Rad)
2 方法 2.1 大鼠心肌梗死后心力衰竭模型的构建大鼠适应性饲养1周, 禁食12 h, 采用LAD术构建急性心力衰竭大鼠模型将大鼠麻醉后, 通过喉咙进行气管插管术, 连接小动物呼吸机维持呼吸。于大鼠胸部沿左侧第三、第四肋间隙打开并结扎左冠状动脉, 结扎完成后迅速分层缝合胸壁。Sham组方法同上, 但开胸穿线后扎松结。
2.2 重组腺病毒介导的SCAD在大鼠心脏特异性过表达模型的构建按随机数字表法将动物分组为: Sham + NS组、LAD + NS组、Sham + Ad-GFP组、Sham + Ad-SCAD组、LAD + Ad-GFP组、LAD + Ad-SCAD组, 共6组。对大鼠心脏开胸进行LAD术的同时, 采用1-guage针头注射器, 吸取纯化后的重组腺病毒颗粒(Ad-SCAD: 5.596 × 10[11] Viral particles, Ad-GFP: 5.596 × 1011 Viral particles), 在结扎部位往下(心尖方向)心室壁多点注射重组腺病毒颗粒(100 μL, 3 ~ 5处)。各组大鼠常规饲养6周。
2.3 鼠尾动脉收缩压测定采用无创血压仪(CA- DA Monitor, 美国KENT公司)测定各组大鼠尾动脉收缩压(systolic blood pressure, SBP), LAD术前测量1次, 术后每2周测量1次, 直至第6周结束。
2.4 超声心动图检查重组腺病毒注射6周后, 采用戊巴比妥钠麻醉大鼠, 采用超声心动图检测大鼠心功能的变化, 取M超曲线, 分别测量大鼠的心脏博出量(cardiac output, CO)、心脏每博输出量(stroke volume, SV)、收缩末期左心室内径(left ventricular dimensions at end systole, LVIDs)、舒张末期左心室内径(left ventricular dimensions at end diastole, LVIDd)、收缩末期左心室容积(left ventricular end systolic volume, LVESV)、舒张末期左心室容积(left ventricular end diastole volume, LVEDV)、心脏射血分数(ejection fraction, EF)和心脏的缩短分数(fractional shortening, FS)。
2.5 动物取材各组大鼠常规饲养6周后, 禁食12 h, 3%戊巴比妥钠经腹腔注射麻醉, 经腹主动脉取血, 静置后分离血清, 液氮速冻置于-80 ℃保存。取血后取出心脏。部分心脏组织经液氮速冻后- 80 ℃保存进行后续实验, 部分心脏经4%多聚甲醛固定进行石蜡包埋切片, 剩余部分心脏组织进行冰冻切片。
2.6 活性氧含量测定部分心脏组织进行冰冻切片, 二氢乙啶(dihydroethidium, DHE)染色使活性氧(reactive oxygen species, ROS)呈红色荧光, 观察产生的红色荧光, 分析ROS在心脏的产生情况。
2.7 心肌组织形态学检查心脏组织多聚甲醛定, 进行石蜡包埋切片, 进行Masson染色及TUNEL染色。Masson染色后心肌纤维呈红色, 胶原纤维呈蓝色, 借此得出大鼠心脏是否出现心肌纤维化以及纤维化的严重程度。采用TUNEL染色法检测心肌细胞凋亡情况并计算凋亡指数。
2.8 线粒体膜肿胀程度检测采用组织线粒体纯化试剂盒提取大鼠心肌组织线粒体。采用酶标仪测定钙诱导的线粒体膜通透性转换孔(mitochondrial permeablity transition pore, mPTP)的开放程度。应用BCA试剂盒测定线粒体蛋白含量。线粒体反应缓冲液组分为150 mmol·L-1 KCl、10 mmol·L-1 Tris、20 mmol · L-1 MOPS、5 mmol · L-1 KH2PO4 (pH7.4)), 以线粒体在540 nm波长处A值的下降幅度(A值变化的量ΔA与初始A值之比, 即ΔA /A)表示大鼠心肌组织线粒体膜肿胀程度, 结果用百分数表示来评价。
2.9 ATP含量测定根据荧光素酶需要消耗ATP催化产生萤光素的原理, 检测心肌组织匀浆中的ATP浓度。实验操作严格按照说明书进行。
2.10 SCAD酶活性检测采用分光光度法检测SCAD酶活性。实验操作严格按照SCAD酶活性检测试剂盒说明书进行。
2.11 游离脂肪酸含量检测采用ELISA法测定大鼠心肌和血清游离脂肪酸含量。具体操作严格按照试剂盒说明书进行。
2.12 Western blot分析提取心脏组织总蛋白后, 采用BCA蛋白定量试剂盒测定570 nm波长处的OD值, 代入标曲进行蛋白定量。配制SDS-PAGE凝胶, 上样, 电泳, 条件为:浓缩胶70 V, 30 min, 分离胶110 V, 60 min。按照典型的"三明治"法进行转膜, 转膜条件: 230 mA恒流, 90 min。转膜结束后洗膜并封闭, 条件为: 5% BSA溶液, 1 h。一抗: SCAD抗体(1 : 1 000)、GAPDH抗体(1 : 1 000), 4 ℃孵育过夜。二抗:兔抗(1 : 10 000)、鼠抗(1 : 10 000)室温孵育1 h, TBST洗膜。采用化学发光仪进行显影。
2.13 Real-time PCR采用TRIzol裂解法提取心肌中总RNA, 通过紫外分光光度计测定总RNA样品纯度并计算出RNA浓度。采用RT-PCR试剂盒(TaKaRa)逆转录后合成cDNA。按照SYBR Green试剂盒说明书配制Real-time PCR反应体系。引物由上海生工合成, 具体引物序列见Tab 1。
| Name | The primer sequence(5′-3′) | Product(bp) |
| SCAD | Forward: CCAGTCTGTGGAACTACCTGAG | 22 |
| Reverse: CCCTTCTTCTTCACCTGCGA | 20 | |
| GAPDH | Forward: AGGAGTAAGAAACCCTGGA | 20 |
| Reverse: CTGGGATGGAATTGTGAG | 18 |
以上所得的数据均采用x ± s表示, 数据的统计和分析均使用SPSS 25.0统计分析软件采用单因素方差分析和t检验。
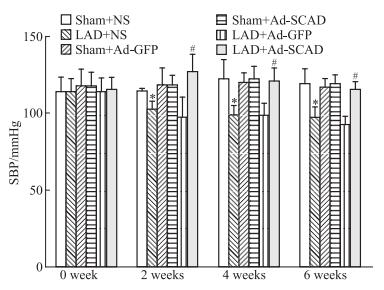
3 结果 3.1 各组大鼠血压比较由Fig 1所示, 与Sham + NS组相比, LAD + NS大鼠呈持续性低血压状态; 与LAD + NS组相比, LAD + Ad-SCAD组术后第2周SBP明显上升(p < 0.05), 第4周和第6周的SBP同样明显上升(均p < 0.05), 但较第2周有所降低, 可能与术后心力衰竭的时间进程有关。表明SCAD重组腺病毒心肌过表达能改善心力衰竭大鼠持续低血压状态。
|
| Fig 1 Comparison of systolic blood pressure(SBP) of rats in each group(x ± s, n = 5) * p < 0.05 vs Sham + NS group; # p < 0.05 vs LAD + NS group |
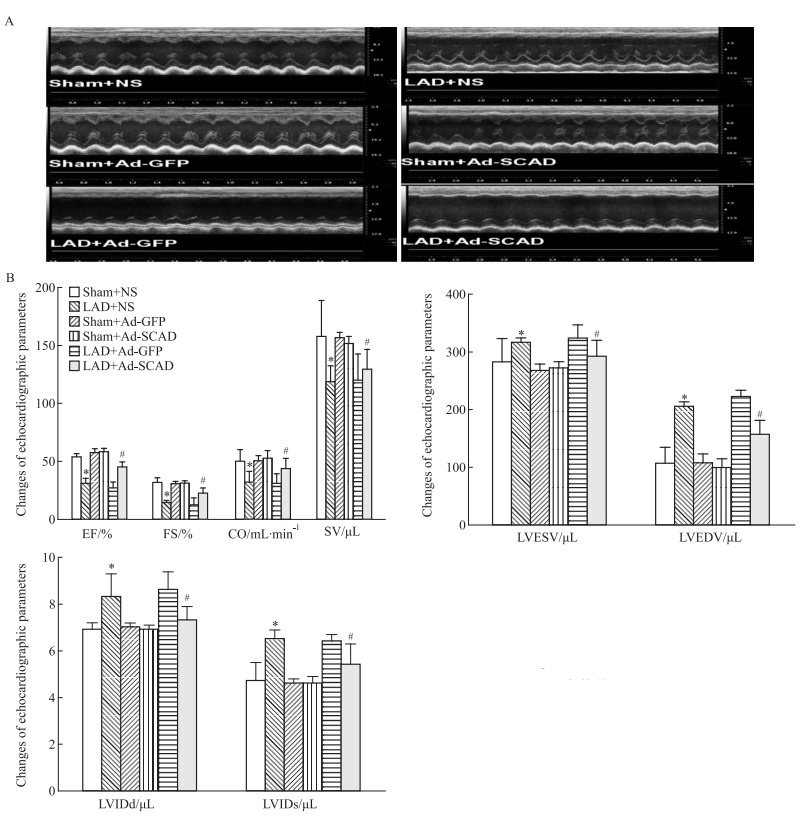
由Fig 2A所示, Sham + NS组、Sham + Ad-GFP组、Sham + Ad-SCAD组左室前、后壁的舒缩功能正常, 组间差异无显著性; LAD + NS组和LAD + Ad-GFP组左心室前壁的舒缩功能基本丧失, 心室腔明显增大; 而LAD + Ad-SCAD组, 左心室前壁舒缩功能同样受损严重, 但尚有微弱的舒缩功能, 心室腔增大, 但较LAD + NS组有所改善。由Fig 2B所示, 与Sham组比较, LAD + NS组CO、SV、LVEF和FS均明显减小(p < 0.05), LVIDd、LVIDs、LVEDV、LVESV明显增大, 表明LAD术后6周大鼠心脏的收缩/舒张功能严重受损, 心脏泵血功能严重障碍, 心功能明显下降, 发展为严重的心力衰竭; 而与LAD + NS组相比, LAD + Ad-SCAD组CO、SV、LVEF和FS明显升高(均p < 0.05), LVIDd、LVIDs、LVEDV、LVESV明显降低。以上结果表明, SCAD重组腺病毒过表达能明显延缓LAD术后心力衰竭的进程, 大鼠的心功能得到很大提升, 心脏收缩功能得到明显改善。
|
| Fig 2 Echocardiographic changes(x ± s, n = 3) A: Echocardio-graphic detection B: Changes of echocardiographic parameters. * p <0.05 vs Sham + NS group; # p < 0.05 vs LAD + NS group |
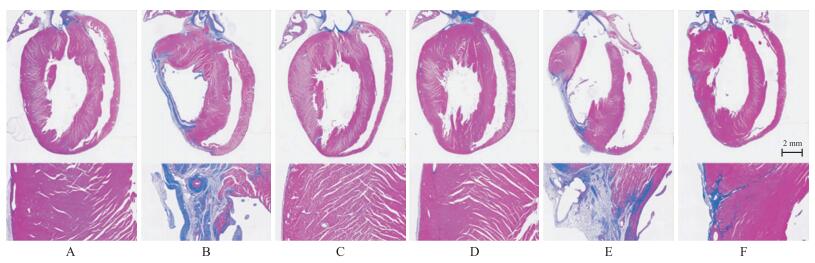
由Fig 3 Masson染色所示, 心肌纤维呈红色, 胶原纤维呈蓝色。Sham + NS组、Sham + Ad-GFP组、Sham + Ad-SCAD组均无明显心肌纤维化; LAD + NS组和LAD + Ad- GFP组左心室前壁结扎位置以下心尖部位出现明显的心肌纤维化, 室壁变薄, 室壁组成只有少量红色的心肌细胞, 基本由蓝色的心肌纤维构成。而LAD +Ad-SCAD组, 左心室前壁结扎位置以下心尖部位出现部分心肌纤维化现象, 梗死区域胶原沉积明显减少, 心肌纤维化明显改善。
|
| Fig 3 Masson staining analysis A: Sham + NS group; B: LAD + NS group; C: Sham + Ad-GFP group; D: Sham + Ad-SCAD group; E: LAD + Ad-GFP group; F: LAD + Ad-SCAD group |
由Fig 4 TUNEL染色结果显示, 凋亡细胞呈棕褐色。其中Sham + NS组、Sham + Ad-GFP组有部分凋亡细胞, 属正常现象; Sham + Ad-SCAD组心肌细胞凋亡有所减少; LAD + NS组和LAD + Ad-GFP组左心室前壁结扎位置以下心尖部位出现大量的心肌细胞凋亡, 凋亡指数明显高于Sham组(均p< 0.05)。与LAD + NS组相比, LAD + Ad-SCAD组左心室前壁结扎部位以下心尖部位出现部分的心肌细胞凋亡情况得到明显的改善, 心肌细胞凋亡明显减少, 凋亡指数明显下降(p < 0.05)。

|
| Fig 4 Light microscopic observation of myocardial cell apoptosis in rat TUNEL staining(200 ×)(x ± s, n = 3) A: Sham + NS; B: LAD + NS; C: Sham + Ad-GFP; D: Sham + Ad-SCAD; E: LAD + Ad-GFP; F: LAD + Ad-SCAD. * p < 0.05 vs Sham + NS group; # p < 0.05 vs LAD + NS group |
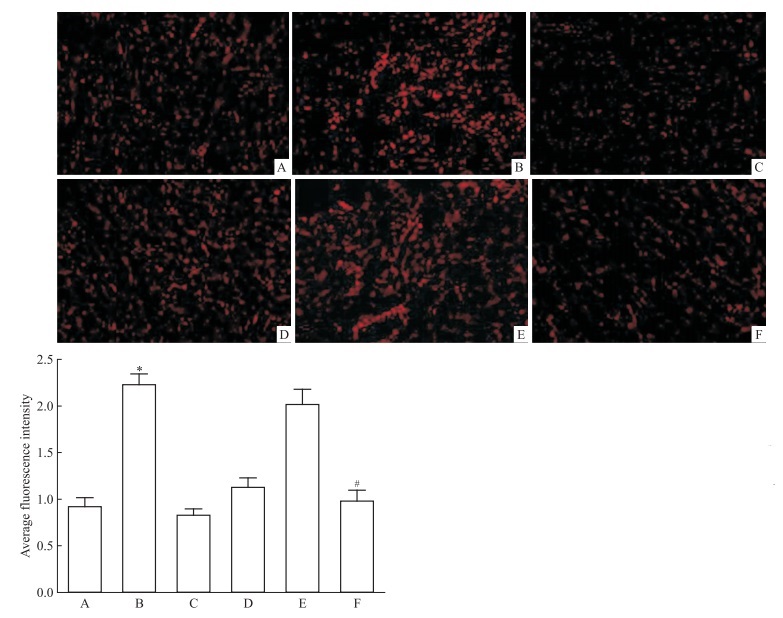
由Fig 5 DHE染色结果显示, 与Sham + NS组相比, LAD + NS、LAD + Ad-GFP组ROS含量出现明显增高(均p < 0.05);与LAD + NS组相比, LAD + Ad-SCAD组心肌ROS含量明显降低(p < 0.05)。
|
| Fig 5 Detection of ROS by DHE staining in myocardial tissues of rats in each group(200 ×)(x ± s, n = 3) A: Sham+ NS; B: LAD + NS; C: Sham + Ad-GFP; D: Sham + Ad-SCAD; E: LAD + Ad-GFP; F: LAD + Ad-SCAD. * p < 0.05 vs Sham + NS group; # p < 0.05 vs LAD + NS group |
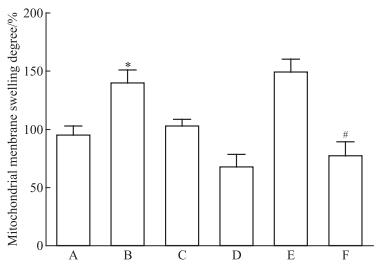
由Fig 6所示, 与Sham + NS组相比, LAD + NS组、LAD + Ad-GFP组线粒体膜肿胀明显上升(p < 0.05), 表明心力衰竭大鼠的线粒体结构受到明显的损伤。与Sham + NS组相比, Sham + Ad-SCAD组线粒体膜肿胀程度下降(p < 0.05)。与LAD + NS组相比, LAD + Ad- SCAD组线粒体膜肿胀程度明显下降(p < 0.05), 表明SCAD重组腺病毒过表达对心肌线粒体具有明显的保护作用。
|
| Fig 6 Swelling changes of mitochondrial in rats of each group(x ± s, n = 3) * p < 0.05 vs Sham + NS group; # p < 0. 05 vs LAD + NS group |
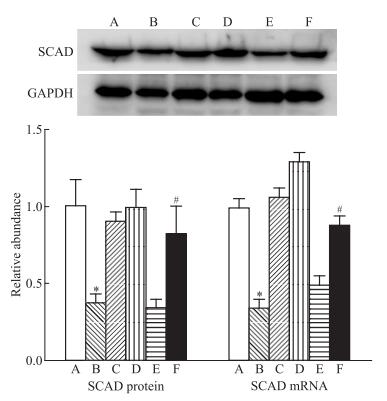
由Fig 7所示, 与Sham + NS组相比, LAD + NS组心肌SCAD mRNA和蛋白表达均明显降低(p < 0.05)。与LAD + NS组相比, LAD + Ad-SCAD组SCAD mRNA和蛋白表达均明显升高(p < 0.05)。表明LAD术后6周, 重组腺病毒介导的SCAD在心肌中存在过表达。
|
| Fig 7 Expression SCAD protein and mRNA 6 weeks after operation(x ± s, n = 3) A: Sham + NS; B: LAD + NS; C: Sham + Ad-GFP; D: Sham + Ad-SCAD; E: LAD + Ad-GFP; F: LAD + Ad-SCAD. * p < 0.05 vs Sham + NS group; # p < 0.05 vs LAD + NS group |
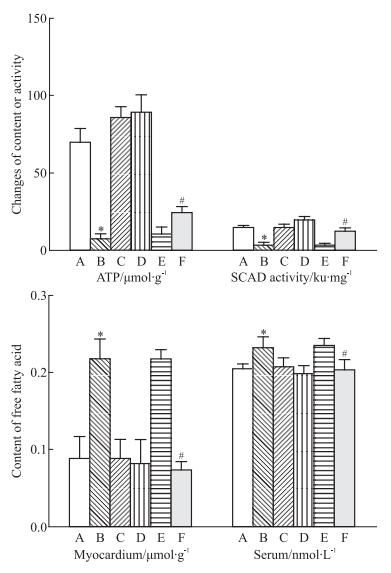
由Fig 8所示, 与Sham + NS组相比, LAD + NS组大鼠SCAD酶活性和ATP含量明显降低、心肌和血清游离脂肪酸含量均明显升高(均p < 0.05)。与LAD + NS组相比, LAD + Ad-SCAD组大鼠SCAD酶活性和ATP含量明显升高, 游离脂肪酸含量均明显降低(均p < 0.05)。表明术后6周重组腺病毒介导的SCAD过表达, 引起SCAD酶活性增高, 增强了心肌线粒体脂肪酸氧化能力, 生成更多的ATP, 游离脂肪酸明显减少。
|
| Fig 8 Comparison of SCAD activity, ATP and free fatty acid content in myocardium of rats in each group(x ± s, n = 3) A: Sham + NS; B: LAD + NS; C: Sham + Ad-GFP; D: Sham + Ad-SCAD; E: LAD + Ad-GFP; F: LAD + Ad-SCAD. * p < 0.05 vs Sham + NS group; # p < 0.05 vs LAD + NS group |
心力衰竭发病机制尤为复杂, 至今尚未完全阐明。目前公认的导致心力衰竭基本机制是心脏舒缩功能障碍, 导致供血不能满足机体活动需要, 能量代谢改变是心脏舒缩功能障碍的关键因素[11]。正常状态下, 约70%的心肌能量来源于心肌线粒体脂肪酸β氧化。然而, 心力衰竭时代谢底物由脂肪酸转变为葡萄糖, 脂肪酸氧化能力显著减弱, 导致心肌供能不足, 葡萄糖氧化无法代偿性增加, 进一步加强了心力衰竭的能量生成障碍[12-14]。
我们前期研究显示, SCAD的表达下调与心力衰竭的发展密切相关[8]。为了进一步明确SCAD在心力衰竭中的作用, 利用SCAD重组腺病毒对心力衰竭大鼠进行心脏多点注射, 研究SCAD过表达对心脏舒缩功能以及心肌线粒体能量代谢的影响。
本研究发现, 在LAD术应激下, 同时进行SCAD重组腺病毒过表达, 能改善大鼠由LAD术后引起的持续性低血压。超声心动图检测结果显示, 过表达SCAD能改善心肌梗死导致的心脏舒缩功能障碍, 各项超声心动图指标得到明显改善。同时, 过表达SCAD能明显改善LAD术后引起的心肌纤维化和心肌细胞的大量丧失, 减少心肌胶原沉积, 改善心肌细胞的凋亡, 降低ROS含量和线粒体膜肿胀程度, 保护线粒体结构, 有效延缓了心力衰竭的病理性重构。
LAD + Ad-SCAD组大鼠SCAD酶活性提高, ATP含量增高, 游离脂肪酸含量减少, 表明SCAD促进了线粒体脂肪酸β氧化反应, 改善了LAD手术导致心肌缺血缺氧引起的心肌能量代谢障碍。以上结果提示, SCAD重组腺病毒过表达可以减缓心肌梗死大鼠向心力衰竭发展的进程, 可能与SCAD对心脏能量代谢的正性调节作用和抑制线粒体凋亡途径, 从而保护心肌细胞的作用密切相关。
综上所述, SCAD重组腺病毒在心力衰竭治疗中可能发挥了至关重要的作用, 这为心力衰竭的防治提供了一个新靶点和新思路, 为进一步研究SCAD在心力衰竭中的作用奠定了基础。然而, SCAD过表达改善心力衰竭的作用机制还有待进一步深入研究。
| [1] |
中华医学会心血管病学分会, 中华心血管病杂志编辑委员会. 中国心力衰竭诊断和治疗指南2014[J]. 中华心血管病杂志, 2014, 42(2): 3-10. Chin Soc Cardiology, Editorial Board of Chin J Cardiol. Guidelines for the diagnosis and treatment of heart failure in China 2014[J]. Chin J Cardiol, 2014, 42(2): 3-10. |
| [2] |
王俊杰, 李红倬. 线粒体能量代谢和氧化应激与心肌肥厚的关系[J]. 山西医药杂志, 2018, 47(6): 53-8. Wang J J, Li H Z. Relationship between mitochondrial energy me- tabolism and oxidative stress and cardiac hypertrophy[J]. Shanxi Med, 2018, 47(6): 53-8. |
| [3] |
Tham Y K, Bernardo B C, Ooi J Y, et al. Pathophysiology of cardiac hypertrophy and heart failure: signaling pathways and novel therapeutic targets[J]. Arch Toxicol, 2015, 89(9): 1401-38. |
| [4] |
杨明珠, 陈依春, 王晓露, 等. 钠-钙交换体单克隆抗体NCX- 3F10对大鼠心室肌主要离子电流的影响及对缺血/再灌注诱发心律失常的抑制作用[J]. 中国药理学通报, 2017, 33(7): 934-41. Yang M Z, Chen Y C, Wang X L, et al. Investigation of effects of monoclonal antibody NCX-3F10 against Na + /Ca2 + exchanger on rat cardiac ionic currents and its suppression on ischemia-reperfu- sion induced cardiac arrhythmias[J]. Chin Pharmacol Bull, 2017, 33(7): 934-41. doi:10.3969/j.issn.1001-1978.2017.07.010 |
| [5] |
Acin-Perez R, Lechuga-Vieco A V, Maria D M M, et al. Ablation of the stress protease OMA1 protects against heart failure in mice[J]. Sci Transl Med, 2018, 10(434): 1-14. |
| [6] |
舒朝辉, 曾振华, 黄秋菊, 等. 短链酰基辅酶A脱氢酶在心脏成纤维细胞胶原表达和细胞增殖中的作用[J]. 中国病理生理杂志, 2016, 32(12): 2184-91. Shu Z H, Zeng Z H, Huang Q J, et al. Effects of short-chain acyl- CoA dehydrogenase on collagen expression and proliferation of rat cardiac fibroblasts[J]. Chin J Pathophysiol, 2016, 32(12): 2184-91. doi:10.3969/j.issn.1000-4718.2016.12.010 |
| [7] |
周四桂, 王平, 路遥, 等. 短链酰基辅酶A脱氢酶在大鼠心脏发育中的表达及其与心肌肥厚的关系[J]. 中国病理生理杂志, 2013, 29(1): 9-14. Zhou S G, Wang P, Lu Y, et al. Expression of short-chain acyl- CoA dehydrogenase during heart develop- ment in rats and relation- ship with cardiac hypertrophy[J]. Chin J Pathophysiol, 2013, 29(1): 9-14. doi:10.3969/j.issn.1000-4718.2013.01.002 |
| [8] |
廖英勤, 李忠洪, 舒朝辉, 等. 短链酰基辅酶A脱氢酶在大鼠心肌梗死后心力衰竭中的变化及有氧运动的干预作用[J]. 中华危重病急救医学, 2019, 31(2): 172-7. Liao Y Q, Li Z H, Shu Z H, et al. Change of short-chain acyl-CoA dehydrogenase in heart failure after myocardial infarction in rats and the intervention of aerobic exercise[J]. Chin Crit Care Med, 2019, 31(2): 172-7. |
| [9] |
Zeng Z H, Huang Q J, Shu Z H, et al. Effects of short-chain acyl-CoA dehydrogenase on cardiomyocyte apoptosis[J]. J Cell Mol Med, 2016, 20(7): 1381-91. doi:10.1111/jcmm.12828 |
| [10] |
廖英勤, 冯静韵, 李忠洪, 等. 短链酰基辅酶A脱氢酶在老年自发性高血压大鼠慢性心力衰竭中的作用[J]. 广东药科大学学报, 2019, 35(3): 412-7. Liao Y Q, Feng J Y, Li Z H, et al. Role of short-chain acyl-CoA dehydrogenase in chronic heart failure of elderly spontaneously hy- pertensive rats[J]. J Guangdong Pharm Univ, 2019, 35(3): 412-7. |
| [11] |
Mori J, Zhang L, Oudit G Y, et al. Impact of the renin-angiotensin system on cardiac energy metabolism in heart failure[J]. J Mol Cell Cardiol, 2013, 63: 98-106. doi:10.1016/j.yjmcc.2013.07.010 |
| [12] |
Fillmore N, And J M, Lopaschuk G D. Mitochondrial fatty acid oxidation alterations in heart failure, ischaemic heart disease and dia- betic cardiomyopathy[J]. Br J Pharmacol, 2014, 171(8): 2080-90. doi:10.1111/bph.12475 |
| [13] |
Legchenko E, Chouvarine P, Borchert P, et al. PPARγ agonist pio- glitazone reverses pulmonary hypertension and prevents right heart failure via fatty acid oxidation[J]. Sci Transl Med, 2018, 10(438): 1-17. |
| [14] |
刘涛, 李晶, 鲍翠玉. 线粒体损伤与糖尿病心肌病发病关系的研究进展[J]. 中国药理学通报, 2018, 34(4): 456-8. doi:10.3969/j.issn.1001-1978.2018.04.004 |
| [15] |
Liu T, Li J, Bao C Y, et al. Research progress of mitochondria in diabetic cardiomyopathy[J]. Chin Pharmacol Bull, 2018, 34(4): 456-8. |