


2. 新疆医科大学公共卫生学院,新疆 乌鲁木齐 830011
2. College of Public Health, Xinjiang Medical University, Urumqi 830011, China
心肌肥厚是一种为维持心输出量和保证组织灌流的适应性反应,压力超负荷引起的心肌肥厚与高血压的发生密切相关[1]。研究表明[2],心肌肥厚的逆转可以降低心血管疾病的死亡率。肉苁蓉(Cistance)素有“沙漠人参”之美誉。苯乙醇总苷(Cistanche phenylethanoid glycosides,CPhGs)是肉苁蓉发挥药效的主要物质基础之一[3],具有抗痴呆、抗氧化、抗肿瘤、免疫调节、缓解疲劳、抗脑缺血/再灌注损伤等多种药理作用[4]。研究显示[5],CPhGs可以抑制因缺血再灌注损伤引起的心肌细胞凋亡并发挥保护心肌组织的作用。然而,肉苁蓉CPhGs能否对压力超负荷引起的心肌肥厚能起到抑制作用,尚不可知。因此,本研究通过构建大鼠腹主动脉缩窄(abdominal aorta coarctation,AAC)模型,探讨CPhGs对压力超负荷大鼠心肌肥厚的作用,以及对磷脂酰肌醇3激酶/蛋白激酶B(phosphatidylinositol 3-kinase/ protein kinase B,PI3K/PKB)通路相关蛋白表达的影响,以研究CPhGs抑制压力超负荷大鼠心肌肥厚的作用机制,为进一步研发对心肌肥厚防控的药物提供实验依据。
1 材料 1.1 实验动物健康雄性SPF级大鼠,70只,体质量(200±20)g, 由新疆医科大学动物实验中心提供。动物生产许可证号与合格证号分别为:SYXK(新)2016-0003,SCXK(新)2016-0002。
1.2 药物与试剂肉苁蓉苯乙醇总苷CPhGs(和田帝辰医药生物科技有限公司,批号:20180502),缬沙坦(北京诺华制药有限公司, 规格:80 mg),0.5%羧甲基纤维素钠(carboxymethylcellulose sodium,CMC-Na)(西安正天药用辅料有限公司),戊巴比妥钠(德国Meck公司),RIPA(美国Thermo公司), p-PI3K、PI3K、p-PKB、PKB、β-actin兔抗单克隆抗体、大鼠血浆内皮素1(endothelin 1, ET-1)和脑利钠肽(brain natriuretic peptide, BNP)酶联免疫吸附试验试剂盒(北京博奥森公司),辣根过氧化酶标记二抗(北京中杉金桥公司),蛋白酶抑制剂、蛋白磷酸酶抑制剂混合物、BCA蛋白定量试剂盒(北京索莱宝公司),ECL显色液(中国Biosharp公司)、PVDF膜(英国Roche公司)。
1.3 主要仪器飞利浦HD11 XE超声诊断仪(德国Philips公司);移液器(德国Eppendorf公司);低温离心机(美国Sigma公司);全波长自动酶联免疫反应检测仪((美国Thermo公司);电泳和转膜装置(美国Bio-Rad公司);FluorChem E化学发光高灵敏凝胶成像仪(美国Protein Simple公司);电热恒温培养箱(上海一恒科学仪器有限公司)。
2 方法 2.1 动物分组、模型制备及给药根据文献[6]采用AAC术制备大鼠压力超负荷心肌肥厚模型。雄性SD大鼠70只,随机分为7组:空白组(Control, Con)、假手术组(Sham)、模型组(Mod)、缬沙坦阳性药对照组(Valsartan, Vst)、CPhGs 125、250、250 mg·kg-1组,涉及药物剂量参照文献[7-8]及预实验结果设置。Con组不进行手术,Sham组分离腹主动脉不予结扎,其余五组建立压力超负荷心肌肥厚模型。术后d 3,CPhGs各剂量组及Vst组(10 mg·kg-1)按每天设定剂量灌胃给予受试物,其余3组均灌胃给予相同体积的0.5%CMC-Na,连续42 d,每日1次;d 43,以2.5%戊巴比妥钠麻醉后,行心脏超声检查,开腹采取腹主动脉血处死大鼠,立即开胸,取出心脏。
2.2 大鼠心脏超声指标的检测在2.5%戊巴比妥钠麻醉下,剃毛后,使用超声诊断仪检测各组大鼠的心功能指标:(1)左心室舒张末期后壁厚度(left ventricular posterior wall thickness,LVPWT)(2)左心室舒张末期内径(left ventricular end-diastolic diameter,LVEDD)(3)左心室短轴收缩率(left ventricular fractional shortening,LVFS)(4)左心室射血分数(left ventricular ejection fractions,LVEF)。每只大鼠重复3次测量后,计算平均值。
2.3 大鼠心脏体质量指数(heart weight/body weight index, HWI)计算大鼠结束心脏超声学检测后,打开腹腔,腹主动脉取血至大鼠死亡后,立即开胸,取出大鼠心脏,用预冷的生理盐水冲洗心腔3次,用干净的滤纸吸干水分,称心脏质量(heart weight, HW)。HWI=HW/体质量(body weight,BW)。
2.4 酶联免疫吸附试验检测大鼠血浆ET-1和BNP水平腹主动脉血液储存于EDTA抗凝采血管,混匀后3 000 r·min-1离心15min,收集上清,-20 ℃条件下冻存。按试剂盒说明书操作。
2.5 显微镜观察大鼠心肌组织病理学改变大鼠心肌组织以4%多聚甲醛固定、石蜡包埋后,经伊红苏木素染色后以中性树胶封片,电子显微镜下观察心肌组织和细胞形态并拍图。用Image J测量细胞表面积,每组选取四张标本,每张随机选取3个视野,每视野测量10~15个心肌细胞面积(area of myocardial cells,AMC),计算平均值。
2.6 Western blot检测p-PI3K, PI3K, p-PKB, PKB蛋白的表达称取心肌组织50mg, 加入液氮研磨充分后加入RIPA裂解液、蛋白酶抑制剂、蛋白磷酸酶抑制剂混合物,提取总蛋白,采用BCA法进行蛋白定量至60 μg,加入4×Loading buffer后在100 ℃下热变性5 min,上样到10%聚丙烯酰胺凝胶,120 V电泳60 min,200 mA恒流电转90 min,PVDF膜湿转。5%脱脂奶粉室温下封闭PVDF膜1 h,1×TBST缓冲液置于摇床振荡清洗10 min,3次,加入相应比例稀释的一抗(目的基因p-PI3K, PI3K, p-PKB, PKB为1 :1 000,内参β-actin为1 :20 000),4 ℃下孵育过夜,清洗3次后室温下孵育二抗1 h。FluorChem E化学发光高灵敏凝胶成像仪拍照显色,分析条带灰度值。蛋白相对表达水平=目的条带灰度值/内参条带灰度值×100%
2.7 统计学分析采用x±s表示,用SPSS25.0软件进行数据分析,通过单因素方差分析(one-way ANOVA)比较各组数据,组间比较采用LSD法。
3 结果 3.1 CPhGs对压力超负荷心肌肥厚大鼠的心脏超声指标的影响Tab 1可见,与Con组和Sham组相比,Mod组的LVPWT显著增加,LVEDD、LVEF、LVFS显著减小(P < 0.01);与Mod组相比,Vst组和CPhGs 125、250、500 mg·kg-1组大鼠的LVPWT减少,LVEDD、LVEF、LVFS增加,CPhGs组随着剂量的增加呈现改变逐渐明显的趋势,Vst组及CPhGs 250、500 mg·kg-1组作用显著(P < 0.05或P < 0.01);与Vst组相比,CPhGs 250、500 mg·kg-1组各指标没有统计学差异。表明中、高剂量的CPhGs对压力超负荷心肌肥厚大鼠有保护作用,其作用与阳性药物相当。
| Group | LVPWT(mm) | LVEDD(mm) | LVFS(%) | LVEF(%) |
| Con | 2.11±0.13 | 7.07±0.30 | 39.84±7.57 | 77.30±8.09 |
| Sham | 2.13±0.18 | 7.34±0.39 | 40.42±4.58 | 78.52±4.93 |
| Mod | 2.70±0.31** | 6.14±0.61** | 32.62±7.00** | 68.53±9.40** |
| Vst | 2.32±0.24## | 6.78±0.40# | 38.10±6.48 | 75.59±7.08 |
| CPhGs 125 mg·kg-1 | 2.56±0.22▲ | 6.33±0.53▲ | 34.57±8.00 | 70.88±9.76 |
| CPhGs 250 mg·kg-1 | 2.42±0.26# | 6.65±0.40# | 38.00±4.03# | 75.90±4.53# |
| CPhGs 500 mg·kg-1 | 2.23±0.24## | 6.86±0.45## | 38.35±3.40# | 76.38±3.83# |
| **P < 0.01 vs Con and Sham; #P < 0.05, ##P < 0.01 vs Mod; ▲P < 0.05 vs Vst | ||||
Tab 2可见,各组大鼠的BW没有明显差异;与Con组和Sham组相比,Mod组大鼠的HW和HWI显著相加(P < 0.01);与Mod组相比,Vst组HW和HWI显著减小(P < 0.01), CPhGs 125、250、500 mg·kg-1组(P < 0.05或0.01)HW和HWI有不同程度的减小,且随着剂量的增加呈现逐渐减小的趋势;与Vst组相比,CPhGs 500 mg·kg-1组与其接近,差异无统计学意义。表明中、高剂量CPhGs可以减小压力超负荷心肌肥厚大鼠的心肌肥厚程度,保护心肌,与Vst作用相当。
| Group | BW(g) | HW(g) | HWI(mg/g) |
| Con | 431.45±26.15 | 1.13±0.11 | 2.62±0.28 |
| Sham | 429.27±22.68 | 1.11±0.12 | 2.60±0.33 |
| Mod | 433.17±23.98 | 1.43±0.18** | 3.31±0.37** |
| Vst | 425.57±21.82 | 1.18±0.18## | 2.77±0.44## |
| CPhGs 125 mg·kg-1 | 431.90±23.85 | 1.39±0.21▲ | 3.20±0.43▲ |
| CPhGs 250 mg·kg-1 | 422.81±20.08 | 1.25±0.16# | 2.95±0.37# |
| CPhGs 500 mg·kg-1 | 424.89±19.82 | 1.16±0.14## | 2.74±0.35## |
| **P < 0.01 vs Con and Sham; #P < 0.05, ##P < 0.01 vs Mod; ▲P < 0.05 vs Vst | |||
Tab 3可见,与Con组和Sham组相比,Mod组大鼠的血浆BNP和ET-1水平显著上升(P < 0.01);与Mod组相比,Vst组大鼠的血浆BNP和ET-1水平显著下降(P < 0.01),CPhGs 125、250、500 mg·kg-1组血浆BNP和ET-1水平有不同程度下降,并且随着剂量的增加呈现逐渐减小的趋势,其中CPhGs 250组BNP显著下降(P < 0.01)、500 mg·kg-1组BNP和ET-1均显著下降(P < 0.01);与Vst组相比,CPhGs 500 mg·kg-1组BNP和ET-1水平降低,没有统计学差异。表明250、500 mg·kg-1中、高剂量的CPhGs可以降低压力超负荷心肌肥厚大鼠的血浆BNP和ET-1水平,高剂量组作用强度与Vst相当。
| Group | BNP/μg·l-1 | ET-1/μg·l-1 |
| Con | 39.84±14.07 | 46.10±7.55 |
| Sham | 31.57±17.74 | 47.66±10.91 |
| Mod | 71.50±16.88**▲▲ | 101.17±13.21**▲▲ |
| Vst | 49.88±15.33## | 69.06±11.71## |
| CPhGs 125 mg·kg-1 | 70.71±19.83▲ | 91.57±15.09▲▲ |
| CPhGs 250 mg·kg-1 | 59.27±19.31 | 73.88±15.49## |
| CPhGs 500 mg·kg-1 | 45.68±17.83## | 67.82±11.32## |
| **P < 0.01 vs Con and Sham; ##P < 0.01 vs Mod; ▲P < 0.05, ▲▲P < 0.01 vs Vst | ||
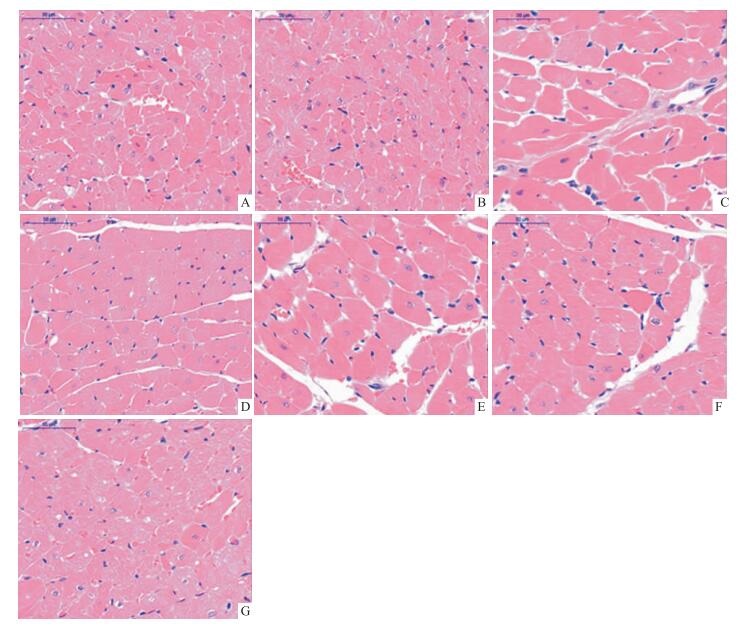
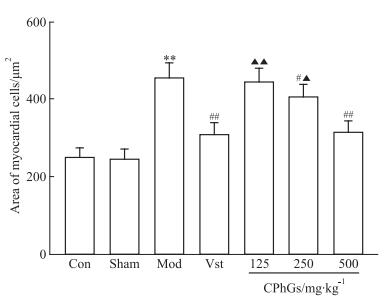
Fig 1和Fig 2可见,与Con组和Sham组相比,Mod组心肌细胞排列紊乱,组织中可见炎性细胞浸润,单位视野内细胞核的数量减少,AMC显著增大(P < 0.01);与Mod组相比,Vst组单位视野内的细胞数量增加,AMC显著减小(P < 0.01),CPhGs 125、250、500 mg·kg-1组的AMC也有不同程度减小,并且随着剂量的增加呈现逐渐减小的趋势, 其中CPhGs 250、500 mg·kg-1组较Mod组有明显差异(P < 0.05或0.01);与Vst组相比,CPhGs 500 mg·kg-1组AMC与其接近,差异无统计学意义。表明中、高剂量CPhGs在一定程度有减小压力超负荷型心肌肥厚大鼠AMC的作用,当剂量达500 mg·kg-1作用与Vst接近。
|
| Fig 1 Picture of myocardial tissues with HE staining(×400, n=4) A:Con; B:Sham; C:Mod; D:Vst; E:CPhGs 125 mg·kg-1; F:CPhGs 250 mg·kg-1; G:CPhGs 500 mg·kg-1 |
|
| Fig 2 Effect of CPhGs on AMC in rats with myocardialhypertrophy induced by pressure overload(x±s, n=4) **P < 0.01 vs Con and Sham; #P < 0.05, ##P < 0.01 vs Mod; ▲P < 0.05, ▲▲P < 0.01 vs Vst |
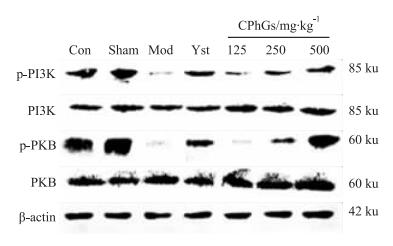
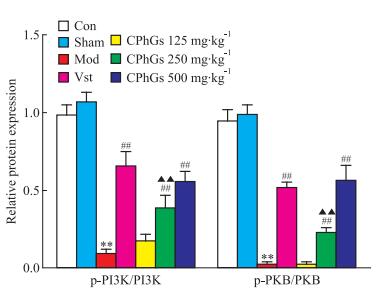
Fig 3和Fig 4可见,与Con组和Sham组相比,Mod组p-PI3K、p-PKB蛋白的相对表达量显著降低(P < 0.01);与Mod组相比,Vst组p-PI3K、p-PKB蛋白的相对表达量显著升高(P < 0.01),CPhGs 125、250、500 mg·kg-1组有不同程度升高,随着剂量的增加, p-PI3K、p-PKB蛋白相对表达量呈逐步增加趋势, 其中CPhGs 250、500 mg·kg-1组较Mod组有明显统计学意义(P < 0.01);与Vst组相比,CPhGs 500 mg·kg-1组p-PI3K、p-PKB蛋白的相对表达量与其接近,无明显差异。表明中、高剂量CPhGs能够增加压力负荷型心肌肥厚大鼠心肌组织的p-PI3K、p-PKB蛋白的相对表达量,高剂量组与Vst的作用相当。
|
| Fig 3 Representative Western blot bands of p-PI3K, PI3K, p-PKB, PKB and β-actin(n=3) |
|
| Fig 4 Effect of CPhGs on expression of p-PI3K and p-PKB in rats with myocardial hypertrophyinduced by pressure overload(x±s, n=3) **P < 0.01 vs Con and Sham; ##P < 0.01 vs Mod; ▲▲P < 0.01 vs Vst |
心肌肥厚作为高血压的主要并发症之一,同时也参与了慢性心衰、冠心病等心血管疾病的病理过程。在高血压前期,心肌通过增加心室壁张力从而适应增加的压力负荷,心肌细胞代偿性增大,导致左室心肌肥厚。心肌肥厚的抑制可以降低心血管疾病发病率及总死亡率,其作用优于单纯降压治疗[9]。因此,高血压的治疗方案不应局限于血压的控制,逆转心肌肥厚是治疗高血压的亟待解决的问题。
肉苁蓉被列为管花肉苁蓉Cistanche tubulosa Wight干燥带鳞叶肉质茎。近年来,肉苁蓉以其显著的生物活性备受人们的关注,国内学者对肉苁蓉的心血管等方面的药理作用进行了较为深入的研究,发现肉苁蓉对心肌具有一定保护作用,但其具体的分子作用机制仍不清楚。研究表明[10],CPhGs能减轻自由基对心肌线粒体膜和浆网膜造成的损伤,降低丙二醛含量,减轻心肌超微结构损伤,提高大鼠心肌线粒体抗氧化酶活性,减少心肌梗死面积,提高心肌组织磷酸肌酸激酶活性,对缺血心肌有保护作用。本实验发现,CPhGs可减小心肌肥厚大鼠的LVPWT、HWI、AMC及心肌肥厚标志物ET-1、BNP水平,同时增加LVEDD、EF、FS,而抑制心肌肥厚,改善大鼠的心功能。随药物浓度增加,CPhGs作用效果增加,呈现剂量依赖关系,其中CPhGs中高剂量组肌肥厚大鼠有明显的保护作用,高剂量组与缬沙坦阳性药组作用相当。
PI3K是心肌细胞肥大和由收缩型向肥厚型转换的最后通路[11],PI3K的2种亚型可参与心肌细胞肥大,其中pll0α参与生理性心肌肥厚,而p110γ参与病理性心肌肥厚,小鼠敲除p110γ后,对心肌病理性刺激可产生保护作用,对于心肌细胞肥大的发生、发展起着至关重要的作用[12]。PKB途径与心肌细胞增殖、生长、代谢、凋亡等多种生物学活动密切相关[13]。叶芳杏等[14]报道玉郎伞单体17-甲氧基-7-羟基-苯并呋喃查尔酮可以通过调控心肌内皮细胞的p-PI3K、p-PKB、p-eNOS等蛋白逆转大鼠压力超负荷心室的重构。杨洋等[15]报道,绿原酸可通过PI3K/PKB通路调控细胞凋亡,抑制异丙肾上腺素诱导的心肌细胞肥大。本研究中, CPhGs中、高剂量组显著增加p-PI3K、p-PKB蛋白相对表达量,且CPhGs高剂量组与Vst组作用相当,进一步证明CPhGs可以通过激活PI3K/PKB信号通路,抑制压力超负荷大鼠心肌肥厚。
综上,本研究证实CPhGs对AAC术后压力超负荷心肌肥厚大鼠有保护作用,可能与其增加PI3K、PKB磷酸化而激活PI3K/PKB信号通路有关。这为临床研究高血压心肌肥厚提供了新思路,可能为高血压心肌肥厚的防控和逆转提供了新的治疗药物。
| [1] |
Chahal N S, Lim T K, Jain P, et al. New insights into the relationship of left ventricular geometry and left ventricular mass with cardiac function: A population study of hypertensive subjects[J]. Eur Heart J, 2010, 31(5): 588-94. doi:10.1093/eurheartj/ehp490 |
| [2] |
McCullough P A, Chan C T, Weinhandl E D, et al. Intensive hemodialysis, left ventricular hypertrophy, and cardiovascular disease[J]. Am J Kidney Dis, 2016, 68(5S1): S5-14. |
| [3] |
星学军, 刁治民, 许正泽. 药用植物肉苁蓉生物学特性及应用价值[J]. 青海草业, 2018, 27(2): 17-20, 29. Xing X J, Diao Z M, Xu Z Z. Desert medicinal plants cistanche biological characteristics and application value[J]. Qinghai Pratacult, 2018, 27(2): 17-20, 29. doi:10.3969/j.issn.1008-1445.2018.02.005 |
| [4] |
曾克武, 廖理曦, 万彦军, 等. 基于靶点"钩钓"策略的肉苁蓉苯乙醇苷药理靶点鉴定及功效解析[J]. 中草药, 2018, 49(1): 173-8. Zeng K W, Liao L X, Wan Y J, et al. Pharmacological targets identification and efficacy analysis of phenylethanoid glycosides from cistanches herba based on "target fishing" strategy[J]. Chin Tradit Herbal Drugs, 2018, 49(1): 173-8. |
| [5] |
于倩.蒙花苷和肉苁蓉苯乙醇苷对大鼠心肌缺血再灌注损伤的保护作用及机制研究[D].吉林: 吉林大学, 2017. Yu Q. Protective effects and mechanisms of linarin and phenylethanoid glycoside-rich extract from cistanche deserticola on myocardial ischemia reperfusion injury[D]. Jilin: Jilin Univ, 2017. |
| [6] |
朱林强, 周永焯, 谢晓明, 等. 大鼠腹主动脉缩窄术致大鼠慢性心衰的建模与体会[J]. 现代医院, 2015(10): 21-4. Zhu L Q, Zhou Y C, Xie X M, et al. The construction of rat chronic heart failure model induced with abdominal aortic coarctation[J]. Mod Hosp, 2015(10): 21-4. doi:10.3969/j.issn.1671-332X.2015.10.007 |
| [7] |
施洋, 樊官伟. 参附注射液对慢性充血性心力衰竭大鼠心肌miRNA表达谱的影响[J]. 中国药房, 2017, 28(22): 3048-52. Shi Y, Fan G W. Effect of shenfu injection on the expression profile of myocardial mi RNA in rats with chronic congestive heart failure[J]. J China Pharm, 2017, 28(22): 3048-52. doi:10.6039/j.issn.1001-0408.2017.22.07 |
| [8] |
王建发, 赵国安. 芍药苷通过cAMP-PKA信号通路对心肌梗死大鼠保护作用的实验研究[J]. 中国循证心血管医学杂志, 2018, 10(4): 479-83. Wang J F, Zhao G A. Study on the protective effect of paeoniflorin against myocardial infarction in rats by the cAMP-PKA singal pathway[J]. Chin J Evid Based Cardiovasc Med, 2018, 10(4): 479-83. doi:10.3969/j.issn.1674-4055.2018.04.26 |
| [9] |
Okwuosa T M, Soliman E Z, Lopez F, et al. Left ventricular hypertrophy and cardiovascular disease risk prediction and reclassification in blacks and whites: the Atherosclerosis Risk in Communities Study[J]. Am Heart J, 2015, 169(1): 155-61. doi:10.1016/j.ahj.2014.09.013 |
| [10] |
吾买尔江·牙合甫, 赵红琼, 冯亮, 等. 管花肉苁蓉醇提物对大鼠血液生化指标及心血管功能的影响[J]. 畜牧与饲料科学, 2016, 37(6-7): 16-20. Wumaierjiang Y, Zhao H Q, Feng L, et al. Effect of cistanche tubulosa ethanol extract on blood biochemical parameters and cardiovascular function in rats[J]. Anim Husb Feed Sci, 2016, 37(6-7): 16-20. |
| [11] |
Qian W, Yu D, Zhang J, et al. Wogonin attenuates isoprenaline-induced myocardial hypertrophy in mice by suppressing the PI3K/Akt pathway[J]. Front Pharmacol, 2018, 9: 896. doi:10.3389/fphar.2018.00896 |
| [12] |
Shao M, Zhuo C, Jiang R, et al. Protective effect of hydrogen sulphide against myocardial hypertrophy in mice[J]. Oncotarget, 2017, 8(14): 22344-52. |
| [13] |
Song D, Liu X, Diao Y, et al. Hydrogen-rich solution against myocardial injury and aquaporin expression via the PI3K/Akt signaling pathway during cardiopulmonary bypass in rats[J]. Mol Med Rep, 2018, 18(2): 1925-38. |
| [14] |
叶芳杏, 何俊慧, 李梅兰, 等. 玉郎伞MHBFC调控eNOS-NO信号通路逆转大鼠心室重构的机制研究[J]. 中国药理学通报, 2018, 34(11): 1516-20. Ye F X, He J H, Li M L, et al. Mechanism of Yulangsan MHBFC regulating eNOS-NO signaling pathway in reversing ventricular remodeling in rats[J]. Chin Pharmacol Bull, 2018, 34(11): 1516-20. doi:10.3969/j.issn.1001-1978.2018.11.009 |
| [15] |
杨洋, 李觉. 绿原酸通过PI3K/Akt信号通路抑制异丙肾上腺素诱导的心肌肥大[J]. 同济大学学报(医学版), 2019, 40(2): 184-9. Yang Y, Li J. Chlorogenic acid inhibits isoproterenol-induced cardiac hypertrophy through PI3K/AKT signaling pathway[J]. J Tongji Univ (Med Sci), 2019, 40(2): 184-9. |

