


陈妍(1985-),女,博士,教授,硕士生导师,研究方向:天然小分子化合物抗肿瘤活性研究,通讯作者,E-mail: 457335071@qq.com
 ,
SHAN Yu,
FENG Xiao,
ZHANG Jing-yu,
ZHANG Min-qin,
ZOU Yu-chi,
FU Qiong,
SHEN Xiang-chun
,
SHAN Yu,
FENG Xiao,
ZHANG Jing-yu,
ZHANG Min-qin,
ZOU Yu-chi,
FU Qiong,
SHEN Xiang-chun
 ,
CHEN Yan
,
CHEN Yan

乳腺癌是危害女性身体健康最常见的恶性肿瘤,而转移是乳腺癌临床治疗失败的主要原因[1]。大量研究表明上皮间质转化(epithelial mesenchymal transformation,EMT)是肿瘤转移的关键步骤,其促进乳腺癌的发生、浸润等多个恶变过程[2]。纤连蛋白(fibronectin,FN)是细胞外基质中一种功能性糖蛋白。临床数据研究显示,FN在正常成人乳腺组织中低表达,而在乳腺肿瘤基质中的mRNA和蛋白水平都显著增加[3]。此外,FN被认为是促进乳腺上皮细胞间质转化的独立诱导因素,其通过特定的结构修饰或与配体结合介导乳腺上皮细胞的EMT过程[4]。
整合素是一种位于细胞表面介导细胞内外信号传导的跨膜糖蛋白受体。研究显示FN可通过RGD位点与整合素受体结合调控细胞多种生理功能[5]。同时研究发现整合素β1受体介导FN诱导胶质瘤细胞的迁移和黏附[6],FN激活整合素αvβ3信号增加了骨肉瘤细胞的转移潜能[7]。以上研究提示,整合素αvβ3信号可能参与FN诱导的EMT过程,抑制整合素信号可能是逆转FN诱导MCF-10A乳腺上皮细胞EMT过程的创新思路。本研究通过建立FN诱导的EMT体外模型,以整合素信号αvβ3为切入点,探讨FN诱导MCF-10A细胞EMT发生的可能机制,同时观察整合素αvβ3特异性抑制剂(Cyclo-RGDfK)对FN诱导的上皮间质转化影响,为Cyclo-RGDfK的临床实践提供更多的理论依据。
1 材料与方法 1.1 仪器立式高压蒸汽灭菌锅LDZX型(上海申安医疗器械厂),超净工作台SW-CJ-1型(中国苏州净化设备有限公司),Heal force型细胞培养箱(中国上海力申科学仪器有限公司),DMIL型倒置显微镜(德国LEICA公司),WP-UP-11-20超纯水机(四川沃特尔水处理设备有限公司),CFX型凝胶成像系统(美国Bio-rad公司),Microfuge20R型冷冻离心机(美国Beckman Coulter公司)。
1.2 药物及试剂乳腺上皮细胞株MCF-10A购自美国ATCC公司,DMEM-F12基础培养基、马血清(horse serum,HS,1312396)购自美国Gibco公司;霍乱毒素(Cholera toxin,C8052)、氢化可的松(hydrocortisone,H0888)、胰岛素(insulin,16634)、生长因子(epithelial growth factor,AF-100-15),纤连蛋白(FN,F2006)购自美国Sigma公司;整合素αvβ3抑制剂(Cyclo-RGDfK,HY-P0023)购自MedChemExpress公司;αv integrin抗体(ab179475)购自Abcam公司;β3 integrin抗体(SC-46655)购买自Santa Cruz Biotechnology公司;抗E-cadherin(BS1098)、N-cadherin(BS2224)、Vimentin(BS1491)和β-actin (BS6007M)单克隆一抗购自Bioword公司;羊抗兔和羊抗鼠IgG-HRP抗体购自Bioword公司。
2 方法 2.1 细胞培养MCF-10A细胞采用(含有5% HS、1%青霉素/链霉素、0.1 mg·L-1霍乱毒素、0.5 mg·L-1氢化可的松、10 mg·L-1胰岛素、20 μg·L-1生长因子)DMEM-F12培养基培养,放置于37 ℃、5%CO2的饱和湿度培养箱内进行培养,培养至细胞铺满培养皿的90%传代,实验所用细胞均处于对数生长期。
2.2 分组及给药取对数生长期MCF-10A细胞接种于培养瓶或培养板中,待细胞长满至90%后,用含1% HS的DMEM-F12培养基处理24 h,给予FN建立EMT模型。将实验设置为3组,正常对照组(Control),模型组(FN,20 mg·L-1),整合素αvβ3抑制剂组(20 mg·L-1 FN +20 nmol·L-1 Cyclo-RGDfK),Cyclo-RGDfK在加入FN前预处理1 h。
2.3 划痕修复实验体外评价细胞的迁移能力接种MCF-10A细胞于12孔板中,待细胞铺满孔底90%时,使用无菌10 μL枪头进行划痕,用PBS洗3~4遍,去除悬浮细胞及细胞碎片,按照前述“2.2”项随机分组后进行给药处理,并分别于0 h和48 h使用Leica DMI1显微镜和LAS EZ软件在50×倍镜下拍照,实验重复3次,并对结果做统计学分析。
2.4 Transwell侵袭实验检测细胞侵袭能力按分组给药处理48 h后,各组细胞用0.25%的胰蛋白酶消化并用无血清培养基重悬后接种于铺有Matrigel胶的Transwell上室中,下室加入含5%HS的完全培养基,继续培养16 h后,取出小室,用棉签蘸去基质胶以及上室的细胞,用4%的多聚甲醛固定细胞10 min,双蒸水清洗3次,苏木精染色5 min,伊红染液染色10 min,取下滤膜,在倒置显微镜下拍照,每个组随机选取5个视野进行计数,以各组穿过微孔滤膜细胞数表示细胞的侵袭能力。
2.5 Western blot检测相关蛋白的表达接种于6孔板中的细胞培养至铺满孔90%后,按2.2项下给药处理48 h后,用预冷的1×PBS轻洗2次,加入含1%蛋白酶抑制剂(PMSF)RIPA裂解细胞提取各给药组细胞总蛋白,4 ℃、12 000 r·min-1高速离心20 min,取上清采用BCA蛋白定量试剂盒进行蛋白定量。将蛋白样品加入10%十二烷基硫酸钠聚丙烯酰胺凝胶电泳分离1.5 h,湿转法转膜1.5 h,5%BSA封闭1 h。加入相应一抗αv integrin(1 :1 000)、β3 integrin(1 :500)、E-cadherin(1 :1 000)、N-cadherin(1 :1 000)及Vimentin(1 :1 000)孵育过夜,1×TBST洗膜后,加入辣根酶标记的二抗(1 :10 000)室温孵育1.5 h,避光加入化学发光液。采用Bio-Rad蛋白质条带显影成像系统获取图像, 并使用Image Lab分析软件计算蛋白印迹结果的灰度值。
2.6 统计学分析采用GraphPad Prism5软件对独立重复3次的实验结果进行统计学分析。统计结果表示为x±s,组间分析比较采用单因素方差分析法。
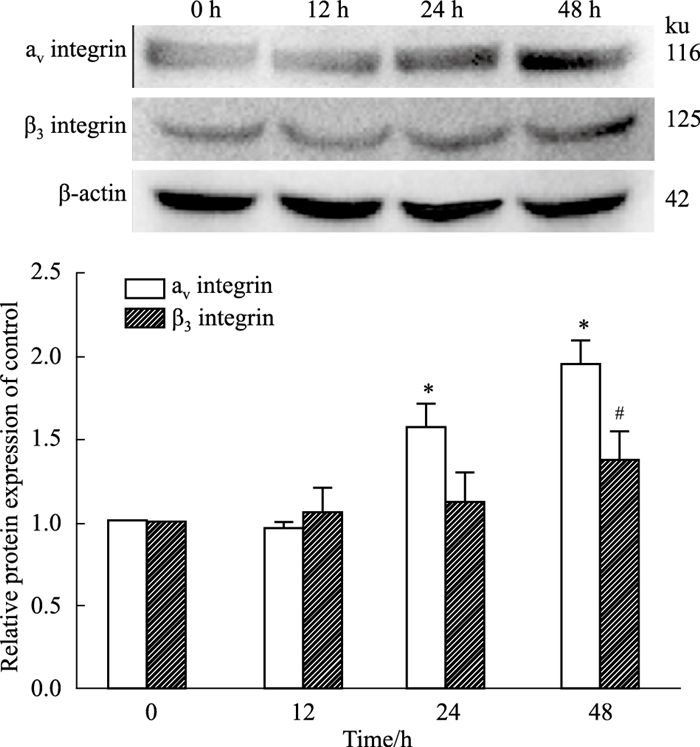
3 结果 3.1 FN增强乳腺上皮细胞MCF-10A整合素αv,β3的蛋白表达FN分别作用乳腺上皮细胞MCF-10A 0、12、24、48 h。与0 h相比,FN作用24 h和48 h后,整合素αv蛋白的表达显著增加(P < 0.05),FN作用48 h后,整合素β3蛋白表达显著上调(P < 0.05),结果如Fig 1所示。结果提示FN能诱导MCF-10A整合素αvβ3蛋白表达升高。
|
| Fig 1 Expression of αv integrin, β3 integrin protein in breast epithelial cell MCF-10A enhanced by FN (x±s, n=3) *P < 0.05 vs 0 h; #P < 0.05 vs FN |
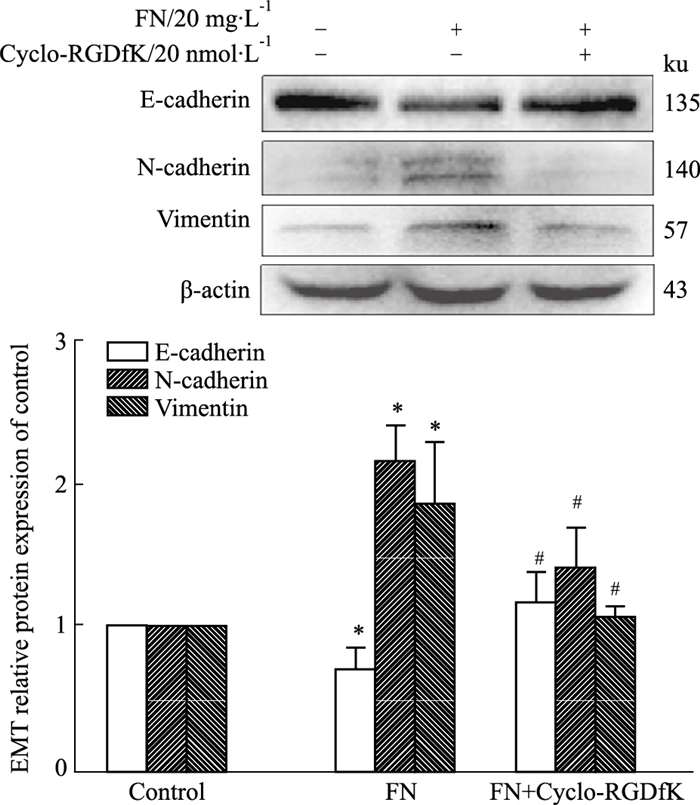
为探讨整合素抑制剂对FN诱导MCF-10A细胞EMT过程的影响,本研究通过Western blot实验检测EMT相关蛋白表达水平。如Fig 2所示,与Control组相比,模型组间质标志物N-cadherin、Vimentin蛋白表达明显上调,上皮标志物E-cadherin蛋白表达明显下调,差异具有统计学意义(P < 0.05)。与FN组相比,整合素αvβ3抑制剂组E-cadherin蛋白表达水平明显升高,N-cadherin和Vimentin蛋白水平显著降低,差异均具有统计学意义(P < 0.05)。结果提示Cyclo-RGDfK可抑制FN诱导的EMT过程。
|
| Fig 2 EMT-related protein expression induced by FN in breast epithelial cell MCF-10A reversed by Cyclo-RGDfK (x±s, n=3) *P < 0.05 vs control; #P < 0.05 vs FN |
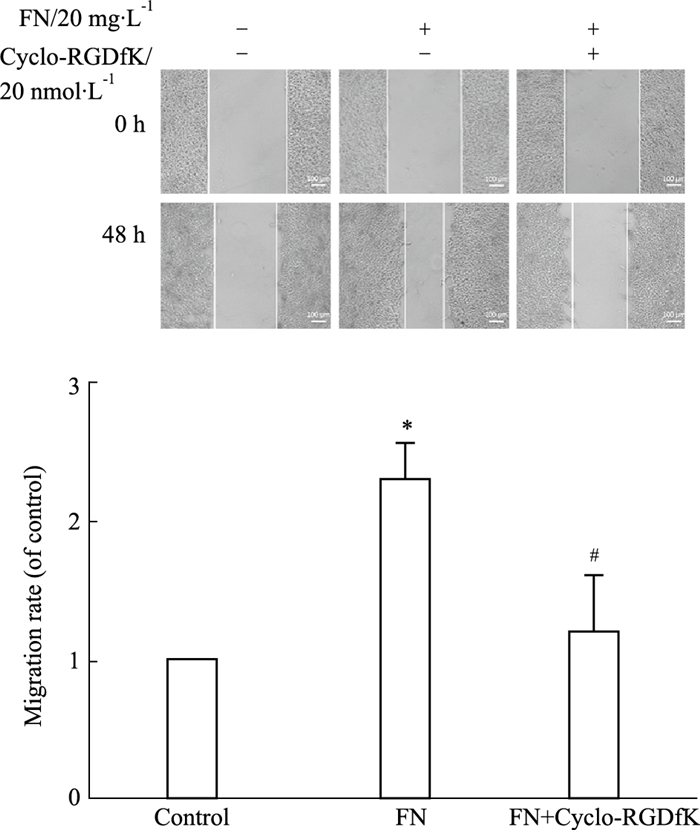
研究结果如Fig 3所示,与空白对照组迁移率(17.4%±3.1%)相比,FN组(35.5%±4.2%)细胞的迁移率显著增加(P < 0.05)。在给予Cyclo-RGDfK干预作用后,与FN组相比,(FN+Cyclo-RGDfK)组(17.5%±2.1%)细胞的迁移率显著降低,差异均具有显著性(P < 0.05)。结果提示Cyclo-RGDfK能明显降低FN诱导MCF-10A细胞迁移率的增加。
|
| Fig 3 Migration induced by FN in breast epithelial cell MCF-10A reduced by Cyclo-RGDfK (50×) (x±s, n=3) *P < 0.05 vs control; #P < 0.05 vs FN |
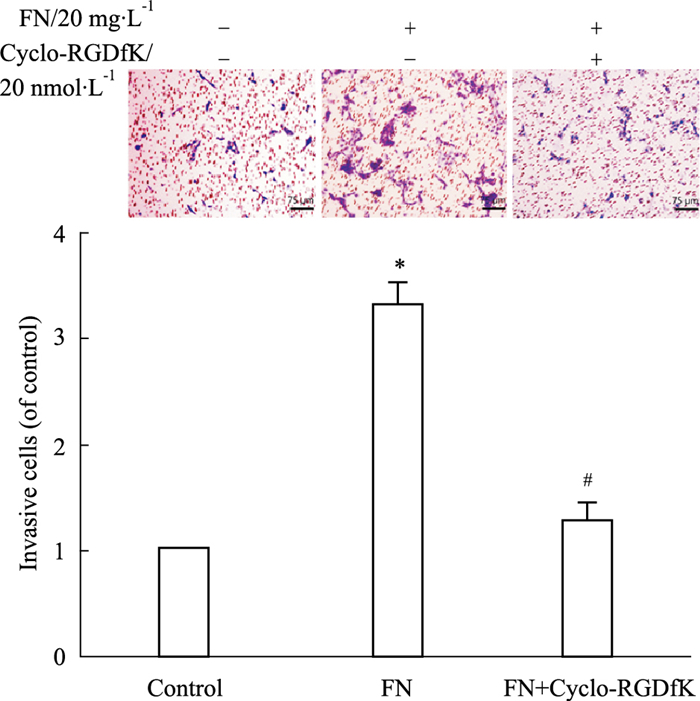
侵袭实验结果如Fig 4所示,与空白对照组的侵袭细胞数目比较,FN组细胞侵袭数目显著增多,侵袭能力明显增强,差异具有显著性(P < 0.05);经Cyclo-RGDfK处理的(FN+Cyclo-RGDfK)组与FN组相比,细胞穿过基底膜能力显著降低,透膜细胞数显著减少,差异具有统计学意义(P < 0.05)。结果表明,FN可增强MCF-10A细胞的侵袭能力,Cyclo-RGDfK能抑制FN诱导侵袭能力增加。
|
| Fig 4 Invasion induced by FN in breast epithelial cell MCF-10A reduced by Cyclo-RGDfK (100×) (x±s, n=3) *P < 0.05 vs control; #P < 0.05 vs FN |
乳腺癌的治疗是一个世界重大卫生问题,90%的乳腺癌患者死于肿瘤的远端转移[1]。乳腺癌的转移常伴随上皮细胞向间质表型转变的EMT过程,经历间质转化的上皮细胞获得类似成纤维细胞的形态,具有细胞骨架重组和增强的迁移、侵袭和转移能力[8]。EMT不仅是上皮细胞转变为肿瘤样细胞的重要条件,同时也是恶性肿瘤浸润和转移的基础。因此,抑制或逆转EMT过程可能是治疗乳腺癌转移的关键策略。
整合素αvβ3是由αv和β3亚基构成的异源二聚体。研究发现,整合素αvβ3参与了恶性肿瘤转移的病理生理过程,在乳腺癌组织中,浸润性肿瘤和远处转移部位均有整合素αvβ3的高表达,是预后不良的标志[9]。整合素αvβ3促使肿瘤细胞粘附于细胞外基质,并在血流过程中与血小板相互作用而滞留在毛细血管内,促进了乳腺癌转移灶的形成[10]。此外,敲低整合素αvβ3基因可使乳腺癌细胞中Vimentin、Snail等间充质标志物的表达降低并抑制细胞的迁移和侵袭能力[11]。
基于以上研究背景,开发整合素αvβ3的抑制剂已变成现代肿瘤靶向药物研发的热点。近几十年来,多种基于整合素的抗体或拮抗剂已经进入到临床试验阶段,整合素αvβ3拮抗剂(MK-0429)以及多整合素拮抗剂(GLPG0187)显示出治疗转移性前列腺癌良好的预后效果[12]。整合素αvβ3抗体(CNTO95)已完成Ⅱ期临床并报批Ⅲ期临床试验,整合素αvβ3拮抗剂(西仑吉肽)在治疗神经胶质母细胞瘤方面疗效显著,正在进行Ⅲ期临床并有望获批上市[13-14]。此外,临床前研究表明,Cyclo-RGDfK能显著降低卵巢癌细胞的迁移[15],但是Cyclo-RGDfK是否可以逆转乳腺癌细胞的EMT过程,目前鲜有文献报道。本研究结果显示FN能显著诱导MCF-10A乳腺上皮细胞发生间质转化,促进其侵袭和迁移,在给予Cyclo-RGDfK作用后可明显抑制FN诱导的间充质标志物N-cadherin和Vimentin蛋白表达上调,上调上皮标志物E-cadherin蛋白表达,同时伤口愈合实验和Transwell侵袭实验结果表明,Cyclo-RGDfK作用后,FN诱导引起的MCF-10A的迁移和侵袭被显著抑制。
纵上所述,Cyclo-RGDfK可逆转FN诱导的EMT过程,降低乳腺上皮细胞的侵袭和转移能力,其可能是治疗乳腺癌转移的有效候选药物,但是在体内的安全性以及有效性还有待进一步阐明。本研究为Cyclo-RGDfK药物开发提供了实验基础,也为乳腺癌的靶向治疗提供了新的思路。
| [1] |
Carpenter R L, Sirkisoon S, Zhu D, et al. Combined inhibition of AKT and HSF1 suppresses breast cancer stem cells and tumor growth[J]. Oncotarget, 2017, 8(43): 47-63. |
| [2] |
Jeong H, Ryu Y J, An J, et al. Epithelial-mesenchymal transition in breast cancer correlates with high histological grade and triple-negative phenotype[J]. Histopathology, 2012, 60(6B): 87-95. |
| [3] |
Bae Y K, Kim A, Kim M K, et al. Fibronectin expression in carcinoma cells correlates with tumor aggressiveness and poor clinical outcome in patients with invasive breast cancer[J]. Human Pathology, 2013, 44(10): 28-37. |
| [4] |
Chen Y, Chen L, Hong D, et al. Baicalein inhibits fibronectin-induced epithelial-mesenchymal transition by decreasing activation and upregulation of calpain-2[J]. Cell Death Dis, 2019, 10(5): 41-56. |
| [5] |
Fernandez Bedoya C, Carrión-Vázquez M, Fernández J M, et al. The mechanical hierarchies of fibronectin observed with single-molecule AFM[J]. J Mol Biol, 2002, 319(2): 33-47. |
| [6] |
郭滟. FN及其整合素β1受体与人脑胶质瘤侵袭行为的相关性研究[D].武汉: 华中科技大学, 2004. Guo X. Study on the relationship between FN and its integrin β receptor and invasive behavior of human glioma[D]. Wuhan: Hust, 2004. |
| [7] |
Shi K, Wang S L, Shen B, et al. Clinicopathological and prognostic values of fibronectin and integrin αvβ3 expression in primary osteosarcoma[J]. World J Surg Oncol, 2019, 17(1): 23-35. |
| [8] |
李汉清. 上皮间质转化的机制研究进展[J]. 中国药理学通报, 2017, 33(10): 42-4. Li H Q. Research progress on the mechanism of epithelial-mesenchymal transformation[J]. Chin Pharmacol Bull, 2017, 33(10): 42-4. |
| [9] |
Liapis H, Flath A, Kitazawa S. Integrin alphaV beta3 expression by bone-residing breast cancer metastases[J]. Diagn Mol Pathol, 1996, 5(2): 127-35. |
| [10] |
Felding-Habermann B, O"Toole T E, Smith J W, et al. Integrin activation controls metastasis in human breast cancer[J]. PNAS, 2001, 98(4): 53-8. |
| [11] |
Luo J, Yao J F, Deng X F. 14, 15-EET induces breast cancer cell EMT and cisplatin resistance by up-regulating integrin αvβ3 and activating FAK/PI3K/AKT signaling[J]. J Exp Clin Cancer Res, 2018, 37(1): 23. |
| [12] |
Cheng C, Komljenovic D, Pan L, et al. Evaluation of treatment response of cilengitide in an experimental model of breast cancer bone metastasis using dynamic PET with 18F-FDG[J]. Hell J Nucl Med, 2011, 14(1): 15-20. |
| [13] |
阮君山, 严令耕, 张蕾, 等. 以整合素为靶点的抗肿瘤转移药物研究进展[J]. 世界临床药物, 2011, 32(10): 14-8. Ruan J S, Yan L G, Zhang L, et al. Research progress of anti-tumor metastasis drugs targeting integrin[J]. World Clin Drugs, 2011, 32(10): 14-8. |
| [14] |
Desgrosellier J S, Cheresh D A. Integrins in cancer: biological implications and therapeutic opportunities[J]. Nat Rev Cancer, 2010, 10(1): 9-22. |
| [15] |
Schneider G, Suszynska M, Kakar S, et al. Vitronectin in the ascites of human ovarian carcinoma acts as a potent chemoattractant for ovarian carcinoma:Implication for metastasis by cancer stem cells[J]. J Cancer Stem Cell Res, 2016, 4(5): 1. |