

2. 河北医科大学第四医院检验科东、石家庄 050000;
3. 河北医科大学第四医乳腺中心,石家庄 050000
2. East Clinical Lab, the Fourth Hospital of Hebei Medical University, Shijiazhuang 050000, China;
3. Breast Cancer Center, the Fourth Hospital of Hebei Medical University, Shijiazhuang 050000, China
阿尔兹海默病(Alzheimer’s disease,AD)又称老年痴呆,是以记忆和认知功能障碍为主要特征的中枢神经系统退行性病变[1]。最近研究发现,神经炎症反应在AD病理学发展方面起到了关键的调节作用[2]。值得注意的是,在AD患者的大脑皮层和皮层下结构出现大量异常活化的星形胶质细胞。这些活化的星形胶质细胞聚集于AD患者脑内淀粉样蛋白和神经纤维缠结周围,并产生促炎症调节因子。这已经构成了AD发病早期出现的重要病理学现象[3]。这就提示我们,调节星形胶质细胞功能可能成为治疗大脑神经炎症反应的重要靶点。
近期大量的研究证实,神经甾体孕酮(progesterone,PG)具有显著的神经保护性作用,尤其在调节AD认知功能方面表现出独特的作用[4, 5]。研究组前期发现,在AD模型大鼠脑内PG分泌水平显著降低,当给予PG体内干预后AD大鼠认知功能得到明显改善[6]。然而,关于PG神经保护机制的探讨尚未完全阐明,其中PG对于脑神经炎症反应的调控机制尚不清楚,NOD样受体蛋白3(NOD-like receptor proteins 3,NLRP3)炎症小体所介导的神经炎症反应分子机制还需要进一步探索。因此,本文旨在研究PG对于Aβ诱导星形胶质细胞异常活化的调节作用,探索诱导NLRP3炎症小体活化可能分子机制,为PG改善AD早期大范围神经炎症反应提供理论依据。
1 材料与方法 1.1 主要试剂与仪器新生SD鼠,清洁级,河北省实验动物中心提供[许可证号:SCXK(冀)2008-1003];神经甾体PG、Aβ1-42片段,内质网应激抑制剂Salubrinal (Sal),内质网应激促进剂Tunicamycin (TM)均购置美国Sigma公司(St. Louis, MO, USA),DMEM培养液和胎牛血清FBS购置Gibco (Carlsbad, CA, USA),NLRP3、pro-IL-1β、β-actin抗体购置Cell Signaling公司(Beverly, MA, USA)。羊抗兔/FITC多克隆抗体购置Bioss公司(Beijing, China)。
1.2 原代星形胶质细胞培养星形胶质细胞来源于新生SD大鼠大脑皮层,无菌条件下破碎组织,制备单细胞悬液,37 ℃,5% CO2条件下孵育培养,每2 d更换培养液,待细胞充分覆盖后,37 ℃震荡去除多余小胶质细胞,应用免疫荧光染色鉴定星形胶质细胞纯度(纯度>95%),纯化后的细胞分别接种于细胞培养板(用于ELISA、Immofluorescence、Western blot试验)。
1.3 ELISA检测取正常培养星形胶质细胞,经过干预处理后,应用ELISA试剂盒检测细胞上清IL-1β的分泌水平改变。首先,建立0~1 000 ng·L-1标准曲线。然后取上清100 μL加入到预先孵育抗IL-1β培养板内。根据试剂盒说明书要求,分别要求依次加入检测试剂。最后应用酶标仪在450 nm处检测细胞上清IL-1β浓度。
1.4 Western blot检测取星形胶质细胞裂解后提取总蛋白,BCA蛋白试剂盒计算蛋白含量,提取蛋白,分别制备10%或15% SDS分离胶分离蛋白,并通过半干转法转移至PVDF膜。PVDF膜应用5%脱脂奶粉封闭,4 ℃分别孵育pro-IL-1β和NLRP3抗体过夜,室温孵育二抗2 h,ECL光化学显色。最后应用Image J分析软件对扫描条带进行定量分析。
1.5 免疫荧光检测取4%甲醛固定星形胶质细胞,0.05% Triton X-100和3% BSA封闭打孔,4 ℃分别孵育NLRP3抗体过夜,室温孵育二抗2 h,DAPI进行核染色,应用荧光显微镜检测细胞。
1.6 药物干预与分组取正常培养星形胶质细胞,随机分为对照组、Aβ组(5 μmol·L-1)、TM组(5 μmol·L-1)、PG保护组(1 μmol·L-1)、Sal处理组(10 μmol·L-1)。Aβ组给予多聚化Aβ1-42干预6 h;TM处理组应用TM干预处理2 h;PG保护组给予PG和TM或Aβ共同处理6 h;Sal处理组应用Sal预处理1 h,然后与PG、Aβ共处理6 h。对照组给予DMEM培养基对照处理。
1.7 统计学方法各组数据均以x±s表示,应用SPSS 15.0统计软件采用单因素方差分析进行统计学处理(One way ANOVA)。
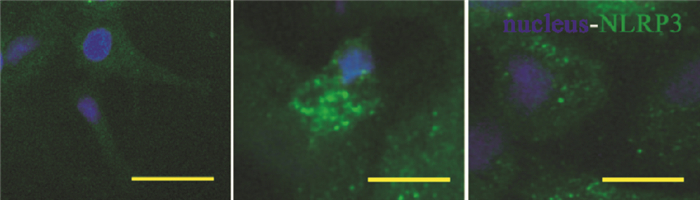
2 结果 2.1 PG抑制Aβ诱导星形胶质细胞NLRP3表达活化如Fig 1免疫荧光结果所示,与对照组相比较,Aβ干预处理6 h,在星形胶质细胞内炎症小体NLRP3出现了大量聚集,在胞质和胞核附近均出现明显表达;相比Aβ组,PG明显抑制了Aβ所致星形胶质细胞NLRP3的大量表达。
|
| 图 1 Aβ-induced NLRP3 inflammasome activation in astrocyte inhibited by PG Left picture was control group, middle picture was Aβ-treated group, right picture was PG-treated group; NLRP3 was stained green, nucleus was stained blue, scale bar=20 μm |
如Fig 2 ELISA结果所示,相比对照组,Aβ组和TM组IL-1β分泌水平均出现明显增加(P < 0.01);相比Aβ组和TM组,PG明显抑制IL-1β分泌水平增加(P < 0.01)。

|
| 图 2 Aβ-induced IL-1β secretion via regulating ER stress in astrocyte inhibited by PG(x±s, n=3) **P < 0.01 vs Aβ-treated group, ##P < 0.01 vs TM-treated group |
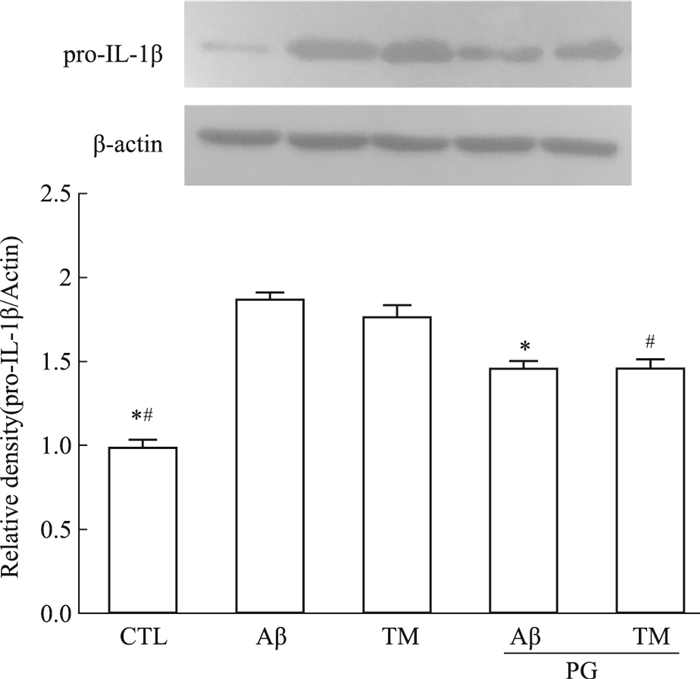
如Fig 3 Western blot结果所示,相比对照组,Aβ和TM均促进了星形胶质细胞pro-IL-1β表达(P < 0.05)。相比Aβ组和TM组,PG明显抑制Aβ或TM所致pro-IL-1β表达水平增加(P < 0.05)。研究结果表明,PG能通过抑制内质网应激活化降低星形胶质细胞成熟型pro-IL-1β片段的形成。
|
| 图 3 Aβ-induced pro-IL-1β expression via regulating ER stress in astrocytes inhibited by PG(x±s, n=3) *P < 0.05 vs Aβ-treated group, #P < 0.05 vs TM-treated group |
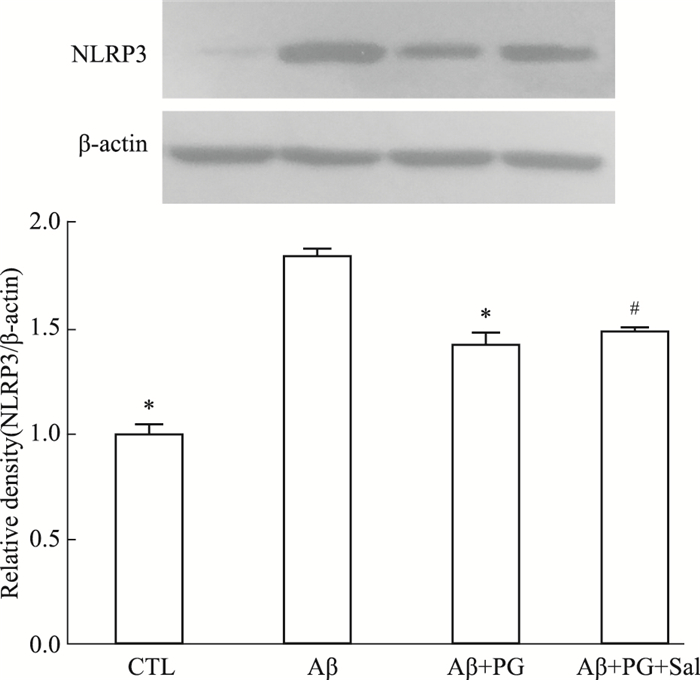
如Fig 4 Western blot结果所示,相比对照组,Aβ组明显促进星形胶质细胞NLRP3表达活化(P < 0.05)。相比Aβ组,PG明显抑制NLRP3表达水平的增加(P < 0.05)。相比于PG保护组,Sal明显性阻断PG对于Aβ所诱导NLRP3表达的抑制作用(P < 0.05)。研究结果说明,PG通过调节内质网应激活化抑制Aβ所致星形胶质细胞NLRP3表达增加。
|
| 图 4 Aβ-induced NLRP3 expression via regulating ER stress in astrocytes inhibited by PG(x±s, n=3) *P < 0.05 vs Aβ-treated group, #P < 0.05 vs PG-treated group |
随着AD致病机制的深入研究,神经炎症反应作为AD重要的病理学特征之一逐渐受到研究者的广泛关注[7]。研究发现,AD患者的大脑皮层和皮层下结构存在广泛的胶质细胞活化,且伴随着大范围炎症反应发生。这已经构成AD早期出现的重要病理学改变。因此,减少Aβ所引起的星形胶质细胞功能损伤可能成为降低其所诱发的大范围神经炎症反应的重要防治策略之一。IL-1β常常被看作是一个“疾病因子”,对脑海马依赖的记忆功能表现出持续的影响[8]。然而,IL-1β的成熟和分泌需要NLRP3炎症小体活化的参与。研究显示,NLRP3炎症小体活化以及其所介导的促炎症反应信号通路对于调节AD损伤方面表现出明显作用[9]。我们研究发现,Aβ能够诱导NLRP3炎症小体在星形胶质细胞内大量活化表达。因此,为了解决AD治疗的重要问题,亟待开发抑制NLRP3炎症小体表达活化有效药物并阐明可能的调控机制。
神经甾体PG作为重要的内源性神经活性甾体化合物,在调节神经细胞功能方面发挥着重要作用,特别是对改善AD方面发挥着潜在的治疗功能[6]。但是,PG对于AD的神经保护机制尚未完全阐明。目前大量研究发现,PG在调节脑缺血和脑损伤方面表现出显著的神经保护性作用,特别是在促进神经元存活,抑制神经元凋亡等方面作用明显[5, 10]。然而,关于PG对于神经炎症反应的调节作用研究较少。我们首先评估神经甾体PG对于NLRP3炎症小体表达的影响,研究发现,PG能够显著性的抑制Aβ所致的星形胶质细胞NLRP3表达,并降低Aβ所诱导的神经炎症反应IL-1β、pro-IL-1β的合成分泌。尽管PG对于NLRP3炎症小体在细胞分子内的调控机制尚未完全阐明,但是可以肯定的是,在溶酶体损伤[11]、线粒体钙离子通量改变[12],以及氧化应激片段ROS形成[13]等应激条件下能明显激活细胞内NLRP3炎症信号。为了证实上述假设,我们应用内质网应激诱导剂TM或Aβ干预星形胶质细胞,然后给予PG处理后发现,PG能够明显抑制TM或Aβ所致IL-1β、pro-IL-1β分泌以及NLRP3的表达合成。与之相反,内质网应激抑制剂Sal显著阻断了PG对于Aβ所致NLRP3表达的抑制作用。在一定程度说明了PG对于AD的神经保护性作用,特别是对于NLRP3相关神经炎症反应的抑制作用,并在调控内质网应激相关AD功能损伤方面存在潜在的联系[14]。该研究结果表明,NLRP3炎症小体可能成为神经甾体PG对于AD治疗的一个潜在的分子调控靶点。
综上所述,本研究阐明了神经甾体PG对于Aβ所致星形胶质细胞NLRP3炎症小体活化的神经保护性机制,并建立了Aβ所致内质网应激活化与星形胶质细胞神经炎症反应的潜在联系,进一步加深我们对于AD致病机制的认识,为AD的临床治疗提供新的治疗思路。
| [1] |
Selkoe D J. Alzheimer's disease: genes, proteins, and therapy[J]. Physiol Rev, 2001, 81(2): 741-66. doi:10.1152/physrev.2001.81.2.741 |
| [2] |
McGeer E G, McGeer P L. Neuroinflammation in Alzheimer's disease and mild cognitive impairment: a field in its infancy[J]. J Alzheimers Dis, 2010, 19(1): 355-61. doi:10.3233/JAD-2010-1219 |
| [3] |
Parachikova A, Agadjanyan M G, Cribbs D H, et al. Inflammatory changes parallel the early stages of Alzheimer disease[J]. Neurobiol Aging, 2007, 28(12): 1821-33. doi:10.1016/j.neurobiolaging.2006.08.014 |
| [4] |
Gonzalez S L, Labombarda F, Gonzalez Deniselle M C, et al. Progesterone neuroprotection in spinal cord trauma involves up-regulation of brain-derived neurotrophic factor in motoneurons[J]. J Steroid Biochem Mol Biol, 2005, 94(1-3): 143-9. doi:10.1016/j.jsbmb.2005.01.016 |
| [5] |
Espinosa-Garcia C, Aguilar-Hernandez A, Cervantes M, et al. Effects of progesterone on neurite growth inhibitors in the hippocampus following global cerebral ischemia[J]. Brain Res, 2014, 1545: 23-34. doi:10.1016/j.brainres.2013.11.030 |
| [6] |
Liu S, Wu H, Xue G, et al. Metabolic alteration of neuroactive steroids and protective effect of progesterone in Alzheimer's disease-like rats[J]. Neural Regen Res, 2013, 8(30): 2800-10. |
| [7] |
Mrak R E, Griffin W S. Glia and their cytokines in progression of neurodegeneration[J]. Neurobiol Aging, 2005, 26(3): 349-54. doi:10.1016/j.neurobiolaging.2004.05.010 |
| [8] |
Blasko I, Veerhuis R, Stampfer-Kountchev M, et al. Costimulatory effects of interferon-gamma and interleukin-1beta or tumor necrosis factor alpha on the synthesis of Abeta1-40 and Abeta1-42 by human astrocytes[J]. Neurobiol Dis, 2000, 7(6 Pt B): 682-9. |
| [9] |
Kitazawa M, Cheng D, Tsukamoto M R, et al. Blocking IL-1 signaling rescues cognition, attenuates tau pathology, and restores neuronal beta-catenin pathway function in an Alzheimer's disease model[J]. J Immunol, 2011, 187(12): 6539-49. doi:10.4049/jimmunol.1100620 |
| [10] |
Garling R J, Watts L T, Sprague S, et al. Does progesterone show neuroprotective effects on traumatic brain injury through increasing phosphorylation of Akt in the hippocampus[J]. Neural Regen Res, 2014, 9(21): 1891-6. doi:10.4103/1673-5374.145355 |
| [11] |
Hornung V, Latz E. Critical functions of priming and lysosomal damage for NLRP3 activation[J]. Eur J Immunol, 2010, 40(3): 620-3. doi:10.1002/eji.200940185 |
| [12] |
Arlehamn C S, Petrilli V, Gross O, et al. The role of potassium in inflammasome activation by bacteria[J]. J Biol Chem, 2010, 285(14): 10508-18. doi:10.1074/jbc.M109.067298 |
| [13] |
Shimada K, Crother T R, Arditi M. Innate immune responses to Chlamydia pneumoniae infection: role of TLRs, NLRs, and the inflammasome[J]. Microbes Infect, 2012, 14(14): 1301-7. doi:10.1016/j.micinf.2012.08.004 |
| [14] |
黄倩倩, 温彬宇, 闫妍, 等. 内质网应激和自噬的交互作用及其在阿尔茨海默病进展与防治中的作用[J]. 中国药理学通报, 2018, 34(11): 1500-4. Huang Q Q, Wen B Y, Yan Y, et al. Crosstalk between endoplasmic reticulum stress and autophagy and its role in pathogenesis and prevention of Alzheimer's disease[J]. Chin Pharmacol Bull, 2018, 34(11): 1500-4. doi:10.3969/j.issn.1001-1978.2018.11.006 |

