

糖尿病性视网膜病变是一种慢性疾病,是人类致盲的主要原因之一,到2010年全球有1.66亿人患有糖尿病视网膜病,并且到2030年这一数字会增加到1.9亿,每年的新增患者达200万[1]。糖尿病视网膜病变发病机制之一是线粒体电子传递链活性氧ROS的增加,它导致视网膜组织损伤加重,使视网膜神经细胞不可逆凋亡[2]。毛细血管内皮细胞及周细胞氧化应激导致的凋亡、炎症反应以及毛细血管血流动力学的改变都会引起视网膜缺血缺氧,而缺血缺氧是导致视网膜新生血管的重要原因,它会促进毛细血管内皮细胞的迁移和增殖,并使血管内皮细胞间的连接变得疏松[3]。大量研究显示,蛋白激酶C(protein kinase C, PKC)通路的激活是导致糖尿病性视网膜病变发病的重要原因之一,在缺氧环境中PKC-β的高表达会导致新生血管的形成,同时抑制PKC-β会导致新生毛细血管的减少[4]。
藏红花酸是藏红花提取物的主要成分,属于类胡萝卜素衍生物,口服藏红花酸可经小肠快速吸收,并以游离或与葡萄糖醛酸结合的方式存在于血浆中[5]。目前藏红花酸可治疗视网膜缺血/再灌注[6]以及氧化应激而导致的视网膜凋亡[7]并且研究发现其可以抑制视网膜微血管内皮细胞的增殖和迁移[8]。本文探讨藏红花酸对糖尿病视网膜病变的保护作用的机制,对于糖尿病视网膜病变的药物治疗提供新的治疗靶点,为进一步的基础及临床研究提供可能基础。
1 材料和方法 1.1 材料 1.1.1 实验动物♂ SD大鼠购自南昌大学动物实验科学部,选用健康♂ SD大鼠体质量约180 g,所有大鼠实验前均经检查眼底,无眼部病变。
1.1.2 试剂藏红花酸购自四川维克奇生物科技有限公司(批号:wkq16041207);链脲佐菌素(streptozotocin, STZ)购自美国Sigma公司;兔抗鼠cleaved-caspase-3购自武汉塞维尔生物公司;兔抗鼠一抗PKC-β抗体、羊抗兔二抗IgG抗体、兔抗鼠一抗GAPDH抗体购自美国Abcam公司;TRIzol试剂盒购自全式金生物科技公司、RNA保存液购自武汉博士德生物有限公司、Premix×TaqTM试剂盒、RNase-free water、SYBR®Premix Ex TaqTMII(Tli RNaseH Plus)购自日本TaKaRa公司;其余试剂均为化学分析纯。
1.1.3 仪器倒置相差显微镜(日本Olympus公司);蛋白凝胶电泳系统美国(Bio-Rad公司);ABI7300实时荧光定量PCR仪(ABI公司);RM2016型病理石蜡切片机(德国徕卡公司);微量移液器(德国Eppendorf公司);眼科显微手术器械(南京康华医疗器械有限公司)。
1.2 造模及分组 1.2.1 造模采用STZ建立糖尿病大鼠模型,STZ按4 g·L-1溶解于0.1 mmol·L-1柠檬酸缓冲液(pH 4.0~4.5),注射量为60 mg·kg-1,72 h后取大鼠尾静脉血,测血糖,当血糖≥16.6 mmol·L-1即为成模大鼠,正常组大鼠将造模药物换成等量生理盐水。
1.2.2 实验分组分4组每组10只大鼠,正常对照组(CON):食道灌胃给0.5% CMC-Na 3 mL;糖尿病对照组(DM):食道灌胃给0.5% CMC-Na 3 mL,DM+藏红花酸低剂量组[DM+CRO(L)]:经食道灌胃给藏红花酸50 mg·kg-1,qd.8周,DM+藏红花酸高剂量组[DM+CRO(H)]:经食道灌胃给藏红花酸100 mg·kg-1,qd.8周。
1.3 免疫组化石蜡切片脱蜡入水,微波抗原修复10 min,过氧化氢封闭10 min,加3% BSA,室温封闭30 min,滴加cleaved-caspase-3抗体,置于湿盒内4℃冰箱孵育24 h,加二抗覆盖组织,室温孵育50 min,玻片置于脱色摇床上洗涤15 min后加DBA显色液,显微镜下控制显色时间,显色棕黄色为阳性,脱水封片,图像采集:采用HPIAS-1000高清晰病理彩色图像分析系统对免疫组织化学染色阳性产物进行分析。记录6个400倍视野阳性单位(PU),取其平均值,用PU值的大小代表阳性产物表达量的多少。
1.4 qRT-PCR引物设计, Bcl-2上游引物5′-AGATCGTGATGAAGTACA-3′,下游引物5′-TGCTCTCAGGCTGGAAGGA-3′;BAX上游引物5′-CACCAGCTCTGAACAGATCAT-3′,下游引物5′-CCTCTGCAGCTCCATGTTGT-3′;PKCβ上游引物5′-GAGGTCCTCATCGTTGTTGT-3′,下游引物5′-TGATAGTCTTGGTCTTCTGC-3′;GAPDH上游引物5′-AGTGCCAGCCTCGTCTCATA3-′下游引物5′-GACTGTGCCGTTGAACTTGC-3′。用TRIzol提取RNA并检测纯度,逆转录按试剂盒说明进行操作,实时荧光定量PCR按SYBR®Premix Ex TaqTMII试剂盒操作进行,反应条件:预变性;60 ℃,30 s;95 ℃,30 s,95 ℃,3 s;PCR扩增40个循环。反应结束后确认荧光定量PCR的扩增曲线和溶解曲线输出CT值,按2ΔΔCT数据分析结果。
1.5 蛋白质印迹提取眼球视网膜神经上皮中总蛋白,将配置好SDS-PAGE胶置于电泳槽中,待用蛋白置于水锅中煮沸5 min后,充分混匀,上样孔中分别加入Marker及样品蛋白20 μL,样品经SDS-PAGE转移至PVDF膜,用5%脱脂奶粉封闭1 h,洗膜两分钟,加入一抗, 置于4 ℃冰箱中孵育过夜,用1×TBST溶液洗膜3次,10 min/次,加入稀释的二抗(1% BSA以1 :10 000稀释),置于水平摇床中,孵育60 min后1×TBST溶液洗膜10 min×3次,后在暗室中进行曝光显影。
1.6 统计学分析采用SPSS19.0对实验结果进行分析,各组数据均以x±s表示,采用单因素方差分析或重复测量方差分析,两组间比较采用t检验。
2 结果 2.1 免疫组化染色结果判定免疫组化结果如Tab 1、Fig 1所示,糖尿病大鼠视网膜中凋亡细胞主要存在于神经节细胞层和内核层,藏红花酸高剂量和低剂量组糖尿病大鼠视网膜内核层及神经节细胞层caspase-3的表达较糖尿病对照组下降,藏红花酸高剂量处理组较藏红花酸低剂量处理组caspase-3表达下降。
| Group | caspase-3 |
| CON | 214.0±40.1 |
| DM+CRO(H) | 1 238.3±64.6#*△ |
| DM+CRO(L) | 1 560.0±167.0#* |
| DM | 1 907.0±145.4# |
| P | 0.000 |
| #p < 0.05 vs CON,*P < 0.05vsDM,△ < 0.01vsDM+CRO(L) | |

|
| 图 1 Expression of caspase-3 in the inner nuclear layer and ganglion cell layer of rats A=CON, B=DM+CRO(H), C=DM+CRO(L), D=DM(400×) |
qRT-PCR检测显示TNF-α mRNA红花酸高剂量及低剂量处理组间表达对比无明显差异,其余各组之间的表达如Tab 2示,与对照组相比差异均有显著性。
| Group | TNF-α/GAPDH |
| CON | 1.325±0.220 |
| DM+CRO(H) | 1.891±0.222#* |
| DM+CRO(L) | 2.019±0.208#* |
| DM | 3.476.0±0.267# |
| P | 0.000 |
| #P<0.05 vs CON, *P<0.01 vs DM | |
如Tab 3示藏红花酸高剂量及低剂量处理组大鼠Bax mRNA的表达较糖尿病对照组大鼠下降,藏红花酸高剂量较低剂量处理组表达下降,差异有统计学意义。Tab 3 Expression of Bax mRNA
| Group | Bax/GAPDH |
| CON | 1.411±0.274 |
| DM+CRO(H) | 2.054±1.428#*△ |
| DM+CRO(L) | 2.518±0.060#* |
| DM | 3.542.0±0.267# |
| P | 0.000 |
| #P<0.01 vs CON, *P<0.01 vs DM, △P<0.05 vs DM+CRO(L) | |
如Tab 4示藏红花酸高剂量及低剂量处理组大鼠Bcl-2 mRNA的表达较糖尿病对照组大鼠升高,藏红花酸高剂量较低剂量处理组表达升高,差异有统计学意义。Tab 4 Expression of Bcl-2 mRNA
| Group | Bcl-2/GAPDH |
| CON | 2.465±0.112 |
| DM+CRO(H) | 1.956±0.120#*△ |
| DM+CRO(L) | 1.514±0.114#* |
| DM | 0.578±0.2183# |
| P | 0.000 |
| #P<0.05 vs CON, *P<0.01 vs DM, △P<0.05 vs DM+CRO(L) | |
如Tab 5示藏红花酸高剂量及低剂量处理组大鼠PKC-β mRNA的表达较糖尿病对照组大鼠均下降,藏红花酸高剂量较低剂量处理组表达下降,差异有统计学意义。
| Group | PKC-β/GAPDH |
| CON | 1.377±0.281 |
| DM+CRO(H) | 2.515±0.876#*△ |
| DM+CRO(L) | 2.930±0.802#* |
| DM | 3.614±0.314# |
| P | 0.000 |
| #P<0.01 vs CON, *P<0.01 vs DM, △P<0.05 vs DM+CRO(L) | |
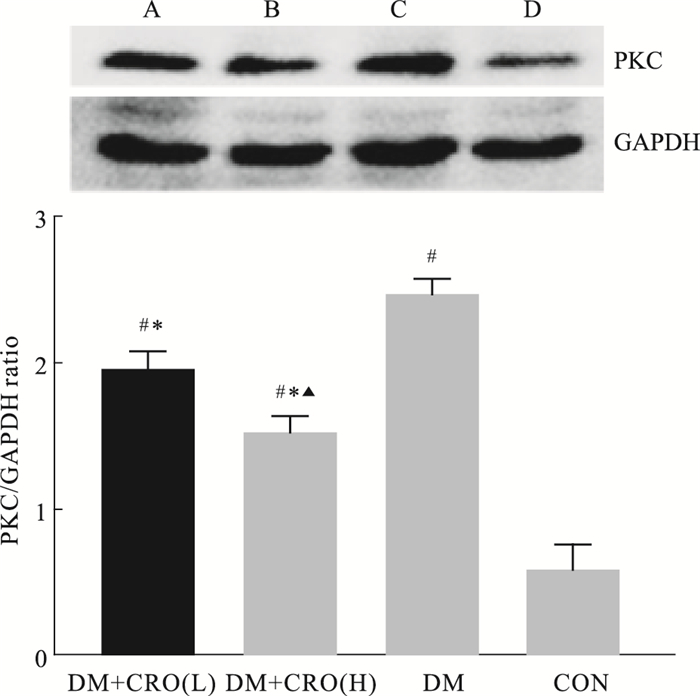
各组PKC蛋白与内参GAPDH蛋白质印记结果如Fig 2所示,藏红花酸高剂量及低剂量处理组大鼠PKC的表达较糖尿病对照组大鼠下降(t=4.95, P=0.00),藏红花酸高剂量较低剂量处理组表达下降,差异有统计学意义(t=5.68,P=0.00)。
|
| 图 2 Expression of PKC in rat retinal nerve epithelium A=DM+CRO(L), B=DM+CRO(H), C=DM, D=CON. #P<0.01 vs CON, *P<0.01 vs DM, △P<0.05 vs DM+CRO(L) |
PKC广泛分布于多种组织、器官和细胞,是多功能丝氨酸和苏氨酸激酶,它控制着糖代谢并参与基因的表达调控,同时PKC的激活是糖尿病视网膜病变发生的重要原因之一[9],本实验通过蛋白质印迹法检测大鼠视网膜神经上皮PKC的表达,发现藏红花酸处理组PKC的表达较糖尿病对照组减少,表明藏红花酸在糖尿病大鼠中可通过抑制PKC基因和蛋白表达进而对大鼠视网膜神经上皮起到保护作用。
既往有研究发现,藏红花酸可以抑制视网膜缺血/再灌注损伤,减少视网膜神经节细胞层及内核层细胞的凋亡[10],并且研究还发现藏红花酸可以抑制caspase-3和caspase-9而保护由H2O2引起的视网膜变性[11],而高糖使视网膜细胞线粒体产生过度氧自由基而导致的糖尿病视网膜产生氧化应激损害[12],本实验通过免疫组化检测caspase-3在视网膜神经上皮表达发现caspase-3主要表达在内核层和神经节细胞层,并且藏红花酸处理组较糖尿病对照组表达降低,藏红花酸高剂量组较藏红花酸低剂量组表达下降,这表明藏红花酸减少糖尿病大鼠视网膜神经上皮细胞的凋亡。研究显示高血糖同时可以激活视网膜内免疫炎症反应,使视网膜内免疫炎症失调,位于视网膜内丛状层的小胶质细胞是主要的免疫炎症反应细胞,小胶质细胞激活而产生的各种神经毒性分子如NF-κB和IL-1β[13],并且caspase-3与炎症因子密切相关,在糖尿病大鼠中细胞外的凋亡系统通常是由TNF-α受体激活,在视网膜血管凋亡时有大量的TNF-α受体激活,该受体的激活导致Bax进入线粒体,导致线粒体的氧自由基增加进一步触发细胞色素C释放进入细胞质中,进而caspase-3诱导细胞的凋亡[14]。研究显示Bcl-2可以减少糖尿病大鼠微血管中血管内皮细胞的损害[15],减少超氧化物的生成,并减少视网膜微血管白细胞的粘附,这些都有利于改善缺血缺氧的损害。本研究显示,藏红花酸处理组大鼠TNF-α及Bax较糖尿病对照组下降,而Bcl-2较糖尿病对照组上升,这表明藏红花酸通过降低TNF-α的表达,减少TNF-α受体的激活减少视网膜内炎症反应,同时减少Bax基因表达,进而减少凋亡蛋白caspase-3的表达,同时抗凋亡相关基因Bcl-2的增加也减少caspase-3表达,从而减少神经节细胞及内核层细胞的凋亡。
综上所述,藏红花酸通过抑制TNF-α、caspase-3的表达,减少凋亡促进基因Bax表达,并提高凋亡抑制基因Bcl-2的表达,进而抑制视网膜中内核层及神经节细胞的凋亡,并且藏红花酸通过抑制PKC基因和蛋白的表达,减少糖尿病视网膜病变通路之一的PKC通路的激活,从而对糖尿病性视网膜病变起到治疗作用。
( 致谢: 本实验分别于江西省分子医学重点实验室和南昌大学动物实验科学部完成,感谢江西省分子医学重点实验室老师对本实验的指导。)
| [1] |
Zheng Y, He M, Congdon N, et al. The worldwide epidemic of diabetic retinopathy[J]. Indian J Ophthalmol, 2012, 60(5): 428-31. doi:10.4103/0301-4738.100542 |
| [2] |
Du Y, Miller C M, Kern T S, et al. Hyperglycemia increases mitochondrial superoxide in retina and retinal cells[J]. Free Radic Biol Med, 2003, 35(11): 1491-9. doi:10.1016/j.freeradbiomed.2003.08.018 |
| [3] |
Miller J W, Adamis A P, Aiello L P, et al. Vascular endothelial growth factor in ocular neovascularization and proliferative diabetic retinopathy[J]. Diabetes Metab Rev, 1997, 13(1): 37-50. doi:10.1002/(SICI)1099-0895(199703)13:1<37::AID-DMR174>3.0.CO;2-K |
| [4] |
Aiello L P. The potential role of PKC beta in diabetic retinopathy and macular edema[J]. Surv Ophthalmol, 2002, 47(2): S263-9. |
| [5] |
Zhang Y, Fei F, Zhen L, et al. Sensitive analysis and simultaneous assessment of pharmacokinetic properties of crocin and crocetin after oral administration in rats[J]. J Chromatogr B Analyt Technol Biomed Life Sci, 2017, 1044-1045: 1-7. doi:10.1016/j.jchromb.2016.12.003 |
| [6] |
Ishizuka F, Shimazawa M, Umigai N, et al. Crocetin, a carotenoid derivative, inhibits retinal ischemic damage in mice[J]. Eur J Pharmacol, 2013, 703(1-3): 1-10. doi:10.1016/j.ejphar.2013.02.007 |
| [7] |
Yamauchi M, Tsuruma K, Imai S, et al. Crocetin prevents retinal degeneration induced by oxidative and endoplasmic reticulum stresses via inhibition of caspase activity[J]. Eur J Pharmacol, 2011, 650(1): 110-9. doi:10.1016/j.ejphar.2010.09.081 |
| [8] |
Umigai N, Tanaka J, Tsuruma K, et al. Crocetin, a carotenoid derivative, inhibits VEGF-induced angiogenesis via suppression of p38 phosphorylation[J]. Curr Neurovasc Res, 2012, 9(2): 102-9. doi:10.2174/156720212800410830 |
| [9] |
Kajita K, Ishizuka T, Miura A, et al. Glucocorticoid-induced insulin resistance associates with activation of protein kinase C isoforms[J]. Cell Signal, 2001, 13(3): 169-75. doi:10.1016/S0898-6568(01)00143-7 |
| [10] |
Ishizuka F, Shimazawa M, Umigai N, et al. Crocetin, a carotenoid derivative, inhibits retinal ischemic damage in mice[J]. Eur J Pharmacol, 2013, 703(1-3): 1-10. doi:10.1016/j.ejphar.2013.02.007 |
| [11] |
Yamauchi M, Tsuruma K, Imai S, et al. Crocetin prevents retinal degeneration induced by oxidative and endoplasmic reticulum stresses via inhibition of caspase activity[J]. Eur J Pharmacol, 2011, 650(1): 110-9. doi:10.1016/j.ejphar.2010.09.081 |
| [12] |
Oshitari T, Yamamoto S, Hata N, et al. Mitochondria-and caspase-dependent cell death pathway involved in neuronal degeneration in diabetic retinopathy[J]. Br J Ophthalmol, 2008, 92(4): 552-6. doi:10.1136/bjo.2007.132308 |
| [13] |
Nam K N, Park Y M, Jung H J, et al. Anti-inflammatory effects of crocin and crocetin in rat brain microglial cells[J]. Eur J Pharmacol, 2010, 648(1-3): 110-6. doi:10.1016/j.ejphar.2010.09.003 |
| [14] |
Adamiec-Mroczek J, Zajac-Pytrus H, Misiuk-Hojło M, et al. Caspase-dependent apoptosis of retinal ganglion cells during the development of diabetic retinopathy[J]. Adv Clin Exp Med, 2015, 24(3): 531-5. doi:10.17219/acem/31805 |
| [15] |
周云丰, 李琳, 许扬, 等. 黄芪甲苷对甲基乙二醛诱导的人视网膜色素上皮细胞损伤的保护作用研究[J]. 中国药理学通报, 2017, 33(7): 915-21. Zhou Y F, Li L, Xu Y, et al. Protective effect of astragalosides Ⅳ on retinal pigment epithelium injury induced by methylglyoxal[J]. Chin Pharmacol Bull, 2017, 33(7): 915-21. doi:10.3969/j.issn.1001-1978.2017.07.007 |

