

2. 南华大学肿瘤研究所, 湖南省胃癌研究中心, 湖南省高校肿瘤细胞与分子病理学重点实验室, 湖南 衡阳 421001;
3. 湖南省中医药专科学校附属医院肿瘤科, 湖南 株洲 412012
2. Cancer Research Institute, Center for Gastric Cancer Research of Hunan Province, Key Lab of Cancer Cellular and Molecular Pathology of Hunan Provincial University, University of South China, Hengyang Hunan 421001, China;
3. Dept of Oncology, the Affiliated Hospital, Hunan College of Traditional Chinese Medicine, Zhuzhou Hunan 412012, China
转化生长因子β1(transforming growth factor-β1,TGF-β1)诱导肿瘤细胞由上皮细胞向间质细胞转化(epithelial-mesenchymal transition,EMT)。信号通路之间相互作用可促进TGF-β1诱导EMT。Rac1通路介导TGF-β1诱导前列腺癌细胞EMT[1]。Rac1促进Wnt3a激活ST2细胞β-catenin[2]。
二烯丙基二硫(diallyl disulfide,DADS)通过干预多条信号通路抑制肿瘤细胞增殖与侵袭。我们之前报道,DADS下调Rac1通路可抑制胃癌细胞EMT[3];DADS下调β-catenin表达与其抑制胃癌细胞EMT有关[4];DADS通过上调miR22下调Wnt-1表达,抑制胃癌细胞侵袭与迁移[5]。
本实验观察DADS对TGF-β1诱导Rac1和β-catenin表达的影响,探讨DADS抑制胃癌细胞EMT是否通过TGF-β1/Rac1通路下调β-catenin表达。
1 材料与方法 1.1 细胞培养人胃癌MGC803细胞株由南华大学肿瘤研究所保存,用含10%小牛血清的RPMI1640培养基培养,置于37 ℃,5% CO2、饱和湿度的培养箱。
1.2 试剂DADS购自Fluka公司,将其与Tween-80按1 :2比例溶解,再用生理盐水稀释100倍,储存于-20 ℃冰箱备用。人重组TGF-β1(R&D Systems,USA);小牛血清(杭州四季青生物工程公司),RPMI1640培养基(Gibco公司);Total RNA Kit(Omega公司),RT试剂盒(Invitrogen公司),PCR试剂(Promega公司);BCA蛋白定量试剂盒(Promega公司);TGF-β1、Rac1、β-catenin抗体购自Abcam公司,E-cadherin和vimentin购自Cell Signaling Technology公司,β-actin抗体、二抗、ECL发光试剂盒购自Santa Cruz公司;TGF-β1受体阻断剂SB431542和Rac1抑制剂NSC23766购自Cayman Chemical公司。
1.3 RT-PCR使用Total RNA Kit提取细胞总RNA后,用RT试剂盒逆转录成cDNA。设计扩增引物,使用试剂盒进行PCR。TGF-β1:F 5′-TCT CCA GGC ATT TCC ACT ATT C-3′,R 5′-CTC AGG CAT TCG TCA ACA TCT A-3′;Rac1:F 5′-TGC CTG CTG TTG TAA ATG TCT C-3′,R 5′-AAA GTT CAG TGC TCG GTG TTC T-3′;β-catenin:F 5′-GGA AGG GAC AGT ATC GTT TGT T-3′,R 5′-GCC TCA GCA TCT ACC AGC ATA G-3′;E-cadherin:F 5′-CTC CCA ATA CAT CTC CCT TCA C-3′,R 5′-CGC CTC CTT CTT CAT CAT AGT AA-3′;vimentin:F 5′-GCG AGG AGA GCA GGA TTT CT-3′,R 5′-TCT TGT AGG AGT GTC GGT TGT T-3′; β-actin: F 5′-CTG GGA CGA CAT GGA GAA AA-3′,R 5′-AAG GAA GGA TGG AAG AGT GC-3′。PCR产物经琼脂糖凝胶电泳,用BIO-RAD成像系统拍照,AlphaImager 2200软件扫描,以β-actin为内对照,计算相对光密度值。
1.4 Western blot将收集的细胞置于细胞裂解液中,冰上放置30 min后,12 000 r·min-1离心10 min,提取上清液,BCA法测定蛋白浓度。蛋白样本经10% SDS-聚丙烯酰胺凝胶电泳后转移至PVDF膜,膜封闭1 h后孵育一抗,4 ℃过夜。用TBST洗膜,二抗孵育1 h,洗膜后用ECL发光,X片显影、定影。
1.5 统计学分析实验数据用x ± s表示,采用SPSS 13.0软件进行统计学分析,组间数据比较采用student′s t-tests或one-way ANOVA分析方法。
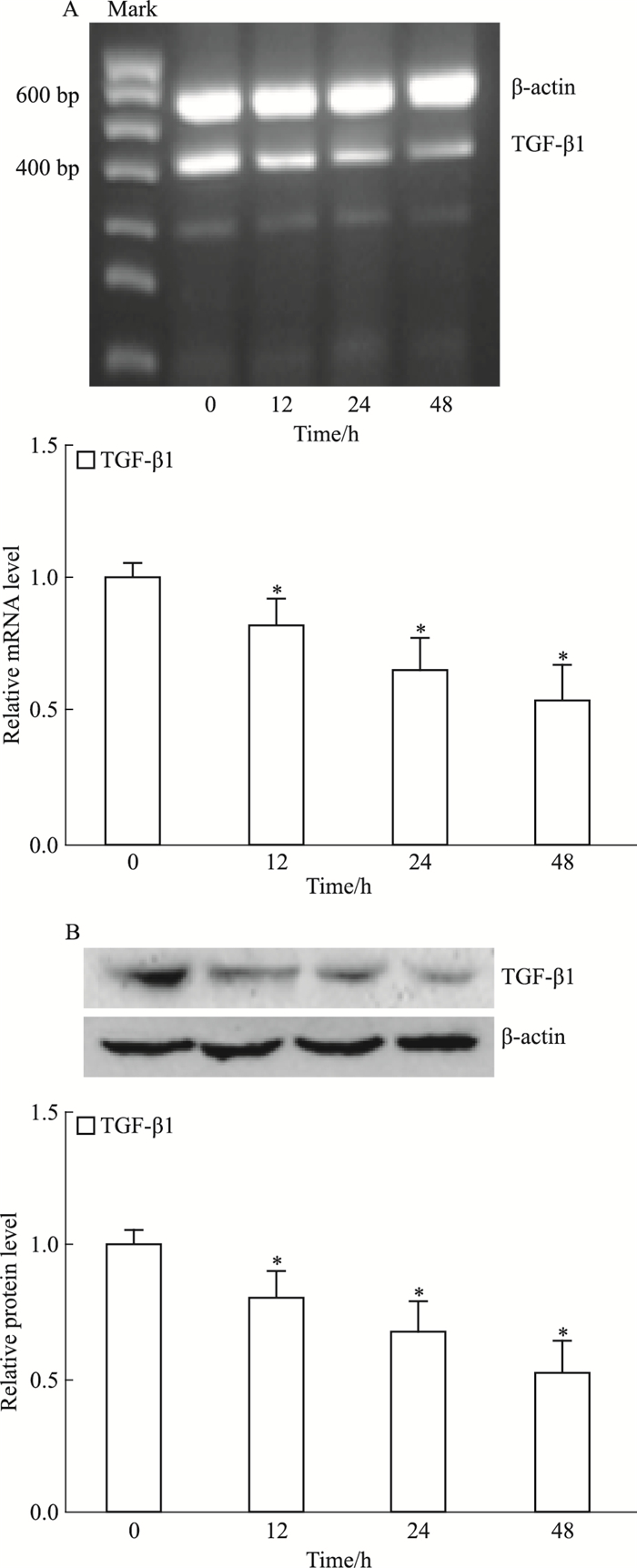
2 结果 2.1 DADS下调TGF-β1表达用30 mg·L-1 DADS处理胃癌MGC803细胞0、12、24、48 h,分别检测TGF-β1 mRNA和蛋白水平。如Fig 1A所示,与0 h组比较,TGF-β1 mRNA水平呈时间依赖性下降(P < 0.05);同时,TGF-β1蛋白水平降低(P < 0.05),其下降趋势与mRNA一致(Fig 1B)。以上结果表明,DADS下调TGF-β1基因表达。
|
| Fig 1 Effect of DADS on expression of TGF-β1 in MGC803 cells(x ± s, n=3) *P < 0.05 vs 0 h |
为了研究DADS下调TGF-β1是否抑制Rac1表达,我们首先观察TGF-β1对Rac1表达的影响。如Fig 2所示,用TGF-β1(5 μg·L-1)处理胃癌MGC803细胞24 h后,Rac1 mRNA和蛋白水平上调(P < 0.05)。

|
| Fig 2 Down-regulation of TGF-β1 by DADS on expression of Rac1 in MGC803 cells(x ± s, n=3) 1: control; 2: DADS; 3: TGF-β1; 4: TGF-β1+SB431542;5: TGF-β1+DADS; 6: TGF-β1+NSC23766;*P < 0.05 vs control; #P < 0.05 vs TGF-β1 |
用TGF-β1(5 μg·L-1)+SB431542 (10 μmol·L-1)处理细胞,观察阻断TGF-β1受体对Rac1表达的影响。与TGF-β1处理组比较,TGF-β1+SB431542组和TGF-β1+DADS组Rac1 mRNA和蛋白表达下调(P < 0.05)(Fig 2),表明TGF-β1受体阻断剂可抑制TGF-β1诱导Rac1表达,DADS可通过下调TGF-β1抑制Rac1表达。同时,TGF-β1(5 μg·L-1)+NSC23766(50 μmol·L-1)处理组Rac1的表达下调(Fig 2),提示Rac1阻断剂NSC23766对Rac1表达也具有抑制作用。
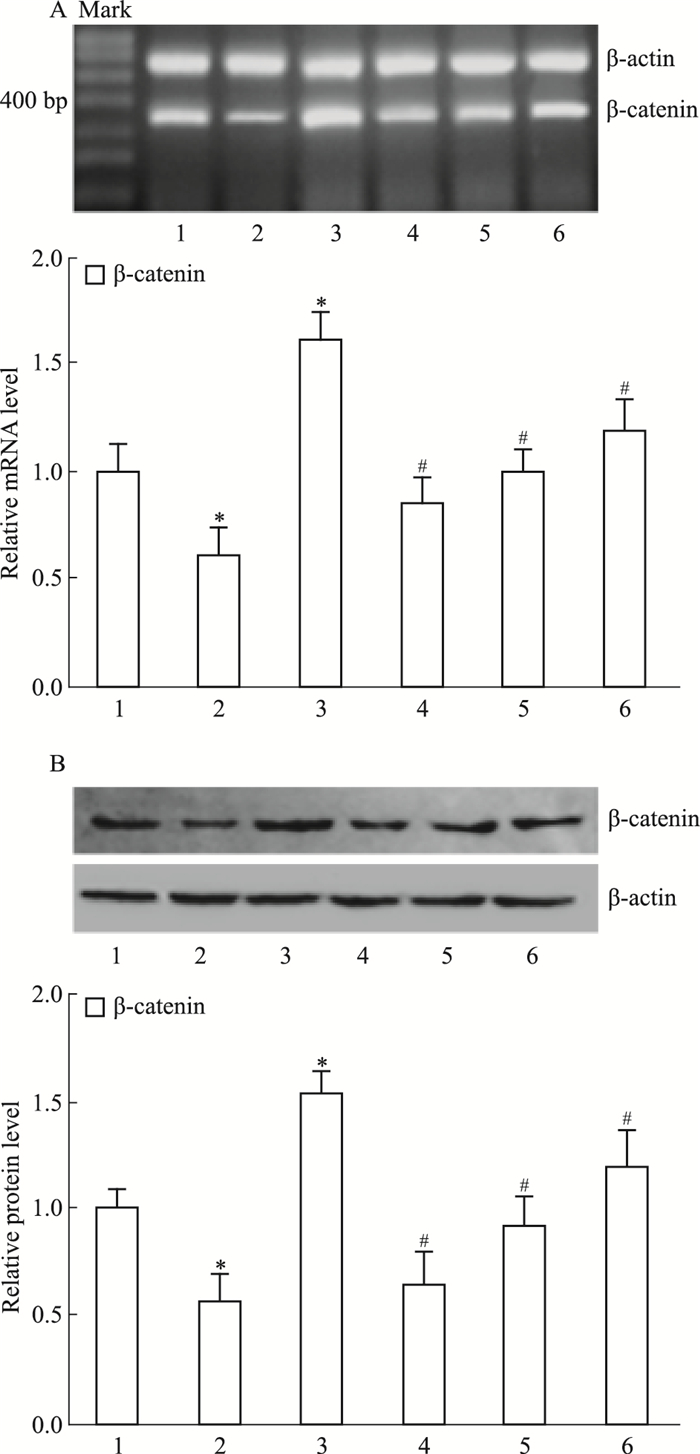
2.3 DADS通过下调TGF-β1/Rac1抑制β-catenin表达如Fig 3所示,用TGF-β1(5 μg·L-1)处理胃癌MGC803细胞24 h后,β-catenin mRNA和蛋白水平上调(P < 0.05)。与TGF-β1处理组比较,TGF-β1+SB431542组Rac1和β-catenin表达下调(P < 0.05)(Fig 3)。
|
| Fig 3 Down-regulation of TGF-β1/Rac1 by DADS on expression of β-catenin in MGC803 cells(x ± s, n=3) 1: control; 2: DADS; 3: TGF-β1; 4: TGF-β1+SB431542;5: TGF-β1+DADS; 6: TGF-β1+NSC23766;*P < 0.05 vs control; #P < 0.05 vs TGF-β1 |
为了确定TGF-β1是否通过Rac1上调β-catenin表达,用TGF-β1(5 μg·L-1)+NSC23766(50 μmol·L-1)处理细胞,观察阻断Rac1对TGF-β1诱导β-catenin表达的影响。与TGF-β1处理组比较,TGF-β1+NSC23766组β-catenin表达下调(P < 0.05)(Fig 3),表明Rac1可介导TGF-β1上调β-catenin。
与TGF-β1处理组比较,TGF-β1+DADS组Rac1和β-catenin表达下调(P < 0.05)(Fig 3),以上结果表明,DADS通过下调TGF-β1/Rac1抑制β-catenin表达。
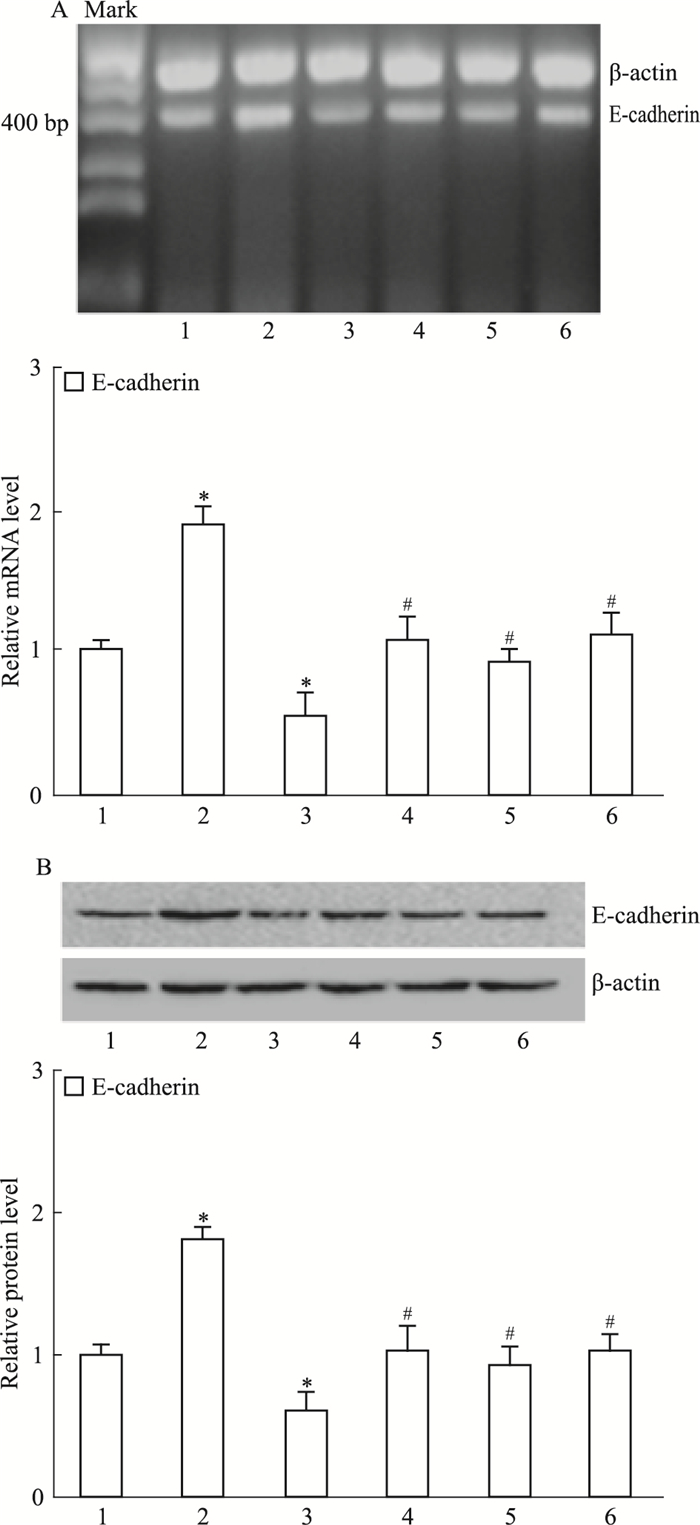
2.4 阻断TGF-β1/Rac1通路上调E-cadherin表达如Fig 4所示,与对照组比较,用TGF-β1(5 μg·L-1)处理胃癌MGC803细胞24 h后,E-cadherin mRNA和蛋白水平下降(P < 0.05);用DADS(30 mg·L-1)处理细胞24 h后,E-cadherin mRNA和蛋白表达水平增加(P < 0.05)。
|
| Fig 4 Down-regulation of TGF-β1/Rac1 by DADS on expression of E-cadherin in MGC803 cells(x ± s, n=3) 1: control; 2: DADS; 3: TGF-β1; 4: TGF-β1+SB431542;5: TGF-β1+DADS; 6: TGF-β1+NSC23766;*P < 0.05 vs control; #P < 0.05 vs TGF-β1 |
与TGF-β1处理组比较,TGF-β1+DADS组E-cadherin mRNA和蛋白表达水平增加(P < 0.05) (Fig 4)。SB431542和NSC23766可抑制TGF-β1下调E-cadherin mRNA和蛋白表达(P < 0.05)(Fig 4)。上述结果表明,DADS抑制TGF-β1/Rac1通路可上调E-cadherin表达。
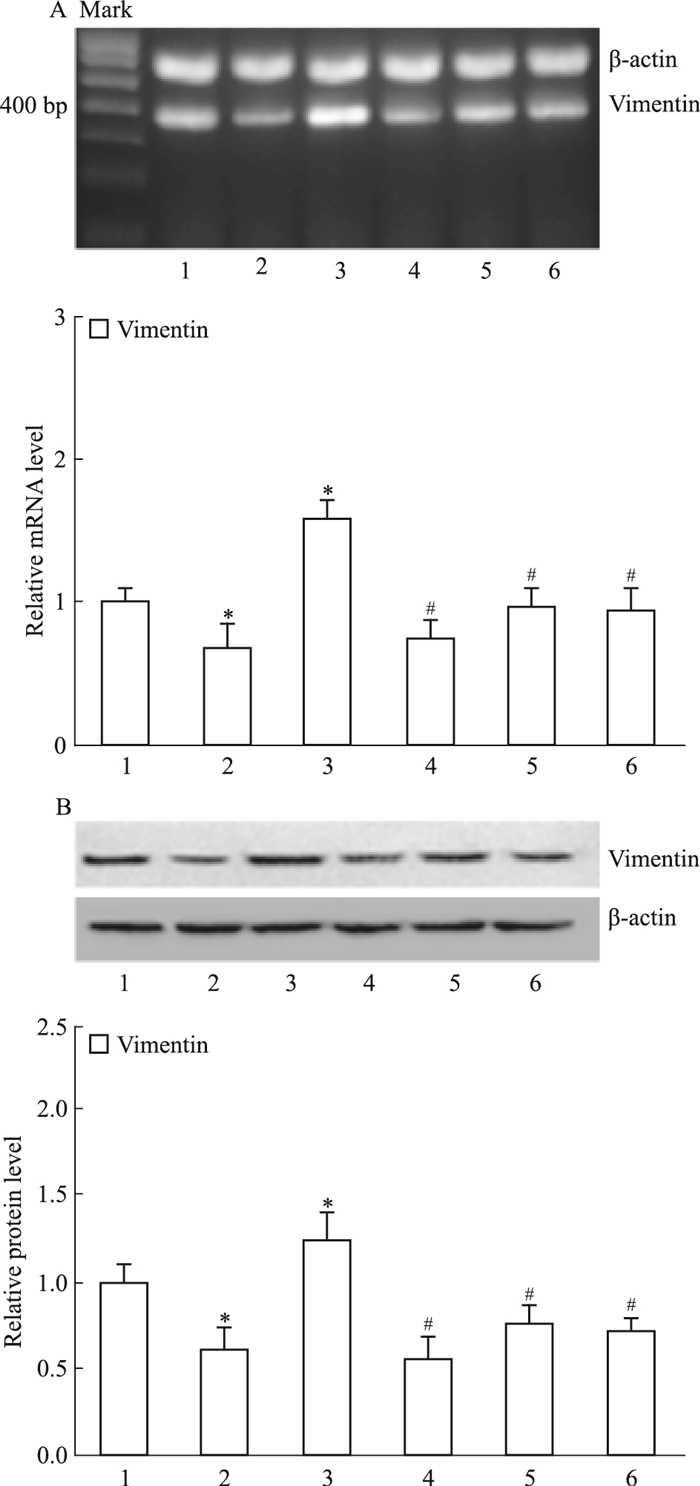
2.5 阻断TGF-β1/Rac1通路下调vimentin表达如Fig 5所示,与对照组比较,用TGF-β1(5 μg·L-1)处理胃癌MGC803细胞24 h后,vimentin mRNA和蛋白水平增加(P < 0.05);而DADS(30 mg·L-1)处理细胞24 h后,vimentin mRNA和蛋白水平较对照组明显降低(P < 0.05)。
|
| Fig 5 Down-regulation of TGF-β1/Rac1 by DADS on expression of vimentin in MGC803 cells(x ± s, n=3) 1: control; 2: DADS; 3: TGF-β1; 4: TGF-β1+SB431542;5: TGF-β1+DADS; 6: TGF-β1+NSC23766;*P < 0.05 vs control; #P < 0.05 vs TGF-β1 |
与TGF-β1处理组比较,TGF-β1+SB431542组和TGF-β1+NSC23766组vimentin mRNA和蛋白水平下降,DADS的作用与SB431542和NSC23766类似(P < 0.05)(Fig 5)。结果表明,DADS可通过抑制TGF-β1/Rac1通路下调vimentin表达。
3 讨论TGF-β1通过其受体激活下游信号通路诱导EMT,从而促进肿瘤细胞侵袭和迁移。TGF-β1上调vimentin、下调E-cadherin,诱导胃癌细胞EMT[6]。本研究证实,DADS下调TGF-β1表达,且可抑制TGF-β1对vimentin和E-cadherin表达的影响,提示DADS可能通过影响TGF-β1下游信号通路抑制胃癌细胞EMT。
我们之前报道,DADS下调Rac1通路和β-cate- nin可抑制胃癌细胞EMT[3, 4]。TGF-β1可诱导肝脏星形细胞Rac1表达[7]。本研究发现,TGF-β1上调胃癌细胞Rac1和β-catenin表达,提示TGF-β1不仅通过其受体激活Rac1和β-catenin信号通路,还可能通过上调Rac1和β-catenin基因表达增强信号通路传导。TGF-β1受体阻断剂SB431542可逆转
TGF-β1诱导食管癌细胞EMT[8]。我们的研究结果显示,DADS和SB431542抑制TGF-β1上调Rac1和β-catenin表达,表明DADS抑制TGF-β1诱导胃癌细胞Rac1和β-catenin表达。此外,我们发现Rac1抑制剂NSC23766抑制TGF-β1诱导Rac1表达。文献报道,NSC23766减少肺上皮细胞释放TGF-β1、抑制EMT,表明Rac1调节TGF-β1表达[9]。我们分析,Rac1与TGF-β1之间可能存在正反馈的调节机制,NSC23766可能抑制内源性TGF-β1表达,从而削弱外源性TGF-β1诱导的Rac1表达。
Rac1与Wnt/β-catenin通路之间存在相互作用。在结肠癌细胞,Rac1募集β-catenin进入核内,增强T细胞因子和淋巴增强因子1介导的基因转录[10]。在乳腺癌细胞,Rac1抑制剂可下调Wnt/β-catenin通路的活性,抑制细胞迁移与侵袭[11]。我们分析,TGF-β1上调胃癌细胞Rac1有助于β-catenin的激活,而DADS抑制TGF-β1诱导Rac1表达可能导致β-catenin活性下调,与其上调vimentin、下调E-cadherin、抑制EMT有关。
Rac1介导β-catenin激活可上调滋养层细胞Snail和MMP9表达,而下调Rac1表达可使β-catenin表达和活性下降,提示Rac1不仅调节β-catenin的活性,也能上调β-catenin表达[12]。ERK介导TGF-β1上调β-catenin表达、诱导肾小管上皮细胞EMT[13]。TGF-β1通过Rac1激活ERK、诱导角质细胞EMT[14]。我们之前报道,DADS下调Rac1[3]和ERK通路[15]。本研究发现,NSC23766抑制TGF-β1上调胃癌细胞β-catenin表达。我们分析,Rac1/ERK通路可能介导TGF-β1上调β-catenin,DADS可通过抑制TGF-β1/Rac1通路下调β-catenin表达。
综上所述,DADS抑制TGF-β1上调vimentin、下调E-cadherin,同时DADS下调Rac1和β-catenin表达。TGF-β1受体阻断剂和Rac1抑制剂可抑制TGF-β1诱导β-catenin表达。上述研究表明,TGF-β1通过Rac1通路上调β-catenin表达;DADS抑制胃癌细胞EMT可能与下调TGF-β1/Rac1通路和β-catenin表达有关。
| [1] |
Al-Azayzih A, Gao F, Somanath P R. P21 activated kinase-1 mediates transforming growth factor β1-induced prostate cancer cell epithelial to mesenchymal transition[J]. Biochim Biophys Acta, 2015, 1853: 1229-39. doi:10.1016/j.bbamcr.2015.02.023 |
| [2] |
Wu X, Tu X, Joeng K S, et al. Rac1 activation controls nuclear localization of beta-catenin during canonical Wnt signaling[J]. Cell, 2008, 133: 340-53. doi:10.1016/j.cell.2008.01.052 |
| [3] |
Su B, Su J, Zeng Y, et al. Diallyl disulfide suppresses epithelial-mesenchymal transition, invasion and proliferation by downregulation of LIMK1 in gastric cancer[J]. Oncotarget, 2016, 7: 10498-512. |
| [4] |
向姝霖, 刘芳, 夏红, 等. 二烯丙基二硫下调β-catenin抑制人胃癌MGC803细胞EMT[J]. 中南医学科学杂志, 2015, 43(5): 487-92. Xiang S L, Liu F, Xia H, et al. DADS inhibits EMT through down-regulation of β-catenin in human gastric cancer MGC803 cells[J]. Med Sci J Centr South China, 2015, 43(5): 487-92. |
| [5] |
唐云云, 唐仪, 刘芳, 等. 二烯丙基二硫上调miR22通过Wnt-1通路抑制人胃癌细胞增殖与迁移侵袭[J]. 中国药理学通报, 2017, 33(8): 1141-7. Tang Y Y, Tang Y, Liu F, et al. Up-regulation of miR22 through Wnt-1 pathway suppresses proliferation, migration and invasion in human gastric MGC803 cells by DADS[J]. Chin Pharmacol Bull, 2017, 33(8): 1141-7. doi:10.3969/j.issn.1001-1978.2017.08.020 |
| [6] |
Zhang H, Liu L, Wang Y, et al. KLF8 involves in TGF-beta-induced EMT and promotes invasion and migration in gastric cancer cells[J]. J Cancer Res Clin Oncol, 2013, 139: 1033-42. doi:10.1007/s00432-012-1363-3 |
| [7] |
Zhang F, Zhuge Y Z, Li Y J, et al. S-adenosylmethionine inhibits the activated phenotype of human hepatic stellate cells via Rac1 and matrix metalloproteinases[J]. Int Immuno Pharmacol, 2014, 19: 193-200. doi:10.1016/j.intimp.2014.01.021 |
| [8] |
Pang L, Li Q, Wei C, et al. TGF-β1/Smad signaling pathway regulates epithelial-to-mesenchymal transition in esophageal squamous cell carcinoma: in vitro and clinical analyses of cell lines and nomadic Kazakh patients from northwest Xinjiang, China[J]. PLoS One, 2014, 9: e0147018. |
| [9] |
Shen H J, Sun Y H, Zhang S J, et al. Cigarette smoke-induced alveolar epithelial-mesenchymal transition is mediated by Rac1 activation[J]. Biochim Biophys Acta, 2014, 1840: 1838-49. doi:10.1016/j.bbagen.2014.01.033 |
| [10] |
Jamieson C, Lui C, Brocardo M G, et al. Rac1 augments Wnt signaling by stimulating β-catenin-lymphoid enhancer factor-1 complex assembly independent of β-catenin nuclear import[J]. J Cell Sci, 2015, 128: 3933-46. doi:10.1242/jcs.167742 |
| [11] |
De P, Carlson J H, Jepperson T, et al. RAC1 GTP-ase signals Wnt-beta-catenin pathway mediated integrin-directed metastasis-associated tumor cell phenotypes in triple negative breast cancers[J]. Oncotarget, 2017, 8: 3072-103. |
| [12] |
Fan M, Xu Y, Hong F, et al. Rac1/β-Catenin signalling pathway contributes to trophoblast cell invasion by targeting Snail and MMP9[J]. Cell Physiol Biochem, 2016, 38: 1319-32. doi:10.1159/000443076 |
| [13] |
Guo L, Peng W, Tao J, et al. Hydrogen sulfide inhibits transforming growth factor-β1-induced EMT via Wnt/catenin pathway[J]. PLoS One, 2016, 11: e0147018. doi:10.1371/journal.pone.0147018 |
| [14] |
Santibáñez J F, Kocic J, Fabra A, et al. Rac1 modulates TGF-beta1-mediated epithelial cell plasticity and MMP9 production in transformed keratinocytes[J]. FEBS Lett, 2010, 584: 2305-10. doi:10.1016/j.febslet.2010.03.042 |
| [15] |
Su B, Su J, He H, et al. Identification of potential targets for diallyl disulfide in human gastric cancer MGC-803 cells using proteomics approaches[J]. Oncol Rep, 2015, 33: 2484-94. doi:10.3892/or.2015.3859 |

