

2. 中国科学技术大学附属第一医院(安徽省立医院)药剂科,安徽 合肥 230001
魏伟(1960-),男,博士,教授,博士生导师,研究方向:抗炎免疫药理学,通讯作者,E-mail:wwei@ahmu.edu.cn
2. Dept of Pharmacy, Anhui Provincial Hospital, the First Affiliated Hospital of USTC, Division of Life Sciences and Medicine, University of Science and Technology of China, Hefei 230001, China
糖尿病肾病(diabetic nephropathy,DN)是糖尿病(diabetes mellitus,DM)最严重的微血管并发症之一[1]。这种疾病是由于伴随持续高血糖和DM状态下的血流动力学因素,导致肾小管、肾小球或肾间质的损害[2]。DN的主要病理特征是肾小球结构肥大、肾小球基底膜增厚、肾小管间质扩张以及细胞外基质成分(如胶原蛋白和纤连蛋白)的异常积聚[3]。足细胞是终末分化的上皮细胞,其形成交叉的足突,构成肾小球滤过屏障,是阻止蛋白质渗漏的关键组分。足细胞损伤、去分化和丢失是DN的病理标志[4]。足细胞凋亡是DN的早期病理表现,因此足细胞凋亡可能在DN病理机理中起到关键作用[5]。PI3K/Akt/FOXO信号通路在细胞存活和凋亡中起到了重要作用,FOXO被Akt在Thr24、Ser256、Ser319上磷酸化,促进它们的出核转运和转录激活[6]。越来越多的证据表明FOXO1具有抑癌作用,因为它在多种癌症中具有抗增殖和促凋亡活性[7]。小檗碱(berberine,BBR)是从黄连中提取的天然化学物质,BBR具有多种生物学和药理学活性,包括抗肿瘤、抗炎和抗氧化应激作用,BBR也被证明具有抗糖尿病作用[8]。研究证明小檗碱能明显改善高糖诱导的足细胞损伤[9],因此本实验的目的是探讨BBR通过调节PI3K/AKT/FOXO1/Bim信号通路改善高糖诱导的足细胞损伤,为临床DN的治疗打下基础。
1 材料 1.1 细胞小鼠肾小球足细胞株(BNCC 337685),购于北京北纳创联生物技术研究院。
1.2 药物BBR由安徽省立医院药剂科药学实验室提取纯化,经RP-HPLC法检测纯度大于96.5 %。精密称取40.365 g BBR粉末,加入10 mL生理盐水,加热涡旋混匀至完全溶解,配制成浓度为1.2×104 μmol·L-1的BBR储备液,用0.22 μm无菌过滤器过滤除菌后冷冻保存。使用前加热溶解,稀释到所需浓度即可用于实验。
1.3 试剂细胞计数试剂盒(CCK-8,货号K1018),美国Protech公司; RPMI 1640培养液(货号:11875),Thermo Fisher科技公司; 凋亡试剂盒(货号AP101):联科生物公司; 胎牛血清:Biological Industries公司; 六孔细胞培养板,Corning公司; WT-1(Rabbit Antibody,货号sc-19232026),Santa Cruz生物科技公司; PI3K(Rabbit Antibody,货号4249)、AKT(Rabbit Antibody,货号4691S)、p-AKT(Rabbit Antibody,货号4060S)、FOXO1(Rabbit Antibody,货号2880)、p-FOXO1(Rabbit Antibody货号9461)、Bim(Rabbit Antibody,货号2933),Cell Signaling公司; nephrin(Rabbit Antibody,货号ab85379),Abcam公司。
1.4 仪器电泳仪(型号DYY-10):北京六一仪器厂; 可调水平摇床(型号STS-1):上海琪特分析仪器有限公司; PH检测计(型号PHS-3C):上海雷磁仪器厂; 酶标仪(型号BioTek Elx×808),美国BioTek公司; 纯水仪(型号HB-RO/05):杭州惠邦净水设备有限公司; Eppendorf Research plus移液器(型号31200000):Eppendorf科技公司; 化学发光成像分析仪(型号Image Quant Las 4 000 mini),美国GE Healthcare Life Sciences公司。
2 方法 2.1 细胞培养将液氮中冻存的细胞于37 ℃水浴中融解离心,在RPMI 1640基础培基中加入10% FBS、1%双抗、0.2% γ干扰素用于培养细胞,细胞于5% CO2、37 ℃的细胞培养箱中培养。
2.2 CCK-8检测取指数生长期的肾小球足细胞进行实验,96孔培养板加入足细胞单细胞悬液200 μL/孔(约含一万个细胞),各组另设5个平行组; 待细胞贴壁完全后,正常对照组(Control,11.1 mmol·L-1葡萄糖)、高糖模型组(HG,30 mmol·L-1葡萄糖)和BBR给药组按照分组给予对应的培基,BBR给药组的浓度设置为:15、30、60、90、120 μmol·L-1。给药24 h后,CCK-8溶液的用量为10 μL/孔。培养板避光继续培养,每隔1 h用酶标仪震荡后测定各组在450 nm处的吸光度,一次实验结果取平均值,重复实验3次。
2.3 细胞凋亡采用Annexin V- FITC/PI双染实验观察小檗碱对高糖诱导足细胞凋亡的影响,足细胞贴壁后分为5组,按照分组给予对应的培基,BBR给药组浓度设置为:30、60、90 μmol·L-1,给药24 h后,消化离心并收集1×105~5×105个细胞。接着每管先加入500 μL稀释5倍的Binding buffer,再加入5 μL Annexin V-FITC和10 μL PI溶液,室温静置避光孵育5 min后转移到流式管中,流式细胞仪上机检测。
2.4 Transwell小室检测细胞迁移能力将Transwell小室放于24孔板中,下室分组及加药处理同2.3项,并加入15%血清的RPMI 1640培养基,上室每孔加入一万个5% FBS的RPMI 1640培养基的足细胞单细胞悬液,培养箱中培养24 h后,用5%结晶紫染色,用PBS洗去多余的结晶紫,用棉签擦去Transwell上室未迁移的细胞,在倒置显微镜下拍照并观察结果。每个样本随机选取5个视野,计算每个视野的细胞数。
2.5 Western blot检测相关蛋白表达足细胞消化计数后按1×108/孔加到6孔板上,细胞贴壁后分组及加药处理同2.3项,培养箱培养24 h,用预冷的PBS轻柔洗涤两次去除死细胞及杂质后,每孔加入100 μL现配的预冷裂解液,置冰上30 min后刮下细胞,离心收集上清液,加入蛋白上样缓冲液,得到上样蛋白。在配好的SDS-PAGE凝胶上用微量注射器上样,然后完成跑胶、转膜、封闭步骤,用目的蛋白抗体孵育过夜,3遍TPBS洗膜后将PVDF膜于适合浓度的二抗工作液-牛奶中37 ℃孵育1 h; 显影后进行灰度图分析得结果。
2.6 统计学分析用SPSS 16.0软件进行分析,数据以x±s表示,数据分析方法为One-way analysis of variance。
3 结果 3.1 BBR对足细胞增殖的影响Fig 1结果显示,高糖模型组与正常对照组相比,足细胞的存活率明显降低(P < 0.01);BBR(30、60、90 μmol·L-1)作用组与高糖模型组相比,能明显促进足细胞增殖。因此后续实验选择了BBR 30、60、90 μmol·L-1这3个浓度进行实验。

|
| Fig 1 Effect of BBR on proliferation of podocytes(x±s, n=3) ##P < 0.01 vs control group: *P < 0.05, **P < 0.01 vs HG group. |
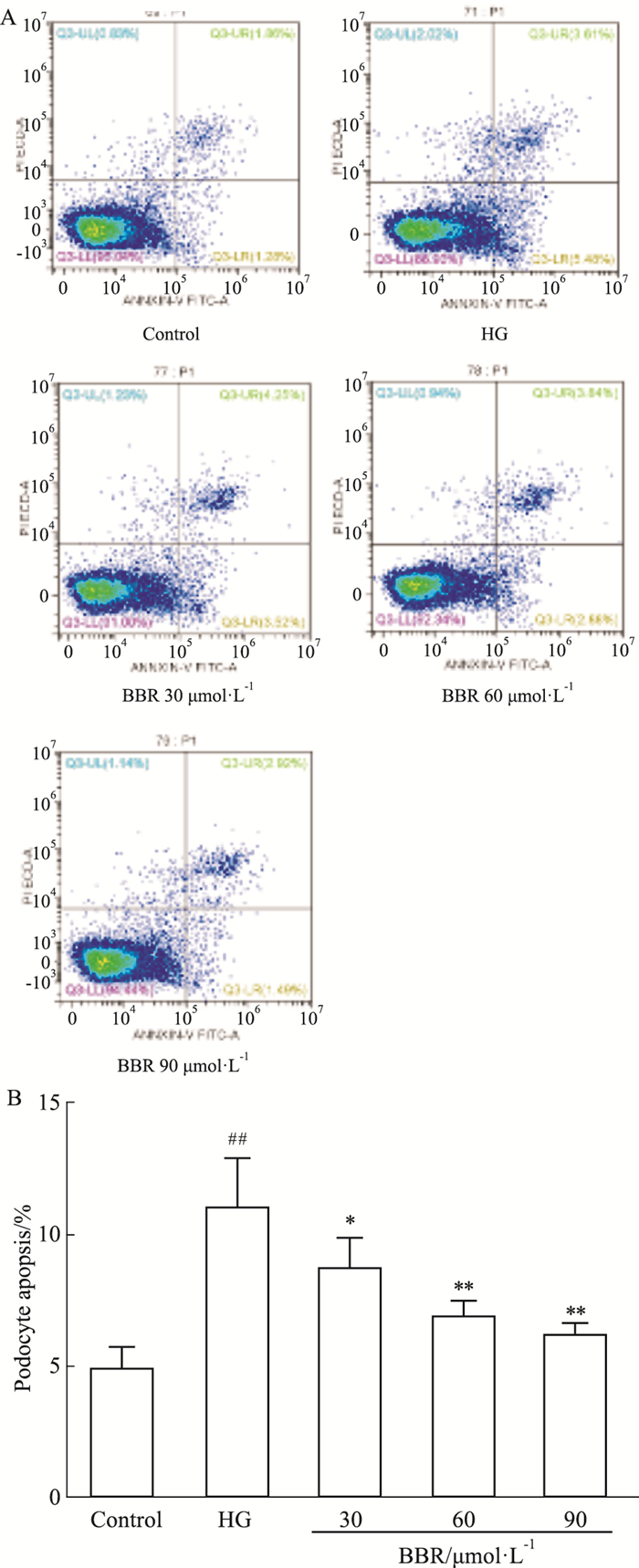
Fig 2结果显示,高糖模型组与正常对照组相比,足细胞的凋亡率有较明显提高(P < 0.01);BBR(30、60、90 μmol·L-1)作用组与高糖模型组比较能明显降低足细胞的凋亡率。
|
| Fig 2 Effect of BBR on apoptosis of podocytes(x±s, n=3) ##P < 0.01 vs control group; *P < 0.05, **P < 0.01 vs HG group. |
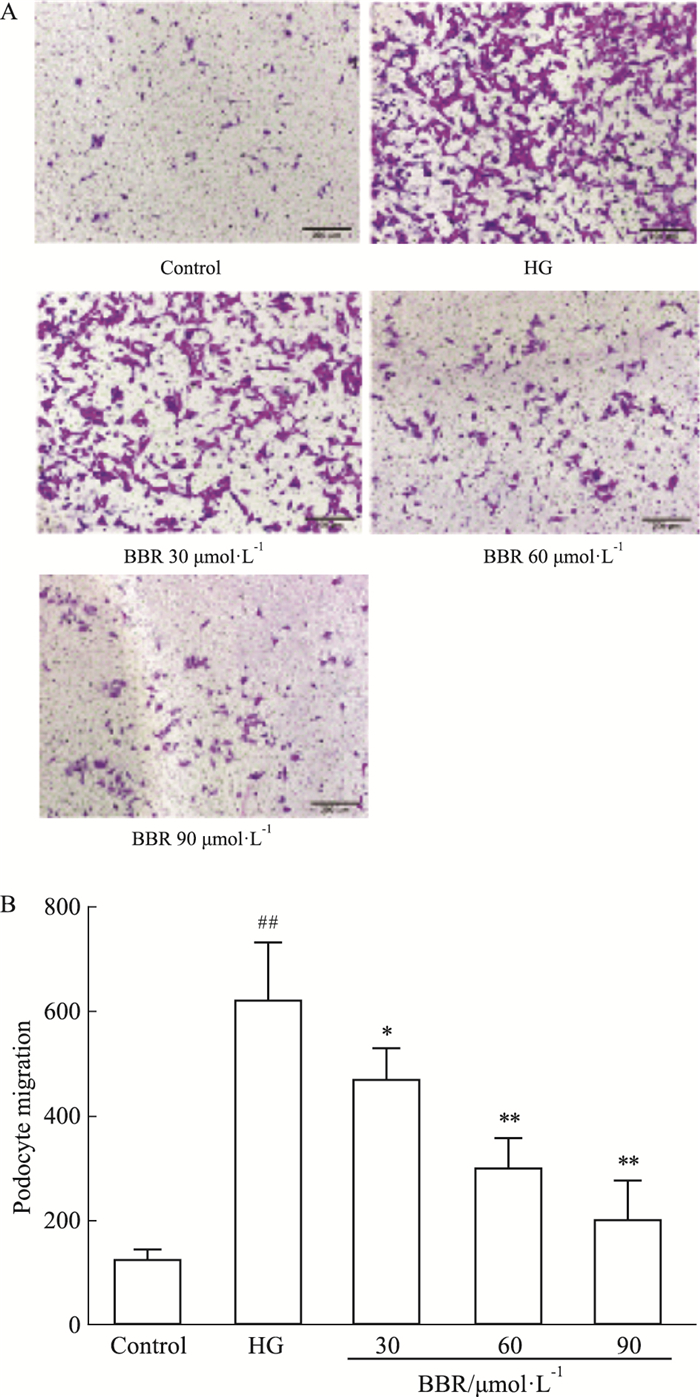
Fig 3结果表明,高糖模型组与正常对照组相比,Transwell下室的足细胞数量明显增加(P < 0.01);BBR(30、60、90 μmol·L-1)作用组与高糖模型组相比,Transwell下室的足细胞数量明显减少。
|
| Fig 3 Effect of BBR on migration of podocytes(x±s, n=3) ##P < 0.01 vs control group; *P < 0.05, **P < 0.01 vs HG group. |
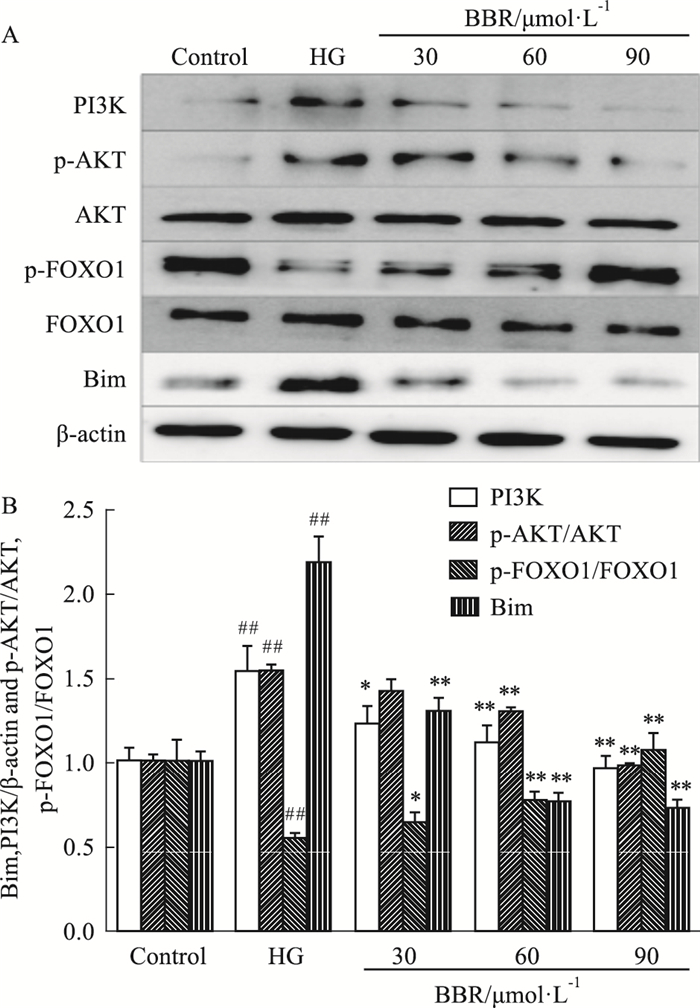
PI3K/AKT/FOXO1/Bim信号通路被认为是细胞存活和凋亡的重要调控因子。Fig 4结果显示,与正常对照组相比,高糖模型组中足细胞上PI3K、p-AKT和Bim蛋白表达量明显升高(P < 0.01),p-FOXO1的蛋白表达量明显降低(P < 0.01),并且BBR(30、60、90 μmol·L-1)作用组能够有效降低足细胞上PI3K、p-AKT和Bim蛋白表达水平,能够有效升高足细胞上p-FOXO1蛋白表达水平。
|
| Fig 4 The expression levels of Bim, PI3K/β-actin and p-AKT/AKT, p-FOXO1/FOXO1 tested by Western blot(x±s, n=3) ##P < 0.01 vs control group; *P < 0.05, **P < 0.01 vs HG group. |
维持足细胞功能完整性的重要蛋白有nephrin、WT-1。Fig 5的Western blot的灰度值结果显示,高糖模型组与正常对照组相比,nephrin、WT-1蛋白表达量明显降低(P < 0.01),与高糖模型组相比,BBR(30、60、90 μmol·L-1)作用组的nephrin和WT-1蛋白表达量明显升高。

|
| Fig 5 The expression levels of nephrin and WT-1 tested by Western blot(x±s, n=3) ##P < 0.01 vs control group; *P < 0.05, **P < 0.01 vs HG group. |
足细胞是肾小球基底膜选择性通透性屏障的关键组成部分,DM诱导的足细胞凋亡导致肾小球滤过屏障功能减弱,这可能导致蛋白尿的发生[10]。足细胞通过狭缝隔膜连接并覆盖肾小球基底膜的表面以调节渗透性。它包裹毛细血管形成过滤缝,可以保持肾小球滤膜的结构完整性,足细胞丢失是导致包括糖尿病肾病在内的一些肾病进展的关键因素。在DN期间,由于足突的丧失,足细胞在高血糖症中发生脱离。WT-1和nephrin是维持细胞骨架的重要分子,细胞骨架在足细胞损伤过程中被下调,此外,结蛋白是另一种细胞骨架蛋白,在足细胞损伤过程中会上调。在本研究中,我们使用30 mmol·L-1葡萄糖成功建立了足细胞损伤模型,正如WT-1和nephrin的下调所证明[11]。
哺乳动物叉头盒O(FOXO)家族包括四个成员:FOXO3,FOXO4,FOXO6和FOXO1。FOXO成员在多种细胞功能中发挥重要作用,如肿瘤抑制、糖尿病并发症、细胞周期停滞、DNA修复、伤口愈合、免疫、代谢调节和细胞分化,FOXO1是一种转录因子,在氧化应激、细胞代谢、增殖和凋亡中起重要作用,并且有证据表明FOXO1的表达与丝氨酸/苏氨酸激酶Akt信号传导途径有关,FOXO1是AKT的下游基因[12]。FOXO转录因子受上游PI3K/Akt磷酸化级联调节,其中FOXO1在肾损伤的发病机理中起重要作用,并且FOXO1从细胞质转移至核激活,p-FOXO1的增加将减少FOXO1的核转位,抑制凋亡基因Bim的表达,防止细胞凋亡的发生[13]。BBR是一种从黄连中分离出来的异喹啉生物碱,BBR具有多种药理活性,如降低血糖和抗氧化应激,抑制炎症,因此BBR是DN治疗中的潜在治疗药物[14]。本实验在体外用高糖刺激足细胞,并使用不同浓度的BBR观察BBR缓解足细胞损伤的机制,通过观察足细胞的凋亡、迁移、足细胞相关蛋白的表达、足细胞上PI3K/AKT/FOXO1/Bim信号通路的蛋白表达,得出BBR在高糖环境下可以降低足细胞的凋亡率、减少足细胞迁移、提高足细胞标志性蛋白的表达,并且可以有效降低高糖环境下足细胞上PI3K、p-AKT和Bim蛋白表达水平,有效升高足细胞上p-FOXO1蛋白表达水平,从而改善足细胞的损伤。
综上所述,高糖环境激活PI3K/AKT信号通路,进而影响了FOXO1从细胞质转移至核被磷酸化,未被磷酸化的FOXO1促进凋亡基因Bim的表达,促进足细胞的凋亡,实验结果显示,BBR能调节此过程。因此,本实验揭示了BBR可能通过调节PI3K/AKT/FOXO1/Bim信号通路改善高糖诱导的足细胞损伤。
| [1] |
贾会玉, 段陈方圆, 李莉, 等. 丹蛭降糖胶囊对糖尿病肾病大鼠TGF-β1/Smads信号通路的调控作用[J]. 中国药理学通报, 2019, 35(05): 714-20. Jia H Y, Duan C F Y, Li L, et al. Control of TGF-β1/Smads signaling pathway in diabetic nephropathy rats by Danzhijiangtang capsule[J]. Chin Pharmacol Bull, 2019, 35(5): 714-20. doi:10.3969/j.issn.1001-1978.2019.05.024 |
| [2] |
王盈盈, 刘青, 唐丽琴, 魏伟. 小檗碱对高糖诱导足细胞功能及相关蛋白表达的影响[J]. 中国药理学通报, 2018, 34(8): 1158-63. Wang Y Y, Liu Q, Tang L Q, Wei W. Effects of berberine on the expression of podocyte function and related proteins induced by high glucose[J]. Chin Pharmacol Bull, 2018, 34(8): 1158-63. doi:10.3969/j.issn.1001-1978.2018.08.024 |
| [3] |
Yu S, Zhao H, Yang W, et al. The alcohol extract of nutt ameliorates diabetes and diabetic nephropathy in db/db mice through miR-192/miR-200b and PTEN/AKT and ZEB2/ECM pathways[J]. Biomed Res Int, 2019, 2019: 5280514. |
| [4] |
Qin X, Zhao Y, Gong J, et al. Berberine protects glomerular podocytes via inhibiting Drp1-mediated mitochondrial fission and dysfunction[J]. Theranostics, 2019, 9(6): 1698-713. doi:10.7150/thno.30640 |
| [5] |
Fu Y, Wang C, Zhang D, et al. miR-15b-5p ameliorated high glucose-induced podocyte injury through repressing apoptosis, oxidative stress, and inflammatory responses by targeting Sema3A[J]. J Cell Physiol, 2019, 234(11): 20869-78. doi:10.1002/jcp.28691 |
| [6] |
Majumder S, Ren L, Pushpakumar S. Hydrogen sulphide mitigates homocysteine-induced apoptosis and matrix remodelling in mesangial cells through Akt/FOXO1 signalling cascade[J]. Cell Signal, 2019, 61: 66-77. doi:10.1016/j.cellsig.2019.05.003 |
| [7] |
Chen D, Yang Y. Quxie capsule inhibits colon tumor growth partially through foxo1-mediated apoptosis and immune modulation[J]. Integr Cancer Ther, 2019, 18: 1534735419846377. |
| [8] |
Dong J, Zuo Z, Yan W, et al. Berberine ameliorates diabetic neuropathic pain in a rat model: involvement of oxidative stress, inflammation, and μ-opioid receptors[J]. Naunyn Schmiedebergs Arch Pharmacol, 2019, 392(9): 1141-9. doi:10.1007/s00210-019-01659-6 |
| [9] |
郭维文, 廖水玉, 李佑生. 小檗碱对高糖诱导的小鼠足细胞凋亡的影响[J]. 上海中医药杂志, 2017, 51(11): 68-71. Guo W W, Liao S Y, Li Y S. Effect of berberine on high glucose-induced apoptosis of mouse podocytes[J]. Shanghai J Tradit Chin Med, 2017, 51(11): 68-71. |
| [10] |
He M, Wang J, Yin Z, et al. MiR-320a induces diabetic nephropathy via inhibiting MafB[J]. Aging, 2019, 11(10): 3055-79. doi:10.18632/aging.101962 |
| [11] |
Yu Q, Zhang M, Qian L, et al. Luteolin attenuates high glucose-induced podocyte injury via suppressing NLRP3 inflammasome pathway[J]. Life Sci, 2019, 225: 1-7. doi:10.1016/j.lfs.2019.03.073 |
| [12] |
Liu Y. Eriodictyol inhibits survival and inflammatory responses and promotes apoptosis in rheumatoid arthritis fibroblast-like synoviocytes through AKT/FOXO1 signaling[J]. J Cell Biochem, 2019, 120(9): 14628-35. doi:10.1002/jcb.28724 |
| [13] |
Ruan H, Luo J, Wang L, et al. Sika deer antler protein against acetaminophen-induced nephrotoxicity by activating Nrf2 and inhibition FOXO1 via PI3K/Akt signaling[J]. Int J Biol Macromol, 2019, 141: 961-87. doi:10.1016/j.ijbiomac.2019.08.164 |
| [14] |
廖翠平, 赵鹿, 董世奇, 等. 小檗属植物抗糖尿病及糖尿病并发症的研究进展[J]. 药物评价研究, 2019, 42(5): 1027-32. Liao C P, Zhao L, Dong S Q, et al. Research progress in antidiabetic and diabetic complications of Berberis[J]. Drug Eval Res, 2019, 42(5): 1027-32. |

