


2. 中国医学科学院 & 北京协和医学院药物研究所, 天然药物活性物质与功能国家重点实验室, 药物靶点研究与新药筛选北京市重点实验室, 北京 100050
2. State Key Lab of Bioactive Substances and Functions of Natural Medicines, Beijing Key Lab of Drug Target and Screening Research, Institute of Materia Medica, Chinese Academy of Medical Sciences and Peking Union Medical College, Beijing 100050, China
帕金森病(parkinson’s disease,PD)是第二大中枢神经系统退行性疾病,帕金森病的主要病理特征是中脑黑质多巴胺能神经元变性死亡并且残存胞浆中形成路易小体[1-2]。寻找安全有效的药物以防止多巴胺能神经元变性死亡对于PD治疗具有重要作用。研究发现,异鼠李素(isorhamnetin,ISO)具有明确的内皮保护作用、能够抗动脉粥样硬化、抗心肌纤维化、抗血小板凝集、抗氧化等[3-5]。然而,异鼠李素对神经退行性疾病损伤模型中细胞保护作用及分子机制尚未完全清楚。
环腺苷酸反应结合蛋白(cAMP response element binding protein,CREB)是通过自身磷酸化实现转录调节的重要转录因子。CREB能够被多种激酶激活,调节细胞内基因转录,参与细胞的增殖、分化和凋亡[6-7]。磷酸肌醇3-激酶(phosphatidyl-inositol 3-kinase,PI3K)/蛋白激酶B(protein kinase B,Akt)信号通路与帕金森病联系密切,在介导多巴胺能神经元存活中起重要作用。Phospho-Akt触发下游靶标磷酸化,导致糖原合成酶激酶-3(glycogen synthase kinase 3β,GSK-3β)和促凋亡B淋巴细胞瘤-2(B-cell lymphoma-2,Bcl-2)家族失活,进一步激活cAMP反应元件结合蛋白[8-9]。
异鼠李素能否通过PI3K/Akt/GSK-3β/CREB信号通路抑制鱼藤酮诱导的PC12细胞毒性损伤未见报道。本实验通过建立鱼藤酮损伤PC12细胞模型,探讨异鼠李素是否能够通过PI3K/Akt/GSK-3β/CREB信号通路抑制多巴胺能神经元损伤。
1 材料与方法 1.1 试剂与仪器大鼠肾上腺嗜铬细胞瘤细胞PC12购自吉妮欧生物有限公司。异鼠李素(R018214)购自上海易恩化学技术有限公司。Roswell Park Memorial Institute-1640(RPMI-1640)培养基(31870082)、胎牛血清(10100147)、马血清(26050088)均购自Thermo Fisher Scientific。鱼藤酮(R8875)、LY294002(L9908)、氮乙酰半胱氨酸(N-acetylcysteine,NAC,A7250)、MTT(M2128)均购自Sigma-Aldrich;乳酸脱氢酶检测试剂盒(LDH Cytotoxicity Assay Kit,C0016)购自碧云天生物技术公司。CREB(sc-377154)、p-CREB(sc-81486)抗体均购自Santa Cruz Biotechnology。Akt(4685)、p-Akt(4060)、GSK3β(12456)、p-GSK3β(5558)和GAPDH(5174)抗体均购自Cell Signaling Technology。电泳仪(PowerPac Basic)、成像仪(Molecular Imager ChemiDoc XRS+System),美国Bio-Rad;酶标仪(SpectraMax M5),美国Molecular Devices。
1.2 PC12细胞培养PC12细胞接种于RPMI-1640完全培养基中,其中含有10%马血清和5%胎牛血清,置于37 ℃ 5% CO2培养箱中,每隔一天换液,待细胞处于对数生长期时,接种于不同培养板中用于后续实验。
1.3 细胞分组实验分为七组:(1)空白对照组;(2)ISO对照组,加入15 μmol·L-1 ISO;(3)鱼藤酮损伤组,加入10 μmol·L-1鱼藤酮损伤24 h;(4)ISO低剂量组,在给予鱼藤酮损伤之前,加入1.5 μmol·L-1 ISO预孵育2 h;(5)ISO中剂量组,在给予鱼藤酮损伤之前,加入5 μmol·L-1 ISO预孵育2 h;(6)ISO高剂量组,在给予鱼藤酮损伤之前,加入15 μmol·L-1 ISO预孵育2 h;(7)NAC阳性对照组,在给予鱼藤酮损伤之前,加入5 mmol·L-1 NAC预孵育2 h。
1.4 MTT检测细胞存活率将PC12细胞接种于96孔板中,实验终点,弃培养液,加入MTT工作溶液100 μL,继续孵育4 h后弃MTT溶液,加入DMSO 100 μL,结晶溶解后测定吸光度。
1.5 LDH释放率检测将PC12细胞接种于96孔板,设置空白对照组、样品对照组、样品最大酶活性组、药物处理组。实验终点前1 h,在样品最大酶活性组中加入LDH释放剂10 μL,继续孵育1 h后取每孔120 μL上清液,进行测定。
1.6 Western blot检测蛋白表达将PC12细胞接种于6孔板,实验终点,PBS洗一次,加入200 μL预冷的蛋白裂解液30 min后提取细胞总蛋白。加入5×loading buffer后沸水浴10 min,之后进行SDS-PAGE电泳,将蛋白转印至PVDF膜。然后5% BSA室温封闭2 h再分别用稀释后的CREB、p-CREB、Akt、p-Akt、GSK3β、p-GSK3β和GAPDH抗体孵育4 ℃过夜。TBST洗涤3次,置于对应二抗中孵育2 h,最终TBST洗涤3次后成像。
1.7 统计学处理采用SPSS 17.0进行统计分析,结果以x±s表示,组间比较采用单因素方差分析。
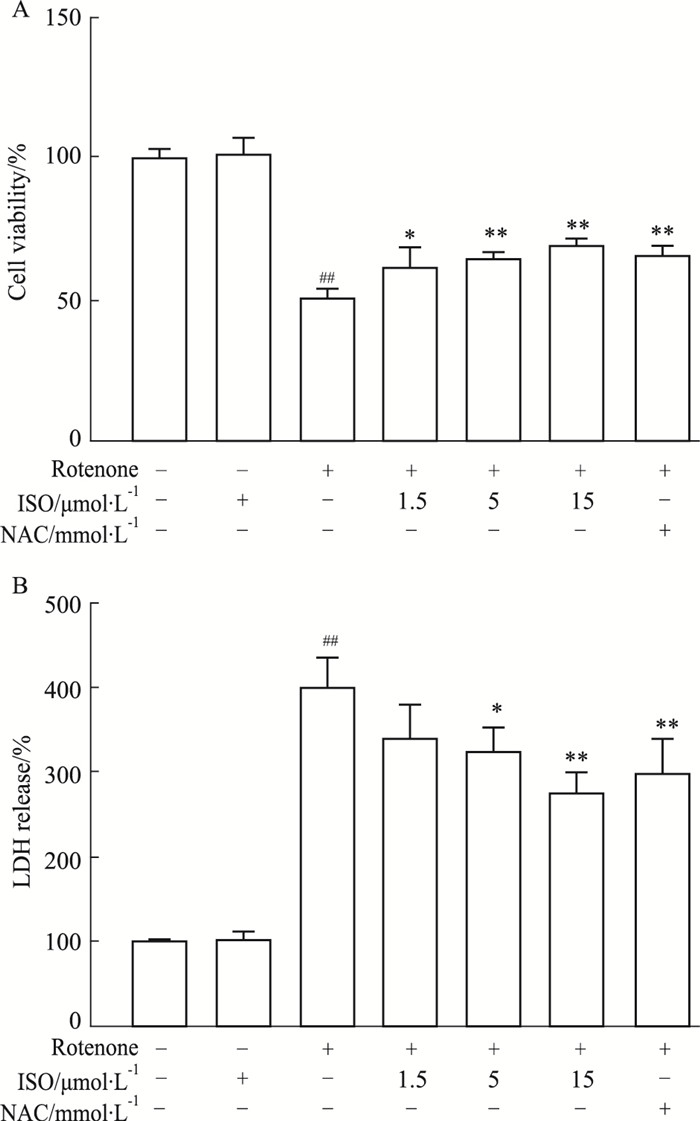
2 结果 2.1 ISO减轻鱼藤酮诱导的PC12细胞损伤MTT检测结果如Fig 1A所示,与空白对照组相比,15 μmol·L-1 ISO单独孵育PC12细胞24 h,对细胞活力没有明显影响。与空白对照组相比,10 μmol·L-1鱼藤酮处理PC12细胞后,细胞存活率明显降低(P<0.01),ISO 1.5,5和15 μmol·L-1及5 mmol·L-1 NAC均能明显提高PC12细胞存活率(P<0.05或P<0.01)。LDH检测结果如Fig 1B所示,与空白对照组相比,ISO对照组PC12细胞LDH释放量无明显变化,鱼藤酮损伤组PC12细胞LDH释放量明显增加(P<0.01),5和15 μmol·L-1 ISO及5 mmol·L-1 NAC均能明显抑制鱼藤酮诱增的LDH释放(P<0.05或P<0.01)。
|
| Fig 1 Protection effects of ISO on PC12 cell viability (x±s, n=4) A: The cell viability was determined using MTT assay; B: The LDH release was detected by the LDH Cytotoxicity Assay Kit. ##P < 0.01 vs sham group, *P < 0.05, **P < 0.01 vs rotenone group. |
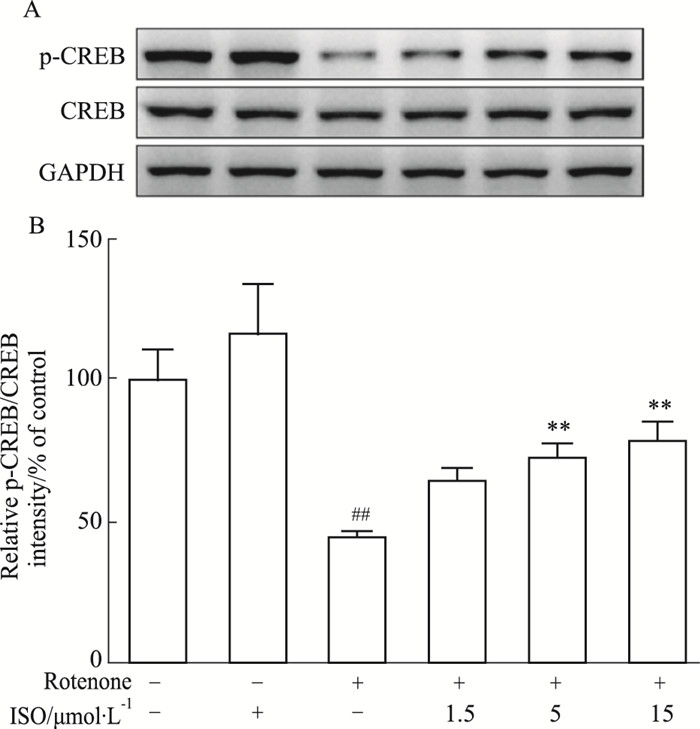
Western blot检测结果表明,鱼藤酮损伤PC12细胞模型组p-CREB/CREB比值明显低于空白对照组(P<0.01)。与鱼藤酮损伤组相比,1.5 μmol·L-1 ISO预处理对p-CREB/CREB比值无明显影响,5和15 μmol·L-1 ISO预处理组p-CREB/CREB比值明显提高(P<0.01)。结果如Fig 2。
|
| Fig 2 Phosphorylation of CREB in PC12 cells enhanced by ISO (x±s, n=4) A: The expression of p-CREB and CREB were detected by Western blot. GAPDH was used as a loading control; B: p-CREB/CREB ratio. ##P < 0.01 vs Control group, **P < 0.01 vs rotenone group. |
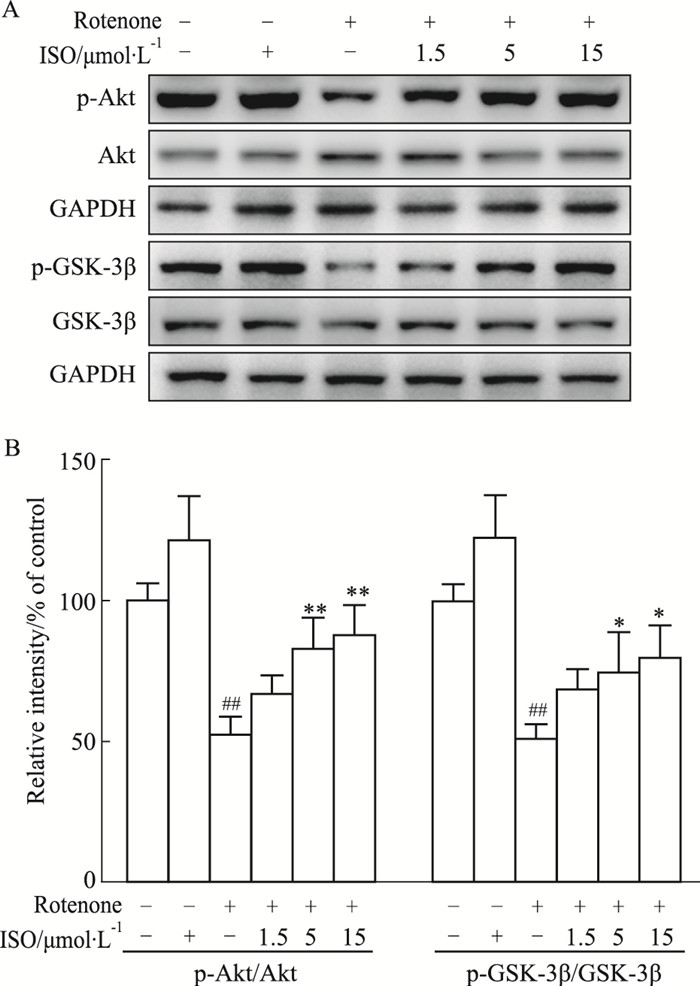
采用Western blot检测鱼藤酮损伤PC12细胞后,p-Akt/Akt比值和p-GSK-3β/GSK-3β比值变化。与空白对照组相比,鱼藤酮损伤组PC12细胞中p-Akt/Akt比值和p-GSK-3β/GSK-3β比值明显降低(P<0.01)。然而,与鱼藤酮损伤组相比,5和15 μmol·L-1 ISO预处理不同程度增强了p-Akt/Akt和p-GSK-3β/GSK-3β比值(P<0.05或P<0.01)。结果如Fig 3。
|
| Fig 3 Levels of p-Akt and p-GSK-3β elevatedby ISO(x±s, n=4) A:The levels of p-Akt, Akt, p-GSK-3β and GSK-3β were detected by Western blot. GAPDH was used as a loading control; B:p-Akt/Akt and p-GSK-3β/GSK-3β ratio.##P < 0.01 vs control group, *P < 0.05, **P < 0.01 vs rotenone group. |
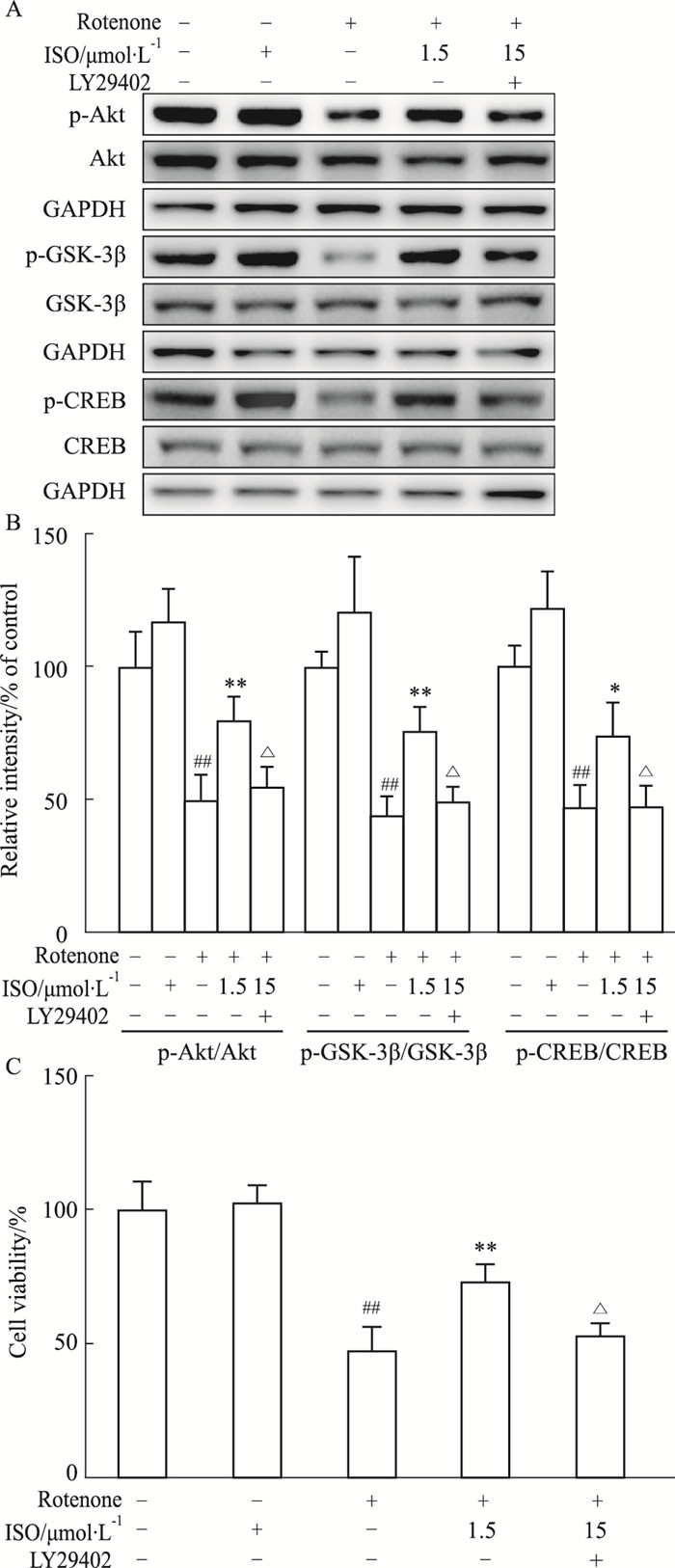
为进一步明确ISO对鱼藤酮损伤PC12细胞的保护作用是否通过PI3K/Akt/GSK-3β信号通路实现,并且PI3K/Akt/GSK-3β通路的激活是否有助于CREB的磷酸化。加入PI3K/Akt特异性抑制剂LY294002预处理PC12细胞。如Fig 4所示,与空白对照相比,鱼藤酮损伤模型组PC12细胞后Akt,GSK-3β,CREB的磷酸化水平明显降低,PC12细胞活力明显降低(P<0.01)。与鱼藤酮损伤组相比,ISO预处理组可以增强p-Akt,p-GSK-3β,p-CREB的表达,提高细胞活力(P<0.01)。加入LY294002后能够部分阻断ISO引起的p-Akt,p-GSK-3β,p-CREB的表达增加,抑制细胞活力增强(P<0.05)。
|
| Fig 4 Effects of ISO on activation of CREB and cell viability in presence of PI3K inhibitor(x±s, n=4) A:The levels of p-Akt, Akt, p-GSK-3β, GSK-3β, p-CREB and CREB were detected by Western blot. GAPDH was used as a loading control; B:p-Akt/Akt, p-GSK-3β/GSK-3β and p-CREB/CREB ratio; C: The protective effect of ISO on rotenone-induced PC12 cells was reversed by LY294002. ##P < 0.01 vs control group, *P < 0.05, **P < 0.01 vs rotenone group, △P < 0.05 vs ISO group. |
实验结果表明,ISO预处理能够激活CREB,增加Akt和GSK-3β磷酸化,发挥PC12细胞的保护作用,免受鱼藤酮毒性导致的细胞凋亡。加入PI3K/Akt特异性抑制剂LY294002,能够抑制CREB和Akt的磷酸化,激活GSK-3β,最终部分阻断ISO对PC12细胞的保护作用。
鱼藤酮是植物毛鱼藤的有效成分,对中枢多巴胺神经系统有选择性损伤,长期接触可引起多巴胺神经退行性病变[2]。PC12细胞是大鼠肾上腺嗜铬细胞瘤细胞,能够合成多巴胺等神经递质,含有合成、分解多巴胺所需要的酶。本实验以鱼藤酮损伤构建PD细胞模型,探讨异鼠李素对鱼藤酮损伤PC12细胞的保护作用,应用PI3K抑制剂处理PC12细胞,观察CREB磷酸化程度,阐明CREB对异鼠李素调控PC12细胞的作用机制。
CREB是一种普遍存在的磷酸化依赖性转录因子,可以通过各种丝氨酸/苏氨酸激酶在Ser133进行磷酸化而被激活。CREB的激活是多种适应性变化的基础,能增强cAMP诱导的基因转录,调控相关的信号转导通路,发挥生物学功能[6]。实验结果表明,鱼藤酮抑制CREB的磷酸化,而ISO预处理能够促进CREB的活化,提高鱼藤酮损伤PC12细胞的活力。GSK-3β是中枢神经系统中高表达的蛋白激酶,参与基因转录、蛋白质合成、细胞周期调控以及细胞程序性死亡等多种细胞过程。文献报道抑制GSK-3β活化可以减少细胞凋亡提高细胞存活[10-11]。本实验研究结果显示,鱼滕酮损伤PC12细胞中GSK-3β被激活,但ISO预处理能够抑制GSK-3β活性,降低鱼藤酮对PC12细胞毒性作用。
GSK-3β能够被多种信号通路调节,影响细胞存活,PI3K/Akt是其中最重要的上游调节通路。研究表明PI3K/Akt通路的激活在预防细胞变性和细胞凋亡中起主导作用[8, 12-13]。在外源性和内源性应激、胰岛素、生长因子和细胞因子的刺激下,Akt磷酸化一系列下游靶标,使GSK-3β磷酸化和失活,激活CREB。不同神经毒素诱导神经元损伤后,Akt ser473的活化受到明显抑制,磷酸化水平明显降低,GSK3β ser9失活也明显受抑制。我们的实验显示了类似的结果,鱼藤酮损伤可降低Akt活性,激活GSK-3β,同时降低CREB磷酸化。目前,PI3K/Akt/GSK-3β途径是研究细胞凋亡的重要通路。激活GSK-3β可能参与缺血再灌注后的神经保护。麦角黄毒素通过下调p-GSK3β和p-Akt水平,抑制6-OHDA诱导的SH-SY5Y细胞凋亡[14]。本实验中,我们进一步加入PI3K抑制剂LY294002可逆转ISO激活CREB,Akt,使GSK-3β失活,以上结果证实PI3K/Akt/GSK-3β/CREB的激活参与了ISO的神经保护作用。
综上所述,ISO预处理可以减轻鱼藤酮对PC12细胞的损伤作用,其神经保护作用可能是通过激活PI3K/Akt/GSK-3β/CREB信号通路实现的。
| [1] |
Hayes M W, Fung V S, Kimber T E, et al. Updates and advances in the treatment of Parkinson disease[J]. Med J Aust, 2019, 211(6): 277-83. doi:10.5694/mja2.50224 |
| [2] |
Tapias V, McCoy J L, Greenamyre J T. Phenothiazine normalizes the NADH/NAD+ ratio, maintains mitochondrial integrity and protects the nigrostriatal dopamine system in a chronic rotenone model of Parkinson's disease[J]. Redox Biol, 2019, 24: 101164. doi:10.1016/j.redox.2019.101164 |
| [3] |
Balakrishnan R, Elangovan N, Mohankumar T, et al. Isolongifolene attenuates rotenone-induced mitochondrial dysfunction, oxidative stress and apoptosis[J]. Front Biosci, 2018, 10: 248-61. doi:10.2741/s513 |
| [4] |
Gao L, Yao R, Liu Y, et al. Isorhamnetin protects against cardiac hypertrophy through blocking PI3K-AKT pathway[J]. Mol Cell Biochem, 2017, 429(1-2): 167-77. doi:10.1007/s11010-017-2944-x |
| [5] |
Wang J, Gong H M, Zou H H, et al. Isorhamnetin prevents H2O2 induced oxidative stress in human retinal pigment epithelial cells[J]. Mol Med Rep, 2018, 17(1): 648-52. |
| [6] |
Jain V, Baitharu I, Prasad D, et al. Enriched Environment Prevents hypobaric hypoxia induced memory impairment and neurodegeneration:Role of BDNF/PI3K/GSK3β pathway coupled with CREB activation[J]. PLoS One, 2013, 4(5): e62235. |
| [7] |
Sun H, Wu H, Liu J, et al. Prenatal stress impairs spatial learning and memory associated with lower mRNA level of the CAMKII and CREB in the adult female rat hippocampus[J]. Neurochem Res, 2017, 42(5): 1496-503. doi:10.1007/s11064-017-2206-z |
| [8] |
Nakaso K, Tajima N, Horikoshi Y, et al. The estrogen receptor beta-PI3K/Akt pathway mediates the cytoprotective effects of tocotrienol in a cellular Parkinson's disease model[J]. Biochim Biophys Acta, 2014, 1842(9): 1303-12. doi:10.1016/j.bbadis.2014.04.008 |
| [9] |
Zhang S, Shao S Y, Song X Y, et al. Protective effects of forsythia suspense extract with antioxidant and anti-inflammatory properties in a model of rotenone induced neurotoxicity[J]. Neurotoxicology, 2016, 52: 72-83. doi:10.1016/j.neuro.2015.09.009 |
| [10] |
Sun C, Wang Y, Mo M, et al. Minocycline protects against rotenone-induced neurotoxicity correlating with upregulation of Nurr1 in a parkinson's disease rat model[J]. Biomed Res Int, 2019, 6843265. |
| [11] |
Rajendran M, Ramachandran R. Fisetin protects against rotenone-induced neurotoxicity through signaling pathway[J]. Front Biosci, 2019, 11: 20-8. doi:10.2741/e843 |
| [12] |
石雪萍, 李静, 冉建华, 等. 人参皂苷Rh2调控PI3K/AKT/GSK-3β信号通路诱导人结肠癌细胞凋亡[J]. 中国药理学通报, 2017, 33(1): 114-9. Shi X P, Li J, Ran J H, et al. Ginsenoside Rh2 induced human colorectal cancer cell apoptosis through PI3K/AKT/GSK-3β pathway[J]. Chin Pharmacol Bull, 2017, 33(1): 114-9. doi:10.3969/j.issn.1001-1978.2017.01.020 |
| [13] |
涂献坤, 杨滨, 涂德文, 等. PI3K/Akt通路在丙泊酚减轻大鼠脑缺血性损伤中的作用[J]. 中国药理学通报, 2019, 35(5): 630-633. Tu X K, Yang B, Tu D W, et al. Propofol attenuates neuroinflammation and brain damage via modulating PI3K/Akt signaling pathway in rats of focal cerebral ischemia[J]. Chin Pharmacol Bull, 2019, 35(5): 630-3. doi:10.3969/j.issn.1001-1978.2019.05.009 |
| [14] |
Song J, Shaw P, Wong N, et al. Chrysotoxine, a novel bibenzyl compound selectively antagonizes MPP+, but not rotenone, neurotoxicity in dopaminergic SH-SY5Y cells[J]. Neurosci Lett, 2012, 521(1): 76-81. doi:10.1016/j.neulet.2012.05.063 |

