


2. 吉林省过敏性疾病重点实验室, 延吉 133002;
3. 延边大学医学院解剖学教研室, 延吉 133002
 ,
GAO Ge1,2,
LIU Han-ye1,2,
YAN Guang-hai2,3,
LI Liang-chang2,3,
ZHANG Jing-yao1,2,
CUI Hong1,2
,
GAO Ge1,2,
LIU Han-ye1,2,
YAN Guang-hai2,3,
LI Liang-chang2,3,
ZHANG Jing-yao1,2,
CUI Hong1,2

2. Jilin Key Lab of Anaphylactic Diseases, Yanji, Jilin 133002, China;
3. Dept of Anatomy, College of Medicine, Yanbian University, Yanji, Jilin 133002, China
肺纤维化(pulmonary fibrosis,PF)是一种慢性、进行性和致死性的肺部疾病。它主要表现为过度分泌促纤维化介质,成纤维细胞的活化和增殖,凋亡抵抗性肌成纤维细胞的持续存在,病灶内炎症细胞的募集等。其发病机制尚不明确[1]。特发性肺纤维化(idiopathic pulmonary fibrosis,IPF)是一种慢性间质性肺病,以普通型间质性肺炎的组织病理学模式为特征。在肺组织损伤早期,出现炎症细胞募集,导致趋化因子和促炎细胞因子释放,进而炎症细胞大量募集、重塑和肺纤维化。IPF确诊后,其平均生存期仅为2.8年,死亡率较大多数肿瘤略高,因此IPF被称为一种“类肿瘤疾病”。而目前在临床上用于抗纤维化药物主要是吡非尼酮和尼达尼布[2],其虽然有助于改善肺功能,缓解疾病症状,但不能显著提高患者的生存率[3]。所以明确IPF发病机制,寻找靶向治疗IPF的药物成为了研究重点。
转化生长因子-β1(transforming growth factor-β1,TGF-β1)的活化是最直接的促进肺组织纤维化因素,其作用于成纤维细胞,分泌大量胶原蛋白质(collagenI A1,COL1A1)或者诱导其分化为肌成纤维细胞,表达α-平滑肌肌动蛋白;而丝裂原活化蛋白激酶(mitogen-activated protein kinases,MAPKs),例如P38 MAPK能被TGF-β1磷酸化;核转录因子-κB(nuclear factor kappa-B,NF-κB)是p38 MAPK的下游信号通路,在炎症和纤维化中发挥重要作用[4, 5]。
FTY-720(Fingolimod)是近年来新开发的免疫抑制剂,它是来源于中药冬虫夏草提取物中具有免疫抑制作用的成分ISP-I改造而成,其对自身免疫性心肌炎、多发性硬化、葡萄膜视网膜炎和动脉粥样硬化具有显著的保护作用[6]。FTY720是1-磷酸鞘氨醇(sphingosine-1-phosphate,S1P)的结构类似物,在体内被鞘氨醇激酶-2磷酸化形成FTY720-磷酸盐(FTY720-p),FTY720-p是S1P1、S1P3受体的激动剂,同时也是S1P1受体的功能拮抗剂。FTY720-p以高亲和力结合S1P1R,诱导受体内化并使免疫细胞对S1P变得不敏感。FTY-720通过靶向TGF-β1信号通路改善肾纤维化[7], 而对肺纤维化的研究尚不清楚。
本研究拟探讨FTY-720对博来霉素诱导的小鼠肺纤维化的影响及其作用机制,并探讨了其机制与TGF-β1/P38 MAPK/NF-κB信号通路的相关性。
1 材料与方法 1.1 实验材料、试剂 1.1.1 实验动物由延边大学实验动物中心提供40只清洁干净雄性BALB/c小鼠,体质量(18±5) g,许可证号:SCXK(吉)2017-0003。经延边大学医学院伦理委员会批准,本实验开始进行,并遵守《实验动物管理条例》。
1.1.2 材料与试剂博来霉素(Sigma, 美国)(货号:203401);FTY-720(Sigma, 美国)(货号:SML0700批号:0000026872);IL-1β(货号:KMC0011)、TNF-α(货号:BMS607-3) ELISA试剂盒(Invitrogen, 美国);Masson染色液(索来宝, 中国)(货号:G1345批号:20180418);anti-TGF-β1(货号:3711批号:7), anti-P38 MAPK(货号:9212), anti-p-P38 MAPK(货号:9215批号:7), anti-NF-κBp65(货号:6956), anti-β-actin(货号:4970批号:17) (Cell Signaling, 美国); anti-COL1A1 (Abcam, 美国)(货号ab34710批号:GR158873-9)。
1.1.3 仪器2135型旋转切片机(德国徕卡公司);分光光度计(Thermo公司);酶联免疫吸附测定仪RT-2100C(美国雷杜公司);5415D低温高速多功能离心机(Eppendorf公司);Western blot转膜仪(Bio-Rad公司);Amersham Imager 600自动化学发光凝胶成像分析仪(General Electric公司);TXD3细胞图片离心机(湘仪集团)。
1.2 实验方法 1.2.1 动物分组及模型制备将40只雄性BALB/c小鼠随机分为8组:生理盐水对照组(Control)、BLM模型组(BLM)、生理盐水+FTY-720对照组(NS+FTY-720)、博来霉素+FTY-720组(BLM+FTY-720),7天、14天分批处死,每组5只。各组小鼠适应性饲养1周后,Control组和NS+F组小鼠于第0天气管内给予生理盐水(100 μL),第1、3、5天分别腹腔注射生理盐水(100 μL)和FTY-720(1 mg·kg-1,100 μL);BLM组和BLM+FTY-720组于第0天气管内给予博来霉素(10 mg·kg-1,100 μL),1、3、5天分别腹腔注射生理盐水(100 μL)和FTY-720(1 mg·kg-1,100 μL);给药第7天和第14天小鼠进行处死,提取肺组织等备用于实验。
1.2.2 标本收集各组小鼠分别在给药7天和14天处死。小鼠吸入乙醚麻醉,颈部皮肤进行消毒并切开,钝性分离皮下组织,暴露气管,行气管切开术,轻轻插入肺泡灌洗液(bronchoalveolar lavage fluid,BALF)软管,结扎固定软管,缓慢向肺组织中注射4℃生理盐水1 mL,并轻轻按摩小鼠胸腔,重复3次,使抽出的肺泡灌洗液不低于0.6 mL。收集的肺泡灌洗液用低温高速多功能离心机,以3 000 r·min-1离心5 min,将上清液保存在-80 ℃,离心后的沉淀物用于制备细胞涂片。收集BALF溶液后,取出小鼠的左肺并置于甲醛中固定,取出右肺并储存在-80 ℃的环境中。
1.2.3 肺组织学检查固定小鼠左肺48 h后,流水冲洗24 h。经常规脱水、包埋等步骤后,切片、铺片以备用于HE和Masson染色。从每只小鼠中随机选择3张切片,并在光学显微镜下观察它们的组织学变化。
1.2.4 BALF中蛋白质含量及总细胞数测定将在-80 ℃冷冻的BALF上清液在室温水浴中快速解冻,通过BCA法测定蛋白质含量。离心BALF后,将生理盐水溶液加入沉淀中,稀释至200 μL,混合并置于细胞涂片离心机中。1 000 r·min-1离心10 min,再1 500 r·min-1离心5 min。将涂好的细胞涂片进行瑞士-吉姆萨染色,并在光学显微镜下进行总细胞计数。
1.2.5 BALF中IL-1β、TNF-α含量的测定酶联免疫吸附实验(ELISA)测定小鼠肺组织BALF中的IL-1β和TNF-α水平。通过使用由标准蛋白质产生的标准曲线计算浓度。
1.2.6 免疫组化检测肺组织中COL1A1的表达将肺组织切片放于60 ℃的干燥器中熔蜡。然后二甲苯脱蜡;梯度浓度酒精脱水至PBS缓冲液,抗原高火修复15分钟(柠檬酸盐缓冲液),自然降温。PBS缓冲液洗片,然后与用一抗标记的一抗孵育过夜。最后,将切片用DAB染色,用苏木精复染,脱水,洗涤并用二甲苯固定。随机选择5个不同的视野观察。
1.2.7 Western blot检测肺组织中TGF-β1、p-P38 MAPK和NF-κB表达根据每个试剂盒的要求,裂解并提取小鼠肺组织蛋白质,将相同量的蛋白质(40 μg)在10%的SDS-PAGE中以70 V恒压电泳,切取目的条带。300 mA低温条件下转膜。在脱脂奶粉封闭液中常温封闭1.5 h。分别用小鼠TGF-β1、β-actin、P38 MAPK、p-P38 MAPK、NF-κB p65抗体4 ℃孵育过夜,将膜取出,在TBST中充分洗涤。洗膜后,加入HRP标记的相应二抗并在室温下温1.5 h。将膜取出,在TBST中洗涤后,使用Amersham Imager 600自动化学发光凝胶成像分析仪进行曝光。
1.3 统计学处理采用GraphPad Prism 6.0进行统计学分析。实验结果计量资料以x±s表示,组间比较采用单因素方差分析。
2 结果 2.1 FTY-720对博莱霉素诱导肺纤维化的作用 2.1.1 FTY-720对肺组织病理学改变的影响Fig 1A小鼠肺组织切片HE染色显示,与对照组比较,BLM 7d肺组织结构紊乱,肺泡壁增厚,可见大量炎性细胞渗出,成纤维细胞增多,至14 d,组织结构破坏明显,肺间质胶原纤维大量沉积。给予FTY-720明显改善肺组织结构紊乱,减少肺间质胶原沉积。如Fig 1B Masson染色可见,对照组肺组织结构正常,模型组蓝色胶原纤维沉积不断增多,至14 d胶原纤维沉积最多,呈弥漫性分布,同时肺泡结构破坏明显。给予FTY720,能明显缓解上述肺组织病理变化。
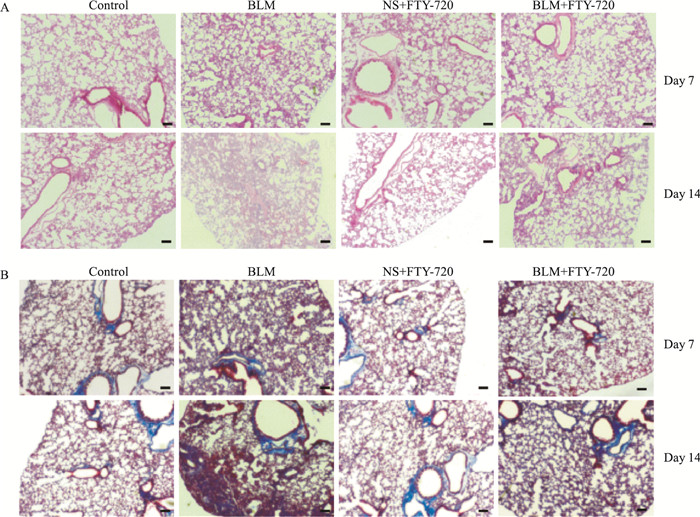
|
| Fig 1 HE staining and Masson staining of lung tissues in mice of control group, BLM group, NS+FTY-720 group and BLM+FTY-720 group A. HE stainingof lung tissues in mice; B. Masson staining of lung tissues in mice. The scale bar=100 μm. |
Fig 2A和Fig 2B结果与对照组相比,BLM小鼠肺组织BALF中蛋白质含量和细胞数显著增加;给予FTY-720后,能显著降低博来霉素诱导小鼠BALF中蛋白质含量和总细胞数。
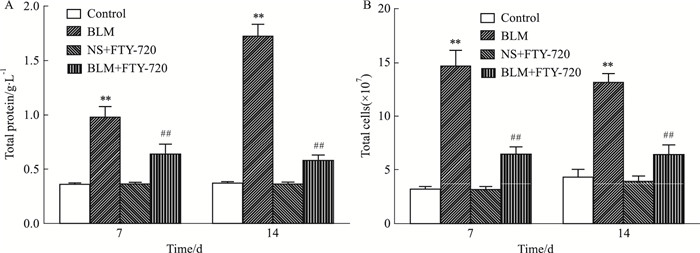
|
| Fig 2 Determination of protein content and total cell number in BALF(x±s, n=5) A. Determination of total protein content in BALF; B. Determination of total cell number in BALF. **P < 0.01 vs control groups. ##P < 0.01 vs BLM groups. |
检测了小鼠肺组织BALF中的细胞因子含量。如Fig 3A和Fig 3B结果所示,相比于对照组小鼠,模型组小鼠BALF中IL-1β、TNF-α含量明显上调;而FTY-720能够明显降低博来霉素诱导小鼠BALF中IL-1β和TNF-α水平。
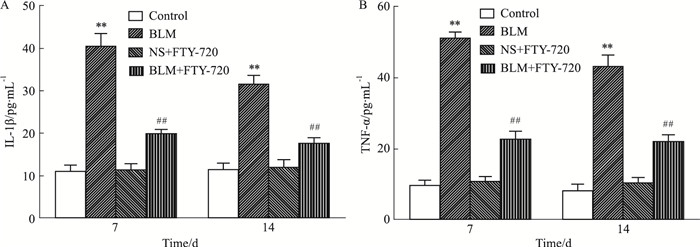
|
| Fig 3 Determination of IL-1β and TNF-α levels in BALF by ELISA(x±s, n=5) A. Determination of IL-1β levels in BALF; B. Determination of TNF-α levels in BALF. **P < 0.01 vs control groups. ##P < 0.01 vs BLM groups. |
Fig 4免疫组织化学结果显示,模型组7 d和14 d小鼠肺组织与对照组比较,COL1A1的阳性表达明显增加,而FTY-720处理后显著降低阳性表达。
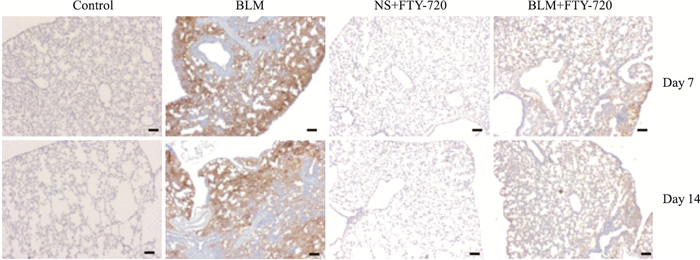
|
| Fig 4 COL1A1 positive expression Immunohistochemical detection of COL1A1 expression in lung tissues. The scale bar=100μm. |
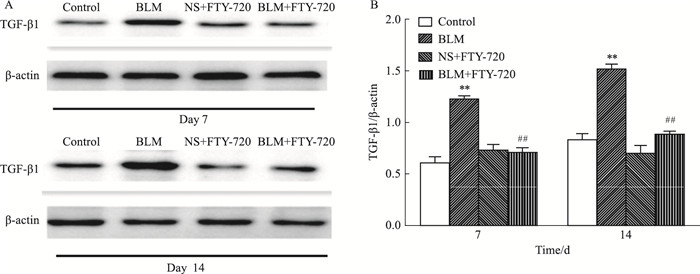
Western blot实验结果显示,BLM诱导小鼠肺组织中TGF-β1蛋白的表达水平较对照组明显上体,FTY-720抑制小鼠TGF-β1蛋白表达水平,如Fig 5所示。
|
| Fig 5 Expression of TGF-β1 proteins detected by Western blot(x±s, n=5) A. Expression levels of TGF-β1 proteins in mouse lung tissues on day 7 and day 14; B. Quantitative analysis of A. **P < 0.01 vs control groups. ##P < 0.01 vs BLM groups. |
Fig 6结果显示,模型组中7 d小鼠肺组织中p-P38 MAPK表达水平明显升高,到14 d略下降;而FTY-720能够明显降低肺纤维化小鼠肺组织p-P38 MAPK的表达。

|
| Fig 6 Expression of p-P38 MAPK proteins detected by Western blot(x±s, n=5) A. Expression levels of p-P38 MAPK proteins in mouse lung tissues on day 7 and day 14; B. Quantitative analysis of A. **P < 0.01 vs control groups. #P < 0.05 vs BLM groups. |
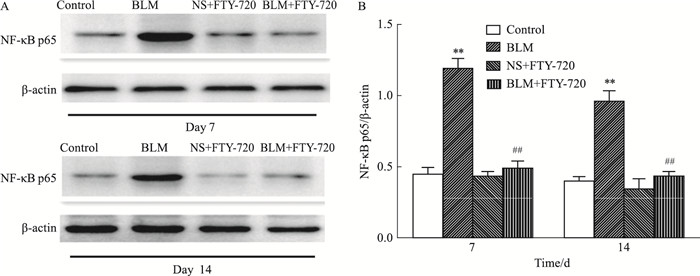
Fig 7结果显示,7 d模型组核内NF-κB p65的水平与生理盐水对照组相比明显增多,14 d模型组核内NF-κBp65的水平较7 d略有降低,但与对照组比较明显上调;给与FTY-720后能明显抑制NF-κB p65的表达。
|
| Fig 7 Expression of NF-κBp65 proteins detected by Western blot(x±s, n=5) A. Expression levels of NF-κB p65 proteins in mouse lung tissues on day 7 and day 14; B. Quantitative analysis of A. **P < 0.01 vs control groups. ##P < 0.01 vs BLM groups. |
肺纤维化是一大类肺疾病的终末期改变,以成纤维细胞增殖、细胞外基质(ECM)大量聚集并伴炎症损伤、组织结构破坏严重为特征,在全球范围内患病人数不断攀升[8]。在本实验中,BLM诱导小鼠肺纤维化模型,所建立的实验模型是早期肺纤维化范畴。本实验HE和Masson染色结果7 d主要表现为炎性细胞浸润,14 d胶原纤维沉积急剧增加。因此,早期肺纤维化是以炎性细胞渗出为起点,研究表明,肺纤维化发生过程的关键阶段正是因为早期肺纤维化的形成[9]。所以本实验主要研究早期肺纤维化发生机制。
有研究表明,博来霉素诱导的肺纤维化中IL-1β以及TNF-α水平明显升高[10]。成纤维细胞表面受体结合IL-1β,参与结缔组织再生成。肺纤维化发生过程中,IL-1β起到介导炎症及损伤,促进修复的作用;而过度修复则引起间质纤维化。TNF-α可直接作用于肺成纤维细胞,促进其增殖;也可以通过偶联表皮生长因子受体(epithelial growth factor receptor,EGFR)发挥作用。因此本实验测定了BALF中IL-1β、TNF-α水平,ELISA结果显示BLM诱导小鼠肺组织BALF中IL-1β、TNF-α水平显著升高;在BLM组中,给药7 d比14 d小鼠BALF中IL-1β、TNF-α水平高,说明炎症反应的高峰期在7 d;FTY-720下调上述因子水平。上述结果说明博来霉素诱导的小鼠肺纤维化,开始以肺部炎症为主要病理表现,而到14天时肺组织炎症逐渐演变为肺纤维化,呈现肺组织细胞外基质过度度沉积。广泛纤维化的特征是以细胞外基质(extracellular matrix,ECM)过度沉积, 主要成分为CollagenI A1[11]。本实验的模型组小鼠肺组织中CollagenI A1大量沉积,而给予FTY-720显著降低了CollagenI A1的水平。同样,博来霉素诱导BALF中的总蛋白浓度、总细胞数增加,FTY-720明显降低上述水平。综上所述,FTY-720抑制炎症细胞的激活并参与肺纤维化的发展。
近年来,TGF-β1/ Smad2 / Smad3被认为是促进肺纤维化的经典信号传导途径。除Smad外,越来越多的证据表明,TGF-β1还能激活各种Smad非依赖性信号通路[12]。因此,本课题组详细分析了非经典途径TGF-β1/ P38 MAPK / NF-κB信号通路通过肺部炎症反应或肺损伤促纤维化的潜在分子机制。研究表明,抑制P38 MAPK和NF-κB可以保护肝脏损伤和抗纤维化[13]。在本实验中发现博来霉素激活TGF-β1/P38 MAPK/NF-κB信号通路,而FTY-720通过抑制上述信号转导通路,抑制炎症因子的产生,保护对博来霉素诱导的小鼠肺纤维化。
本研究证实了FTY-720对小鼠肺纤维化的保护作用,其机制与TGF-β1//P38 MAPK/NF-κB信号通路有关,表明FTY-720可能成为治疗肺纤维化的新希望。
| [1] |
孙云晖, 王一新, 马雪梅, 等. IL-37抑制IL-18在大鼠肺纤维化模型中的表达及意义的探讨[J]. 中国免疫学杂志, 2017, 33(10): 1464-7. Sun Y H, Wang Y X, Ma X M, et al. Expression and significance discussion of IL-37 inhibits IL-18 in rat pulmonary fibrosis models[J]. Chin J Immunol, 2017, 33(10): 1464-7. doi:10.3969/j.issn.1000-484X.2017.10.005 |
| [2] |
Knuppel L, Ishikawa Y, Aichler M, et al. A novel antifibrotic mechanism of nintedanib and pirfenidone. Inhibition of collagen fibril assembly[J]. Am J Respir Cell Mol Biol, 2017, 57(1): 77-90. doi:10.1165/rcmb.2016-0217OC |
| [3] |
Spagnolo P, Wells A U, Collard H R. Pharmacological treatment of idiopathic pulmonary fibrosis:an update[J]. Drug Discov Today, 2015, 20(5): 514-24. doi:10.1016/j.drudis.2015.01.001 |
| [4] |
孟哲, 李海禹, 陶海龙. 基于TGF-β1/Smad3信号通路探讨虾青素对心肌成纤维细胞Ⅰ、Ⅲ型胶原表达的影响[J]. 中国药理学通报, 2018, 34(6): 841-5. Meng Z, Li H Y, Tao H L. Effect of astaxanthin on expression of type Ⅰ and type Ⅲ collagen in cardiac fibroblasts and its mechanism based on TGF-β1/Smad3 signaling pathway[J]. Chin Pharmacol Bull, 2018, 34(6): 841-5. doi:10.3969/j.issn.1001-1978.2018.06.020 |
| [5] |
Zhang H F, Wang Y L, Gao C, et al. Salvianolic acid A attenuates kidney injury and inflammation by inhibiting NF-κB and p38 MAPK signaling pathways in 5/6 nephrectomized rats[J]. Acta Pharmacol Sin, 2018, 39(12): 1855-64. doi:10.1038/s41401-018-0026-6 |
| [6] |
Gao F, Gao Y, Meng F, et al. The sphingosine 1-phosphate analogue FTY720 alleviates seizure-induced overexpression of P-glycoprotein in rat hippocampus[J]. Basic Clin Pharmacol Toxicol, 2018, 123(1): 14-20. doi:10.1111/bcpt.12973 |
| [7] |
Tian T, Zhang J, Zhu X, et al. FTY720 ameliorates renal fibrosis by simultaneously affecting leucocyte recruitment and TGF-β signalling in fibroblasts[J]. Clin Exp Immunol, 2017, 190(1): 68-78. doi:10.1111/cei.13003 |
| [8] |
梁海海, 李天宇, 解岩, 等. Lin28B/let-7d环路调控成纤维细胞功能参与肺纤维化发生[J]. 中国药理学通报, 2017, 33(2): 175-80. Liang H H, Li T Y, Xie Y, et al. Lin28B/let-7d axis contributes to pulmonary fibrosis by affecting mesenchymal phenotypic properties of lung fibroblasts[J]. Chin Pharmacol Bull, 2017, 33(2): 175-80. doi:10.3969/j.issn.1001-1978.2017.02.007 |
| [9] |
Du S, Li H, Cui Y, et al. Houttuynia cordata inhibits lipopolysaccharide-induced rapid pulmonary fibrosis by up-regulating IFN-gamma and inhibiting the TGF-beta1/Smad pathway[J]. Int Immunopharmacol, 2012, 13(3): 331-40. doi:10.1016/j.intimp.2012.03.011 |
| [10] |
Jia L, Sun P, Gao H, et al. Mangiferin attenuates bleomycin-induced pulmonary fibrosis in mice through inhibiting TLR4/p65 and TGF-β1/Smad2/3 pathway[J]. J Pharm Pharmacol, 2019, 71(6): 1017-28. doi:10.1111/jphp.13077 |
| [11] |
孙金玲, 郑金旭, 史小东, 等. 柴胡皂甙D通过调控TGF-β1/Smads信号通路抑制人胚肺成纤维细胞增殖和胶原蛋白产生[J]. 细胞与分子免疫学杂志, 2019, 35(3): 256-61. Sun J L, Zheng J X, Shi X D, et al. Saikosaponin D inhibits proliferation and collagen production of human embryonic lung fibroblasts by regulating TGF-β1/Smads signaling pathway[J]. Chin J Cell Mol Immunol, 2019, 35(3): 256-61. |
| [12] |
Lee I C, Ko J W, Park S H, et al. Copper nanoparticles induce early fibrotic changes in the liver via TGF-β/Smad signaling and cause immunosuppressive effects in rats[J]. Nanotoxicology, 2018, 12(6): 637-51. doi:10.1080/17435390.2018.1472313 |
| [13] |
Gehrke N, Nagel M, Straub B K, et al. Loss of cellular FLICE-inhibitory protein promotes acute cholestatic liver injury and inflammation from bile duct ligation[J]. Am J Physiol Gastrointest Liver Physiol, 2018, 314(3): G319-33. doi:10.1152/ajpgi.00097.2017 |