

2. 桂林医学院附属医院广西神经系统疾病临床医学研究中心, 广西 桂林 541004;
3. 桂林医学院附属医院广西脑与认知重点实验室, 广西 桂林 541004;
4. 桂林医学院附属医院神经内科, 广西 桂林 541004;
5. 桂林医学院附属医院药学部, 广西 桂林 541004
 ,
XIANG Wen-jing1,4,
ZHOU Zi-xian1,4,
JIANG Yan-lin1,5,
LU Mei-lian1,2,3,
WEN Jian1,2,5,
LIAO Ru-jia1,2,3,4
,
XIANG Wen-jing1,4,
ZHOU Zi-xian1,4,
JIANG Yan-lin1,5,
LU Mei-lian1,2,3,
WEN Jian1,2,5,
LIAO Ru-jia1,2,3,4

2. Guangxi Clinical Research Center for Neurological Diseases, Affiliated Hospital of Guilin Medical University, Guilin Guangxi 541004, China;
3. Guangxi Key Lab of Brain and Cognitive Neuroscience, Affiliated Hospital of Guilin Medical University, Guilin Guangxi 541004, China;
4. Dept of Neurology, Affiliated Hospital of Guilin Medical University, Guilin Guangxi 541004, China;
5. Dept of Pharmacy, Affiliated Hospital of Guilin Medical University, Guilin Guangxi 541004, China
脑出血(intracerebral hemorrhage,ICH)是一种突然起病的血液循环障碍疾病,临床上表现为一过性或永久性的功能障碍,是脑卒中的重要类型,患者多死于脑出血早期并发症[1]。中国脑出血致死患者约占脑血管病致死患者61.7 %,已成为我国首要致死疾病[2]。尽管ICF1病理生理研究已取得巨大进步,但有效治疗手段尚局限于超早期止血、控制颅内高压、溶栓和神经保护药物应用等。从疗效上看,脑出血的病死率、复发率仍然很高,并发症、后遗症仍很多[3]。目前研究显示,脑出血后继发性脑损伤是其主要损伤机制,包括红细胞降解产物的神经毒性、炎症反应、脑水肿、血脑屏障的破坏以及补体系统的激活等,其中炎症反应是脑出血后继发性损伤的重要病理生理过程[4]。炎性反应是导致脑出血后多种细胞死亡、继发神经功能障碍重要原因。多个研究均发现小胶质细胞是参与中枢炎症反应的重要细胞类型。脑损伤后多种因子刺激小胶质细胞激活,使处于静息态小胶质细胞极化,更多转化为具有神经毒性的M1型小胶质细胞。小胶质细胞极化过程是指静息态小胶质细胞受到某些因子刺激后发生形态与功能变化,转化为经典M1型小胶质细胞和可变M2型小胶质细胞。M1型小胶质细胞通过释放炎症因子发挥神经毒性作用,M2型小胶质细胞释放抗炎因子及调控细胞吞噬发挥神经保护作用。多个研究指出,M1型小胶质细胞通过释放多种具有神经毒性的细胞因子包括白细胞介素1β(interleukin 1β,IL-1β)、肿瘤坏死因子(tumor necrosis factor,TNF)α及IL-6、IL-8等。上述因子通过激活血管内皮细胞和白细胞,改变内皮细胞抗凝状态,损伤内皮细胞、增加血管通透性,导致某些重要神经毒性分子释放,如花生四烯酸及其代谢产物、氮氧化物等,以及调节粘附分子并促进其他炎症因子表达等加重损伤。因此,将激活后的M1型小胶质细胞转化为具有神经保护作用的M2型小胶质细胞可能是减轻脑出血后继发性脑损伤的重要途径。
金花茶多糖(camellia nitidissima polysaccharides,CNP)由广西特有植物金花茶提取提纯。之前的研究已经发现金花茶多糖具有调血脂,降糖等功效[5-6],而其在中枢的作用尚未见报道。本课题探索金花茶多糖在脑出血中的作用及可能的作用机制,为金花茶多糖作为脑损伤的一种潜在治疗药物提供实验依据。
1 材料与方法 1.1 实验动物SPF级♂ 8~12周龄C57BL/6小鼠,体质量(25±3)g, 购于湖南斯莱克景达实验动物有限公司(许可证号:SCXK(湘) 2016-0002), 所用动物实验方法与处理措施均由桂林医学院实验动物伦理委员会批准并执行。
1.2 试剂与仪器金花茶多糖由桂林医学院药学院邹登峰教授提供;IL-6、IL-1β和TNFα的ELISA检测试剂盒(南京建成生物工程公司,批号分别为E20160628、20171134B、20170945B);伊文思蓝粉末购于源叶生物科技有限公司;IBA-1多克隆抗体(批号66827-1-Ig)购于Proteintech公司;CD206(批号29c3790)、CD16抗体(批号88e2569)均购于Affinity Biosciences公司;PCR相关试剂(Takara公司,美国); 脑立体定位仪、高速颅骨磨钻(瑞沃德生命科技有限公司,深圳),实时定量PCR仪(ABI/7500Fast, 美国);冰冻切片机(Thermo NX50,美国);酶标仪(BioTek/ELx808,美国);荧光显微镜(Leica DM4B,德国);旷场实验平台(欣软科技,上海)
1.3 基底节脑出血模型构建脑出血采用自体血注射法。♂ C57BL/6小鼠通过10%水合氯醛麻醉,脑立体定位仪上固定,以右侧脑基底节进针点,位置为前颅起,前后: -0.0 mm,左右: +1.0 mm, 深度:-3.0 mm。抽取小鼠尾动脉血30 μL注入,骨蜡封闭并缝合。对照组采用相同的方法注入等量生理盐水,其余处理相同。
1.4 实验动物分组与给药将小鼠随机均分为3组:假手术组(Sham组)、模型组(ICH组)、金花茶多糖组(CNP组),金花茶多糖组在脑出血模型成功后灌胃给予金花茶多糖(500 mg·kg-1),在脑出血后即刻给予及此后连续3 d。假手术组给予等体积生理盐水。
1.5 神经功能缺陷评分(neurological deficit score, NDS)参考文献采用28分评分法。具体如下:身体对称性(0~4分),步态(0~4分),45度攀爬实验(0~4分),转圈实验(0~4分),前肢对称性(0~4分),强迫转圈(0~4分),触须反应(0~4分)。0分为正常,4分为严重障碍。综合以上分数为该实验最终得分,以综合得分在5~15分作为纳入标准。
1.6 运动功能评价通过旷场实验评价各组小鼠运动功能情况。旷场设备由开口的方形盒子构成(长×宽×高为:45 cm×45 cm×45 cm)。将小鼠面朝一个特定的方向放入旷场箱中央,让其自由探索10 min。并通过软件进行运动轨迹的自动追踪和小鼠的运动路程、运动速度等参数的分析,最后通过对应软件统计小鼠的运动量。
1.7 感觉功能评价通过粘附移除实验评价各组小鼠感觉功能情况。将小鼠置于一旷场内熟悉1 min,在其左右前爪分别粘贴一块1 cm×1 cm的胶布,再将其轻放于旷场内开始计时,以120 s为上限统计其将两块胶布移除的潜在时间。
1.8 ELISA检测取损伤灶及损伤周边脑组织100 mg,按50 mg :1 ml加入冷生理盐水,冰浴下匀浆5 min,于4 ℃下2 000 r ·min-1离心15 min,分离出上清,取1 ml均分2份,置于-80 ℃冰箱待测。IL-1β、TNF α和IL-6用ELISA试剂盒检测,具体操作按说明书进行,结果以10-5 g·g-1湿重脑组织表示。
1.9 免疫组化染色术后24小时,将小鼠麻醉,用预冷的生理盐水灌流后,再用4%的多聚甲醛固定,30%的蔗糖溶液脱水。当样本彻底脱水后即开始切片,厚度为20 μm。PBS洗脑片,每次5 min,共3次。驴血清室温封闭脑片2 h,加入相应一抗4 ℃过夜。PBS清洗,每次5 min,共3次,加入相应的二抗后室温孵育2 h。PBS清洗,每次5 min共3次,最后封闭液封片,在荧光显微镜下观察。
1.10 实时荧光定量PCR (quantitative real-time PCR)总RAN提取试剂盒提取总RNA后,通过逆转录试剂盒逆转录为cDNA,通过特定引物与荧光定量PCR试剂盒进行PCR检测。PCR特定引物如下:IL-6引物序列如下: forward primer (5′-GGCGGATCGGATGTTGTGAT-3′)、reverse primer (5′-GGACCCCAGACAATCGGTTG-3′)。IL-1β引物序列如下: forward primer (5′-GCAACTGTTCCTGAACTCAACT-3′)、reverse primer (5′-ATCTTTTGGGGTCCGTCAACT-3′)。IL-10引物序列如下: forward primer (5′-TCAAGGATGCACATCAAAAGGC-3′)、reverse primer (5′-AGGCAGCAACTTCCTCCCT-3′)。BDNF引物序列如下: forward primer (5′-TCATACTTCGGTTGCATGAAGG-3′)、reverse primer (5′-AGACCTCTCGAACCTGCCC-3′)。内参GAPDH引物序列如下:forward primer (5′-AGGTCGGTGTGAACGGATTTG-3′)、reverse primer (5′-TGTAGACCATGTAGTTGAGGTCA-3′)。
1.11 脑出血后含水量测定脑出血3 d后小鼠经乙醚深度麻醉后断头取脑,采用干湿重法测量含水量。经大脑中线切开,去掉嗅叶与小脑后称量大脑湿重。然后把大脑于100 ℃条件下烘干72 h。根据湿重(WW)与干重(DW),按照下列公式计算大脑含水量:大脑含水量/%=(WW-DW) /WW×100%。
1.12 Evans Blue检测血脑屏障的通透性通过伊文思蓝染料(evans blue dye,EB)来评价血脑屏障的通透性。方法如下:小鼠腹腔注射4%的EB无菌生理盐水溶液250 μl,3 h后处死小鼠灌流,分离大脑备用。匀浆,4 ℃,12 000 r·min-1离心30 min,上清液与三氯乙酸等体积混合后4 ℃过夜。4 ℃,12 000 rpm离心30 min,取上清液,于620 nm波长下采用紫外可见分光光度计测定其吸光度。根据已知EB溶液标准曲线,计算样本EB的含量,EB浓度表示为pg·g-1组织重量。EB标准曲线的制备:采用50%三氯乙酸为校零标准品,按1 :3比例加入无水乙醇。使用50%三氯乙酸配制不同浓度(50、1 000 mg·L-1)的EB溶液,于620 nm波长下采用紫外可见分光光度计测定其吸光度。
1.13 统计学方法统计数据均用
如Fig 1所示,为探索金花茶多糖在脑出血中的作用,我们采用了小鼠自体血注射构建脑基底节出血模型,并在脑出血后即刻,以及每天连续给药3 d,并对各组小鼠进行神经功能评分,结果显示脑出血后整体神经功能下降,而给予金花茶多糖后3 d后可改善整体神经功能。
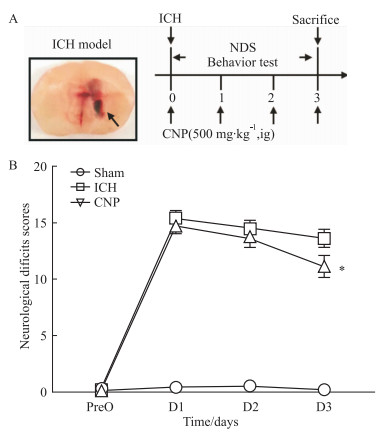
|
Fig 1 Intracerebral hemorrhage (ICH) model
A. experimental schedule; B. andneurological deficits scores. Results are presented as  , n=8 per group. *P < 0.05 vs ICH group. , n=8 per group. *P < 0.05 vs ICH group.
|
为进一步评估金花茶多糖在脑出血中的神经保护作用,我们在给予金花茶多糖3 d后,采用了旷场实验与粘附移除实验分别评估脑出血后的运动功能与感觉功能。结果如Fig 2所示,与假手术组比,模型组的运动功能与感觉功能均下降,而金花茶多糖组小鼠的运动功能与模型组比均显著改善,但感觉功能与模型组比无差异。
|
Fig 2 Neurological impairment in acute stages of ICH alleviated by CNP( |
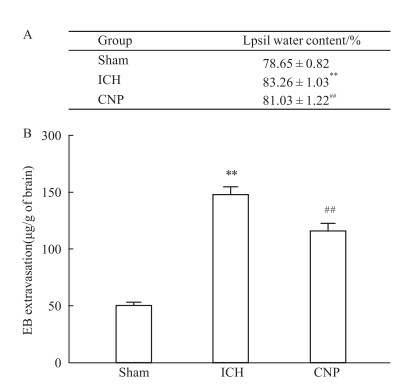
脑水肿与血脑屏障损伤是脑出血急性期的典型病理特征。为进一步证实金花茶多糖的神经保护作用,我们通过脑水肿检测与伊文思蓝染色检测给予金花茶多糖后脑出血周边区组织的病理改变。脑水肿结果显示模型组手术侧明显发生水肿,而金花茶多糖组与模型组比显著减少脑水肿(Fig 3A)。伊文思蓝染色结果显示模型组发生血脑屏障损伤,而金花茶多糖组较模型组相比减轻血脑屏障损伤(Fig 3B)。

|
Fig 3 Brain edema and blood-brain barrier destruction in acute stages of ICH attenuated by CNP( |
脑出血急性期会产生典型的炎症反应,一些典型的炎症因子包括IL-1β、TNF α和IL-6的表达显著升高。Fig 4显示脑出血3 d后模型组炎症因子与假手术组比升高,而金花茶多糖组与模型组比减少炎症因子的表达水平。
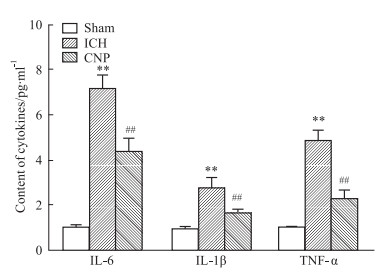
|
Fig 4 Neuroinflammation in acute stages of ICH reduced by CNP( |
既往报道显示脑出血后的炎症反应与小胶质细胞激活密切相关。因此我们检测了小胶质细胞激活情况。Fig 5结果,显示脑出血3 d后,在损伤周边区模型组小胶质细胞与假手术组比数量升高,且大多数细胞处于激活状态,而金花茶多糖组与模型组比显著抑制小胶质细胞激活,但小胶质细胞数量无差异。
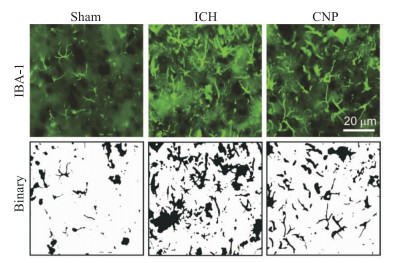
|
Fig 5 Microglial activation in acute stages of ICH inhibited by CNP( |
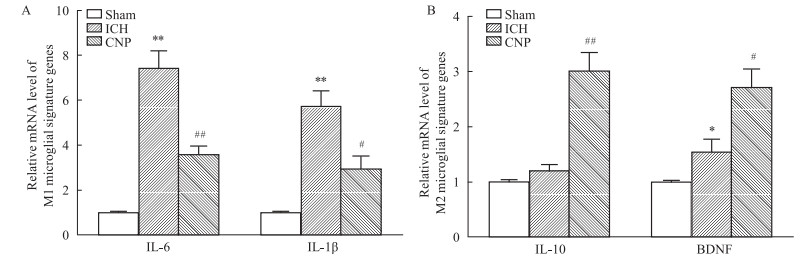
为进一步确定小胶质细胞的激活情况,我们对极化后M1型与M2型进行分析。Fig 6结果显示,脑出血3 d后,在损伤周边区模型组小胶质细胞与假手术组比小胶质细胞M1型比例升高,而金花茶多糖组与模型组比,小胶质细胞M1型比例显著下降,而M2型比例升高。
|
| Fig 6 Gene expression of M2 increased by CNP and gene expression M1 decreased by CNP in acute stages of ICH The levels of M1 and M2 markers in microglia were detected using real-time quantitative PCR. Results are presented as ±s, n=10~12 per group. *P < 0.05, **P < 0.01 vs Sham group; #P < 0.05, ##P < 0.01 vs ICH group. |
已知小胶质细胞极化后形成M1型后,小胶质细胞膜表面标志物CD16/32表达升高,而小胶质细胞极化后形成M2后,则小胶质细胞膜表面标志物CD206表达升高。为进一步验证金花茶多糖促进了小胶质细胞极化后更多地由M1型转化为M2型,我们通过免疫荧光分别检测M1型与M2型小胶质细胞膜表面标志物CD16和CD206。Fig 7结果显示,脑出血3 d后,损伤周边区模型组与假手术组比,小胶质细胞CD16和CD206表达均升高,但给予金花茶多糖后抑制了CD16的表达且进一步促进了CD206的表达。

|
Fig 7 M2 polarization enhanced by CNP and M1 polarization of microglia suppressed by CNP in acute stages of ICH( |
脑出血是致死致残率最高的疾病之一,脑出血后伴随运动功能、感觉功能、学习记忆等神经功能损害给患者及社会带来沉重精神与经济负担[9]。现有研究显示,脑出血急性期继发性脑损伤是影响脑出血预后关键。包括血压、炎症、红细胞降解产物、补体系统等是继发性脑损伤关键因素,针对上述因素的调控均可显著改善或减轻脑出血预后[10-11]。近期,一个脑出血重要的多中心Ⅲ期临床实验发现,靶向红细胞降解产物的药物-甲磺酸去铁胺(DFO)能一定程度改善脑出血患者功能(只是效果不如预期)[12],该结果提示DFO联合其它靶点药物可能效果更好或其它病理过程可能更重要。本研究发现靶向脑出血后炎症反应可明显减轻脑出血急性期神经功能障碍,连续给予金花茶多糖可显著减轻脑出血急性期多种炎症因子包括IL-1β、TNF α和IL-6的表达,同时改善整体的神经功能评分与运动功能障碍。该结果也提示:①金花茶多糖在脑出血后可能具有神经保护作用;②金花茶多糖可能是通过抑制炎症反应减轻脑损伤。
金花茶多糖来自于广西特有国家一级保护植物金花茶提取物。现有研究显示,其可通过抗氧化、抗炎减轻急性肝损伤,提高机体免疫力,降血糖等多种作用,然而其在中枢神经系统疾病中的作用则尚未见报道,我们的研究证实了金花茶多糖在脑出血急性期具有神经保护作用,同时可明显减轻血脑屏障的损伤及减少脑水肿。后者可能是促进神经功能恢复的重要原因,而金花茶多糖抑制炎症反应则可能是其改善血脑屏障损伤与减轻脑水肿的重要因素。本研究使用的金花茶多糖属于混合产物,由包括葡萄糖、半乳糖、阿拉伯糖和甘露糖等在内的多种单糖组成,而具体是哪种或哪几种单糖起主要作用还有待进一步研究。
脑出血后的炎症反应主要由小胶质细胞介导。研究显示脑损伤后4 h小胶质细胞即可激活并分泌多种炎症因子产生炎症反应,该作用甚至可以持续数周。小胶质细胞激活后转化为M1型是其发挥炎症反应的关键[13]。因此,调控小胶质细胞活性,抑制其转化为M1型是抑制脑出血后的炎症反应的关键。目前调控小胶质细胞极化,使其从促炎作用的M1型转化为神经保护作用的M2进而改善神经功能已经在包括脑出血在内的多种神经损伤疾病中进行了探索,如促进某些基因如TSG-6,或小分子化合物如AG-490以及与天然产物提取物如姜黄素等均可调控小胶质细胞极性[14-15]。本研究也证实金花茶提取物-金花茶多糖可促进小胶质细胞由具有神经毒性的M1型转化为神经保护作用的M2型,这可能是其抑制炎症的关键原因之一。
综上所述,金花茶多糖可明显减轻脑出血急性期神经功能评分、改善运动动能,减轻脑水肿与血脑屏障损伤,其神经保护作用可能与其促进小胶质细胞由M1型转化为M2型,抑制炎症有关。本研究为充分发掘与开发广西特色药材金花茶提供理论依据。
( 致谢: 本实验在桂林医学院附属医院神经科学实验室完成,感谢课题组老师同学的帮助和支持。)
| [1] |
Salman R A-S. A new era for comorbid cerebral ischaemia and haemorrhage[J]. Lancet Neurol, 2018, 17(6): 482-3. |
| [2] |
王陇德, 刘建民, 杨弋, 等. 我国脑卒中防治仍面临巨大挑战-《中国脑卒中防治报告2018》概要[J]. 中国循环杂志, 2019, 34(2): 105-19. Wang L D, Liu J M, Yang Y, et al. The prevention and treatment of stroke still face huge challenges-brief report on stroke prevention[J]. Chin Cir J, 2019, 34(2): 105-19. |
| [3] |
Feero W G, Wicklund C A, Veenstra D. Precision medicine, genome sequencing, and improved population health[J]. JAMA, 2018, 319(19): 1979-80. |
| [4] |
Liao R, Chen Y, Cheng L, et al. Histamine H1 receptors in neural stem cells are required for the promotion of neurogenesis conferred by H3 receptor antagonism following traumatic brain injury[J]. Stem Cell Reports, 2019, 12(3): 532-44. |
| [5] |
黄思茂, 曹后康, 高雅, 等. 金花茶多糖对四氯化碳致小鼠急性肝损伤的保护作用及其机制的研究[J]. 中药药理与临床, 2016, 32(6): 117-20. Huang S M, Cao H K, Gao Y, et al. Protective effect and mechanism of polysaccharides of Camellia nitidissima on acute hepatic injury[J]. Pharmaco Clin Chin Mater Med, 2016, 32(6): 117-20. |
| [6] |
邹登峰, 张可锋, 谢爱泽. 金花茶多糖抗小鼠免疫性肝损伤作用的研究[J]. 华西药学杂志, 2014, 29(5): 525-7. Zhou D F, Zhang K F, Xie A Z. Protective effect of Camellia nitidissima polysaccharides on immunological liver injury in the mice[J]. West Chi JPharmace Sci, 2014, 29(05): 525-7. |
| [7] |
Karuppagounder S S, Alin L, Chen Y, et al. N-acetylcysteine targets 5 lipoxygenase-derived, toxic lipids and can synergize with PGE2 to inhibit ferroptosis and improve outcomes following hemorrhagic stroke in mice[J]. Ann Neurol, 2018, 84(6): 854-72. |
| [8] |
Joy M T, Ben Assayag E, Shabashov-Stone D, et al. CCR5 is a therapeutic target for recovery after stroke and traumatic brain injury[J]. Cell, 2019, 176(5): 1143-57. |
| [9] |
Li Z, Jiang Y, Li H, et al. China's response to the rising stroke burden[J]. BMJ, 2019, 364(1): 1879-80. |
| [10] |
廖儒佳.组胺H3受体拮抗剂对脑外伤的神经保护作用及机制研究[D].浙江大学, 2017. Liao R J. Protection of histamine H3 receptor antagonists against traumatic brain injury and the involved mechanisms[D]. Zhejiang Univ, 2017. |
| [11] |
田宁, 蒋艳林, 陈梅容, 等. 醉茄素类化合物在神经系统疾病中的研究进展[J]. 中国药理学通报, 2019, 35(1): 4-7. Tian N, Jiang Y L, Chen M R, et al. Roles of withaferin compounds in nervous system disorders[J]. Chin Pharmacol Bull, 2019, 35(1): 4-7. |
| [12] |
Selim M, Foster L D, Moy C S, et al. Deferoxamine mesylate in patients with intracerebral haemorrhage (i-DEF):a multicentre, randomised, placebo-controlled, double-blind phase 2 trial[J]. The Lancet Neurology, 2019, 18(5): 428-38. |
| [13] |
Liu R, Liao X Y, Pan M X, et al. Glycine exhibits neuroprotective effects in ischemic stroke in rats through the inhibition of M1 microglial polarization via the NF-kappaB p65/Hif-1alpha signaling pathway[J]. J Immunol, 2019, 202(6): 1704-14. |
| [14] |
Liu Z, Ran Y, Huangh S, et al. Curcumin protects against ischemic stroke by titrating microglia/macrophage polarization[J]. Front Aging Neurosci, 2017, 9(1): 1-10. |
| [15] |
Li R, Liu W, Yin J, et al. TSG-6 attenuates inflammation-induced brain injury via modulation of microglial polarization in SAH rats through the SOCS3/STAT3 pathway[J]. J Neuroinflammation, 2018, 15(1): 1-18. |