

2. 河北医科大学生理教研室, 河北 石家庄 050017
2. Dept of Physiology, Hebei Medical University, Shijiazhuang 050017, China
大量研究表明[1],慢性间歇性低压低氧(chronic intermittent hypobaric hypoxia,CIHH)具有明显的心血管保护效应。我们以往的研究显示[2],CIHH对于缺血/再灌注引起的大鼠心肌损伤具有明显的对抗作用。例如,CIHH具有抗心律失常作用,并可促进心脏缺血/再灌注后心功能的恢复。CIHH这种心脏保护作用可维持两周左右时间,其机制可能与心肌抗氧化能力增强[3]、KATP通道的开放[4]、热休克蛋白表达增强[5]、线粒体通透转换孔开放抑制有关。此外,在自发性高血压、肾血管性高血压或代谢综合征大鼠模型,CIHH处理可明显降低升高的动脉血压。CIHH这种抗高血压作用可能与动脉血管的舒张增强,以及压力感受性反射的易化有关。但CIHH对心血管功能的保护作用机制远未完全阐明。
众所周知,发育的幼年动物与成年动物在形态与功能各方面均表现出明显差异,并且随着动物年龄的增加,动物的大部分生理、生化指标都会发生改变[6],例如动物功能、神经可塑性、对低氧的反应性等方面[7]。我们以往研究显示,相同程度的CIHH处理对不同年龄大鼠可引起完全不同的作用。在成年大鼠,应用4~6周、每日6 h、模拟5 km高原的CIHH处理可产生心脏保护效应,但对幼年大鼠则引起心脏损伤,而4~6周、每日5 h、模拟3 km高原的CIHH可使幼年大鼠出现心脏保护作用[8]。这说明发育大鼠与成年大鼠对CIHH处理的反应性是不同的。同样,在成年大鼠和成年肾血管性高血压大鼠,我们发现CIHH可增强胸主动脉环舒张,但不知CIHH对发育幼年大鼠胸主动脉舒张作用如何。本研究旨在探讨CIHH处理对发育大鼠胸主动脉舒张功能的影响及其机制。
1 材料 1.1 试剂苯肾上腺素(phenylephrine, PE)(货号:P0398),乙酰胆碱(acetylcholine, ACh)(货号:A2661),吲哚美辛(indomethacin, Indo)(货号:I7378),格列苯脲(glibenclamide, Gli)(货号:G0639),以上药物购自Sigma公司;四甲基哌啶氧化物(tetramethylpiperidinooxy, Tempo)(货号:ALX-430-081-G001),购自Alexis公司。药物保存在-20 ℃,使用药物时,用二甲基亚砜配制Gli,用蒸馏水配制其余药物,用K-H液稀释成浴槽所需浓度,所有药物及液体都现用现配。
1.2 溶液K-H液(mmol·L-1):NaCl 118.0、KCl 4.7、CaCl2 2.5、MgSO4 1.2、NaHCO3 25.0、KH2PO4 1.2、glucose 11.0,pH 7.4。
2 方法 2.1 动物分组和间歇性低氧处理本研究中对动物的处置均参照《实验动物护理和使用指南》进行,符合动物伦理学要求。实验动物的使用、操作流程均经河北医科大学实验动物使用伦理委员会审查和批准。
实验所用Sprague-Dawlay大鼠购自河北医科大学实验动物中心,♂,体质量(150~360) g,合格证号:708068,许可证号:SCXK(冀)2003-1-003。新生Sprague-Dawlay ♂大鼠随机分为8组:CIHH处理组(CIHH)、CIHH后1周组(CIHH-p1)、CIHH后2周组(CIHH-p2)、CIHH后3周组(CIHH-p3)、对照组(Con)、对照一周组(Con-1)、对照两周组(Con-2)与对照三周组(Con-3)。CIHH各组动物从出生前1~3 d开始,随母鼠一起置于低压氧舱内,接受每天5 h,模拟海拔3 km的低压低氧处理,共42 d。对照组动物除不接受低压低氧处理外,其余与CIHH处理组动物相同。每周定时记录动物体质量及一般状况。
2.2 离体动脉环制备动物麻醉使用戊巴比妥钠,腹腔注射法(50 mg·kg-1)。麻醉后,取出胸主动脉,置于K-H液中,剪成动脉环(长约3 mm)。将动脉环用细不锈钢丝(0.1 mm)穿起,浸泡在恒温浴槽内(成都仪器厂,浴槽内有5 mL K-H液,温度保持在37 ℃,持续通入95% O2和5% CO2混合气),将动脉环一端和张力换能器相连,利用BL-420E+生物机能实验系统(成都泰盟科技有限公司),记录标本的张力变化。
2.3 离体动脉环舒张描记 2.3.1 动脉环活性判定将动脉环的初始张力调节为1 g,每20 min更换一次浴槽内的K-H液。初次平衡40 min后,检测标本活性。先使用PE(10-6 mol·L-1),诱发动脉环收缩,然后给予ACh (10-5 mol·L-1),使血管环舒张,若舒张反应大于70%,则被判定为动脉环内皮完整。
2.3.2 常氧条件下的动脉环舒张内皮完整的动脉环,冲洗换液后再平衡40 min,通过累加给药观察血管环反应。先用PE(10-6 mol·L-1)使动脉环再次收缩,其收缩反应的最大值被记录为Emax,然后依次累加给予ACh(10-9~10-5 mol·L-1),观察血管环舒张效应,记录下各浓度ACh诱发的动脉环舒张值,和Emax相比较,计算出舒张反应的相对值(%Emax),并绘制量-效曲线图。
另外,对部分CIHH组大鼠内皮完整的动脉环,记录最大收缩值Emax后,直接冲洗换液后平衡40 min,分别给予Indo(10-5 mol·L-1)、Gli(10-5 mol·L-1)或者Tempo(10-6 mol·L-1),30 min后,给予PE(10-6 mol·L-1)使动脉环收缩后,同样以累加给药法给予ACh(10-9~10-5 mol·L-1),观察常氧条件下PE收缩后ACh诱发的血管舒张情况受前列环素、KATP通道和氧自由基的影响。
2.3.3 急性低氧条件下的动脉环舒张常规处理动脉环后,记录PE(10-6 mol·L-1)使动脉环收缩的最大值,冲洗换液平衡40 min,再次给予PE(10-6 mol·L-1)使动脉环收缩,以累加给药法给予ACh(10-7~10-5 mol·L-1)诱发舒张。在此次给予PE前20 min改为持续通入95% N2和5% CO2混合气导致K-H液中氧浓度降低,观察急性低氧对动脉环舒张的影响。
同样,对部分CIHH组大鼠内皮完整的动脉环,记录最大收缩值Emax后,平衡40 min,观察急性低氧条件下PE收缩后ACh诱发的血管舒张情况受前列环素、KATP通道和氧自由基的影响。
2.4 统计学处理所有数据均用
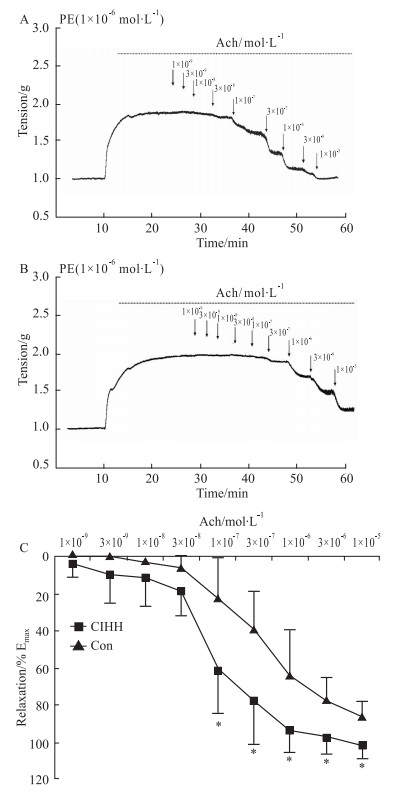
常氧条件下,由ACh(10-7 mol·L-1浓度以上)诱发的胸主动脉环内皮依赖性舒张反应在CIHH处理组大鼠较对照组大鼠明显增强,且呈浓度依赖性,随着ACh浓度的增加,增强作用更加明显。CIHH处理大鼠的量-效曲线较对照大鼠明显向左下移位(P < 0.05)。结果表明,CIHH处理对发育大鼠胸主动脉舒张具有明显增强效应。
|
Fig 1 Relaxation in isolated aorta ring induced by ACh
(10-9~10-5 mol·L-1) under normoxia ( |
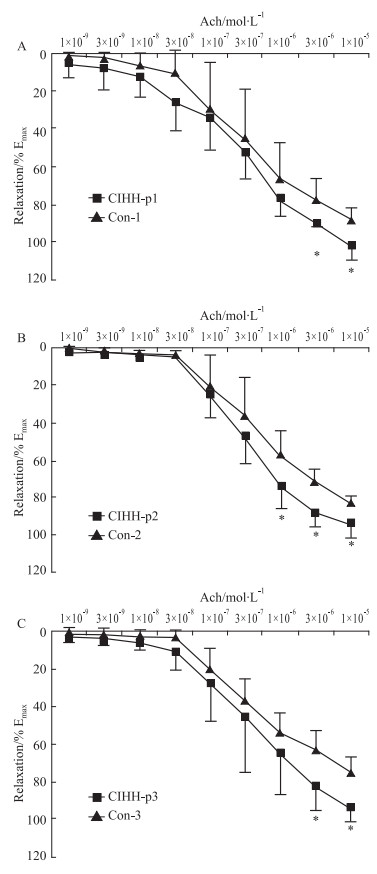
CIHH处理后各组大鼠胸主动脉环舒张均明显大于各自对照组大鼠,显示CIHH对动脉舒张的增强效应在CIHH处理后3周依然存在。结果表明,CIHH对发育大鼠动脉舒张增强效应至少可维持3周时间(P < 0.05)。
|
Fig 2 Duration of ACh-induced (10-9~10-5 mol·L-1) thoracic aorta relaxation post CIHH groups under normoxia ( |
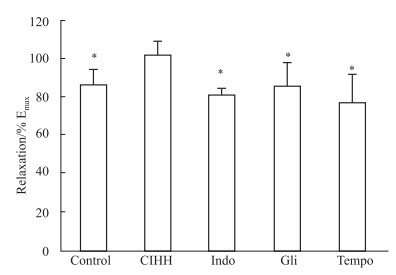
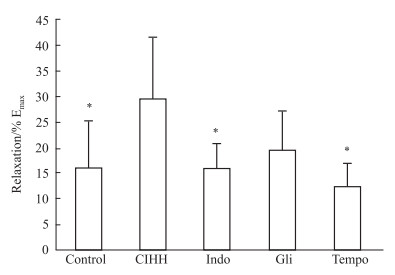
为探讨CIHH对发育大鼠胸主动脉舒张增强效应的产生机制,我们在累加给予ACh前分别给予Indo(10-5 mol·L-1)、Gli (10-5 mol·L-1)和Tempo(10-6 mol·L-1)30 min预处理。结果表明,CIHH对发育大鼠胸主动脉舒张增强效应可被Indo、Gli和Tempo完全阻断(P < 0.05)。
|
Fig 3 Effect of Indo, Gli and Tempo pre-treatment on ACh-induced (10-7~10-5 mol·L-1) thoracic aorta relaxation of CIHH and control groups under normoxia ( |
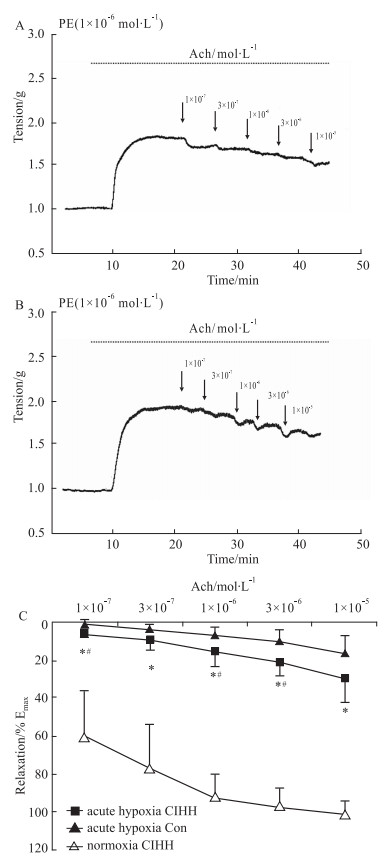
急性低氧条件下,由ACh诱发的大鼠胸主动脉环内皮依赖性舒张反应明显减弱,其量-效曲线明显向左下移位(P < 0.05)。CIHH处理组与Con组大鼠相比较,CIHH处理大鼠动脉环舒张减弱的程度明显小于Con组大鼠(P < 0.05),此作用可被Indo和Tempo所消除(P < 0.05)。结果表明,CIHH处理减轻急性低氧对动脉舒张功能的抑制,抑制作用与前列环素和氧自由基有关。
|
Fig 4 Relaxation in isolated aorta ring induced by ACh (10-7~ 10-5 mol·L-1) under acute hypoxia ( |
本研究应用离体动脉环张力描记方法,首次观察CIHH处理对发育大鼠离体主动脉环ACh诱发的内皮依赖性舒张的影响及其机制。结果显示,CIHH可明显增强发育大鼠胸主动脉ACh诱发的内皮依赖性舒张,此效应可维持至少3周时间,并可被Indo、Gli和Tempo所阻断。结果提示,CIHH对血管内皮依赖性舒张增强作用与前列环素、ATP敏感钾通道(KATP)和氧自由基有关。此外,研究结果亦显示,CIHH处理可对抗急性低氧对血管舒张的抑制,从而进一步证实CIHH对血管功能的保护作用。
血管内皮细胞覆盖于血管内表面,在维持血管的收缩舒张之间的平衡等方面具有十分重要的意义。ACh可通过血管内皮细胞产生NO,通过NO-cGMP途径,导致血管舒张[9]。通常以ACh诱发的血管舒张衡量NO所介导的血管内皮依赖性舒张功能。有研究报道,CIHH可通过增加NO发挥心血管保护作用[10]。本研究结果显示,CIHH对ACh诱发的主动脉舒张具有明显的增强效应,提示CIHH的增强血管舒张作用可能通过增加血管内皮NO产生所实现。
|
Fig 5 Effect of Indo, Gli and Tempo pre-treatment on ACh-induced (10-7~10-5 mol·L-1) thoracic aorta relaxation of CIHH and control groups under acute hypoxia ( |
前列环素(prostaglandin,PG)是一种舒血管物质,在环氧合酶等的作用下,会形成前列环素(PGI2)。PGI2可通过刺激腺苷酸环化酶(AC),使血小板中cAMP增加而抑制血管平滑肌收缩,导致血管舒张[11]。本研究结果显示,应用环氧合酶的非特异性抑制剂吲哚美辛预孵育动脉环,可以阻断CIHH处理对ACh诱发的主动脉内皮依赖性舒张增强效应,提示CIHH的增强主动脉舒张作用可能与血管内皮环氧合酶作用增强、或者PG合成与释放增多有关。
K+通道可调节血管平滑肌收缩,在调节血管张力中发挥重要作用[12]。本研究结果显示,应用KATP非特异性抑制剂格列苯脲预孵育动脉环可以阻断CIHH处理对ACh诱发的血管内皮依赖性舒张增强效应,提示CIHH对主动脉舒张的增强效应可能与促进KATP通道开放有关。我们以往的研究也已证实,CIHH增强成年大鼠血管舒张作用可通过激活阿片受体,从而促进KATP通道开放所引起[13]。
本研究结果显示,对大鼠主动脉的舒张增强效应可被氧自由基清除剂Tempo所取消,表明CIHH对主动脉舒张增强效应与体内自由基产生有关。有研究报道[14],自由基参与在缺血预处理等心脏保护作用的信号转导通路,通过自由基清除剂清除自由基后可消除心脏保护作用。联系本研究结果,可以推测CIHH作为一种应激刺激,可导致体内一定程度的氧自由基增加,通过自由基参与的信号转导通路,引起NO产生增加,从而增强血管的舒张反应,以及对抗急性低氧对血管舒张的抑制。
综上所述,CIHH处理具有增强发育大鼠胸主动脉舒张并对抗急性低氧对动脉舒张的抑制,CIHH对动脉舒张的保护作用可能与前列腺素生成增多、KATP通道开放及氧自由基作用有关。
| [1] |
Zhang Y, Zhou Z N. Beneficial effects of intermittent hypobaric hypoxia on the body[J]. Chin J Appl Phys, 2012, 28(6): 504-9. |
| [2] |
Mallet R T, Manukhina E B, Ruelas S S, et al. Cardioprotection by intermittent hypoxia conditioning:evidence, mechanisms, and therapeutic potential[J]. Am J Physiol Heart Circ Physiol, 2018, 315(2). |
| [3] |
张翼, 钟宁, 朱海峰, 等. 间歇性低氧对大鼠心肌的抗心律失常与抗氧化效应[J]. 生理学报, 2000, 52(2): 89-92. Zhang Y, Zhong N, Zhu H F, et al. Antiarrhythmic and antioxidative intermittent hypoxia exposure on rat myocardium[J]. Acta Physiol Sin, 2000, 52(2): 89-92. doi:10.3321/j.issn:0371-0874.2000.02.001 |
| [4] |
Bu H M, Yang C Y, Ma H J, et al. K(ATP) channels and MPTP are involved in the cardioprotection of chronic intermittent hypobaric hypoxia in developing rat[J]. J Physiol Sci, 2015, 65(4): 367-76. doi:10.1007/s12576-015-0376-5 |
| [5] |
Zhong N, Zhang Y, Fang Q Z, et al. Intermittent hypoxia exposure-induced heat-shock protein 70 expression increases resistance of rat heart to ischemic injury[J]. Acta Pharmacol Sin, 2000, 21(5): 467-72. |
| [6] |
朗天琦, 邹世颖, 侯曼, 等. SD大鼠90d喂养试验生理生化指标正常参考值的研究[J]. 中国兽医杂志, 2016, 52(12): 99-101. Lang T Q, Zou S Y, Hou M, et al. Study on the normal reference interval of hematological and serum biochemical indexes in 90d feeding study on SD rats[J]. Chin J Veter Med, 2016, 52(12): 99-101. |
| [7] |
吴凡, 苗雨阳, 张蔷. 慢性间歇性低氧对老年大鼠血压和心肌线粒体氧化应激的影响[J]. 中华老年医学杂志, 2017, 36(5): 563-8. Wu F, Miao Y Y, Zhang Q. The effects of chronic intermittent hypoxia on blood pressure and mitochondrial oxidative stress in aged rats[J]. Chin J Geriatr, 2017, 36(5): 563-8. doi:10.3760/cma.j.issn.0254-9026.2017.05.022 |
| [8] |
Zhang H, Yang C Y, Wang Y P, et al. Effects of different modes of intermittent hypobaric hypoxia on ischemia/reperfusion injury in developing rat hearts[J]. Acta Physiol Sin, 2007, 59(5): 660-6. |
| [9] |
温进坤.一氧化氮与平滑肌细胞[M]//温进坤, 韩梅, 主编.血管平滑肌细胞.第1版.北京: 科学出版社, 2005: 243-75. Wen J K. Nitric oxide and smooth muscle cells[M]//Wen Jin-kun, Han Mei, Chief editor. Vascular smooth muscle cells. First edition. Beijing: Science Press, 2005: 243-75. |
| [10] |
阴文超, 潜金桥. 一氧化氮的心脏保护作用研究进展[J]. 国际麻醉学与复苏杂志, 2019, 40(2): 185-9. Yin W C, Qian J Q. Research progress in cardioprotective effects of nitric oxide[J]. Int J Anesth Resus, 2019, 40(2): 185-9. doi:10.3760/cma.j.issn.1673-4378.2019.02.018 |
| [11] |
戴媛媛, 陈雪茁, 崔亚娇, 等. 前列腺素的血管活性及其与心血管疾病的关系[J]. 药学研究, 2017, 36(1): 40-7. Dai Y Y, Chen X Z, Cui Y J, et al. The relationship between vascular activities of prostaglandins and cardiovascular diseases[J]. J Pharm Res, 2017, 36(1): 40-7. |
| [12] |
Neckar J, Szarszoi O, Koten L, et al. Effects of mitochondrial K(ATP) modulators on cardioprotection induced by chronic high altitude hypoxia in rats[J]. Cardiovasc Res, 2002, 55(3): 567-75. doi:10.1016/S0008-6363(02)00456-X |
| [13] |
袁芳, 李宏伟, 宋士军, 等. 阿片受体介导慢性间歇性低压低氧对大鼠主动脉乙酰胆碱诱导舒张的增强反应[J]. 生理学报, 2013, 65(3): 269-75. Yuan F, Li H W, Song S J, et al. Effect of chronic intermittent hypobaric hypoxia on vasorelaxation mediated by opioid receptors in rat aorta[J]. Acta Physiol Sin, 2013, 65(3): 269-75. |
| [14] |
张玉洁, 胡晶晶, 李荣巧, 等. PKC、Rho激酶在卡托普利舒张大鼠离体胸主动脉环中的作用[J]. 中国药理学通报, 2018, 34(10): 1397-402. Zhang Y J, HU J J, Li R Q, et al. Role of PKC and Rho kinase in isolated rat thoracic aortic rings with captopril[J]. Chin Pharmacol Bull, 2018, 34(10): 1397-402. doi:10.3969/j.issn.1001-1978.2018.10.014 |

