


2. 广西医科大学药学院, 广西 南宁 530021;
3. 广西医科大学生命科学研究院, 广西 南宁 530021
 ,
TIAN Wei2,
KANG Jian-kang3,
ZHAO Yu-hua1,
ZHAI Li-na3,
LIANG Dan-dan2,
LI Jun-ying2,
HOU Hua-xin2,
LI Dan-rong1
,
TIAN Wei2,
KANG Jian-kang3,
ZHAO Yu-hua1,
ZHAI Li-na3,
LIANG Dan-dan2,
LI Jun-ying2,
HOU Hua-xin2,
LI Dan-rong1

2. College of Pharmacy, Guangxi Medical University, Nanning 530021, China;
3. Institute of Life Sciences, Guangxi Medical University, Nanning 530021, China
卵巢癌是一类常见的妇科恶性肿瘤,发病率占女性所有恶性肿瘤的2.5%,其死亡人数占女性癌症死亡人数的5%,死亡率一直居女性生殖道恶性肿瘤的首位[1]。癌细胞的远处转移是导致卵巢癌高死亡率的主要原因。目前仍缺乏靶向卵巢癌细胞转移、侵袭的药物,解决这一难题迫在眉睫。大黄酸(Rhein)是一种有多种生物活性的蒽醌化合物,可用于抗菌、抗肿瘤,其抗肿瘤如鼻咽癌、肝细胞癌、肺癌和卵巢癌等作用已被大量研究证实[2]。课题组前期通过研究发现Rhein调控Rac1/LIMK1/Cofilin信号通路影响卵巢癌细胞的运动能力,表明Rhein可能通过Ras相关的C3肉毒素底物1(Rac1)这个靶点来调控一系列的信号通路来抑制卵巢癌的浸润转移[3]。Rac1来自Rho家族,具有GTPase活性,在卵巢癌的发生、侵袭和转移等过程中发挥着重要的作用。基于Rac1这个潜在的靶点蛋白,课题组利用分子对接,将Rhein的母核C3位进行结构修饰,合成了一系列含酰胺结构的新型Rhein衍生物,其中,1,8-二苄氧基-9,10-蒽醌-N-(2-羟乙基)-3-甲酰胺(简称衍生物4a)在抑制肿瘤活性方面表现出与众不同的细胞形态学变化,能使细胞产生大量空泡。故本研究以不同浓度的衍生物4a干预卵巢癌细胞SKOV3,初步探讨其对细胞的增殖、侵袭及迁移的影响及可能的机制。
1 材料 1.1 细胞本实验所用SKOV3细胞株购于中国医学科学院肿瘤研究所,由广西医科大学生命科学研究院传代保存。细胞培养条件参照细胞培养说明书。实验细胞均为对数生长期细胞。
1.2 主要材料与试剂1,8-二苄氧基-9,10-蒽醌-N-(2-羟乙基)-3-甲酰胺(分子量为507.53,由本课题组合成,结构经核磁共振鉴定,纯度>98%(HPLC)]5.08 mg加入到1 mL的DMSO中配置成10 mmol·L-1的母液,过滤分装,-20 ℃保存备用。Rhein(aladdin公司,货号R111265);CCK-8试剂盒(广州博莱斯生物科技有限公司,货号C10201),波形蛋白(Vimentin,货号5741S)、β-连环蛋白(β-cantenin,货号8480S)、Rac1(货号2465)、基质金属蛋白酶2(MMP2,货号40994S)、基质金属蛋白酶9(MMP9,货号13667S)、β-actin(货号3700S)、E-钙粘蛋白(E-caderin,货号3195P)抗体(CST公司);羊抗兔荧光二抗(CST公司,货号5151P),兔抗鼠荧光二抗(LI-COR公司,货号LI031);Transwell小室(Corning公司,货号3422);Matrigel(Corning公司,货号356234)。
1.3 仪器EVOS FL Auto型全自动细胞成像系统(美国);全波长酶标仪Microplate reader(美国);Odessey双色红外成像系统(美国)
2 方法 2.1 分子对接评价衍生物4a、Rhein与靶蛋白Rac1的结合能力分子对接是一种利用计算机通过配体和受体结合来辅助药物设计的重要技术。本研究选取衍生物4a、Rhein为配体,Rac1为受体以MOE.2008对接软件进行分子对接。结合能数值越低,化合物与蛋白受体结合能力越强。通过结合能数值、氢键的作用力以及氨基酸残基的结合数目评价受试物与Rac1的结合活性。
2.2 CCK-8法检测细胞存活率以5 000个每孔的SKOV3细胞接种于96孔板,培养24 h。加药组是含不同浓度的Rhein及衍生物4a的培养基,空白组是相同体积的完全培养基。设置溶剂对照孔(0.1% DMSO)。培养48 h后,各孔加入20 μL的CCK-8溶液,再次孵育1 h,并测量孔板450 nm波长的吸光度(OD)值。细胞活力/%=[(加药组OD值-溶剂对照孔OD值)/空白组OD值]×100%。根据所得数值计算半数抑制浓度(IC50)。
2.3 HE染色观察细胞的形态将2.5×104个/mL的细胞悬液接种到放有已高压灭菌盖玻片的6孔板中,每孔溶液体积为2 mL,贴壁24 h后,除空白组外,分别加入2 μmol·L-1、4 μmol·L-1、8 μmol·L-1的衍生物4a处理细胞,继续培养24 h。固定,依次加入苏木精、伊红染料,分别染色5 min、1 min,吹干,封片。光镜下观察细胞质和细胞核的颜色及形态,并拍照。
2.4 划痕实验检测细胞的迁移能力将细胞接种于6孔板上,贴壁生长24 h,使用10 μL的无菌移液器枪头垂直细胞进行划痕。加入无血清的含不同药物浓度(0.5、1、2、4、8 μmol·L-1)培养基。在0、24、48 h分别取样,显微镜下拍摄划痕愈合情况,并计算细胞的愈合率。计算公式如下:愈合距离A=a0-aN,愈合距离B=a0,N为24 h和48 h。愈合率/%=(愈合距离A/愈合距离B)×100%。
2.5 Transwell实验检测细胞的侵袭能力将稀释后的Matrigel基质胶加到Transwell小室的上室中,取不含血清的相同浓度(8 μmol·L-1)的Rhein和衍生物4a的细胞悬液接种于上室,含10%胎牛血清的培养基加入下室,不加药物的孔作为空白组。选取不同时间点,分别于培养24 h和48 h后取出小室,弃上室中的悬液,固定,结晶紫染色10 min,晾干,镜下拍照,并以每个小室取上、下、左、右、中5个不同视野统计穿过基质胶的细胞数目。
2.6 Western blot检测相关蛋白表达情况衍生物4a作用于细胞后,提取细胞总蛋白,取30 μg蛋白样品上样,电泳后,转膜,封闭,一抗(Rac1、MMP-2、MMP-9、Vimentin、β-cantenin、E-canderin、β-actin稀释比例为1 :1 000)4 ℃过夜。二抗(兔抗稀释比例1 :10 000,鼠抗稀释比例1 :5 000)室温1 h。使用Odyssey红外扫膜仪扫描蛋白条带,通过ImageJ软件测定各组样品灰度值。
2.7 统计学方法实验所得数据采用统计学软件SPSS 20.0进行分析处理。计量资料以
Rhein与衍生物4a的分子结构式如下图所示:

|
| Fig 1 Molecular structure of Rhein and derivative 4a A:Rhein; B:Rhein derivative 4a containing amide bond. |
分子对接结果如Fig 2所示,Rhein和衍生物4a均能有效嵌入Rac1蛋白的活性腔结合口袋内,与Rhein相比,进入活性腔的衍生物4a能与Rac1蛋白周围较多的氨基酸如Ile21,Ile33,Ala159,Pro29,Phe28,Ala13,Pro34发生疏水作用,且与周围氨基酸形成的氢键数目(4条)也多于Rhein形成的氢键数目(2条)。Rhein和衍生物4a与Rac1对接能量分别为-11.82 kcal·mol-1、-29.10 kcal·mol-1。同时Western blot结果发现,不同浓度的衍生物4a对Rac1蛋白具有一定的抑制作用(Fig 3)。可见改构后的衍生物4a与Rac1蛋白结合能力较强,可抑制Rac1蛋白的表达。

|
| Fig 2 Molecular docking results of Rhein and derivative 4a with Rac1 A:Rhein; B:Derivative 4a |

|
Fig 3 Regulatory effects of derivative 4a on Rac1 protein ( |
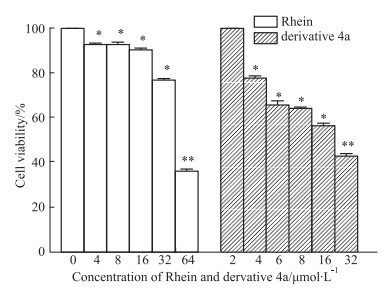
CCK-8结果表明,随着衍生物4a和Rhein浓度的增加,SKOV3细胞的增殖能力逐渐减弱,与空白组相比,其抑制作用具有剂量-效应关系。其中Rhein和衍生物4a作用48 h后的IC50分别为(51.47±1.81) μmol·L-1、(25.27±3.99) μmol·L-1。改构后的衍生物4a对细胞的IC50值明显低于先导化合物Rhein。
|
Fig 4 Effects of different concentrations of derivative 4a and Rhein on growth activity of SKOV3 cells ( |
在光学显微镜下可以观察到,随着衍生物4a浓度的增加,细胞中出现大量空泡,且空泡数量由少变多,空泡体积由小变大,空泡主要分布于细胞核周边。特别是从4 μmol·L-1开始,细胞形态由正常的多边形变为长梭形,细胞胞质减少,但核膜仍保持完整。个别细胞的细胞核染色加深,部分细胞出现核边集,如Fig 5所示。

|
Fig 5 Morphological effects of different concentrations of derivative 4a on SKOV3 cells(×400,  |
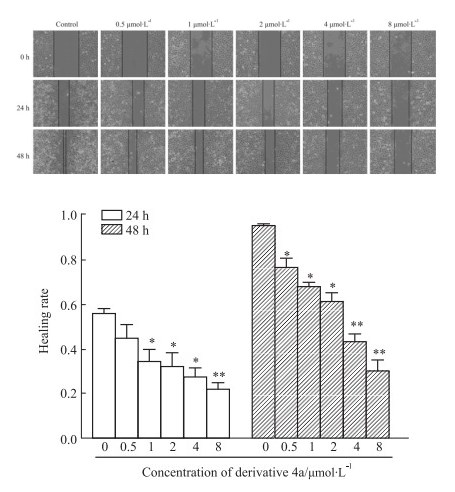
Fig 6划痕实验结果显示,与空白组相比,衍生物4a处理组明显抑制细胞的划痕愈合率,差异有统计学意义(P < 0.05)。随着衍生物4a作用时间的延长,划痕愈合率明显减少,衍生物4a抑制SKOV3细胞的迁移能力且呈现剂量和时间依赖性。
|
Fig 6 Inhibitory effect of derivative 4a on SKOV3 cell migration(×100)( |
随着时间的增加,SKOV3细胞穿过transwell小室基底膜的数目逐渐增多。与Rhein组相比,衍生物4a处理后的SKOV3细胞穿过小室膜的数量明显减少,细胞侵袭能力明显降低(P < 0.05),说明衍生物4a比Rhein具有更强的抑制SKOV3细胞侵袭能力,见Fig 7。

|
Fig 7 Effects of Rhein and derivatives 4a on invasive ability of ovarian cancer SKOV3 cells(200×)( |
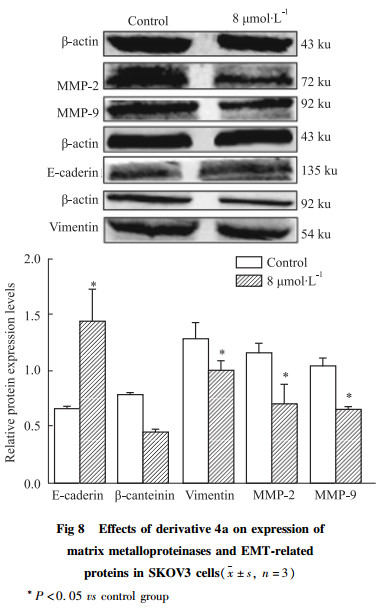
Western blot结果显示,与空白组相比,8 μmol·L-1衍生物4a处理SKOV3细胞24 h后,细胞EMT的标志蛋白E-caderin蛋白表达升高(P < 0.05),Vimentin、β-cantenin蛋白表达水平均明显降低(P < 0.05),同时基质金属蛋白酶MMP-2、MMP-9表达水平与空白组相比也明显降低(P < 0.05),结果见Fig 8。
|
Fig 8 Effects of derivative 4a on expression of matrix metalloproteinases and EMT-related proteins in SKOV3 cells( |
大量研究表明,Rac1参与细胞板状伪足的形成,这与肿瘤细胞迁移和侵袭能力的调控密切相关[4]。Rac1在多种肿瘤细胞的浸润转移的信号通路中均有报道,如软骨肉瘤细胞、胶质瘤细胞和卵巢癌细胞等,提示Rac1有可能作为抑制肿瘤细胞浸润转移的治疗靶点[5]。基于Rac1这个潜在的靶点蛋白,本课题组以Rhein为先导化合物,在C3位通过酰化反应合成了1,8-二苄氧基-9,10-蒽醌-N-(2-羟乙基)-3-甲酰胺,分子对接结果显示,新合成的衍生物4a与Rac1蛋白C末端的活性腔产生的相互作用的氨基酸残基较多、形成的氢键数量多且距离短。结合能低于先导化合物Rhein。不同浓度的衍生物4a可以抑制SKOV3细胞的Rac1蛋白表达水平。同时,细胞迁移和侵袭实验结果也发现衍生物4a抑制SKOV3细胞的迁移能力和侵袭能力,且抑制能力优于Rhein。推测衍生物4a调控浸润转移的能力与其结合Rac1蛋白的C末端形成效应结合的识别结构域[6],调控细胞膜黏附能力,影响细胞板状伪足的形成和改变GDP/GTP交换的构象,从而与抑制Rac1的表达水平有关。
细胞外基质(ECM)是由基底膜和细胞间质组成,肿瘤细胞通过其表面受体与ECM中的各种成分粘附后激活或分泌蛋白降解酶类来降解基质,从而形成局部溶解区,构成了肿瘤细胞转移运行通道[7]。基质金属蛋白酶(MMPs)对ECM的降解是肿瘤细胞侵袭和转移的关键环节之一[8]。其中,在MMPs家族中,MMP-2和MMP-9被认为在卵巢癌的浸润转移中起关键作用[9]。所以本研究探讨了衍生物4a对MMP-2、MMP-9表达的影响,结果表明,衍生物4a作用后,SKOV3细胞的MMP-2和MMP-9表达下调。有文献报道[10],MMPs又可以通过Rac1-Ros和β-cantenin等途径诱导上皮细胞-间充质转化(EMT)的发生。EMT是指在某些因素作用下,上皮细胞失去细胞极性,丢失细胞间的紧密连接和黏附连接,获得了浸润性和游走迁移能力,变成了间质细胞形态和特性的细胞,EMT与肿瘤的转移密切相关[11]。EMT过程的一个关键性特征就是E-cadherin向Ncadherin的转变,细胞的E-cadherin的表达下调,间质性标志蛋白Vimentin、β-cantenin的表达上调[12]。E-cadherin介导的黏附缺失被认为是肿瘤细胞侵袭和转移形成的先决条件[13-14]。Kuwabara等[15]研究显示,E-cadherin表达阴性的致瘤细胞系RERF-Lc-AI,在其过表达E-cadherin后,由原来的容易导致卵巢癌转移变为对卵巢癌转移不敏感,表明E-cadherin下调可能参与了卵巢癌的特异性转移。本研究采用能够抑制卵巢癌SKOV3细胞的浸润转移浓度衍生物4a处理细胞后,结果显示,衍生物4a作用细胞后E-caderin蛋白上调,Vimentin、β-cantenin蛋白下调,表明衍生物4a可抑制SKOV3细胞EMT的发生。综合上述结果,衍生物4a可能通过抑制MMP-2和MMP-9的表达进而抑制了卵巢癌SKOV3细胞EMT的发生。
然而,衍生物4a能诱导细胞产生大量空泡与其显著降低卵巢癌SKOV3细胞的侵袭转移能力存在何种关系,该过程涉及哪些信号传导通路,仍有待进一步研究。
| [1] |
Torre L A, Trabert B, De Santis C E, et al. Ovarian cancer statistics[J]. CA Cancer J Clin, 2018, 68(4): 284-96. doi:10.3322/caac.21456 |
| [2] |
Lin M L, Chung J G, Lu Y C, et al. Rhein inhibits invasion and migration of human nasopharyngeal carcinoma cells in vitro by down-regulation of matrix metalloproteinases-9 and vascular endothelial growth factor[J]. Oral Oncol, 2009, 45(6): 531-7. doi:10.1016/j.oraloncology.2008.07.012 |
| [3] |
唐敏, 李鸿, 周国梅, 等. Rhein调控Rac1/LIMK1/Cofilin通路与抑制卵巢癌细胞运动与侵袭[J]. 中国药理学通报, 2016, 32(3): 366-72. Tang M, Li H, Zhou G M, et al. Rhein inhibits the movement and invasion of human ovarian carcinoma cells through Rac1/LIMK1/cofilin signaling pathway[J]. Chin Pharmacol Bull, 2016, 32(3): 366-72. doi:10.3969/j.issn.1001-1978.2016.03.014 |
| [4] |
宋厚盼, 陈昫, 李茹柳. Rho鸟苷三磷酸酶调节细胞迁移中细胞骨架结构的研究进展[J]. 广州中医药大学学报, 2013, 30(2): 275-80. Song H P, Chen X, Li R L. Advances in Rho guanosine triphosphatase regulation of cytoskeletal structure in cell migration[J]. J Guangzhou Univ, 2013, 30(2): 275-80. |
| [5] |
Kawauchi T. The in vivo roles of STEF/Tiam1, Rac1 and JNK in cortical neuronal migration[J]. EMBO J, 2003, 22(16): 4190-201. doi:10.1093/emboj/cdg413 |
| [6] |
Modha R, Campbell L J, Nietlispach D, et al. The Rac1 polybasic region is required for interaction with its Effector PRK1[J]. J Biol Chem, 2008, 283(3): 1492-500. doi:10.1074/jbc.M706760200 |
| [7] |
Yukinaga H, Shionyu C, Hirata E, et al. Fluctuation of Rac1 activity is associated with the phenotypic and transcriptional heterogeneity of glioma cells[J]. J Cell Sci, 2014, 127(8): 1805-15. doi:10.1242/jcs.139733 |
| [8] |
Oh J, Takahashi R, Kondo S, et al. The membrane-anchored MMP inhibitor RECK is a key regulator of extracellular matrix integrity and angiogenesis[J]. Cell, 2001, 107(6): 789-800. doi:10.1016/S0092-8674(01)00597-9 |
| [9] |
柯星, 吴梦, 陈献. 肿瘤相关M2型巨噬细胞在卵巢癌组织中的分布及意义[J]. 免疫学杂志, 2016, 32(7): 589-95. Ke X, Wu M, Chen X. Distribution and clinical significance of M2-type macrophages in ovarian cancer tissues[J]. Immunol J, 2016, 32(7): 589-95. |
| [10] |
程先硕, 杨之斌, 殷正丰. 基质金属蛋白酶与肿瘤上皮间质转化的研究进展[J]. 中国肿瘤生物治疗杂志, 2011, 18(4): 437-40. Chen X S, Yang Z B, Yin Z F. Matrix metalloproteinases and epithelial-mesenchymal transition in tumor:An advance[J]. Chin J Cancer Biot, 2011, 18(4): 437-40. doi:10.3872/j.issn.1007-385X.2011.04.019 |
| [11] |
Kalluri R, Weinberg R A. The basics of epithelial-mesenchymal transition[J]. J Clin Invest, 2009, 119(6): 1420-8. doi:10.1172/JCI39104 |
| [12] |
Vergara D, Merlot B, Lucot J P, et al. Epithelial-mesenchymal transition in ovarian cancer[J]. Cancer Lett, 2010, 291(1): 59-66. doi:10.1016/j.canlet.2009.09.017 |
| [13] |
Gamallo C, Palacios J, Suarez A, et al. Correlation of E-cad expression with differentiation grade and histological type in breast carcinomas[J]. Am J Pathol, 1993, 142(4): 987-93. |
| [14] |
Kim M J, Jang S J, Yu E. Loss of E-cadherin and cytoplasmic-nuclear expression of β-catenin are the most useful immunoprofiles in the diagnosis of solid-pseudopapillary neoplasm of the pancreas[J]. Hum Pathol, 2008, 39(2): 251-8. doi:10.1016/j.humpath.2007.06.014 |
| [15] |
Kuwabara Y, Yamada T, Yamazaki K, et al. Establishment of an ovarian metastasis model and possible involvement of E-cadherin down-regulation in the metastasis[J]. Cancer Sci, 2008, 99(10): 1933-9. |