

2. 重庆医科大学附属第一医院神经内科, 重庆 400016
2. Dept of Neurology, the First Affiliated Hospital of Chongqing Medical University, Chongqing 400016, China
急性脑缺血疾病因其极高的致残率和死亡率,且多数幸存者通常伴有学习和记忆缺陷、认知功能障碍等后遗症,为患者及其家属带来巨大压力[1]。因此,改善脑缺血后遗症,尤其是认知功能障碍是此类疾病治疗的重点和难点。有研究发现,大脑在缺血损伤后会进行自身修复,神经发生则在自身修复中发挥着尤为关键的作用,也已成为目前研究的热点之一。
神经发生主要是神经干细胞(neural stem cell,NSC)在一定条件下增殖、分化、迁移、整合,并恢复神经功能的过程[2]。最初认为神经发生仅在哺乳动物的胚胎期,而成年脑组织神经元是不再进行增生和分化的终极细胞[3]。然而,近年来研究发现,成年哺乳动物脑内的两个区域也同样存在内源性神经发生:侧脑室的室管膜下(subventricularzone,SVZ)和海马齿状回(dentategyrus,DG)的颗粒细胞下层(subgranularzone,SGZ)[4]。但由于脑缺血后内源性神经发生的细胞数量较少,且存活率较低,缺血后的组织重构和功能恢复远远不足,因此,神经学一直致力于寻找有效的治疗方法和药物靶点,刺激内源性神经发生,更好地恢复患者的大脑功能。
经颅直流电刺激(transcranial direct current stimulation,tDCS)是一种运用恒直弱电流(一般小于2 mA)调节神经细胞活动的物理治疗方式[5],它通过微弱的直流电作用于大脑皮质,改变神经元膜电位的电荷分布,产生去极化或超极化现象,从而起到改变大脑皮质的兴奋性,调控大脑功能的作用[6]。目前,临床上tDCS多用于辅助康复治疗,如脑卒中患者运动功能的恢复;动物实验研究中tDCS多用于改善阿尔兹海默症模型鼠的学习记忆功能障碍。对tDCS是否能够影响小鼠急性脑缺血后海马区内源性神经发生研究较少。
N-甲基-D-天冬氨酸(N-methyl-D-aspartic acid,NMDA)受体参与调控中枢神经系统的生长发育,在学习和记忆功能的发育中尤为重要[7]。NMDA受体的亚基NR2a和NR2b在海马和大脑皮层中高度表达,参与神经干细胞发育过程,如细胞迁移、促进神经元轴突和树突的生成、激活突触重建,影响神经发生恢复脑功能。那么,tDCS能否通过促进脑缺血小鼠海马内源性海马神经发生,改善学习记忆功能,该作用是否与其增强NMDA受体功能有关?因此,本研究拟采用双侧颈总动脉夹闭法(bilateral common carotid artery occlusion,BCCAO)建立小鼠急性脑缺血模型,探索tDCS对急性脑缺血后海马神经发生的促进作用及其可能机制。
1 材料与方法 1.1 材料 1.1.1 试剂5-溴脱氧尿嘧啶核苷(5-bromo-2-deoxyuridine,BrdU,批号:HMBF8725V,纯度99%);大鼠抗BrdU单克隆抗体、兔抗DCX单克隆抗体、兔抗NeuN单克隆抗体均购自英国Abcam公司;Dy Light488标记山羊抗兔IgG、Dy Light549标记山羊抗大鼠IgG购自美国abbkine公司;兔抗β-actin、NR2b多克隆抗体购自北京博奥森公司;兔抗NR2a单克隆抗体购自上海傲图公司;其余试剂均为国产分析纯。
1.1.2 仪器Morris水迷宫(深圳瑞沃德公司);光学显微镜(Nikon,日本);激光共聚焦显微镜(ZEISS,德国);定量PCR仪(BIO-RAD,美国);Denley Dragon Wellscan MK3酶标仪(Thermo,美国);凝胶成像系统(Bio-Rad,美国)。
1.2 方法 1.2.1 实验动物与分组清洁级雄性成年健康C57BL/6小鼠,体质量(24±2)g,由重庆医科大学实验动物中心提供,许可证号:SCXK(渝)2018-0003。120只小鼠随机分为假手术组(Sham)、模型组(Model),tDCS低、高剂量组(tDCS75和150 μA,即tDCSL和tDCSH组),每组30只。其中Morris水迷宫每组随机选择6只,HE染色、免疫荧光染色、qRT-PCR、Western blot每组各4只。
1.2.2 动物模型的制备[8]小鼠记录体质量后3.5%水合氯醛腹腔注射麻醉,颈部皮肤用酒精仔细消毒后沿着正中剪开,暴露气管,用玻璃分针从气管两侧钝性分离双侧颈总动脉,注意避免伤及迷走神经,动脉夹闭20 min后恢复血供,缝合伤口,Sham组仅分离双侧颈部总动脉不进行夹闭。
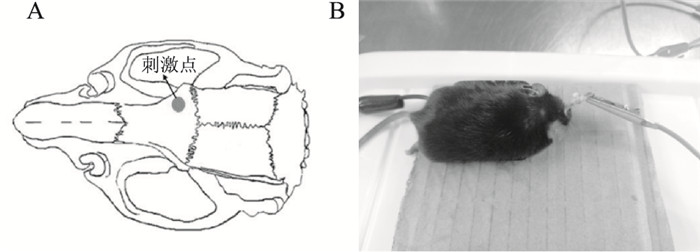
1.2.3 实验动物的给药如Fig 1所示,对小鼠进行电极的安装并给予恢复期,用牙科水泥将阳极电极,即填充了棉花和铜线的内径为2 mm的塑料管(接触面积为3.14 mm2),固定在右侧额叶区(前卤+2 mm,矢状缝+1.5 mm),阴极参考电极(接触面积为5 cm2)通过粘性电极片固定于小鼠胸腹部,每次刺激开始前将电极用生理盐水润湿以降低电刺激阻抗。造模24 h后给予相应强度的tDCS,每天30 min,重复5 d后, 间隔2 d,再次给予tDCS,每天30 min,重复5 d,总计10 d[9]。Sham组与Model组给予假刺激,即只连通电路不给予电流刺激。免疫荧光组小鼠在造模d 9~13各组给予腹腔注射BrdU(50 mg·kg-1),每天1次,持续5 d。
|
| Fig 1 Schematic diagram of mouse tDCS installation A:Location of stimulation electrode (anode) in mouse brain; B:Electrode configurations in mice. The anodal electrode was installed onto the skull above the right frontal cortex, while the cathodal electrode was placed onto the ventralthorax. |
造模后d 28,每组6只小鼠进行Morris水迷宫实验,在前5 d的定位航行实验中,每天进行4次试验,在每次试验期间,四组小鼠分别从四个象限面向池壁放入水中,给予60 s寻找水下隐藏的平台并记录找到的时间,60 s内未找到的小鼠记为60 s并进行引导;d 6的探索实验中,移去平台,记录60s小鼠穿越虚拟平台的次数。通过顶置相机和行为跟踪软件记录小鼠的移动。
1.2.5 HE染色造模后d 7,每组4只小鼠心脏灌注后进行取脑,脑组织用多聚甲醛固定,乙醇梯度脱水,石蜡包埋后再(前囟3.3~4.5 mm)连续切片,片厚5 μm,用于HE染色[2]。显微镜下观察海马CA1区神经元细胞的形态结构并拍照。用Image-ProPlus 6.0图像分析软件计算正常神经元数目。
1.2.6 BrdU免疫荧光造模后d 14,每组4只小鼠心脏灌注后取脑,脑组织用多聚甲醛固定,蔗糖溶液梯度脱水后,再用冰冻切片机进行连续冰冻切片,片厚10 μm。切片甲酰胺修复、盐酸变性、硼酸中和、Triton-x破膜、山羊血清封闭后加BrdU(1 :200)一抗过夜,暗室内加DyLight 594标记羊抗大鼠荧光二抗(1 :200)、DAPI染色后甘油封片。激光共聚焦显微镜观察海马DG区BrdU阳性细胞表达并拍照。用Image-ProPlus 6.0图像分析软件进行分析。
1.2.7 DCX免疫荧光造模后d 14,每组4只小鼠,按照前述BrdU免疫荧光的方法取材后获得冰冻切片。切片冷丙酮固定、柠檬酸修复、Triton-x破膜、山羊血清封闭后加DCX(1 :200)一抗过夜。暗室内加DyLight 488标记羊抗兔荧光二抗(1 :200)、DAPI染色后甘油封片。激光共聚焦显微镜观察海马DG区DCX蛋白阳性表达并拍照。用Image-ProPlus 6.0图像分析软件进行分析。
1.2.8 BrdU/NeuN免疫荧光造模后d 28,每组4只小鼠,按照前述BrdU免疫荧光的方法取材后获得冰冻切片。切片甲酰胺修复、盐酸变性、硼酸中和、Triton-x破膜、山羊血清封闭后加BrdU/NeuN(1 :200)一抗过夜。暗室内加DyLight 594标记羊抗大鼠和DyLight 488标记羊抗兔荧光二抗(1 :200)、DAPI染色后甘油封片。激光共聚焦显微镜观察海马DG区BrdU/NeuN阳性细胞表达并拍照。用Image-ProPlus 6.0图像分析软件进行分析。
1.2.9 逆转录定量PCR(qRT-PCR)检测海马NR2a、NR2b的mRNA表达造模d 14,每组4只小鼠麻醉后断头取脑,冰上迅速分离双侧海马组织,保存于液氮中,按照说明书提取海马RNA,逆转录为cDNA后,以β-actin为内参,在实时荧光定量PCR仪上扩增进行反应,引物序列如表 1所示。记录循环阈值(Ct值)作为统计参数,mRNA的表达水平用2-ΔΔCt法进行计算。
| Gene name | Forward primer | Reversed primer |
| β-actin | CCACCATGTACCCAGGCATT | AGGGTGTAAAACGCAGCTCA |
| NR2a | CTACGCCAGGATTCTCTAAACCAG | CAGAAATGTCAGAATGGGCTACCT |
| NR2b | AAGAAGAATCGGAACAAACTGCG | CCTTGTCTTTCAGGCTCACGCT |
造模后d 14,每组4只小鼠麻醉后断头取脑,冰上迅速分离双侧海马组织,保存于液氮中。提取蛋白后BCA法测定总蛋白浓度,SDS-聚丙烯酰胺凝胶:电泳、转印等步骤后[2],加一抗β-actin(1 :2 000)、NR2a(1 :1 000)、NR2b(1 :1 000),4 ℃过夜;洗膜,加二抗(1 :2 000),室温孵育2 h,洗膜后加ECL化学发光试剂显影,用Image Lab 4.1进行图像分析。
1.2.11 统计学方法实验数据均以x±s表示,采用SPSS 19.0分析数据,水迷宫实验中平台潜伏期采用重复测量的双因素方差分析(Tow-way ANOVA),其余采用单因素方差分析(One-way AVONA)。两组间比较用t检验。使用GraphPad Prism 7.0软件作图。
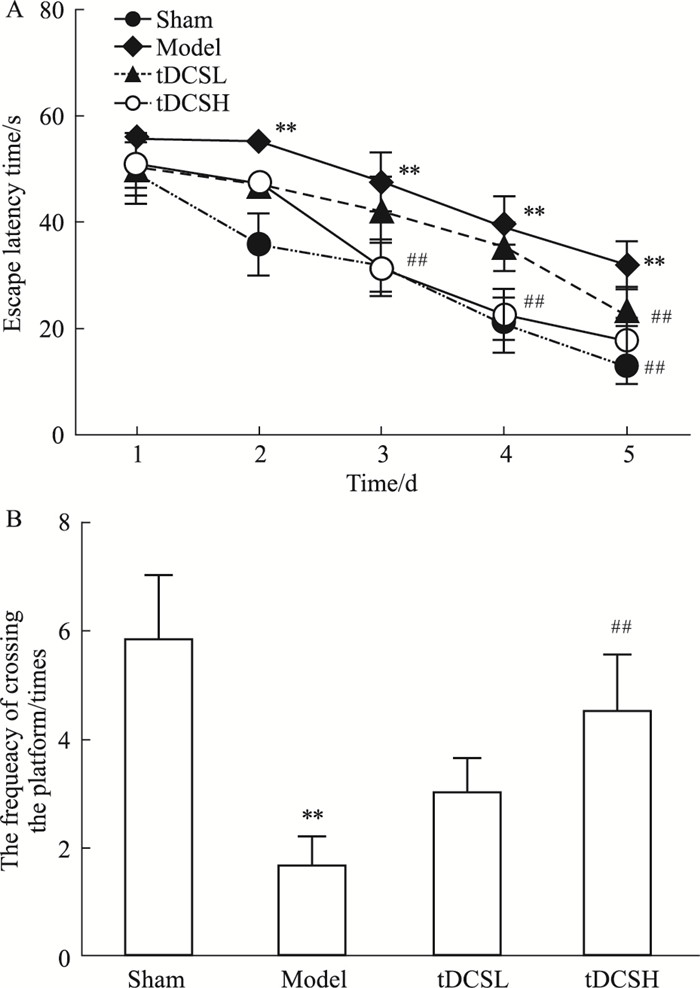
2 结果 2.1 tDCS对脑缺血小鼠空间学习记忆能力的影响如Fig 2所示,在定位航行实验中,随着训练天数的增加,各组小鼠的平台潜伏期均逐渐缩短。与Sham组相比,Model组小鼠从d 2起寻台潜伏期显著延长(P < 0.01);与Model组相比,tDCS高刺激治疗组小鼠寻台潜伏期显著缩短(P < 0.01)。在空间探索实验中,与Sham组相比,Model组小鼠跨越平台次数显著减少(P < 0.01);与Model组相比,tDCS低刺激组在统计学上无显著性差异;tDCS高刺激组显著增加小鼠穿越平台次数(P < 0.01)。
|
| Fig 2 Effect of tDCS on learning and memory functions after cerebral ischemia in mice(x±s, n=6) A:Escape latency time; B:The frequency of crossing the platform. **P < 0.01 vs sham; ##P < 0.01 vs model |
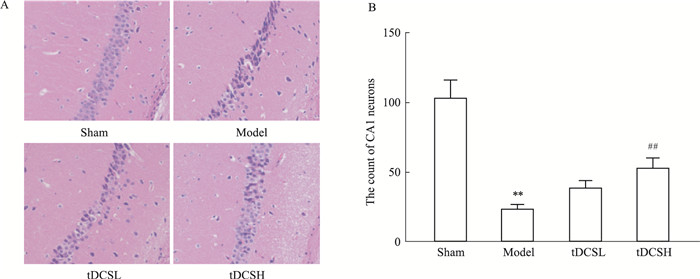
如Fig 3的HE染色所示,Sham组小鼠海马CA1区神经元细胞排列紧密,饱满,呈圆形,胞内结构清晰,染色呈蓝色;而Model组神经元细胞排列紊乱,破碎,不规则,正常神经元细胞数目相比Sham组显著减少(P < 0.01)。tDCS治疗后神经元形态得到改善,与Model组相比,tDCS低刺激组差异无显著性;tDCS高刺激组正常神经元数目明显增加(P < 0.01)。
|
| Fig 3 Effect of tDCS on pathological changes in hippocampus CA1 region of cerebral ischemia mice (x±s, n=4) A:Pathological changes in hippocampal CA1 region (×400);B:The count of CA1 neurons in hippocampus.**P < 0.01 vs sham; ##P < 0.01 vs model |
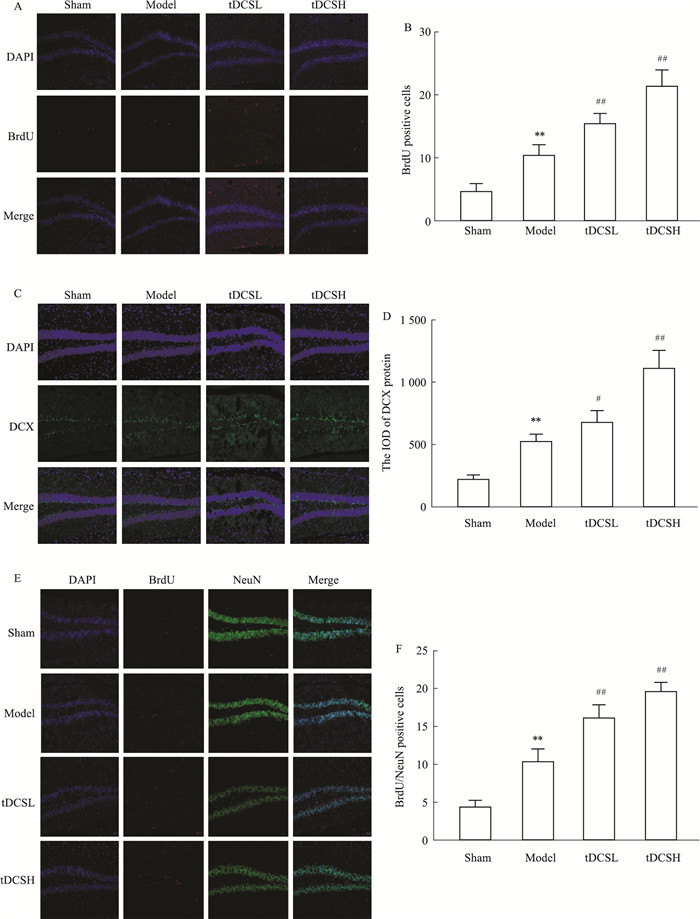
如Fig 4A、B所示,与Sham组相比,Model组小鼠海马齿状回BrdU阳性细胞表达明显增加(P < 0.01);给予tDCS治疗后,两个刺激组阳性细胞数均在Model组基础上明显增加(P < 0.01)。如Fig 4C、D所示,与Sham组相比,Model组小鼠海马齿状回DCX蛋白阳性表达明显增加(P < 0.01);与Model组相比,给予tDCS低刺激后,阳性表达在Model组基础上进一步增加(P < 0.05);给予tDCS高刺激后,阳性表达明显增加(P < 0.01)。如Fig 4E、F所示,与Sham组相比,Model组小鼠海马齿状回BrdU/NeuN阳性细胞表达明显增加(P < 0.01);给予tDCS治疗后,两个刺激组阳性细胞数均在Model组基础上明显增加(P < 0.01)。
|
| Fig 4 Effect of tDCS on hippocampal neurogenesis in cerebral ischemiamice (x±s, n=4) A:BrdU positive cells in the hippocampal dentate gyrus(100×); B: The count of BrdU positive cells; C:DCX positive cells in the hippocampal dentate gyrus(100×); D: The count of DCX positive cells; E:BrdU/NeuN positive cells in the hippocampal dentate gyrus(100×); F: The count of BrdU/NeuN positive cells. **P < 0.01 vs sham; #P < 0.05, ##P < 0.01 vs model |
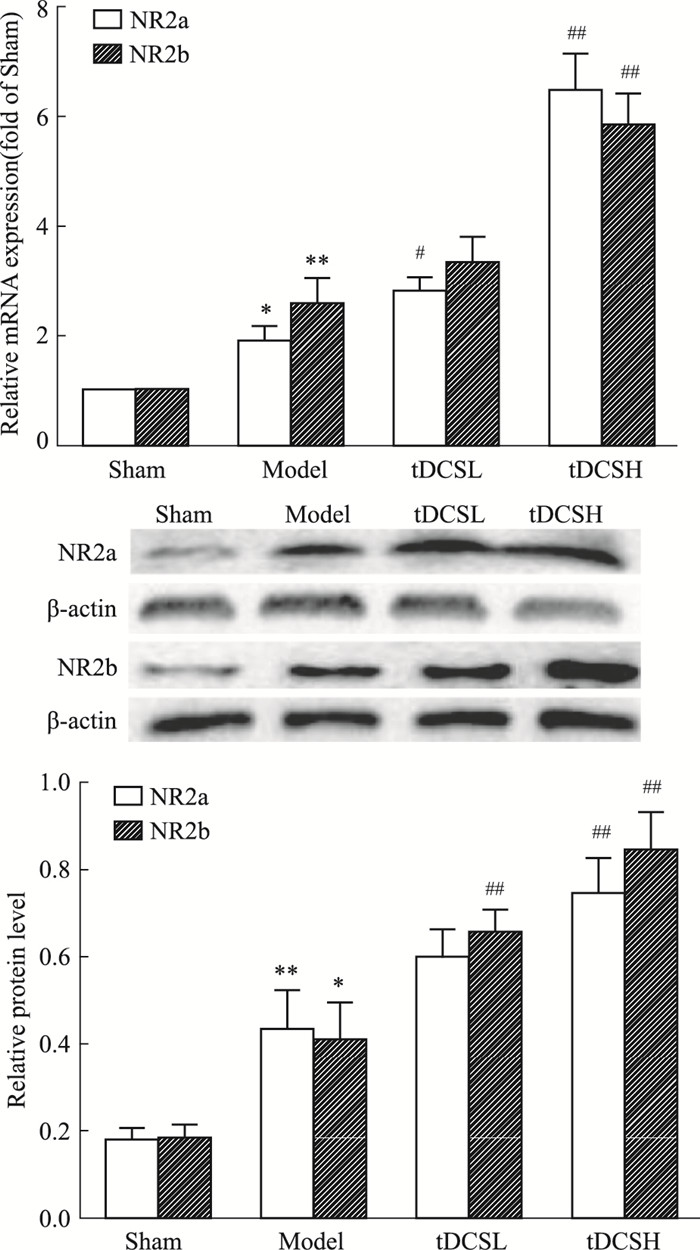
如Fig 5所示,与Sham组相比,Model组小鼠NR2a的mRNA表达(P < 0.05)和蛋白表达(P < 0.01)均明显增加;在给予tDCS低刺激后,NR2a的mRNA表达在Model组基础上进一步增加(P < 0.05),而蛋白表达差异无显著性(P>0.05);在给予tDCS高刺激后,NR2a的mRNA表达和蛋白表达相比于Model组均明显增加(P < 0.01)。与Sham组相比,Model组小鼠NR2b的mRNA表达和蛋白表达均明显增加(P < 0.05);给予tDCS治疗后,高刺激组NR2b的mRNA和蛋白表达均在Model组基础上明显增加(P < 0.01)。
|
| Fig 5 Effect of tDCS on mRNA and protein expression of NR2a and NR2b in hippocampus of cerebral ischemia mice (x±s, n=4) *P < 0.05, **P < 0.01 vs sham; #P < 0.05, ##P < 0.01 vs model |
脑缺血性疾病是严重危害人类健康的常见病和多发病[11]。随着医学的飞速发展,急性脑缺血的治疗逐渐取得巨大成果,但缺血性认知功能障碍,尤其是学习记忆功能障碍的治疗问题仍需攻克。目前认为,脑缺血导致认知功能障碍,主要原因在于海马CA1区神经元凋亡,而这种功能障碍恢复不良可能与缺乏足够的新生神经元相关。神经发生是脑缺血后的自身修复,内源性神经干细胞被激活后发育成熟并替补受损神经元,促进神经功能恢复。因此,增加内源性神经元数目,促进神经发生可能是认知功能恢复的关键因素之一。本研究采用小鼠急性脑缺血模型,模拟急性脑缺血病的病理生理进程,研究脑缺血后内源性神经发生及tDCS的促进作用及可能机制。
随着物理因子治疗中枢神经系统疾病的安全有效性逐步提高,tDCS作为一种无创口、安全性高、适应症广泛,通过在靶部位施加微弱电流调节大脑功能的治疗方式,在近些年逐渐成为研究热点。tDCS在治疗帕金森等神经和精神疾病展示出了极好的发展前景,但其是否对急性脑缺血后内源性神经发生有促进作用及其机制还尚不清楚。应用不同强度的tDCS刺激缺血后小鼠,通过观察各项指标,以期证明tDCS可显著促进缺血后小鼠的内源性神经发生以及脑功能恢复。
研究证实脑缺血后内源性神经干细胞在9~13 d为增殖高峰,28 d后分化为成熟神经元[12]。BrdU作为一种核苷酸类似物,具有比核苷酸更好的亲和力,能够在细胞增殖时替代核苷酸插入DNA链中,因此,可以通过外源性注射BrdU观察神经干细胞增殖情况;DCX在脑生长发育中至关重要,在迁移和分化的神经元轴突上持续表达,常用来研究神经元前体细胞的迁移和分化[13];神经元特异性核蛋白NeuN特异性标记成熟神经元,BrdU/NeuN双标普遍用于标记新生的成熟的神经元。本研究中,脑缺血小鼠海马HE染色显示CA1区神经元细胞核不规则,呈固缩状态,排列紊乱,结构不完整,数目明显减少;Morris水迷宫寻台时间明显延长,穿越虚拟平台次数明显减少,这些结果提示脑缺血导致海马神经元凋亡,且学习记忆功能显著下降;同时,脑缺血小鼠的海马齿状回BrdU、DCX、BrdU/NeuN的阳性细胞表达均明显增加,提示NSC被激活增殖、分化、迁移并发育为成熟神经元,脑缺血后海马区出现神经发生,但结合Morris水迷宫结果提示虽然缺血后机体出现内源性神经发生以进行自我修复,但远不足以改善缺血后认知功能的恢复。给予150 μA刺激强度的tDCS治疗可明显增加正常神经元数量,缩短寻台时间,增加穿台次数,这些结果提示高刺激强度的tDCS治疗可明显改善CA1区神经元病理损害并提高学习、记忆等认知能力;同时,BrdU、DCX和BrdU/NeuN阳性细胞数在Model组基础上进一步显著增加,内源性神经发生明显增强,提示tDCS治疗可能通过进一步促进内源性神经发生,从而恢复缺血后脑功能重建。
成年海马神经发生受到网状多靶点调控,其中NMDA亚基NR2a和NR2b参与突触可塑性及记忆形成过程,在神经元发育过程中的树突状分支中起重要作用,从而发挥介导海马神经生长的作用。本研究结果显示,无论是模型组小鼠还是给予tDCS治疗后的脑缺血小鼠其增强内源性神经发生作用均与NR2a和NR2b表达上调相关,提示NR2a和NR2b表达上调参与了缺血后内源性神经发生过程,而tDCS可通过进一步提高其表达,促进缺血后内源性神经发生,改善学习记忆功能障碍。
综上所述,tDCS可促进急性脑缺血后小鼠内源性神经发生,从而改善学习记忆功能障碍,其机制可能与促进NR2a和NR2b表达上调有关。由于急性脑缺血参与因素的复杂性和tDCS作用的广泛性,tDCS对急性脑缺血后小鼠的保护作用的参与机制仍需要进行更深入的研究。
( 致谢: 本文实验在重庆医科大学药学院生物化学与分子药理学重点实验室完成,特此致谢!)
| [1] |
Toda T, Gage F H. Review:adult neurogenesis contributes to hippocampal plasticity[J]. Cell Tissue Res, 2018, 373(1): 693-709. |
| [2] |
陈莉莉, 杨雪梅, 谌贝贝, 等. 肝X受体激活对全脑缺血/再灌注小鼠海马神经干细胞增殖及认知功能的影响[J]. 中国药理学通报, 2018, 34(2): 185-90. Chen L L, Yang X M, Chen B B, et al. Effect of liver X receptor activation on hippocampal neural stem cell proliferation and cognitive function in global cerebral ischemia/reperfusion mice[J]. Chin Pharmacol Bull, 2018, 34(2): 185-90. doi:10.3969/j.issn.1001-1978.2018.02.009 |
| [3] |
Ming G L, Song H. Adult neurogenesis in the mammalian brain:significant answers and significant questions[J]. Neuron, 2011, 70(4): 687-702. doi:10.1016/j.neuron.2011.05.001 |
| [4] |
Smith L K, White C W, Villeda S A. The systemic environment:at the interfaceof aging and adult neurogenesis[J]. Cell Tissue Res, 2018, 371(1): 105-13. doi:10.1007/s00441-017-2715-8 |
| [5] |
Lefaucheur J P. Methods of therapeutic cortical stimulation[J]. Memory, 2013, 21(1): 79-96. doi:10.1080/09658211.2012.706615 |
| [6] |
Brunoni A R, Amadera J, Berbel B, et al. A systematic review on reporting and assessment of adverse effects associated with transcranial direct current stimulation[J]. Int J Neuropsychopharmacol, 2011, 14(8): 1133-45. doi:10.1017/S1461145710001690 |
| [7] |
Wegner F, Kraft R, Busse K, et al. Glutamate receptor properties of human mesencephalic neural progenitor cells:NMDA enhances dopaminergic neurogenesis in vitro[J]. J Neurochem, 2009, 111(1): 204-16. doi:10.1111/j.1471-4159.2009.06315.x |
| [8] |
Tulsulkar J, Shah Z A. Ginkgo biloba prevents transient global ischemia-induced delayed hippocampal neuronal death through antioxidant and anti-inflammatory mechanism[J]. Neurochem Int, 2013, 62(2): 189-97. doi:10.1016/j.neuint.2012.11.017 |
| [9] |
Anton P, Paloma S N, Lea J F, et al. Transcranial direct current stimulation modulates neurogenesis and microglia activation in the Mouse Brain[J]. Stem Cells Int, 2016, 20(16): 1-9. |
| [10] |
Tian L, Nie H, Zhang Y, et al. Recombinant human thioredoxin-1 promotes neurogenesis and facilitates cognitive recovery following cerebral ischemia in mice[J]. Neuropharmacology, 2014, 77(2): 453-64. |
| [11] |
何小苏, 邹红群, 李启艳, 等. 替格瑞洛对大鼠全脑缺血/再灌注损伤的神经保护作用[J]. 中国药理学通报, 2019, 35(3): 413-8. He X S, Zou H Q, Li Q Y, et al. Neuroprotective effect of ticagrelor against global cerebral ischemia/reperfusion injury in rats[J]. Chin Pharmacol Bull, 2019, 35(3): 413-8. doi:10.3969/j.issn.1001-1978.2019.03.023 |
| [12] |
Maekawa M, Namba T, Suzuki E, et al. NMDA receptor antagonist memantine promotes cell proliferation and production of mature granule neurons in the adult hippocampus[J]. Neurosci Res, 2009, 63(4): 259-66. doi:10.1016/j.neures.2008.12.006 |
| [13] |
Brown J P, Couillard-Després S, Cooper-Kuhn CM, et al. Transient expression of doublecortin during adult neurogenesis[J]. J Com Neurol, 2003, 467(1): 1-10. |

