

魏伟(1960-),男,博士,教授,博士生导师,研究方向:抗炎免疫药理学,通讯作者,E-mail:wwei@ahmu.edu.cn
 ,
ZHOU Zheng-wei,
TAO Juan,
TAI Yu,
WANG Dan-dan,
WANG Zhen,
GUO Pai-pai,
WANG Qing-tong
,
ZHOU Zheng-wei,
TAO Juan,
TAI Yu,
WANG Dan-dan,
WANG Zhen,
GUO Pai-pai,
WANG Qing-tong
 ,
WEI Wei
,
WEI Wei

干燥综合征(Sjögren’s syndrome,SS)是一种慢性炎症性自身免疫病,临床表现为口干、眼干等症状,其主要侵犯外分泌腺体(如唾液腺),同时使皮肤等其他器官受到一定程度的损害。腺体中可出现大量淋巴细胞浸润,并累及多系统病变(如神经系统组织受损;累及关节,引起关节肿痛等)[1-2]。动物模型是研究SS病理机制和药物治疗疗效观察的重要方法,采用何种简单高效的技术或敏感的评价指标对SS模型进行动态观察与评价至关重要,尤其是活体观察SS模型动物病程变化及唾液腺腺体炎症的产生和发展过程。唾液腺病理改变,虽然可以反映SS病变的发生,但是实验动物必须处死才能获取样本病理进行观察,导致实验无法连续进行,且不能对SS模型动物的病程进行实时动态观察,此外小动物的腺体组织较小,活检技术难度较大。CT检查辐射较大,长周期的实验过程,对实验操作者和实验动物均有一定损害。血液生化指标个体间差异较大,且不够敏感。因此,探索小动物(如小鼠)腺体病程变化的无创、动态和灵敏的检查方法是目前SS实验研究中面临的重要问题之一。近年来,随着小动物超声成像系统的发展,其在多种疾病模型中评价及应用价值逐渐得到认可。并且超声检查具有无创性、无辐射、实时动态监测等优点,逐渐成为SS的一项重要临床诊断技术,已逐步应用SS患者的诊断与疗效观察,但基础研究中对此技术的应用和超声观察指标的定量分析方法尚不成熟[3-4]。本实验以C57BL/6雌性小鼠建立SS模型,采用小动物超声成像实时观察SS小鼠颌下腺的大小和血流量改变,与传统指标进行相关性分析,为超声诊断在SS评价中的应用,以及分析方法的建立提供实验依据和参考。
1 材料与方法 1.1 材料 1.1.1 实验动物健康♀近交系C57BL/6小鼠,20只,SPF级,体质量20 g左右,周龄8周,购买于常州卡文斯实验动物有限公司(合格证号:SCXK(苏)2016-0010),饲养于安徽医科大学实验动物中心。本研究中的相关操作均根据动物实验相关指南进行,并经由安徽医科大学实验动物中心动物研究伦理委员会批准。
1.1.2 仪器与试剂毛果芸香碱(批号:LRAA3042)和不完全弗氏佐剂(批号:SLBX2135)均购自Sigma公司;卡介苗(Bacille CalmettE-Guerin, BCG)购于新华区群硕实验用品销售部(批号:20181209DG);异氟烷为瑞沃德生命科技有限公司产品(批号:217181101);TM-100型医用超声耦合剂购自天津市西苑寺制作所(批号:20180502);BCA蛋白定量试剂盒购于Thermo Fisher Scientific公司(批号:PF205489);VisualSonics Vevo 2100高分辨小动物超声成像系统为FUJIFILM公司产品;AS-01型小动物气体麻醉机为英国Norvap公司产品。
1.2 方法 1.2.1 干燥综合征模型的建立在无菌超净台上取C57BL/6小鼠颌下腺,冰上用预冷的PBS研磨20 min,3000 rmp离心15 min取上清,BCA法进行蛋白定量,调整蛋白浓度为5 g·L-1。再将80 ℃灭活1 h的BCG溶于液体石蜡中,研磨2~3 h,终浓度为4 g·L-1 BCG的完全弗氏佐剂。蛋白中加入等体积完全弗式佐剂冰上混合研磨,使颌下腺提取蛋白终浓度为2.5 g·L-1,除正常对照组外,d 0和7,各组小鼠背部酒精消毒后背部皮内多点注射抗原,每只小鼠共注射0.1 mL抗原。d 14,用不完全弗氏佐剂将颌下腺抗原浓度调整为2.5 g·L-1,注射抗原方法同前[5-6]。
1.2.2 全身情况及唾液量与饮水量观察每天观察全身情况,小鼠全身皮肤有无搔抓、破损现象,口唇情况等;d 0、21、28和35分别测量小鼠的唾液量与饮水量,采用小动物麻醉机对小鼠进行麻醉后,注射0.025 g·L-1毛果芸香碱溶液(1.2 mg·kg-1),5 min后开始收集唾液,共收集10 min唾液量(将事先称好的无菌小棉球塞入小鼠舌下,10 min后取出称重)[7];小鼠饮水量以3 d为单位进行检测,分别在d 0、21、28和35检测。
1.2.3 颌下腺指数和病理学检查d 35处死小鼠,取出颌下腺称重,计算颌下腺指数(腺体质量与小鼠体质量的比值)。另外取颌下腺用10%福尔马林固定,HE染色,光镜下观察,根据Cutler的方法进行病理组织学评估:0级:散在淋巴细胞浸润;1级:少量淋巴细胞浸润;2级:中度淋巴细胞浸润(无淋巴灶形成),轻度颌下腺血管及腺导管水肿;3级:每5个低倍镜下有1个淋巴细胞灶(浸润淋巴细胞>50个相当于1个淋巴灶),中度血管及腺管水肿、扩张;4级:每5个低倍镜下有2~3个淋巴细胞浸润灶,腺泡萎缩,重度血管及腺管水肿等损伤。1级相当于1分,2分以上为发病[8]。
1.2.4 小动物超声扫描检查SS小鼠造模前后d 0、21、28和35对小鼠颌下腺进行超声检查,采用异氟烷对小鼠进行吸入性麻醉,并对超声扫描部位进行脱毛处理。将小鼠采用仰卧位固定于检查板上,并涂抹一定量的耦合剂于小鼠颌下腺部位待超声扫描。采用MS550探头对小鼠颌下腺进行超声检查,并选择General imaging模式,在B-Mode模块下对小鼠颌下腺部位进行纵切扫查(Fig 1)。此模式下成像的小动物解剖结构,以黑/灰/白的色阶显示(黑色:表示无回声,通常为低密度组织,如坏死组织、血管和积液;灰色:表示低回声,通常为中密度组织,如脾、胆、肝等器官;白色:表示强回声,通常为高密度组织,如气泡和结石等),圈出腺体长轴纵切面积。采用Color Doppler-mode又称为彩超模式,观察小鼠颌下腺腺体内是否有血流信号及丰富程度。整个超声扫查过程,保持探头对准小鼠颌下腺部位且压力适中,并控制超声探头位置与腺体的间距,防止腺体受压变形,以免影响观察实验结果。采集图像,对Color Doppler检测结果进行半定量评分,0分,腺体内部偶见少量斑状血流信号(0~1个血流斑点);1分,腺体内部有少量血流信号(2~3个血流斑点);2分,腺体内有较多的血流信号(4~5个血流斑点);3分,腺体内部血流信号较丰富(6个及以上血流斑点);左右侧腺体评分不一致时,以高分侧评分为最终分数。

|
| Fig 1 Ultrasonic probe positioning: axial incident |
应用Graphpad prism 6.0软件统计,计量资料以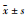
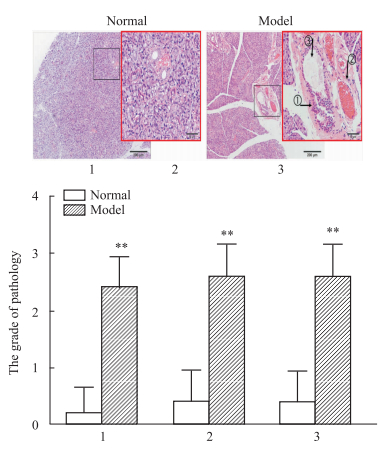
如Fig 2所示,采用自身抗原诱导小鼠SS模型,分别在d 0、21、28和35检测小鼠相对唾液量和相对饮水量,模型组小鼠的相对唾液量在d 28和35均较正常组显著降低(P < 0.01)(Fig 2A),而相对饮水量较正常组明显升高(P < 0.01)(Fig 2B),从d 0开始每周称量小鼠的体重,模型组较正常组在d 28和35体重有所减轻,但未见统计学差异(Fig 2C)。d 35处死小鼠,取颌下腺称重,计算颌下腺指数,模型组较正常组颌下腺指数升高,且具有统计学意义(P < 0.05)(Fig 2D)。d 35处死小鼠,取出颌下腺进行HE染色,正置显微镜下观察,如Fig 3所示,模型组小鼠与正常组小鼠相比,颌下腺内有大量淋巴细胞浸润,并形成淋巴细胞浸润灶,并伴有严重的血管及腺管水肿和扩张,病理分析具有统计学差异,提示模型建立成功。

|
Fig 2 Detection of routine indicators in mice at different periods
A: Relative salivary volume ( , n=10); B: Relative water intake ( , n=10); B: Relative water intake ( , n=10); C: Body weight ( , n=10); C: Body weight (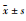 , n=10); D: Submandibular gland index ( , n=10); D: Submandibular gland index (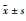 , n=10). *P < 0.05, **P < 0.01 vs normal , n=10). *P < 0.05, **P < 0.01 vs normal
|
|
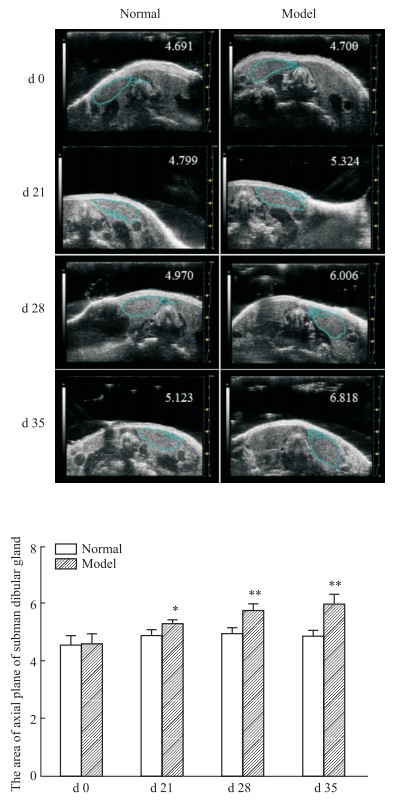
Fig 3 Pathology of submandibular gland (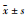 |
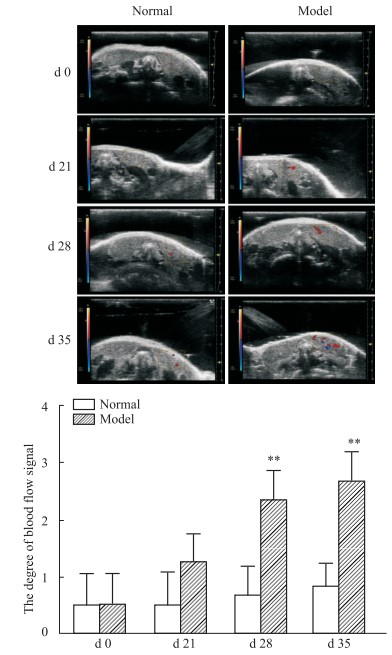
如Fig 4所示,在B-Mode模块下采用小动物超声成像系统检测不同时期小鼠颌下腺的影像,模型小鼠与正常小鼠相比,d 21即出现颌下腺超声轴面Area值明显增高,且具有统计学差异(P < 0.01),但模型小鼠和正常小鼠的颌下腺超声回声强度均未见明显改变;如Fig 5所示,在Color Doppler-mode模块下检测不同时期小鼠颌下腺的超声影像,模型小鼠与正常小鼠相比,d 28开始颌下腺超声血流信号明显增高,且具有统计学差异(P < 0.01)。
|
Fig 4 Ultrasonic axial area of submandibular gland in different periods (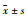 |
|
Fig 5 Ultrasonic blood flow signal grade of submandibular gland in different periods (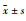 |
如Fig 6A 和B 所示,对常规SS诊断指标饮水量和唾液量与颌下腺超声轴面Area值进行相关性分析,饮水量与超声颌下腺轴面Area值具有显著正相关(r=0.74,P < 0.01),唾液量与超声颌下腺轴面Area值存在显著负相关(r=-0.77,P < 0.01)。如Fig 6 C和D所示,饮水量与颌下腺Color Doppler评分(血流信号等级)具有显著正相关(r=0.89,P < 0.01),唾液量与Color Doppler评分(血流信号等级)存在显著负相关(r=-0.86,P < 0.01)。病理检查显示的腺体血管扩张程度评分与超声Color Doppler评分(血流信号等级)具有显著正相关(r=0.78,P < 0.01),腺体导管水肿程度评分与超声轴面Area值具有显著正相关(r=-0.83,P < 0.01)(Fig 6 E和F)。

|
| Fig 6 Correlation analysis between conventional detection indexes and ultrasonic indexes (n=20) |
SS是一种累及外分泌腺体和淋巴细胞浸润的全身性异常炎症免疫反应为特征的疾病,其局部临床表现为口干、眼干和牙齿脱落[9]。动物模型是研究SS病理机制和疗效观察的重要前提,但目前评价动物模型方法和技术的缺乏很大程度限制了对该疾病的研究进展。因小动物超声检查具有无创伤、无辐射和实时动态检测等优点,所以逐渐成为多种疾病动物模型评价的标准。在临床上,干燥综合征患者早期的唾液腺腺体淋巴细胞浸润,腺体导管和血管扩张水肿,超声表现为腺体形态增大或正常,晚期腺体细胞被纤维组织取代,腺体实质回声不均匀,最终表现为腺体纤维化和腺体形态萎缩[10]。而本研究通过自身免疫诱导法建立干燥综合征模型,通过小动物超声和传统常规检测指标的观察发现,模型小鼠症状与临床干燥综合征早期病人症状相似,表现为模型小鼠血管和腺体导管扩张,淋巴细胞浸润,腺体肿胀。临床上超声诊断原发性SS的灵敏度、特异度、准确率、阳性预测值以及患者的依从性均较传统检测方法有所提高[11-12]。超声成像系统是否可以应用到SS动物模型的基础研究,准确性和灵敏度如何,以及检测结果应该怎样统计分析目前尚无相关报道。
传统的SS动物模型评价手段包括饮水量和唾液量的测量,病理切片的观察等,存在多种不足之处,如饮水量的检测存在较大的个体差异以及多种外界环境因素的干扰而无法准确测量。唾液量的检测需要先对小鼠进行麻醉,再腹腔注射一定剂量的毛果芸香碱,会引起胃肠道平滑肌收缩[13],可能会影响研究者后续的体内实验结果,过量的药物剂量还会引起小鼠全身性中毒、支气管痉挛和呕吐等不良反应,严重者还会导致小鼠死亡,样本减少。而病理切片的观察需要处死小鼠取颌下腺,不仅耗费模型小鼠的样本量,还无法针对模型小鼠腺体进行病程连续性观察或者给药前后的疗效自身比较。本研究发现,颌下腺超声在发病初期即可观察到腺体的轻度肿大,在出现明显的临床表现即唾液量降低和饮水量升高之前,诊断更为灵敏,与临床治疗和病理改变具有显著相关性。
综上所述,采用小动物超声成像可以为SS实验动物模型提供非侵入式且连续性的结构及功能的观察。超声干预的小鼠可以前后自身做对照,数据更加可信,且重复性高,能够减少对样本动物的创伤和死亡率。并且其高分辨率的影像可以给研究者提供更清晰的结果,例如裸鼠前列腺原位模型体积小, 超声检测能够在不损伤脏器前提下准确获得深部瘤体体积[14]。但是超声检查也有其局限性:操作的规范依赖于操作者的技术水平,且易受到操作者主观意识的影响,因此要对操作者进行深度培训,并且由检测者以外的实验人员进行客观的分析统计。总之,本研究使用小动物超声系统分析SS动物模型腺体病变,希望为评价SS动物模型及其他组织疾病模型提供一个新的视角和检测方法,从而更好推动疾病模型的基础研究。
| [1] |
Brito-Zerón P, Sisó-Almirall A, Bové A, et al. Primary Sjögren syndrome: an update on current pharmacotherapy options and future directions[J]. Expert Opin Pharmacother, 2013, 14(3): 279-89. doi:10.1517/14656566.2013.767333 |
| [2] |
Pilar B Z, Manuel R C. Advances in the understanding and treatment of systemic complications in Sjögren's syndrome[J]. Curr Opin Rheumatol, 2014, 26(5): 520-7. doi:10.1097/BOR.0000000000000096 |
| [3] |
李居献, 杨广辉, 孔凡沛, 等. 超声评分系统在干燥综合征中的诊断价值[J]. 临床医药文献杂志(电子版), 2018, 5(75): 152-3. Li J X, Yang G H, Kong F P, et al. Diagnostic value of ultrasound scoring system in Sjögren's syndrome[J]. J Clin Med Lit(Electronic Version), 2018, 5(75): 152-3. |
| [4] |
王涛.超声弹性成像在干燥综合征涎腺病变中的临床研究[D].芜湖: 皖南医学院, 2018. Wang T. Clinical study of ultrasonic elastography in salivary gland disease of Sjögren's syndrome[D]. Wuhu: Wannan Medical College, 2018. |
| [5] |
贾波.干燥综合征小鼠模型的建立及病机探讨[D].北京: 北京中医药大学, 2002. Jia B. The establishment of a mouse model for Sjögren's syndrome and the study of its pathogenic mechanisms[D]. Beijing: Beijing University of Chinese Medicine, 2002. |
| [6] |
魏伟, 吴华勋, 顾芳.一种干燥综合征小鼠模型的造模方法[P].中国专利, 201610560982.9. Wei W, Wu H X, Gu F. A method of modeling Sjögren's syndrome mouse model[P]. Chinese patent, 201610560982.9. |
| [7] |
Gu F, Xu S, Zhang P, et al. CP-25 alleviates experimental Sjögren's syndrome features in NOD/Ltj mice and modulates T lymphocyte subsets[J]. Basic Clin Pharmacol Toxicol, 2018, 123(4): 423-34. doi:10.1111/bcpt.13025 |
| [8] |
黄侠. Y-320对干燥综合征模型小鼠Th17细胞及唾液腺功能的影响[D].恩施: 湖北民族学院, 2018. Huang X. Effect of Y-320 on Th17 cells and salivary gland function in experimental Sjögren's syndrome (ESS) mice[D]. Enshi: Hubei University For Nationalities, 2018. |
| [9] |
张玲玲, 魏伟. 治疗自身免疫病药物研究进展[J]. 中国药理学通报, 2019, 35(2): 149-56. Zhang L L, Wei W. Advance in drug treatment of autoimmune diseases[J]. Chin Pharmacol Bull, 2019, 35(2): 149-56. doi:10.3969/j.issn.1001-1978.2019.02.001 |
| [10] |
Pereira D L, Vilela V S, Dos Santos T C, et al. Clinical and labo-ratorial profile and histological features on minor salivary glands from patients under investigation for Sjögren's syndrome[J]. Med Oral Patol Oral Cir Bucal, 2014, 19(3): 237-41. |
| [11] |
张雪珍, 林一钦, 何丽珍, 等. 涎腺超声检测在原发性干燥综合征诊断与随访中的应用价值[J]. 浙江医学, 2018, 40(11): 1261-4. Zhang X Z. Lin Y Q, Lin Y Q, He L Z. The value of parotid gland ultrasound detection in the diagnosis and follow-up of primary Sjögren's syndrome[J]. Zhejiang Med J, 2018, 40(11): 1261-4. doi:10.12056/j.issn.1006-2785.2018.40.11.2017-1246 |
| [12] |
姚远. 超声评分系统在干燥综合症中的诊断价值[J]. 世界最新医学信息文摘, 2018, 18(42): 176-7. Yao Y. Diagnostic value of ultrasound scoring system in Sjögren's syndrome[J]. World Latest Med Inf, 2018, 18(42): 176-7. |
| [13] |
李金菊, 慕邵峰, 曾淑君, 等. 内皮细胞乙酰胆碱靶标不同于M受体的药理学特征[J]. 中国药理学通报, 2003, 19(6): 660-4. Li J J, Mu S F, Zeng S J, et al. Pharmacological characteristics of the endothelial-target for acetylcholine different from muscarinic receptors[J]. Chin Pharmacol Bull, 2003, 19(6): 660-4. doi:10.3321/j.issn:1001-1978.2003.06.017 |
| [14] |
饶玉良, 孙祖越. 前列腺癌转移动物模型特性的比较学分析[J]. 中国药理学通报, 2018, 34(6): 760-4. Rao Y L, Sun Z Y. Advances in constructing metastatic animal models of prostate cancer[J]. Chin Pharmacol Bull, 2018, 34(6): 760-4. doi:10.3969/j.issn.1001-1978.2018.06.006 |