

2. 广西农产资源化学与生物技术重点实验室,广西 玉林537000
2. Guangxi Key Lab of Agricultural Resources Chemistry and Biotechnology, Yulin Guangxi 537000, China
中脑黑质多巴胺能神经元丢失为帕金森病(Parkinson’s disease,PD)主要病理特征。PD多巴胺能神经元死亡与胶质细胞活化、氧化应激、炎症损伤等因素关系密切。褪黑激素可通过抗氧化、抗细胞凋亡、清除自由基、抑制炎症因子表达及抗神经毒性,发挥神经保护作用[1-2]。研究发现,褪黑激素能够抑制6-羟基多巴所致PD大鼠模型黑质星形胶质细胞的增殖和活化,并使黑质纹状体部位酪氨酸羟化酶(tyrosine hydroxylase,TH)阳性多巴胺能神经元数量增多,发挥PD保护作用[3]。褪黑激素可改善PD动物模型的行为学功能,减少多巴胺能神经元死亡,延缓PD发展[4],但相关分子机制还不明确。Sirtuin 3(SIRT3)属于线粒体蛋白,具有调节氧化应激、能量代谢、保护线粒体功能等作用,在PD等神经疾病中发挥一定保护作用[5-6]。多项研究表明[7-8],褪黑激素可上调SIRT3发挥抗氧化、抑制炎症损伤。但SIRT3是否介导褪黑激素对PD多巴胺能神经元的保护作用,还不清楚。本研究探讨了褪黑激素保护PD多巴胺能神经元的作用机制是否与SIRT3功能相关,以进一步了解褪黑激素的神经保护作用分子机制,为PD治疗药物研制提供参考。
1 材料 1.1 实验动物C57BL/6小鼠,8~10周龄,♂,体质量约20 g,购自广西医科大学动物实验中心,动物生产许可证号为SCXK(桂)2014-0002。适用性饲养3 d后,开展相关试验。
1.2 试剂1-甲基, 4-苯基, 1, 2, 3, 6-四氢吡啶(1-methyl-4-phenyl-1, 2, 3, 6-tetrahydropyridine,MPTP)(M0896)、褪黑激素(M5250)购自美国Sigma公司;SIRT3(ab86671)、超氧化物歧化酶2(superoxide dismutase 2,SOD2)(ab13533)、诱导型一氧化氮合酶(inducible nitric oxide synthase,iNOS)(ab15323)抗体购自英国Abcam公司;TH(sc73152)、离子钙结合蛋白1(ionized calcium bindingadaptor molecule-1,Iba-1) (sc32725)抗体购自美国Santa Cruz公司;磷酸甘油醛脱氢酶(glyceraldehyde phosphate dehydrogenase,GAPDH)(AF0006)抗体和相关二抗购自碧云天生物技术公司;二喹啉甲酸(bicinchoninic acid,BCA)蛋白浓度检测试剂盒、预染蛋白Marker购自美国Thermo Fisher公司;氧化应激与炎症因子测定试剂盒均购自南京建成生物工程研究所;TRIzol购自美国Invitrogen公司;逆转录试剂盒、DNA聚合酶购自日本TaKaRa公司。
1.3 仪器ABI ViiA7荧光定量PCR仪(美国ABI公司);Hema9600基因扩增仪(珠海黑马医学仪器有限公司);荧光显微镜、激光共聚焦显微镜(日本Olympus公司);Multiskan FC酶标仪(美国Thermo Fisher公司);高速冷冻离心机(美国Eppendorf公司);蛋白电泳与转膜系统(美国Bio-Rad公司)。
2 方法 2.1 模型构建与动物分组48只小鼠随机分为对照组、模型组、治疗组,每组16只。模型组和治疗组小鼠每天给予30 mg·kg-1 MPTP腹腔注射1次,连续注射7 d,建立亚急性PD模型,对照组小鼠同时给予等量生理盐水;治疗组小鼠在MPTP腹腔注射的同时再给予褪黑激素(10 mg·kg-1)腹腔注射,连续给药14 d,对照组和模型组同时给予等量生理盐水。给药结束正常饲养3 d后,处死分离脑组织,组织切片或裂解,以待进一步分析检测。
2.2 免疫组化检测黑质区TH、Iba-1表达随机选取各组小鼠,快速断头取脑,分离中脑黑质组织,石蜡切片,厚度为20 μm,每连续5张切片取1张,分别行TH和Iba-1染色。切片用0.1 mol·L-1磷酸盐缓冲液(phosphate buffered solution,PBS)冲洗3次,每次5 min;再用3% H2O2灭活内源性过氧化氢酶,0.1 mol·L-1 PBS冲洗3次,每次5 min;5%牛血清蛋白封闭液室温封闭30 min;加入适量兔抗小鼠TH、Iba-1一抗(1 :100),4 ℃湿盒内孵育过夜;0.1 mol·L-1 PBS冲洗3次,每次5 min;加入山羊抗兔二抗,室温孵育20 min,0.1 mol·L-1 PBS冲洗3次,每次5 min;加入生物素标记室温孵育40 min;经PBS冲洗后二氨基联苯胺显色,梯度乙醇脱水、二甲苯透明、中性树胶封片、光镜下观察并摄片。应用Image-Pro Plus 6.0图形分析软件分析黑质区TH阳性细胞的相对吸光度值,并在显微镜下对黑质区Iba-1阳性细胞进行计数。
2.3 氧化应激及炎症因子水平检测随机选取各组小鼠,快速断头处死,分离中脑组织,组织剪碎,加适量组织裂解液,低温匀浆机中研磨完全裂解,4 ℃,10 000 r·min-1离心15 min,取上清,保存于-20 ℃冰箱中待测。用酶联免疫吸附测定(enzyme-linked immunosorbent assay,ELISA)法严格按说明书操作步骤检测肿瘤坏死因子α(tumour necrosis factor α,TNF-α)和白介素1β(interleukin 1β,IL-1β)含量,采用硫代巴比妥酸比色法检测丙二醛(malonaldehyde,MDA)含量,分别采用DCFH-DA荧光探针、黄嘌呤氧化酶法测定中脑组织活性氧(reactive oxygen species,ROS)、SOD水平。
2.4 实时定量聚合酶链式反应(polymerase chain reaction,PCR)分析SIRT3 mRNA水平按照试剂盒步骤提取RNA,去基因组,检测纯度无蛋白质污染,配制逆转录反应液,轻柔混匀后进行逆转录反应,条件如下:42 ℃ 60 min,72 ℃ 15 min,-20 ℃保存备用。SIRT3基因引物序列:上游引物5′-ATGCCTGAAGACAGCTCCAACAC-3′,下游引物5′-AGACATCCCTGGTCAGCCTTTCC-3′;GAPDH基因引物序列:上游引物5′-GGAGAAACCTGCCAAGTATGATGAC-3′,下游引物5′-GAGACAACCTGGTCCTCAGTGTA-3′。按照Premix TaqⅡ试剂盒反应体系加入试剂和引物,进行PCR反应。反应条件为:95 ℃预变性5 min:95 ℃变性10 s,60 ℃退火15 s,72 ℃延伸15 s,45个循环;72 ℃延伸10 min。通过细胞阈值循环数值和标准曲线,对样品初始cDNA进行相对量计算。
2.5 Western blot检测蛋白表达水平随机选取各组小鼠,快速断头取脑,分离中脑黑质组织,组织剪切,加入蛋白裂解液,低温匀浆机中研磨,充分裂解后,4 ℃,10 000 r·min-1离心15 min,取上清。采用BCA法测定各样品总蛋白浓度,调整蛋白浓度,沸水浴5 min使蛋白变性,蛋白上样量为每孔20 μg,十二烷基硫酸钠聚丙烯酰胺凝胶电泳,恒压转至聚偏二氟乙烯膜,5%脱脂奶粉室温封闭2 h后加入封闭液稀释的SIRT3、Iba-1、SOD2、iNOS抗体和内参GAPDH抗体,4 ℃孵育过夜,洗膜缓冲液(Tris buffered saline tween,TBST)洗膜,加入相应二抗室温孵育2 h,再用TBST洗膜,膜放于电化学发光液中反应2 min,保鲜膜封闭,暗室中用X胶片感光、显影、定影、扫描保存图片。采用Image-Pro Plus 6.0软件分析目标蛋白表达条带的灰度值,以GAPDH蛋白表达量作为内参。
2.6 统计学分析用SPSS 20.0统计软件进行分析,计量资料以
免疫组化结果显示,与对照组比较,模型组小鼠黑质区TH阳性细胞数目显著减少(P < 0.05),褪黑激素干预后,治疗组小鼠黑质区TH阳性细胞数目则明显多于模型组,差异比较具有统计学意义(P < 0.05),见Fig 1。

|
Fig 1 Effect of melatonin on number of TH-positive neurons in substantia nigra of PD mice (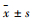 |
与对照组比较,模型组小鼠黑质区Iba-1阳性细胞数目明显增多(P < 0.05),褪黑激素干预后,治疗组小鼠黑质区Iba-1阳性细胞数目则明显少于模型组,两组间比较差异具有统计学意义(P < 0.05),见Fig 2。Western blot检测结果也表明,模型组小鼠黑质组织Iba-1表达水平明显高于对照组(P < 0.05),与模型组比较,治疗组Iba-1表达水平则显著降低(P < 0.05),见Fig 3。

|
Fig 2 Effect of melatonin on number of Iba-1-positive cells in substantia nigra of PD mice (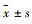 |

|
Fig 3 Effect of melatonin on Iba-1 protein expression in substantia nigra of PD mice (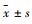 |
ELISA检测结果表明,模型组小鼠中脑组织氧化应激指标ROS和MDA、炎症因子TNF-α和IL-1β水平均高于对照组(P < 0.05),SOD活性低于对照组(P < 0.05)。褪黑激素干预后,治疗组小鼠中脑组织氧化应激及炎症均获得一定程度改善,ROS、MDA、TNF-α和IL-1β水平降低,SOD活性增强,组间比较差异均具有统计学意义(P < 0.05),见Tab 1。

| Group | ROS /ku·g-1 |
SOD /ku·g-1 |
MDA /μmol·g-1 |
TNF-α /ng·L-1 |
IL-1β /ng·L-1 |
| Control | 31.4±5.8 | 221.6±17.2 | 4.1±0.5 | 51.2±4.3 | 62.5±9.6 |
| Model | 96.2±9.7# | 135.8±20.1# | 7.3±0.8# | 78.7±6.6# | 98.3±6.4# |
| Melatonin | 64.1±8.3* | 178.5±24.3* | 5.4±0.6* | 61.3±5.4* | 74.9±8.1* |
| #P < 0.05 vs control; *P < 0.05 vs model. | |||||
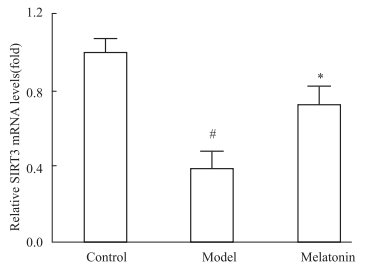
实时定量PCR结果显示,与对照组比较,模型组黑质组织SIRT3 mRNA水平显著降低(P < 0.05),褪黑激素干预后,治疗组黑质组织SIRT3 mRNA水平相比模型组表现出一定程度提升,差异具有统计学意义(P < 0.05),见Fig 4。
|
Fig 4 Effect of melatonin on level of SIRT3 mRNA expression in substantia nigra of PD mice (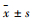 |
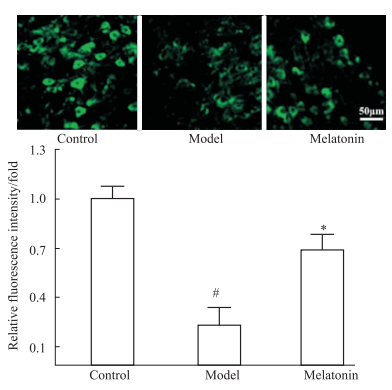
免疫荧光结果表明,与对照组比较,模型组黑质组织SIRT3染色荧光强度明显减弱(P < 0.05),与模型组比较,治疗组荧光则显著增强(P < 0.05),见Fig 5。Western blot结果显示,与对照组比较,模型组黑质组织SIRT3、SOD2蛋白表达量明显减小(P < 0.05),iNOS表达量显著增多(P < 0.05),褪黑激素干预后,治疗组黑质组织3种蛋白表达则呈现相反的变化趋势,与模型组比较均具有统计学意义(P < 0.05),见Fig 6。
|
Fig 5 Effects of melatonin on expression of SIRT3 in substantia nigra of PD mice by immunofluorescence ( |

|
Fig 6 Effects of melatonin on expression of SIRT3 and its downstream proteins in substantia nigra of PD mice by Western blot ( |
本研究发现,褪黑激素能够减少MPTP所致PD小鼠黑质多巴胺能神经元的丢失,并抑制小胶质细胞活化,与Naskar等[9]研究结果一致。此外,Bassani等[10]发现,在鱼藤酮大鼠PD模型上,褪黑激素保护TH阳性神经元及维持多巴胺水平,褪黑激素在6-羟基多巴大鼠PD模型形成4 d后仍可改善运动症状,同时还可减少TH阳性神经元的坏死并能保护纹状体内神经元的超微结构。
本研究还发现,褪黑激素可降低PD模型小鼠中脑组织ROS、MDA、TNF-α、IL-1β水平,增强SOD活性,从而抑制氧化应激及炎症损伤。毛崇丹等[11]研究显示,褪黑激素能提高小鼠蛛网膜下腔出血后神经细胞的存活率,增加脑组织谷胱甘肽水平,减少脑神经元凋亡,降低MDA水平,抑制IL-1β与IL-6分泌,发挥神经保护作用;褪黑激素可提高创伤性脑损伤小鼠脑组织抗氧化酶SOD等的含量,抵抗氧化应激伤害。Paul等[12]研究表明,褪黑激素可改善同型半胱氨酸所致PD大鼠的行为异常、多巴胺能神经元丢失及氧化应激,提高谷胱甘肽水平和抗氧化酶活性,以上文献报道为本研究结论提供支持。
研究报道,褪黑激素通过上调SIRT3表达、提高SOD2活性抵抗心肌缺血/再灌注损伤[7];还通过SIRT3-SOD2信号通路缓解胆汁酸诱导的肝细胞线粒体氧化应激[13]。褪黑激素还可通过SIRT3-SOD2-ROS途径促进自噬,进而减轻重金属镉诱发的肝脏毒性[14]。在缺血性卒中模型小鼠中,褪黑素通过激活SIRT1信号通路,减轻线粒体氧化应激损伤和细胞死亡[15]。本研究结果显示,褪黑激素可通过上调SIRT3、SOD2基因表达,下调iNOS蛋白表达,缓解MPTP所致多巴胺能神经元损伤,作用机制与相关报道结果一致。
综上所述,褪黑激素干预后,MPTP所致PD小鼠中脑黑质TH表达增多、Iba-1表达减少,ROS与炎症因子水平下降,SIRT3、SOD2基因表达上调,iNOS基因表达下调,结果表明,褪黑激素通过SIRT3-SOD2信号通路抵抗PD多巴胺能神经元损伤,作用机制与其抑制小胶质细胞激活,及减轻氧化应激与炎症损伤有关。
( 致谢: 本实验是在玉林师范学院生命科学实验中心和广西农产资源化学与生物技术重点实验室完成,感谢各位老师的指导与帮助,另外还要感谢南方医科大学珠江医院药学部实验室老师给予的帮助。)
| [1] |
Alghamdi B S. The neuroprotective role of melatonin in neurological disorders[J]. J Neurosci Res, 2018, 96(7): 1136-49. |
| [2] |
刘亭, 毕竟, 王盼, 等. MAPK/ERK信号通路参与褪黑素对阿尔茨海默病大鼠小脑的神经保护作用[J]. 中国药理学通报, 2019, 35(3): 402-7. Liu T, Bi J, Wang P, et al. Neuroprotective effect of melatonin in cerebellums in Alzheimer's disease animal models via MAPK /ERK signaling pathway[J]. Chin Pharmacol Bull, 2019, 35(3): 402-7. |
| [3] |
王维苹, 朱耀峰, 张金, 等. 褪黑素对帕金森病模型大鼠代谢机能和DA能神经元的保护作用[J]. 解剖学研究, 2017, 39(2): 81-4. Wang W P, Zhu Y F, Zhang J, et al. The protective effect of melatonin on dopaminergic neurons and on the metabolic function in rats with Parkinson's disease[J]. Anat Res, 2017, 39(2): 81-4. |
| [4] |
Carriere C H, Kang N H, Niles L P. Chronic low-dose melatonin treatment maintains nigrostriatal integrity in an intrastriatal rotenone model of Parkinson's disease[J]. Brain Res, 2016, 1633: 115-25. |
| [5] |
蒋德旗, 王勇, 李明星, 等. Sirtuin3在神经相关疾病发生中的作用研究现状[J]. 中国临床药理学杂志, 2019, 35(5): 493-6. Jiang D Q, Wang Y, Li M X, et al. Current situation of effects of Sirtuin3 in neurological diseases[J]. Chin J Clin Pharmacol, 2019, 35(5): 493-6. |
| [6] |
Zhang M, Deng Y N, Zhang J Y, et al. SIRT3 protects rotenone-induced injury in SH-SY5Y cells by promoting autophagy through the LKB1-AMPK-mTOR pathway[J]. Aging Dis, 2018, 9(2): 273-86. |
| [7] |
Feng J, Chen X, Liu R, et al. Melatonin protects against myocardial ischemia-reperfusion injury by elevating Sirtuin3 expression and manganese superoxide dismutase activity[J]. Free Radic Res, 2018, 52(8): 840-9. |
| [8] |
Han L, Wang H, Li L, et al. Melatonin protects against maternal obesity-associated oxidative stress and meiotic defects in oocytes via the SIRT3-SOD2-dependent pathway[J]. J Pineal Res, 2017, 63(3): e12431. |
| [9] |
Naskar A, Prabhakar V, Singh R, et al. Melatonin enhances L-DOPA therapeutic effects, helps to reduce its dose, and protects dopaminergic neurons in 1-methyl-4-phenyl-1, 2, 3, 6-tetrahydropyridine-induced parkinsonism in mice[J]. J Pineal Res, 2015, 58(3): 262-74. |
| [10] |
Bassani T B, Gradowski R W, Zaminelli T, et al. Neuroprotective and antidepressant-like effects of melatonin in a rotenone-induced Parkinson's disease model in rats[J]. Brain Res, 2014, 1593: 95-105. |
| [11] |
毛崇丹, 甄恩迪, 刘阳阳, 等. 褪黑激素抑制NLRP3炎性小体减轻小鼠蛛网膜下腔出血早期脑损伤[J]. 中华神经外科疾病研究杂志, 2017, 16(5): 417-21. Mao C D, Zhen E D, Liu Y Y, et al. Melatonin relieved early brain injury by NLRP3 pathway in the mouse model of subarachnoid hemorrhage[J]. Chin J Neurosurg Dis Res, 2017, 16(5): 417-21. |
| [12] |
Paul R, Phukan B C, Justin Thenmozhi A, et al. Melatonin protects against behavioral deficits, dopamine loss and oxidative stress in homocysteine model of Parkinson's disease[J]. Life Sci, 2018, 192: 238-45. |
| [13] |
Chen Y, Qing W, Sun M, et al. Melatonin protects hepatocytes against bile acid-induced mitochondrial oxidative stress via the AMPK-SIRT3-SOD2 pathway[J]. Free Radic Res, 2015, 49(10): 1275-84. |
| [14] |
Pi H, Xu S, Reiter R J, et al. SIRT3-SOD2-mROS-dependent autophagy in cadmium-induced hepatotoxicity and salvage by melatonin[J]. Autophagy, 2015, 11(7): 1037-51. |
| [15] |
刘阳阳, 梁国标, 甄恩迪, 等. 褪黑素通过沉默信息调节因子1减轻线粒体氧化应激对脑缺血/再灌注小鼠的作用[J]. 中国脑血管病杂志, 2017, 14(10): 519-24. Liu Y Y, Liang G B, Zhen E D, et al. Effect of melatonin on reducing mitochondrial oxidative stress in mice with ischemia/reperfusion via a silent information regulator 1[J]. Chin J Cerebrovasc Dis, 2017, 14(10): 519-24. |

