

糖尿病肾病(diabetic nephropathy,DN)是糖尿病常见且危险的并发症,以炎症、肾小球系膜基质扩张、弥漫性肾小球基底膜增厚、间质纤维化和肾小管萎缩为主要特征,DN已被认为是终末期肾病(end stage renal disease,ESRD)的主要原因,晚期糖基化终末产物(advanced glycation end products,AGEs)在DN的发生和发展过程中起着关键作用。随着近年来的深入研究,发现AGEs在DN炎性损伤中扮演重要角色[1],其中巨噬细胞是介导DN炎性肾损伤的关键炎性细胞。巨噬细胞广泛分布在机体的各个器官和组织中,被称为单核-巨噬细胞系统,主要参与免疫、炎性反应及内环境稳态的维持,AGEs可以刺激巨噬细胞释放炎性细胞因子白细胞介素-1β(interleukin-1β,IL-1β)和肿瘤坏死因子-α(tumor necrosis factor,TNF-α),TNF-α可诱导细胞凋亡并且对肾小球系膜细胞和肾小管细胞具有细胞毒性,导致直接肾损伤[2]。研究表明,巨噬细胞在肾脏中的积聚与DN血肌酐、蛋白尿和间质纤维化水平呈正相关,与肾功能呈负相关;巨噬细胞浸润也与糖尿病动物高血糖水平、肾小球免疫复合物沉积及进行性纤维化、趋化因子增加密切相关[3]。
梓醇(catalpol)是一种从生地黄中提取出来的环烯醚萜苷类化合物,研究表明,梓醇可以改善db/db糖尿病小鼠尿多且浑浊的状况,恢复其受损肾功能,减轻肾脏病理变化,减轻肾小球系膜细胞外基质沉积,其机制与AGEs/RAGE/Sphk1信号通路的抑制有关[4]。梓醇能够抑制AGEs诱导的单核细胞炎症因子分泌,通过抑制细胞内氧化应激水平、核转录因子(nuclear factor kappa-B,NF-κB)的转位,从而抑制AGEs介导的炎症[5]。有研究发现单核巨噬细胞和肾小球系膜细胞共培养,AGEs上调不规则趋化因子(fractalkine,Fkn)降低系膜细胞中基质金属蛋白酶(matrix metalloproteinases,MMPs)表达,导致细胞外基质的积聚且提高单核细胞的迁移从而加剧DN[6]。综上所述,本实验采用体外巨噬细胞与系膜细胞共培养模型,探究梓醇干预AGEs刺激巨噬细胞对肾系膜细胞损伤的作用,为减轻糖尿病肾病炎性损伤提供理论研究依据。
1 材料 1.1 试剂与材料小鼠肾系膜细胞(MMCs)从中国科学院上海细胞库购入;小鼠巨噬细胞(RAW264.7)由南京中医药大学药理实验室惠赠。梓醇(catalpol)标准品(HPLC≥98%),成都瑞芬思生物科技有限公司,批号:Z-005-180315;氨基胍(aminoguanidine)、MTT,Sigma公司,批号:079K1734V、MKBN7264V;DMEM/F-12 1 :1(1×)细胞培养基、胰酶、胎牛血清,美国Gibco公司;RIPA组织/细胞裂解液、DAPI染液、Triton X-100、山羊血清,Solarbio科技有限公司,批号:R0020、20190315、T8200、408J051;通用型组织固定液,武汉谷歌生物科技有限公司,批号:163618;FN、COL-Ⅳ、TGF-β抗体,英国Abcam公司;β-actin,Bioworld公司;Anti-rabbit IgG,美国CST公司;FITC-羊抗兔IgG,BOSTER生物工程有限公司,批号:BST13K28C05;小鼠白细胞介素-6(interleukin-6,IL-6)、白细胞介素-12(interleukin-12,IL-12)、TNF-α ELISA试剂盒,上海酶联生物科技有限公司,批号:201902。
1.2 仪器Synergy HT酶标仪,美国Bio-Tek公司;电泳仪,美国BIO-RAD公司;CO2细胞培养箱,日本SANYO公司;冷冻离心机,美国BECKMAN公司;化学发光成像仪,美国GE公司;Ti型倒置荧光显微镜,日本Nikon公司;Transwell 3450、3413共培养板,美国Corning公司。
2 方法 2.1 AGEs的制备称取适量的牛血清白蛋白(BSA)溶于PBS中,配制成浓度为50 g·L-1的溶液,再与0.5 mol·L-1的葡萄糖溶于0.2 mol·L-1 PBS(pH 7.4)中。待溶解后,37 ℃避光孵育4个月,使其形成AGEs-BSA(即AGEs)。在平行条件下配制不含葡萄糖的上述BSA溶液,制备0-BSA(无糖基化BSA)溶液作为对照。4个月后,使用孔径为分子量1万的透析袋,置于10 mmol·L-1PBS(pH 7.4)中, 4 ℃透析24 h,以除去未完全反应的葡萄糖。制备好的AGEs用0.22 μm滤器过滤除菌,-20 ℃保存备用,经BCA蛋白定量测浓度为22.6 g·L-1。
2.2 细胞培养小鼠系膜细胞(MMCs)和小鼠巨噬细胞(RAW264.7)培养于含1g·L-1胎牛血清和0.1g·L-1青霉素-链霉素DMEM/F12培养基中,取对数生长期细胞进行实验。
2.3 MTT法检测系膜细胞增殖取对数生长期的RAW264.7以1×108·L-1每孔1 mL接种于24孔板内,另取MMCs以5×107·L-1每孔0.5 mL接种于0.4 μm的Transwell小室,于细胞培养箱中培养24 h。当细胞贴壁时,24孔板和Transwell小室换无血清的DMEM/F12培养基饥饿培养24 h,依次分为空白对照组、模型组、氨基胍组(终浓度10.0 μmol·L-1)、梓醇组(终浓度0.1、1.0、10.0 μmol·L-1),每组设4个复孔,各组加药培养1 h后,下层加入终浓度100 mg·L-1的AGEs刺激RAW264.7,将Transwell小室移至24孔板上方共培养23 h。从孵箱中拿出共培养板舍去上层小室内培养液,MTT法测定吸光度值(490 nm),并计算细胞增殖率。
细胞增殖率/%=[(ODx-ODControl)/ODControl]×100%
2.4 免疫荧光法检测肾系膜细胞表达COL-Ⅳ荧光强度将细胞爬片置于Transwell小室,取对数生长期的RAW264.7以1×108·L-1每孔2 mL接种于6孔板内,另取MMCs以2×108·L-1每孔0.5 mL接种于0.4 μm小室爬片。分组与给药处理按“2.3”项,每组设置3个复孔。冰PBS小心冲洗爬片3次,固定液固定15 min,用PBS稀释的Triton X-100通透20 min,加入PBS配制山羊血清封闭1 h,每片加0.2 mL COL-Ⅳ一抗4 ℃过夜。d 2每片爬片加入PBS稀释的0.2 mL FITC-羊抗兔IgG孵育2 h,PBS洗3次,滴加DAPI染液,5 min后PBS洗4遍吸去爬片液体后上机检测,使用Image Pro Plus 6软件统计分析。
2.5 Western blot法检测肾系膜细胞相关蛋白表达取对数生长期RAW264.7以1×108·L-1每孔2 mL接种于6孔板内,另外取对数生长期MMCs以2×108·L-1每孔2 mL接种于0.4 μm的Transwell小室。分组与给药处理同“2.3”项,每组设置3个复孔。吸除小室内液体,用不含EDTA的胰酶将MMCs吹打混悬于小室中并离心收集,加入裂解液提蛋白,并测定蛋白浓度。蛋白样品按体积加上样缓冲液,95 ℃煮5 min后,进行聚丙烯酰氨凝胶电泳,转膜至PVDF膜上,加入0.5 g·L-1 BSA封闭液,室温2 h后加入一抗4 ℃过夜。d2 PBST洗3次,加入HRP二抗,室温2 h后ECL显色。利用Image J软件分析各组灰度值β-actin为内参计算FN、COL-Ⅳ、TGF-β蛋白表达量。
2.6 ELISA法检测巨噬细胞上清液中IL-6、IL-12、TNF-α的分泌取对数生长期的RAW264.7以1×108·L-1每孔1 mL接种于24孔板内,另取MMCs以5×107·L-1,每孔0.5 mL接种于0.4 μm的Transwell小室,分组与给药处理同“2.3”项,每组设置3个复孔。拿出共培养板,吸出下层巨噬细胞上清液,按说明书检测上清中IL-6、IL-12、TNF-α水平。
2.7 统计学分析实验结果使用SPSS22.0进行分析,数据以±s表示。组间比较方差齐性采用F检验。
3 结果 3.1 梓醇对AGEs刺激巨噬细胞介导系膜细胞增殖的影响与空白对照组相比,AGEs刺激巨噬细胞介导系膜细胞增殖率升高(P < 0.01),而梓醇(0.1、1.0、10.0 μmol·L-1)、氨基胍(10.0 μmol·L-1)可不同程度的抑制由AGEs刺激巨噬细胞介导系膜引起的细胞增殖(P < 0.05,P < 0.01)(Tab 1)。
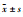
| Group | Concentration/μmol·L-1 | OD value490 nm | Proliferationrate/% |
| Control | — | 0.23±0.02 | — |
| Model | — | 0.31±0.01## | 36.60 |
| Aminoguanidine | 10.0 | 0.25±0.03** | 12.53 |
| Catalpol | 0.1 | 0.28±0.02* | 24.62 |
| 1.0 | 0.26±0.02** | 13.89 | |
| 10.0 | 0.25±0.03** | 9.95 | |
| ##P < 0. 01 vs control; *P < 0. 05, **P < 0. 01 vs model | |||
免疫荧光结果显示,与空白对照组相比,AGEs刺激巨噬细胞介导系膜细胞COL-Ⅳ(Fig 1)蛋白荧光明显增强(P < 0.01),而加入梓醇(10.0 μmol·L-1)、氨基胍(10.0 μmol·L-1)干预后COL-Ⅳ蛋白荧光减弱(P < 0.01)。
|
Fig 1 Effect of catalpol on fluorescent expression of COL-IV in MMCs mediated by AGEs-stimulated RAW264.7 macrophages( |
与空白对照组相比,AGEs刺激巨噬细胞介导系膜细胞FN、COL-Ⅳ、TGF-β(Fig 2)蛋白表达上调(P < 0.01),而梓醇(0.1、1.0、10.0 μmol·L-1)、氨基胍(10.0 μmol·L-1)可不同程度的下调其表达(P < 0.05,P < 0.01),且梓醇的下调程度与浓度相关。

|
Fig 2 Effect of catalpolon expression of FN, COL-Ⅳ and TGF-β in MMCs mediated by AGEs-stimulated RAW264.7 macrophages( |
与空白对照组相比,AGEs可明显提高巨噬细胞IL-6、IL-12、TNF-α分泌水平(P < 0.01),而梓醇(0.1、1.0、10.0 μmol·L-1)、氨基胍(10.0 μmol·L-1)可不同程度的抑制其分泌(P < 0.05,P < 0.01),且梓醇的抑制程度与浓度相关(Tab 2、Tab 3、Tab 4)。
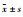
| Group | Concentration/μmol·L-1 | IL-6/ng·L-1 |
| Control | — | 85.34±3.82 |
| Model | — | 120.10±6.51## |
| Aminoguanidine | 10.0 | 96.41±4.78** |
| Catalpol | 0.1 | 112.44±10.97* |
| 1.0 | 96.03±3.76** | |
| 10.0 | 88.52±4.77** | |
| ##P < 0. 01 vs control; *P < 0. 05, **P < 0. 01 vs model | ||
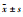
| Group | Concentration/μmol·L-1 | IL-12/ng·L-1 |
| Control | — | 5.29±0.23 |
| Model | — | 7.94±0.85## |
| Aminoguanidine | 10.0 | 5.73±0.14* |
| Catalpol | 0.1 | 6.19±1.13 |
| 1.0 | 5.45±1.04* | |
| 10.0 | 5.41±0.41** | |
| ##P < 0. 01 vs control; *P < 0. 05, **P < 0. 01 vs model | ||
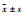
| Group | Concentration/μmol·L-1 | TNF-α/ng·L-1 |
| Control | — | 438.00±32.90 |
| Model | — | 680.08±44.23## |
| Aminoguanidine | 10.0 | 638.83±30.64 |
| Catalpol | 0.1 | 646.75±46.99 |
| 1.0 | 615.92±44.19 | |
| 10.0 | 581.33±22.55** | |
| ##P < 0. 01 vs control; **P < 0. 01 vs model | ||
DN是糖尿病严重的微血管并发症,研究表明肾脏疾病的发展与巨噬细胞在肾组织中的迁移、浸润、炎症介质的高表达密切相关,并且可能是各种机制下游的共同环节[7]。
高血糖是DN炎症发病机制的主要始动因素,长期高血糖导致AGEs在体内过多蓄积,一方面刺激巨噬细胞,通过分泌炎症因子如IL-6、IL-12、TNF-α和诱导型一氧化氮合酶(inducible nitric oxide synthase,iNOS)等促进炎症反应,导致肾固有细胞损伤,如肾小球系膜细胞增生、血管内皮细胞泡沫化和足细胞凋亡[8-9];另一方面在糖尿病环境下,AGEs刺激肾系膜细胞,使其分泌单核细胞趋化蛋白(monocyte chemotactic protein-1,MCP-1)等反过来激活、促进巨噬细胞从血液向肾脏富集并分泌大量炎症因子加重肾系膜细胞的损伤,扩大炎症加快DN的发展[10-11]。
研究发现转化生长因子-β(transforming growth factor-β,TGF-β)是纤维化最关键的调节因子和纤维化的早期生物标志物,高血糖和炎症可以刺激TGF-β的活性,被激活的TGF-β通过促进多种分子如纤维粘连蛋白(fibronectin,FN)、Ⅳ型胶原(Collage TypeⅣ,COL-Ⅳ)的分泌加速DN中的肾纤维化进程,进而加重DN[12]。研究结果表明[13],TGF-β激活激酶-1(TGF-β activated kinase-1,TAK1)抑制剂可通过TAK1 /MAPKs、MAPKs /NF-κB途径抑制AGEs对巨噬细胞的激活和炎症因子的表达。此外,肾小球系膜细胞分泌的FN、COL-Ⅳ等细胞外基质又可与AGEs形成交叉连接或通过与晚期糖基化终产物受体(receptor of advanced glycation endproducts,RAGE)结合来影响DN的病理过程[14],FN也可通过促进粘着斑激酶(focal adhesion kinase,FAK)和Src家族激酶(Src family kinase,SFK)活化从而诱导巨噬细胞迁移。研究表明,芳基烃受体(aryl hydrocarbon receptor,AhR)可通过氧化应激级联调控环氧合酶-2(cyclooxygenase-2,COX-2)、前列腺素E2(prostaglandin E2,PGE 2)表达和细胞外基质沉积参与Nε-羧甲基赖氨酸(Nε-carboxymethyllysine,CML一种主要的晚期糖基化终产物)诱导的系膜细胞激活和巨噬细胞浸润[15]。
本实验建立了AGEs刺激巨噬细胞与肾系膜细胞共培养模型,AGEs刺激巨噬细胞后,其炎症因子IL-6、IL-12、TNF-α分泌水平升高,与此同时肾系膜细胞FN、COL-Ⅳ、TGF-β蛋白表达水平升高,而加入梓醇再用AGEs刺激巨噬细胞后可下调其炎症因子及系膜细胞蛋白表达水平,这提示梓醇可通过下调巨噬细胞炎症因子水平缓解其对系膜细胞造成的损伤,其具体机制有待进一步探讨。
( 致谢: 本实验于江苏省中药药效与安全性评价重点实验室完成,感谢实验室老师的指导和同学们的帮助。)
| [1] |
Han Q, Zhu H, Chen X, et al. Non-genetic mechanisms of diabetic nephropathy[J]. Frontiers of Med, 2017, 11(3): 319-32. doi:10.1007/s11684-017-0569-9 |
| [2] |
Xu X, Qi X, Shao Y, et al. Blockade of TGF-β-activated kinase 1 prevents advanced glycation end products-induced inflammatory response in macrophages[J]. Cytokine, 2016, 78: 62-8. doi:10.1016/j.cyto.2015.11.023 |
| [3] |
Ninichuk V, Khandoga A G, Segerer S, et al. The role of interstitial macrophages in nephropathy of type 2 diabetic db/db mice[J]. Am J Pathol, 2007, 170(4): 1267-76. doi:10.2353/ajpath.2007.060937 |
| [4] |
Lv X, Dai G, Lv G, et al. Synergistic interaction of effective parts in Rehmanniae Radix and Cornus officinalis ameliorates renal injury inC57BL/KsJ-db/db diabetic mice:Involvement of suppression of AGEs/RAGE/SphK1signaling pathway[J]. J Ethnopharmacol, 2016, 185(2): 110-9. |
| [5] |
Choi H J, Jang H J, Chung T W, et al. Catalpol suppresses advanced glycation end-products-induced inflammatory responses through inhibition of reactive oxygen species in human monocytic THP-1 cells[J]. Fitoterapia, 2013, 86: 19-28. doi:10.1016/j.fitote.2013.01.014 |
| [6] |
Wang Y, Wei Q, Liu Q, et al. Crosstalk between monocytes and renal mesangial cells via interaction of metalloproteinases and fractalkine in diabetic nephropathy[J]. Mol Med Rep, 2013, 8(6): 1817-23. doi:10.3892/mmr.2013.1703 |
| [7] |
Anders H J, Ryu M. Renal microenvironments and macrophage phenotypes determine progression or resolution of renal inflammation and fibrosis[J]. Kidney Int, 2011, 80(9): 915-25. doi:10.1038/ki.2011.217 |
| [8] |
Guo Y, Lin C, Xu P, et al. AGEs induced autophagy impairs cutaneous wound healing via stimulating macrophage polarization to M1 in diabetes[J]. Scientific Reports, 2016, 6(1): 36416. doi:10.1038/srep36416 |
| [9] |
Kumar, S. Cellular and molecular pathways of renal repair after acute kidney injury[J]. Kidney Int, 2018, 93(1): 27-40. doi:10.1016/j.kint.2017.07.030 |
| [10] |
富莹雪, 陈玉萍, 卞文青, 等. 梓醇对AGEs刺激肾系膜细胞介导巨噬细胞极化的影响[J]. 中国药理学通报, 2017, 33(10): 1399-404. Fu Y X, Chen Y P, Bian W Q, et al. Effect of catalpol on RAW264.7 macrophage polarization mediated by AGEs-stimulated mouse mesangial cells[J]. Chin Pharmacol Bull, 2017, 33(10): 1399-404. doi:10.3969/j.issn.1001-1978.2017.10.014 |
| [11] |
Haller H, Bertram A, Nadrowitz F, et al. Monocyte chemoattractant protein-1 and the kidney[J]. Current Opinion Nephrol Hypertens, 2016, 25(1): 42-9. doi:10.1097/MNH.0000000000000186 |
| [12] |
Tian L, Fu P, Zhou M, et al. Role of urotensin Ⅱ in advanced glycation end product-induced extracellular matrix synthesis in rat proximal tubular epithelial cells[J]. International J Mol Med, 2016, 38(6): 1831-8. doi:10.3892/ijmm.2016.2789 |
| [13] |
付欣, 徐兴欣, 邵云侠, 等. 转化生长因子-β激活激酶1抑制剂对AGEs诱导小鼠骨髓来源巨噬细胞活化作用及机制[J]. 中国药理学通报, 2016, 32(03): 355-61. Fu X, Xu X X, Shao Y X, et al. Effect of TGF-β activated kinase-1 inhibitor on bone marrow-derived macrophages activation and its mechanism[J]. Chin Pharmacol Bull, 2016, 32(03): 355-61. doi:10.3969/j.issn.1001-1978.2016.03.012 |
| [14] |
Qiu Y Y, Tang L Q, Wei W. Berberine exerts renoprotective effects by regulating the AGEs-RAGE signaling pathway in mesangial cells during diabetic nephropathy[J]. Mol Cell Endocrinol, 2017, 443: 89-105. doi:10.1016/j.mce.2017.01.009 |
| [15] |
Sheu M L, Lee W J, Liu S H, et al. Aryl hydrocarbon receptor deficiency attenuates oxidative stress-related mesangial cell activation and macrophage infiltration and extracellular matrix accumulation in diabetic nephropathy[J]. Antioxidants Redox Signal, 2016, 24(4): 217-31. doi:10.1089/ars.2015.6310 |

