


2. 湖北民族大学 科技学院医学院, 湖北 恩施 445000;
3. 湖北民族大学 医学院中药学教研室, 湖北 恩施 445000
胡泽华(1975-),男,博士,副教授,研究方向:中药药效物质基础研究,通讯作者,E-mail:hzh75418427@126.com
2. Medical College, Science and Technology College, Hubei Minzu University, Enshi Hubei 445000, China;
3. Dept of Traditional Chinese Medicine, Medical College, Hubei Minzu University, Enshi Hubei 445000, China
肝纤维化(hepatic fibrosis,HF)是指各种慢性肝病引起的细胞外基质在肝脏过度沉积,其病理特征为肝内纤维结缔组织异常增生[1],及时有效的抗纤维化治疗是防止慢性肝病向终末期肝病转化的必要措施。Beta-谷甾醇(Beta-sitosterol,BS)是一种常见的植物甾醇,广泛存在于植物叶子、植物油和果蔬中,具有良好的抗氧化、抗炎、免疫调节、抗肿瘤等药理活性[2],被广泛应用于医药保健品领域。炎症是病毒、药物、酒精等病因引起慢性肝病发展的一个动态和共同过程,慢性炎症进一步发展最终引起肝纤维化甚至肝癌。Gupta等[3]和Valerio等[4]报道,Beta-谷甾醇具有类似氢化可的松的抗炎作用,能提高IL-10的活性,抑制NF-κB的迁移。以炎症为切入点,本文将初次探讨Beta-谷甾醇对四氯化碳诱导小鼠肝纤维化的作用及机制。
1 材料 1.1 实验动物C57BL/6小鼠,♂,体质量(17±3)g,购于北京维通利华实验技术有限公司,许可证号:SCXK京2016-0011。
1.2 药品与试剂BS(LOT:R08S7F20751,纯度>98%,上海源叶生物科技有限公司);CCL4(国药集团化学试剂有限公司,临用前溶于橄榄油);ALT、AST试剂盒(AST, ALT:LOT:20171017,南京建成生物工程研究所);TNF-α试剂盒(美国BD公司);鼠源α-SMA(LOT:GR239100-1)、collagenⅠ、TβR1(LOT:GR201638-3)、Smad2/3(LOT:GR221934-8)、NF-κB和p-NF-κB一抗(英国Abcam公司);β-actin一抗、山羊抗兔二抗(武汉博士德生物工程有限公司)
1.3 仪器显微镜(Nikon E200,日本);电子天平(YP5002, 上海越平);酶标仪(Thermo Scientific Multiskan GO,美国);石蜡切片机(Thermo Fisher HM325,美国);蛋白电泳仪(Bio-Rad, 美国);蛋白湿转仪(Bio-Rad, 美国)。
2 方法 2.1 BS配制每只动物灌胃体积在0.1~0.4 mL适宜。取一瓶BS 20 mg研磨成细粉加橄榄油,在温水浴中加速溶解,定容到41.7 mL,配成高剂量0.48 g·L-1的溶液,然后从中取20 mL溶液加橄榄油,定容到30 mL,配成中剂量0.32 g·L-1的溶液,再从该溶液中取10 mL加橄榄油,定容到20 mL,配成低剂量0.16 g·L-1的溶液,每管溶液约为10只小鼠1周的用量。
2.2 动物分组、给药[5-6]与造模50只小鼠适应性喂养一周后,随机分为5组:正常组(control group,CG)、CCL4模型组(carbon tetrachloride group,CTG)、2 mg·kg-1 Beta-谷甾醇组(BS-L)、4 mg·kg-1 Beta-谷甾醇组(BS-M)、6 mg·kg-1 Beta-谷甾醇组(BS-H)。模型组小鼠腹腔注射含25% CCL4的橄榄油溶液1.6 mL·kg-1,每周2次,30 d共9次。药物组在造模同时,d 1~15灌胃BS,每次灌0.25 mL,正常组灌胃等体积生理盐水。所有小鼠30 d后禁食不禁水,24 h后处死,按要求做后续操作。
2.3 肝脏外观形态观察及肝指数测定小鼠称重,眼球采血,颈椎脱臼处死后,取肝脏,用高倍相机在同背景同视野下拍外观形态。生理盐水洗血,滤纸吸干,称量肝重。肝指数=肝脏重量(g)/体质量(g)×100%
2.4 血清学指标检测小鼠采血后,静置分离得血清,按照kit要求测谷丙转氨酶(alanine aminotrans,ALT)、谷草转氨酶(aspartate aminotransferase,AST)和肿瘤坏死因子-α(tumor necrosis factor α,TNF-α)的含量。
2.5 HE染色肝脏用10%甲醛固定24 h,HE染色,石蜡切片在二甲苯脱腊3次,过梯度乙醇各5 min,水洗1 min,苏木精染色5 min,水洗1 min,1%盐酸乙醇分化,流水冲洗2 min,伊红染2 s,乙醇脱水2 min,二甲苯透明、封固、镜检。
2.6 Masson染色常规脱水包埋,切片脱腊至水,Harris苏木精染色10 min,流水稍洗,1%盐酸乙醇分化,流水冲洗2 min,丽春红酸性品红染液染5 min,流水稍洗,磷钼酸溶液5 min,苯胺蓝复染5 min,1%冰醋酸处理1 min,95%乙醇多次脱水,二甲苯透明,中性树胶封片。
2.7 免疫组织化学检测α-SMA、CollagenⅠ含量石蜡切片脱蜡至水,高温高压修复2 min,冷却至室温,转入TBS缓冲液冲洗3次,每次5 min,3%双氧水阻断内源性过氧化物酶室温20 min,TBS冲洗3次,每次5 min,10%山羊血清孵育20 min,一抗(α-SMA:1 :150,CollageⅠ:1 :600)4 ℃过夜,次日复温后,TBS冲洗3次,每次5 min,每张切片滴50 μL二抗,室温孵育30 min,TBS冲洗3次,每次5 min,DAB显色,流水冲洗,苏木精复染2 min,水洗,1%盐酸乙醇分化2 s,温水返蓝,梯度乙醇脱水干燥,二甲苯透明,封片。
2.8 Western blot检测α-SMA、CollageⅠ、TβR1、Smad2/3、NF-κB和p-NF-κB蛋白表达称肝脏组织100 mg,加1 mL Ripa裂解液匀浆破组织,再超声破碎(超声时间3 s,间隔10 s,超声10次),冰上裂解30 min,12 000 r·min-1, 4 ℃,离心20 min,取上清,BCA法测蛋白浓度后,加5×上样缓冲液,100 ℃变性5 min,-20 ℃保存。配10%的分离胶,电泳条件:60 V,30 min浓缩,110 V,70 min分离,电转条件:110 V恒压,75 min。5%脱脂奶粉封闭1 h,一抗:α-SMA:1 :3 000、collagenⅠ:1 :3 000、TβR1:1 :100、Smad2/3:1 :500、NF-κB/p-NF-κB:1 :1 000,4 ℃过夜,TBST洗脱,孵二抗:1 :80 000,90 min,TBST洗脱,曝光。
2.9 统计学处理采用SPSS 24.0软件分析,结果以x±s表示,多组间比较采用单因素方差分析,两两比较采用Dunnet-t检验。
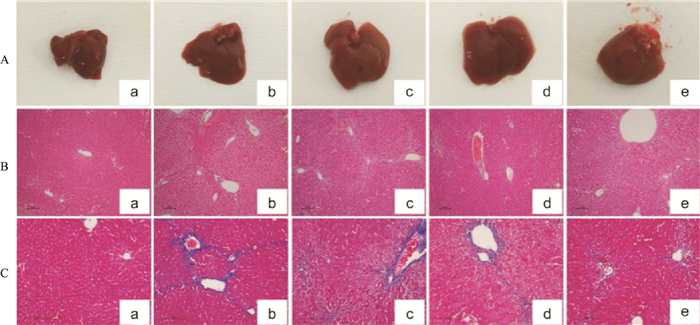
3 结果 3.1 BS对CCL4诱导小鼠肝纤维化肝脏大体形态与组织结构的影响大体观察肝脏表面颜色和光滑度,HE染色观察肝内结构,炎症水肿等,Masson染色观察胶原生成情况。正常组肝脏包膜光滑,呈红褐色,小鼠肝细胞结构正常,肝小叶结构正常,无胶原沉积;CCL4组肝脏表面弥漫明显大小不一的塌陷区,边缘泛白,肝小叶被破坏,肝不同程度的水肿、结构紊乱、明显肿胀变形,有点状、片状坏死及炎性细胞浸润,肝索紊乱,大量胶原沉积分离原来的肝小叶形成假小叶;BS各组量效依赖地减少肝脏表面塌陷数量,肝索较整齐,炎性细胞减少,水肿改变不明显,胶原沉积仍可见,但少于CCL4组。见Fig 1。
|
| Fig 1 Effect of different doses of BS on liver morphology by eye, HE and Masson staining A: Morphology by eye, B: Morphology by HE, C: Morphology by Masson; a:CG, b:CTG, c:BS-L, d:BS-M, e:BS-H |
肝指数一定程度上反映肝脏肿胀。CTG组肝指数高于CG组(P < 0.05), BS较CTG组,量效依赖地降低肝指数(P < 0.05)。见Fig 2。

|
| Fig 2 Effect of different doses of BS on liver index(x±s, n=10) **P < 0.01 vs CG; ##P < 0.01 vs CTG |
与CG组比,CTG组ALT、AST活性明显升高(P < 0.01),BS组量效依赖地降低其表达(P < 0.05或P < 0.01),其中,对ALT的降低效果更好。见Fig 3。

|
| Fig 3 Effect of different doses of BS on activities of ALT, AST(x±s, n=10) **P < 0.01 vs CG; #P < 0.05 vs CTG; ##P < 0.01 vs CTG |
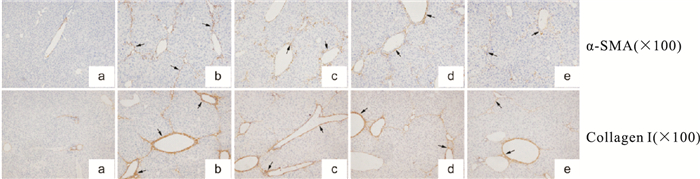
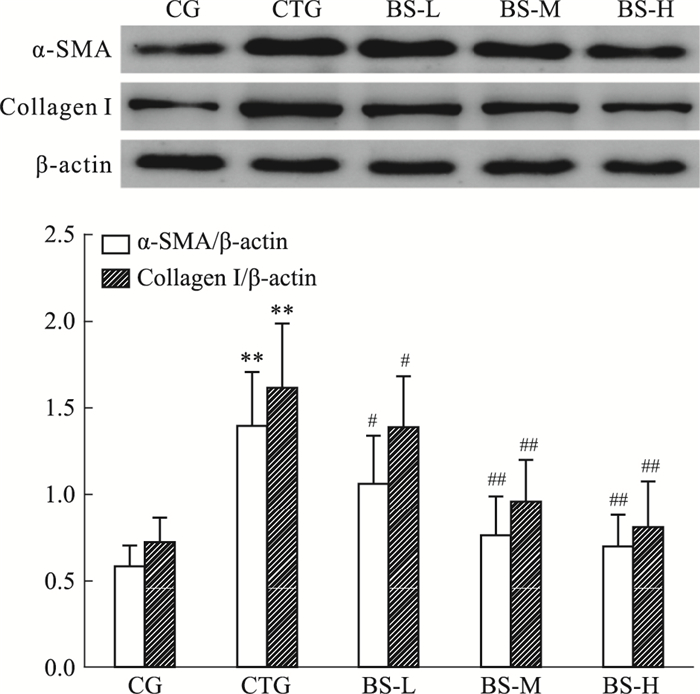
肝星状细胞的激活是肝纤维化的关键步骤。α-SMA是肝星状细胞活化的标志[7],而CollagenⅠ是肝星状细胞活化后释放的最主要的细胞外基质[8]。利用Western blot和免疫组织化学进行BS对α-SMA、CollagenⅠ的探究。镜下可见:与正常组比,CCL4组α-SMA、CollagenⅠ表达明显增加,BS量效依赖地降低了α-SMA、CollagenⅠ表达,见Fig 4;Western blot的结果提示,CCL4明显增加了α-SMA、CollagenⅠ蛋白含量(P < 0.01),较正常组,不同剂量的BS降低了CCL4诱导地α-SMA、CollagenⅠ的表达(P < 0.05或P < 0.01),且呈剂量依赖性。见Fig 5。
|
| Fig 4 Effect of different doses of BS on α-SMA and Collagen I by IHC(×100) a:CG, b:CTG, c:BS-L, d:BS-M, e:BS-H |
|
| Fig 5 Effect of different doses of BS on α-SMA and Collagen I by Western blot(x±s, n=10) **P < 0.01 vs CG; #P < 0.05 vs CTG; ##P < 0.01 vs CTG |
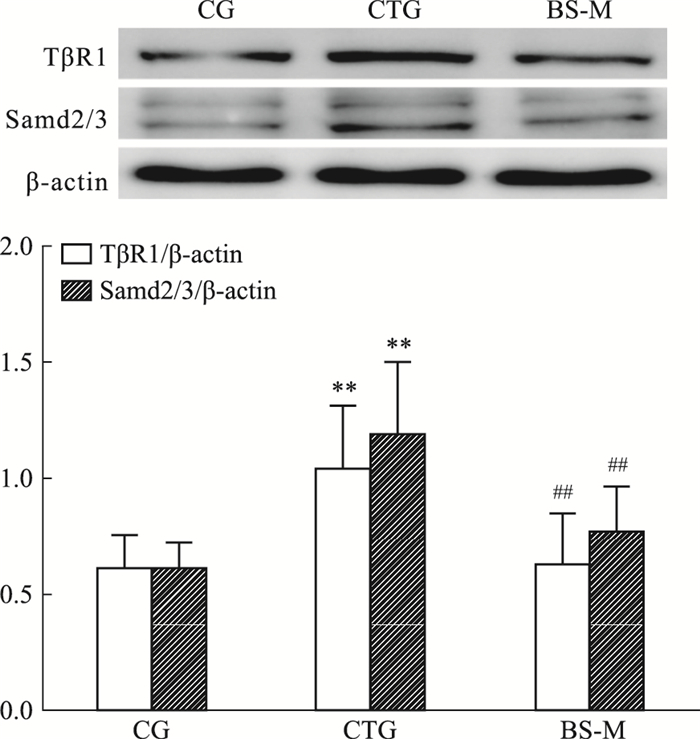
TGF-β是HSCs活化过程和细胞外基质生成过程中的致纤维化因子,通过激活其受体,再激活Smad蛋白,进而激活细胞内信号,是纤维化的一条经典通路。CCL4诱导肝纤维化时,TGF-β受体(TβR1)和Smad2/3发生显著性高表达(P < 0.01),中剂量的BS降低了TβR1、Smad2/3的表达(P < 0.01)。见Fig 6。
|
| Fig 6 Effect of BS-M on TβR1 and Smad2/3 by Western blot(x±s, n=6) **P < 0.01 vs CG; ##P < 0.01 vs CTG |
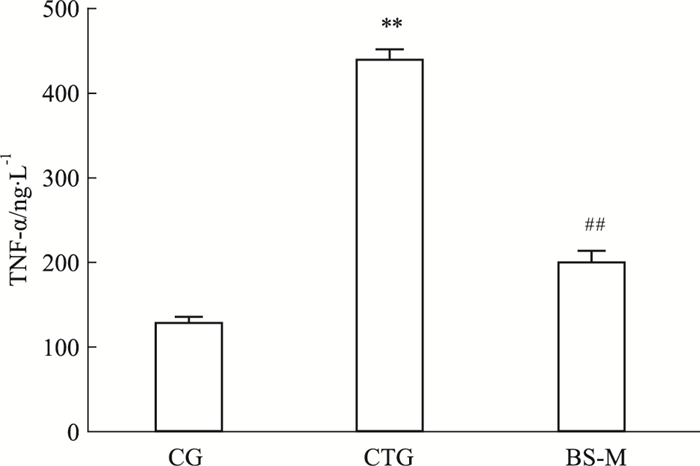
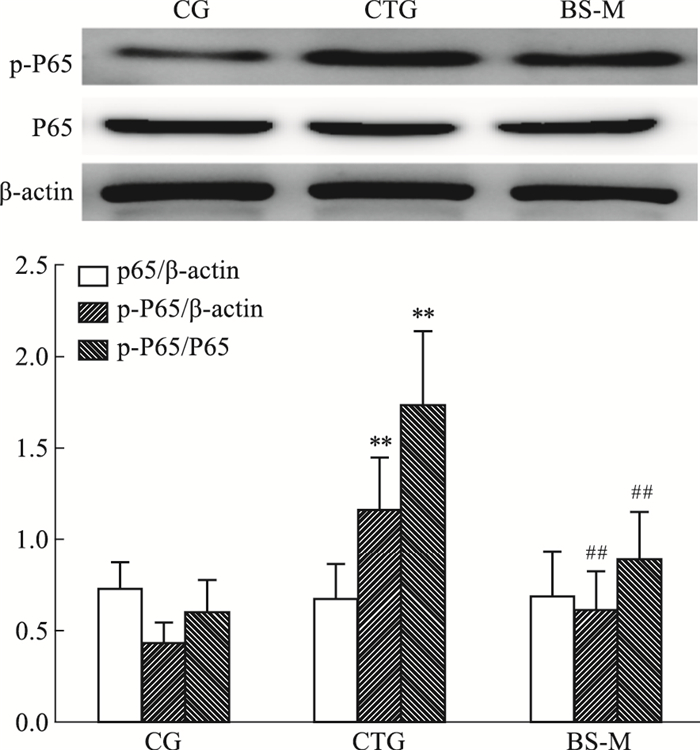
炎症因子,如TNF-α,是CCL4诱导的肝纤维化的参与者[9],且增加炎症因子数量的NF-κB也会被CCL4激活[10]。较正常组、CTG组TNF-α显著性增高,BS-M降低其表达(P < 0.01)。见Fig 7;如Fig 8,较正常组,p-NF-κB、NF-κB在CTG组表达增高,BS-M亦降低其表达(P < 0.01)。见Fig 8。
|
| Fig 7 Effect of BS-M on TNF-α by Elisa(x±s, n=10) **P < 0.01 vs CG; ##P < 0.01 vs CTG |
|
| Fig 8 Effect of BS-M on NF-κB by Western blot(x±s, n=6) **P < 0.01 vs CG; ##P < 0.01 vs CTG |
甾醇分动物甾醇、植物甾醇和菌类甾醇,BS是四环三萜类,是植物甾醇最常见的类型之一,占总甾醇的50%~65%[11],是一种重要的天然甾体,被誉为“生命的钥匙”[12],BS最初研究都集中在降胆固醇功效及机制上,同时降胆固醇功效也是目前研究最多和最深的。后有研究显示,植物甾醇还有抗炎症、免疫调节、抗肿瘤、中枢神经系统调节作用[2],其分子机制尚不清楚,也未形成完整的信号通路模型。以抗肿瘤和抗炎作用为结合点,本文初步探讨了其对肝纤维化的作用与作用机制。
CCL4是一种选择性肝毒性物质,能活化HSCs,促使肝纤维化。肝纤维化是终末期肝病发生的基础,发病机制异常复杂,HSCs活化是肝纤维化发生的细胞学基础,另外,各种细胞、细胞因子等也参与此过程[13]。去除致病因素是最佳治疗策略,但许多慢性肝病中,致病因素和相关因素往往难以消除,这表明开发抑制肝纤维化进展并诱导其消退的特异性抗纤维化药物的重要性。本实验BS甾醇降低肝指数,降低血清ALT、AST活性,减少细胞外基质CollagenⅠ的沉积和HSCs活化标志物α-SMA的表达,提示BS能降低肝脏损伤并抑制纤维化进程。
TGF-β可以激活HSCs并使其增殖,活化的HSCs可以通过自分泌和旁分泌的途径持续不断的释放细胞外基质,激活邻近的HSCs,导致持续不断地发生纤维化。TGFβ/Smad信号通路是肝纤维化过程讨论得最为广泛的分子机制,本实验中,CCL4组明显升高了TGFβ和Smad2/3的蛋白含量,BS降低其表达,提示BS干预了此条信号通路的转导,减轻纤维化程度。
NF-κB信号通路能加快HSCs的激活,其抑制剂能降低肝纤维一些重要蛋白的表达并诱导HSCs产生凋亡,延缓纤维化进程[14],也有学者报道,在胆总管结扎的肝纤维化中,TNF-α也加重纤维化程度[15]。同时,本课题前期工作也验证TNF-α参与肝纤维,本实验中,选择TNF-α-NF-κB这条经典的炎症通路做了探讨,结果发现CCL4组,TNF-α和p- NF-κB高表达,BS明显地降低了其表达,提示BS亦干预了此条炎症通路的转导。
综上所述,BS对CCL4诱导的小鼠肝纤维化有保护作用,其机制可能与TGFβ/Smad2/3和TNF-α- NF-κB相关。
( 致谢: 本实验在湖北民族大学医学实验中心和附属民大医院风湿性疾病发生与干预湖北省重点实验室完成,感谢支持。)
| [1] |
Saxena N K, Anania F A. Adipocytokine and hepatic fibrosis[J]. Trends Endoefinol Metab, 2015, 26(3): 153-61. doi:10.1016/j.tem.2015.01.002 |
| [2] |
刘威良, 姬昱, 黄艾祥. β-谷甾醇的研究及开发进展[J]. 农产品加工, 2019, 1(1): 77-9, 82. Liu W L, Ji Y, Huang A X. Research and development progress of β- sitosterol[J]. Farm prod process, 2019, 1(1): 77-9, 82. |
| [3] |
Gupta M B, Nath R, Srivastava N, et al. Anti-inflammatory and antipyretic activities of beta-sitosterol[J]. Planta Medica, 1980, 39(2): 157-63. |
| [4] |
Valerio M, Awad A B. β-Sitβ-Sitosterol down-regulates some pro-inflammatory signal transduction pathways by increasing the activity of tyrosine phosphatase SHP-1 in J774A.1 murine macrophages[J]. Int Immunopharmacol, 2011, 11(8): 1012-7. doi:10.1016/j.intimp.2011.02.018 |
| [5] |
Wong H S, Chen J H, Leong P K, et al. β-sitosterol protects against carbon tetrachloride hepatotoxicity but not gentamicin nephrotoxicity in rats via the induction of mitochondrial glutathione redox cycling[J]. Molecules, 2014, 19(11): 17649-62. doi:10.3390/molecules191117649 |
| [6] |
Kim K S, Yang H J, Lee J Y, et al. Effects of β-sitosterol derived from Artemisia capillaris on the activated human hepatic stellate cells and dimethylnitrosamine-induced mouse liver fibrosis[J]. BMC Complement Altern Med, 2014, 14: 363. doi:10.1186/1472-6882-14-363 |
| [7] |
Barcena-Varela M, Colyn L, Fernandez-Barrena M G. Epigenetic mechanisms in hepatic stellate cell activation during liver fibrosis and carcinogenesis[J]. Int J Mol Sci, 2019, 20(10): E2507. doi:10.3390/ijms20102507 |
| [8] |
Puente A, Fortea J I, Cabezas J, et al. LOXL2-A new target in antifibrogenic therapy?[J]. Int J Mol Sci, 2019, 20(7): E1634. doi:10.3390/ijms20071634 |
| [9] |
Beringer A, Miossec P. IL-17 and TNF-α cooperation contributes to the pro-inflammatory response of hepatic stellate cells[J]. Clin Exp Immunol, 2019, 198(1): 111-20. doi:10.1111/cei.13316 |
| [10] |
Sun X, Huang X, Zhu X, et al. HBOA ameliorates CCl4-incuded liver fibrosis through inhibiting TGF-β1/Smads, NF-κB and ERK signaling pathways[J]. Biomed Pharmacother, 2019, 115: 108901. doi:10.1016/j.biopha.2019.108901 |
| [11] |
Blanco-Vaca F, Cedo L, Julve J. Phytosterols in cancer: From molecular mechanisms to preventive and therapeutic potentials[J]. Curr Med Chem, 2018, 25: 1-14. doi:10.2174/092986732501180122140757 |
| [12] |
Nes W D. Biosynthesis of cholesterol and other sterols[J]. Chem Rev, 2011, 111(10): 6423-51. doi:10.1021/cr200021m |
| [13] |
张晨曦, 卞勉励, 陈星燃, 等. 肝窦内皮细胞在肝脏疾病中的作用[J]. 中国药理学通报, 2017, 33(2): 149-53. Zhang C X, Bian M L, Chen X R, et al. Roles of liver sinusoidal endothelial cells in liver diseases[J]. Chin Pharmacol Bull, 2017, 33(2): 149-53. doi:10.3969/j.issn.1001-1978.2017.02.001 |
| [14] |
Zheng H, Wang X, Zhang Y, et al. Pien-Tze-Huang ameliorates hepatic fibrosis via suppressing NF-κB pathway and promoting HSC apoptosis[J]. J Ethnopharmacol, 2019, 5: 111856. doi:10.1016/j.jep.2019.111856 |
| [15] |
Roh Y S, Cho A, Cha Y S, et al. Lactobacillus aggravate bile duct ligation-induced liver inflammation and fibrosis in mice[J]. Toxicol Res, 2018, 34(3): 241-7. doi:10.5487/TR.2018.34.3.241 |

