


 ,
CONG Li,
ZHANG Yong,
XIANG Li-ping,
XIE Xiao-lin,
BO Ping-juan,
XIANG Xue-ping,
FU Xiao-hua
,
CONG Li,
ZHANG Yong,
XIANG Li-ping,
XIE Xiao-lin,
BO Ping-juan,
XIANG Xue-ping,
FU Xiao-hua

动脉粥样硬化是一种以脂质堆积和动脉管壁慢性炎症为特征的疾病,巨噬细胞在动脉粥样硬化发生发展中扮演重要角色。研究显示[1],促进早期活化巨噬细胞凋亡,可以降低细胞密度,减少病变面积,有效抑制动脉粥样硬化的早期进展。染料木素(genistein,GEN)是一类富含于豆类植物中的异黄酮类化合物,既是一种植物雌激素,又是天然的酪氨酸激酶抑制剂,具有药源丰富、毒副作用小等优点,在抗肿瘤、抗氧化和保护心血管等方面具有药理活性。课题组前期体内、体外研究证实,GEN及其新型合成类似物能够调控炎症信号通路,抑制动脉粥样硬化[2-3]。本实验以脂多糖(lipopolysaccharides,LPS)活化的RAW264.7细胞为受试对象,探讨GEN对活化巨噬细胞外源性凋亡途径的影响,为其防治动脉粥样硬化提供实验依据。
1 材料与方法 1.1 材料 1.1.1 细胞培养RAW264.7细胞购于中国科学院细胞库(上海),置于37 ℃、5% CO2培养箱中,以含10%胎牛血清和1%链霉素/青霉素的高糖DMEM培养基培养,待细胞处于对数生长期时开始实验。将RAW264.7细胞接种于12孔板(5×107·L-1),贴壁后,依据慢病毒感染说明书分别加入表达绿色荧光蛋白的肿瘤坏死因子α诱导蛋白8样分子2(tumor necrosis factor-α-induced protein 8-like 2,TIPE 2)对照和TIPE 2过表达慢病毒颗粒。
1.1.2 试剂与抗体GEN(446-72-0),Sigma公司,纯度≥98%;LPS(L8880),Solarbio公司,纯度≥99%;高糖DMEM培养基、胎牛血清、磷酸盐缓冲液(phosphate buffered saline,PBS)、链霉素/青霉素(03-034-1B),BI公司;CCK 8试剂盒、Annexin V-FITC/PI试剂盒、TRIzol、AceQ qPCR SYBR Green Master Mix、HiScript Ⅱ Q RT SuperMix for qPCR、GAPDH抗体,Vazyme公司;COX-2、iNOS、TIPE 2抗体,Affinity公司;caspase-8、caspase-3、Akt、p-Akt抗体,ImmunoWay公司;兔IgG、鼠IgG,ComWin Biotech公司;β-actin抗体,CMCTAG公司;RIPA细胞裂解液、BCA蛋白浓度测定试剂盒,Beyotime公司;慢病毒颗粒,Genechem公司。
1.1.3 仪器二氧化碳培养箱(美国Thermo,3131),多功能酶标仪(美国Bio-Tek,Synergy 2),流式细胞仪(美国BD,FACS Cantoll 488N),荧光显微镜(日本Olympus,IX51)、倒置相差显微镜(日本Olympus,VMD-P300B),高速冷冻离心机(德国Eppendorf,5404C),电泳槽、电转膜仪(美国Bio-Rad,552BR)、荧光定量PCR仪(美国Bio-Rad,CFX Connect),化学发光凝胶成像系统(上海天能科技有限公司,Tanon-5500)。
1.2 方法 1.2.1 CCK 8检测细胞活力制备单细胞悬液(5×107·L-1),接种于96孔板(100 μL/孔),待细胞贴壁后,加入10 μmol·L-1 GEN预孵育2 h,再用1 mg·L-1 LPS处理24 h。吸弃上清,PBS洗2遍,每孔加入10 μL CCK 8试剂和90 μL完全培养基,轻摇混匀,置于培养箱内孵育2 h。设置空白孔、对照孔,每组3个复孔,使用多功能酶标仪检测各孔在450 nm处的OD值。细胞活力/%=(处理孔-空白孔)/(对照孔-空白孔)×100%。
1.2.2 Annexin V-FITC/PI检测细胞凋亡制备单细胞悬液(5×107·L-1),接种于12孔板(1 mL/孔),待细胞贴壁后,10 μmol·L-1 GEN预孵育2 h,再用1 mg·L-1 LPS孵育24 h后加药处理。胰酶(不含EDTA)消化后,收集细胞至离心管(800 r·min-1,7 min离心),PBS洗2遍,加入100 μL结合缓冲液重悬细胞,将细胞密度调整至3×105·mL-1,取195 μL细胞悬液加入5 μL Annexin V-FITC,混匀后室温避光孵育10 min;用200 μL结合缓冲液洗涤细胞(800 r·min-1,7 min);再用190 μL结合缓冲液重悬细胞,加入5 μL碘化丙啶溶液,轻轻混匀后上流式细胞仪检测细胞凋亡率。
1.2.3 qRT-PCR采用TRIzol法提取总RNA,多功能酶标仪检测RNA纯度和浓度,依据HiScriptⓇ Ⅱ Q RT SuperMix for qPCR(+gDNA wiper)逆转录试剂说明书合成cDNA,采用AceQⓇqPCR SYBRⓇGreen Master Mix试剂盒进行相对荧光定量检测,以2-△△Ct法分析基因表达。引物序列见Tab 1。
| Gene | Primer sequence(5′- 3′) | |
| 18S | Forward | AGTCCCTGCCCTTTGTACACA |
| Reverse | CGATCCGAGGGCCTCACTA | |
| TNF-α | Forward | CAAGGGACAAGGCTGCCCCG |
| Reverse | GCAGGGGCTCTTGACGGCAG | |
| IL-6 | Forward | AACGATGATGCACTTGCAGA |
| Reverse | CTCTGAAGGACTCTGGCTTTG | |
| caspase-3 | Forward | GAGCCAGAGCAGAGACTTGG |
| Reverse | CATCATCCACACAAACCAGAA | |
| caspase-8 | Forward | GCTGCCCTCAAGTTCCTGT |
| Reverse | GATTGCCTTCCTCCAACATC | |
| TIPE 2 | Forward | TCAGAAACATCCAAGGCCAGAC |
| Reverse | CGGACCGACCAGCCATTTTAC |
使用预冷的PBS洗细胞3遍,加入细胞裂解液于冰上裂解10 min并离心(12 000×g,4 ℃,10 min),提取总蛋白,BCA试剂盒测定蛋白浓度。取40 μg样品,于10% SDS-PAGE凝胶中电泳;将蛋白转移至PVDF膜(polyvinylidene fluoride membranes,PVDF)上;在5%脱脂牛奶中室温封闭1 h,TBST(TBS包含0.05% Tween-20)洗3遍;加入一抗4 ℃孵育过夜,抗体稀释比为iNOS(1 :2 000)、COX-2(1 :2 000)、caspase-8(1 :1 000)、caspase-3(1 :1 000)、TIPE 2(1 :1 000)、Akt(1 :1 000)、p-Akt(1 :1 000)、β-actin(1 :10 000)、GAPDH(1 :10 000),TBST洗3遍;加入二抗室温孵育1 h,抗体稀释比为羊抗兔(1 :10 000)、羊抗鼠(1 :10 000),TBST洗3遍,ECL化学发光显影,凝胶成像系统检测蛋白表达水平。
1.2.5 统计学方法数据均以x±s表示,应用SPSS 20.0统计软件和GraphPad Prism 6.0进行t检验或单因素方差分析。
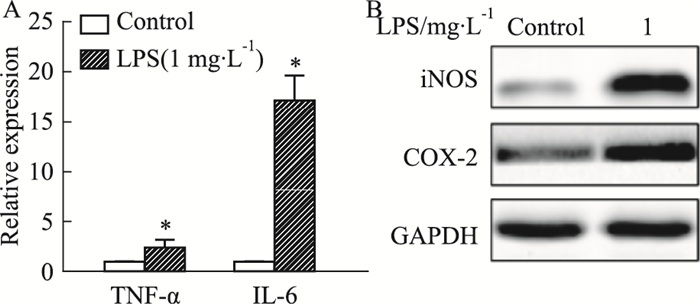
2 结果 2.1 GEN促进LPS活化的RAW264.7细胞凋亡 2.1.1 制备LPS活化RAW264.7细胞模型与对照组相比,1 mg·L-1 LPS组TNF-α、IL-6 mRNA(P < 0.05,Fig 1A )和iNOS、COX-2蛋白表达(Fig 1B )均上调,说明LPS能够活化RAW264.7细胞用于后续实验。
|
| Fig 1 Effects of LPS on inflammatory mediators in RAW264.7 cells(x±s, n=3) RAW264.7 cells were incubated with LPS (1 mg·L-1) for 24 h. The levels of TNF-α, IL-6 mRNA were detected by qRT-PCR (A); the expressions of iNOS, COX-2 were detected by Western blot (B). *P < 0.05 vs Ctrl group. |
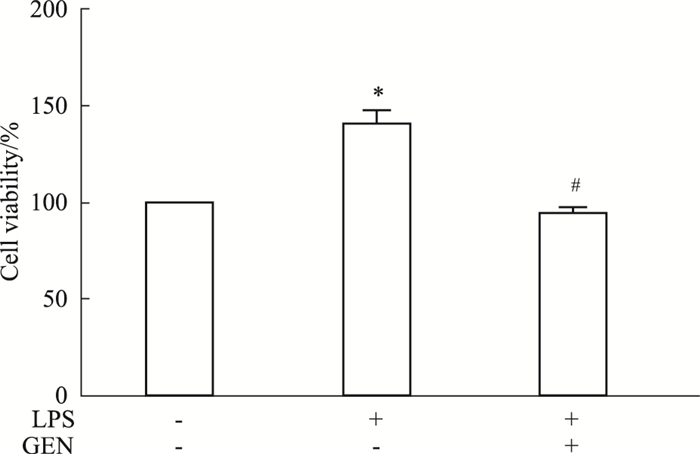
如Fig 2所示,与对照组相比,LPS组细胞活力明显增强(P < 0.05);与LPS组相比,GEN+LPS组细胞活力明显减弱(P < 0.05)。
|
| Fig 2 Effects of GEN on viability of activated RAW264.7 cells(x±s, n=3) RAW264.7 cells were preincubated with GEN(10 μmol·L-1) for 2 h, then incubated with LPS for 24 h. CCK 8 kits were used to detect cell viability. *P < 0.05 vs Ctrl group; #P < 0.05 vs LPS group. |
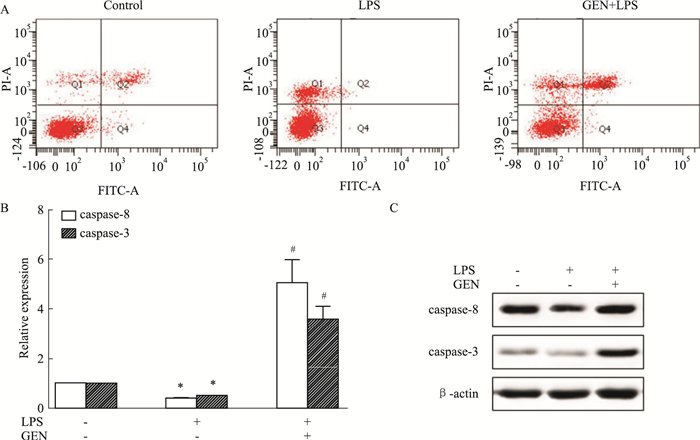
如Fig 3A所示,对照组、LPS组、GEN+LPS组细胞凋亡率依次为0.120±0.75、0.007±1.06、0.243±0.96。如Fig 3B、C所示,与对照组相比,LPS组caspase-8和caspase-3 mRNA及蛋白表达均减少;与LPS组相比,GEN+LPS组caspase-8和caspase-3 mRNA及蛋白表达均增多。
|
| Fig 3 Effects of GEN on apoptosis of activated RAW264.7 cells(x±s, n=3) RAW264.7 cells were pre-incubated with GEN for 2 h, then incubated with LPS for 24 h. The cell apoptosis rate (A) was detected by Annexin V-FITC/PI kits; the levels of caspase-8 and caspase-3 mRNA were detected by qRT-PCR (B); the expressions of caspase-8 and caspase-3 were detected by Western blot (C). *P < 0.05 vs Ctrl group; #P < 0.05 vs LPS group. |
如Fig 4所示,与对照组相比,LPS组TIPE 2 mRNA和蛋白表达均减少;与LPS组相比,GEN+LPS组TIPE 2表达增多。

|
| Fig 4 Effects of GEN on TIPE 2 in activated RAW264.7 cells(x±s, n=3) RAW264.7 cells were preincubated with GEN for 2 h, then incubated with LPS for 24 h. qRT-PCR (A) and Western blot (B) were used to detect the level of TIPE 2 mRNA and protein expression, respectively. *P < 0.05 vs Ctrl group; #P < 0.05 vs LPS group. |
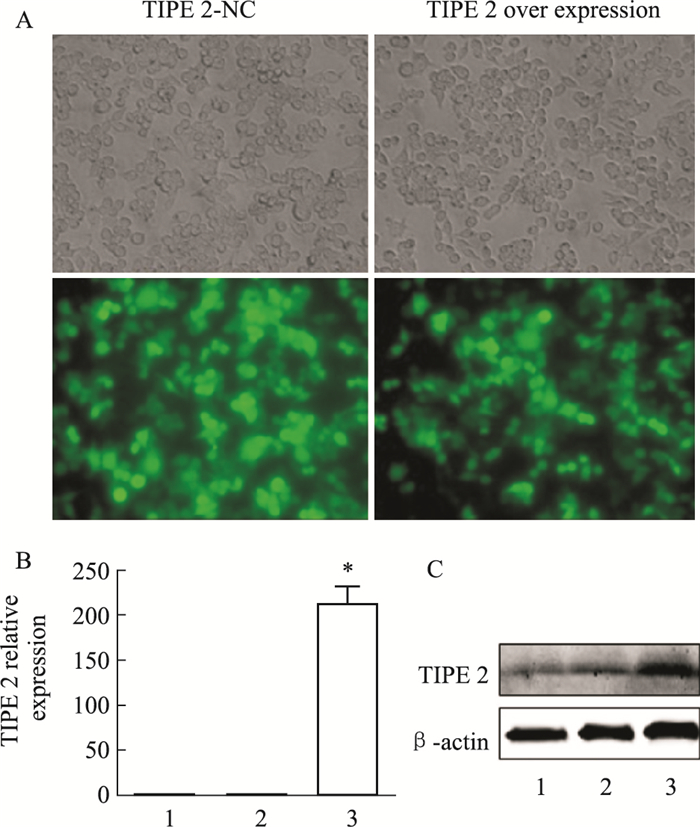
分别将TIPE 2对照和TIPE 2过表达慢病毒颗粒感染至RAW264.7细胞,72 h后荧光显微镜观察感染效率在90%以上(Fig 5A);与TIPE 2对照组相比,TIPE 2过表达组TIPE 2 mRNA和蛋白表达均上调(Fig 5B ),证实慢病毒已感染目的细胞,并上调TIPE 2表达,可用于后续实验。
|
| Fig 5 RAW264.7 cells infected by lentiviral vector RAW264.7 cells were infected with TIPE 2-NC (multiplicity of infection, MOI=40) and TIPE 2-over expression (MOI=40) lentiviral particles with GFP. Cells were captured under phase contrast and fluorescence microscopy (A); qRT-PCR (B) and Western blot (C) were used to detect the level of TIPE 2 mRNA and protein expression (x±s, n=3). *P < 0.05 vs TIPE 2-NC group.1:Control; 2:TIPE2-NC; 3:TIPE2 over expression |
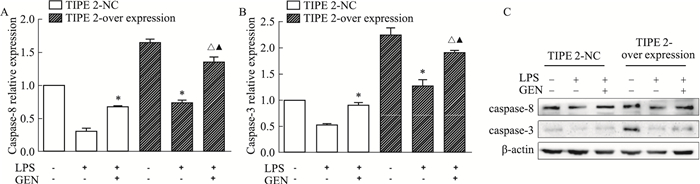
如Fig 6所示,与TIPE 2对照+LPS组相比,TIPE 2对照+GEN+LPS组和TIPE 2过表达+LPS组caspase-8、caspase-3 mRNA和蛋白表达均上调;与TIPE 2对照+GEN+LPS组相比,TIPE 2过表达+GEN+LPS组caspase-8、caspase-3 mRNA和蛋白表达均上调。
|
| Fig 6 Effects of TIPE 2-overexpression on apoptosis of activated RAW264.7 cells promoted by GEN(x±s, n=3) Cells were preincubated with GEN for 2 h, then incubated with LPS for 24 h. The levels of caspase-8 (A) and caspase-3 (B) mRNA were detected by qRT-PCR; the expressions of caspase-8 and caspase-3 were detected by Western blot (C). *P < 0.05 vs TIPE 2-NC+LPS group; △P < 0.05 vs TIPE 2-over expression+LPS group; ▲P < 0.05 vs TIPE 2-NC+LPS+GEN group. |
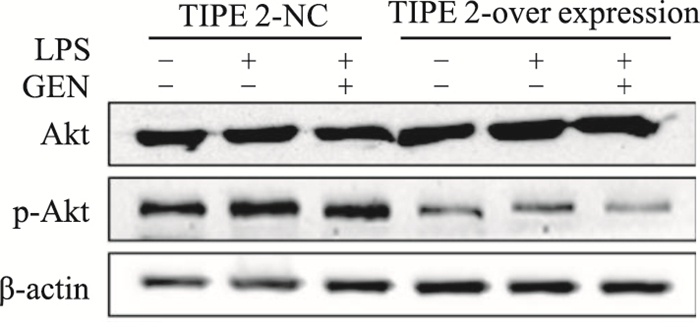
如Fig 7所示,与TIPE 2对照+LPS组相比,TIPE 2对照+GEN+LPS组和TIPE 2过表达+LPS组p-Akt蛋白表达下调,Akt蛋白表达无明显改变;与TIPE 2对照+GEN+LPS组相比,TIPE 2过表达+GEN+LPS组p-Akt蛋白表达下调,Akt蛋白表达无明显变化。
|
| Fig 7 Effects of GEN and TIPE 2 on activity of Akt in activated RAW264.7 cells Cells were preincubated with GEN for 2 h, then incubated with LPS for 24 h. The expressions of Akt and p-Akt were detected by Western blot. |
巨噬细胞在动脉粥样硬化各发展阶段都发挥重要作用,从病变起始到斑块破裂和心血管临床事件的发生。促进活化巨噬细胞凋亡不仅可以抑制炎症因子的释放,还可以减少巨噬细胞源性泡沫细胞的形成,抑制动脉粥样硬化早期斑块的发生[4]。LPS是革兰氏阴性细菌外膜的主要成分,通过与模式识别受体TLR4(toll-like receptor 4,TLR4)结合形成复合物,激活巨噬细胞;还可以增强血管炎症介质释放,促进动脉粥样硬化发展[5]。基于此,本研究拟通过LPS活化RAW264.7细胞模型,针对影响活化巨噬细胞凋亡的分子机制,探讨防治动脉粥样硬化的策略。结果显示,1 mg·L-1 LPS孵育RAW264.7细胞24 h,可以促进TNF-α、IL-6、COX-2和iNOS的合成,证实了LPS能够活化巨噬细胞,符合文献报道。
凋亡是由基因控制的细胞程序性死亡,涉及凋亡蛋白的激活、表达及调控,目前主要有3条细胞凋亡途径,分别为内质网通路、线粒体通路和死亡受体通路。Fas相关死亡结构域蛋白(fas-associated protein with death domain,FADD)与受体结合后,诱导蛋白质构像改变,暴露死亡域,结合caspase-8形成死亡诱导信号复合物,激活外源性细胞凋亡途径[6]。caspase-3位于执行性凋亡蛋白的最下游,在细胞凋亡中必不可少。文献报道,蛇床子素可以通过调控PI3K/Akt/Bcl-2激活线粒体凋亡途径诱导外阴癌细胞凋亡,抑制癌细胞增殖[7]。向丽萍等[8]研究证实,GEN能够调控miR-21表达,上调CHOP和caspase-3,激活内质网凋亡途径,促进活化巨噬细胞凋亡。课题组前期研究表明,10 μmol·L-1 GEN预孵育RAW264.7细胞2 h能够促进活化巨噬细胞凋亡[8],故我们采用10 μmol·L-1 GEN作用于RAW264.7细胞开展后续实验。本研究显示,GEN可以降低活化巨噬细胞活力,增加凋亡率,并上调caspase-8和caspase-3蛋白表达。这些结果提示,GEN通过外源性凋亡途径促进活化巨噬细胞凋亡可能是其发挥药理作用的机制之一。
TIPE 2是一种先天免疫的负调控因子,在免疫细胞和免疫器官中均表达丰富,可以作为炎性疾病的药物作用靶标,既能够抑制T细胞受体和Toll样受体介导的细胞活化,又能够直接结合caspase-8,促进Fas介导细胞凋亡[9]。Lou等[10]研究显示,氧化低密度脂蛋白(oxidized low-density lipoprotein,ox-LDL)通过下调TIPE 2表达促进动脉粥样硬化,而TIPE 2能够调节巨噬细胞对ox-LDL的反应。Zhang等[11]研究表明,TIPE 2调控p38和ERK1/2激酶信号,抑制血管平滑肌细胞表型转换与增殖,并抑制小鼠颈动脉新生内膜的形成。本实验结果显示,GEN上调活化巨噬细胞TIPE 2表达,而过表达TIPE 2能够促进活化巨噬细胞凋亡,并与GEN具有协同作用。这表明,GEN可能通过上调TIPE 2表达促进活化巨噬细胞凋亡。
Akt是一种丝氨酸/苏氨酸蛋白激酶,通过多个胞外、胞内信号,产生促炎和抗炎细胞因子及吞噬、自噬和凋亡作用,在巨噬细胞生物学和炎性疾病中发挥重要功能。涂献坤等[12]研究表明,丙泊酚可以调节PI3K/Akt信号通路促进神经细胞存活,从而减轻大鼠脑缺血性损伤。另有文献报道,GEN可以调控PI3K-Akt信号通路发挥抗氧化作用,而TIPE 2缺乏将激活Akt,抑制细胞死亡,促进迁移[13-14]。本研究结果显示,过表达TIPE 2抑制活化巨噬细胞Akt磷酸化,且与GEN具有协同作用,这表明GEN对活化巨噬细胞Akt活性的抑制与TIPE 2表达改变有关。
综上所述,我们的研究表明,GEN可能通过上调TIPE 2表达,抑制LPS诱导的RAW264.7细胞Akt磷酸化,进而激活外源性凋亡通路,促使活化巨噬细胞凋亡。调控TIPE 2表达及Akt磷酸化对研究GEN防治动脉粥样硬化具有指导意义,但GEN可能是一种涉及多种药理学作用机制的天然化合物,其促进活化巨噬细胞凋亡的机制仍需进一步研究。
( 致谢: 本实验在湖南师范大学小分子靶向药物研究与创制实验室完成,衷心感谢各位老师及同学对本实验的指导和帮助。)
| [1] |
Santos-Gallego C G. MafB and the role of macrophage apoptosis in atherosclerosis: A time to kill, a time to heal[J]. Atherosclerosis, 2016, 252: 194-6. doi:10.1016/j.atherosclerosis.2016.06.026 |
| [2] |
Zhang Y, Li L, You J, et al. Effect of 7-difluoromethyl-5, 4'-dimethoxygenistein on aorta atherosclerosis in hyperlipidemia ApoE (-/-) mice induced by a cholesterol-rich diet[J]. Drug Des Devel Ther, 2013, 7: 233-42. doi:10.2147/DDDT.S37512 |
| [3] |
Cong L, Yang S, Zhang Y, et al. DFMG attenuates the activation of macrophages induced by coculture with LPC-injured HUVE-12 cells via the TLR4/MyD88/NF-κB signaling pathway[J]. Int J Mol Med, 2018, 41(5): 2619-28. doi:10.3892/ijmm.2018.3511 |
| [4] |
Erbilgin A, Seldin M M, Wu X, et al. Transcription factor Zhx2 deficiency reduces atherosclerosis and promotes macrophage apoptosis in mice[J]. Arterioscler Thromb Vasc Biol, 2018, 38(9): 2016-27. doi:10.1161/ATVBAHA.118.311266 |
| [5] |
Lu Z, Li Y, Brinson C W, et al. Cooperative stimulation of atherogenesis by lipopolysaccharide and palmitic acid-rich high fat diet in low-density lipoprotein receptor-deficient mice[J]. Atherosclerosis, 2017, 265: 231-41. doi:10.1016/j.atherosclerosis.2017.09.008 |
| [6] |
Tummers B, Green D R. caspase-8: regulating life and death[J]. Immunol Rev, 2017, 277(1): 76-89. doi:10.1111/imr.12541 |
| [7] |
董思雨, 卢烨, 赵燕燕, 等. 蛇床子素通过PI3K/Akt通路诱导外阴鳞癌SW962细胞凋亡[J]. 中国药理学通报, 2019, 35(6): 797-802. Dong S Y, Lu Y, Zhao Y Y, et al. Osthole induces apoptosis of vulvar squamous cell carcinoma SW962 through PI3K/Akt signaling pathway[J]. Chin Pharmacol Bull, 2019, 35(6): 797-802. doi:10.3969/j.issn.1001-1978.2019.06.013 |
| [8] |
向丽萍, 丛丽, 张勇, 等. 金雀异黄素调控miR-21表达促进LPS活化的RAW264.7细胞凋亡[J]. 药学学报, 2019, 54(2): 281-7. Xiang L P, Cong L, Zhang Y, et al. Genistein regulates miR-21 to promote the apoptosis in LPS-activated RAW264.7 cells[J]. Acta Pharm Sin, 2019, 54(2): 281-7. |
| [9] |
Sun H, Gong S, Carmody R J, et al. TIPE2, a negative regulator of innate and adaptive immunity that maintains immune homeostasis[J]. Cell, 2008, 133(3): 415-26. doi:10.1016/j.cell.2008.03.026 |
| [10] |
Lou Y, Liu S, Zhang C, et al. Enhanced atherosclerosis in TIPE2-deficient mice is associated with increased macrophage responses to oxidized low-density lipoprotein[J]. J Immunol, 2013, 191(9): 4849-57. doi:10.4049/jimmunol.1300053 |
| [11] |
Zhang G, Zhang W, Lou Y, et al. TIPE 2 deficiency accelerates neointima formation by downregulating smooth muscle cell differentiation[J]. Cell Cycle, 2013, 12(3): 501-10. doi:10.4161/cc.23325 |
| [12] |
涂献坤, 杨滨, 涂德文, 等. PI3K/Akt通路在丙泊酚减轻大鼠脑缺血性损伤中的作用[J]. 中国药理学通报, 2019, 35(5): 630-3. Tu X K, Yang B, Tu D W, et al. Propofol attenuates neuroinflammation and brain damage via modulating PI3K/Akt signaling pathway in rats of focal cerebral ischemia[J]. Chin Pharmacol Bull, 2019, 35(5): 630-3. doi:10.3969/j.issn.1001-1978.2019.05.009 |
| [13] |
Ding W, Chen X, Li W, et al. Genistein protects genioglossus myoblast against hypoxia-induced injury through PI3K-Akt and ERK MAPK pathways[J]. Sci Rep, 2017, 7(1): 5085. doi:10.1038/s41598-017-03484-4 |
| [14] |
Gus-Brautbar Y, Johnson D, Zhang L, et al. The anti-inflammatory TIPE2 is an inhibitor of the oncogenic Ras[J]. Mol Cell, 2012, 45(5): 610-8. doi:10.1016/j.molcel.2012.01.006 |