

2. 邵阳学院附属第二医院,湖南 邵阳 422000
2. The Second Affiliated Hospital of Shaoyang, Shaoyang Hunan 422000, China
胰岛素抵抗(insulin resistance,IR)是2型糖尿病(type 2 diabetes,T2D)的主要特征和前期表现,是多种原因所导致的组织或靶细胞对胰岛素的敏感性和/或反应性降低,表现为外周组织尤其是肝脏、肌肉、脂肪组织等对葡萄糖的摄取和利用障碍。作为胰岛素信号通路中的重要信号分子,Akt(PKB)一方面使糖原合酶激酶(glycogen synthase kinase,GSK)-3β磷酸化(如Ser9)而失活,导致下游的糖原合酶(glycogen synthase,GS)活化,促进糖原的合成[1];同时Akt使叉头框转录因子O1(forkhead box-O1,FoxO1)磷酸化并从细胞核转移至胞质,失去其激活糖异生相关酶基因转录的活性,结果抑制糖异生[2]。研究表明褪黑素(melatonin,MLT)与机体葡萄糖稳态的维持有关[3],如随着年龄的增长褪黑素水平降低,而IR和T2D则呈上升趋势。基于此,本实验诱导建立HepG2 IR细胞模型,以此研究MLT对胰岛素抵抗细胞葡萄糖代谢的影响作用。
1 材料与方法 1.1 材料HepG2细胞株购自中科院上海细胞所;MLT由Neurim Pharmaceuticals公司提供;胎牛血清(FBS)、胰岛素、DAPI等为Sigma公司产品,兔抗人p-Akt(Ser473)(货号:4060s)、p-GSK(Ser9)(9323P)、FoxO1(2880p)及p-FoxO1(Ser256)(9461P)一抗均为CST产品,辣根过氧化物酶标记羊抗兔二抗(sc-2012)购于北京博奥森公司。酶标仪(Millipore公司),荧光倒置显微镜(Nikon公司),凝胶成像系统(Tanon公司)。
1.2 细胞培养与处理HepG2细胞采用L-DMEM (10% FBS)培养液、37℃、5% CO2饱和湿度下培养。待细胞生长到培养瓶底80%左右时进行传代,转入6孔板,并分为对照组(control)和IR模型组(IR),分别以含葡萄糖(5.5 mmol·L-1)或高糖(25 mmol·L-1)高胰岛素(1 μmol·L-1)的DMEM培养24 h;IR组再用含MLT(10 nmol·L-1)或生理盐水的DMEM培养液培养6 h。
1.3 葡萄糖消耗为检测细胞在基础状态和胰岛素刺激下的葡萄糖摄取,各组分别换为含胰岛素(0或100 nmol·L-1)的无血清低糖DMEM培养基培养6 h,各自以未接种细胞的空白孔作对照,葡萄糖氧化酶法检测培养液中葡萄糖含量,计算各组细胞的葡萄糖消耗量。
1.4 糖原含量测定PBS洗涤后用胰酶消化并离心收集各组细胞,按糖原检测试剂盒说明加入碱液300 μL以破坏其他成分而保留糖原,双蒸水定容,加入显色液,沸水浴5 min,冷却后于620 nm波长下测OD值,计算出糖原含量。
1.5 Western blot分析冷PBS漂洗3次后裂解细胞,常规方法提取总蛋白,BCA法定量,沸水中煮5 min后上样电泳分离,转膜,脱脂奶粉室温下封闭2 h,p-Akt、p-GSK、FoxO1、p-FoxO1一抗(1:1 000)4℃孵育过夜,TBST洗膜3次,二抗室温孵育2 h,显影。
1.6 细胞免疫荧光分析将盖玻片置于6孔板,使细胞爬片培养并分组处理,4%多聚甲醛固定,通透10 min(Triton-X100),1% BSA封闭30 min,FoxO1一抗(1:100)4℃过夜,FITC标记二抗(1:100)室温孵育40 min,DAPI避光染核5 min,荧光显微镜下观察拍照。
1.7 统计学分析数据以均数±标准差(x±s)表示,采用单因素方差分析。
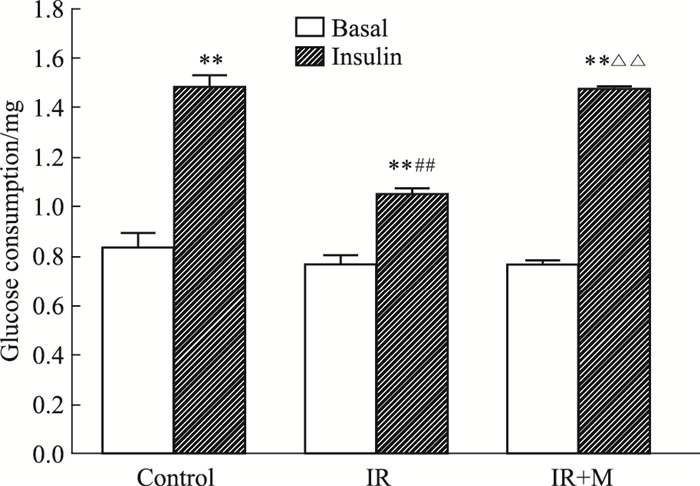
2 结果 2.1 MLT促进IR HepG2细胞葡萄糖的摄入各组细胞葡萄糖的基础摄入(无胰岛素作用)或消耗量无显著差异。胰岛素刺激后,对照组葡萄糖消耗量增加了78%(P < 0.01);IR组细胞糖消耗量虽也有增加,但明显低于对照组P < 0.01,而胰岛素抵抗组经MLT处理后,葡萄糖消耗量较IR组有明显提高(P < 0.01,Fig 1)。
|
| Fig 1 Reversing of glucose consumption by melatonin in IR HepG2 cells(x±s, n=3) **P < 0.01 vs basal; ##P < 0.01 vs control; △△P < 0.01 vs IR |
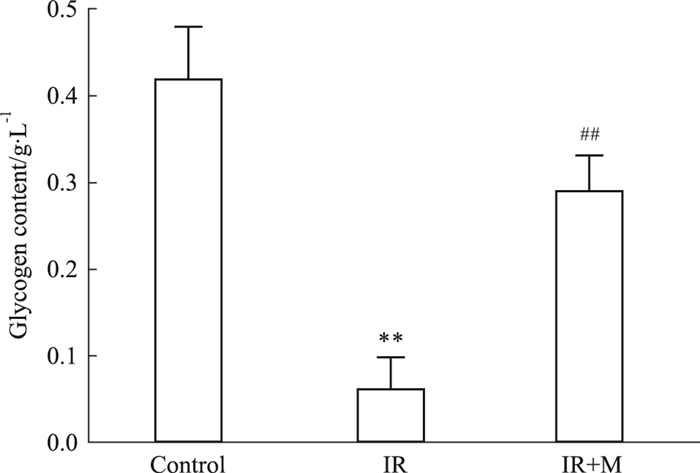
Fig 2显示:IR组细胞糖原含量仅为对照组细胞的14%(P < 0.01),但经MLT处理后其糖原含量明显增加,约为IR组细胞的3倍以上(P < 0.01)。提示MLT能提高胰岛素抵抗状态下细胞的糖原合成。
|
| Fig 2 Effects of melatonin on glycogen synthesis IR HepG2 cells (x±s, n=3) **P < 0.01 vs control; ##P < 0.01 vs IR |
蛋白分析显示:与对照组相比,IR组细胞p-Akt和p-GSK-3β蛋白水平明显降低(P < 0.01),分别降低了约23%和30%;而该胰岛素抵抗模型细胞经MLT处理后,其p-Akt和p-GSK-3蛋白水平分别增加48%和66%(P < 0.01) (Fig 3)。

|
| Fig 3 Effects of melatonin on levels of p-Akt and p-GSK-3β in insulin resistant HepG2 cells (x±s, n=3) *P < 0.01 vs control; #P < 0.01 vs IR |
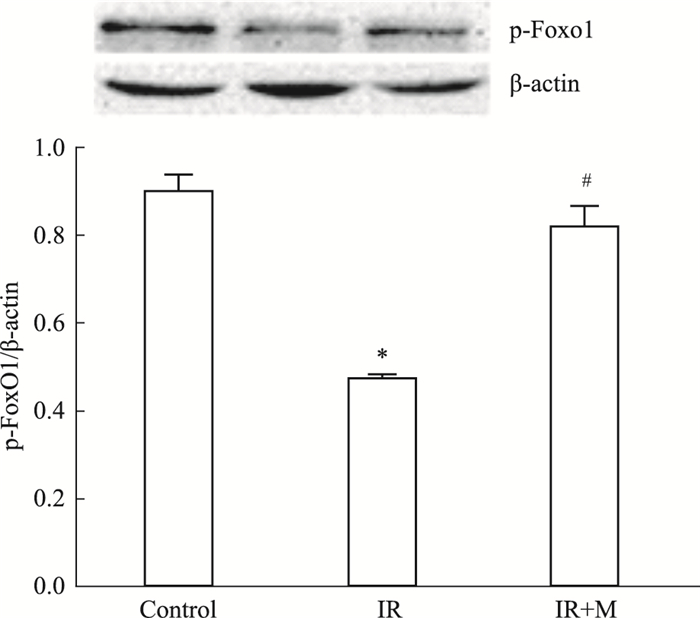
蛋白分析显示(Fig 4):与对照组相比,IR组细胞p-FoxO1蛋白降低近48%,差异明显(P < 0.01);经过MLT处理后,p-FoxO1蛋白水平与IR组细胞相比上调约42%(P < 0.01)。免疫荧光监测则显示胰岛素刺激后,对照组和MLT处理IR细胞胞质中FoxO1蛋白较多,而IR组细胞质FoxO1蛋白则基本无表达(Fig 5)。
|
| Fig 4 Up-regulation of p-FoxO1 by melatonin in insulin resistant HepG2 cells (x±s, n=3) *P < 0.01 vs control; #P < 0.01 vs IR |

|
| Fig 5 Level of FoxO1 in cytoplasm in HepG2 cells(40×) |
肝脏作为胰岛素的重要靶器官,参与了胰岛素对糖、脂、蛋白质的代谢调节,因此肝脏对胰岛素不敏感是IR的重要体现之一。肝细胞以糖原形式对葡萄糖进行储存,同时又通过糖异生作用和糖原分解以补充血糖,即产生内源性葡萄糖。抑制肝细胞葡萄糖的内生是胰岛素调节机体葡萄糖稳态的途径之一,肝胰岛素抵抗时,胰岛素的此抑制作用减弱,以致高分泌量的胰岛素亦无法代偿,最终导致机体糖代谢紊乱[4-6]。本研究中采用高糖高胰岛素培养的HepG2细胞对胰岛素介导的糖摄取减少、糖原合成降低(P < 0.01),说明该细胞对糖的利用能力减弱,提示细胞发生胰岛素抵抗。但研究结果显示褪黑素逆转了高糖高胰岛素的这一作用,提示褪黑素对高糖高胰岛素等胰岛素抵抗高危诱导因素下的肝细胞具有保护作用。
Akt是胰岛素信号通路中的一个重要分子,Akt的活化直接参与了肝脏糖原合成与分解以及糖异生的过程。一方面Akt通过Akt/GSK-3β信号通路调节糖原合成并维持葡萄糖稳态[7]。GSK-3β是一种富含有丝氨酸(Ser)和苏氨酸(Try)的激酶,胰岛素通过PI3K通路可使Akt磷酸化而激活,进而使下游靶蛋白GSK-3β磷酸化而丧失激酶活性,导致糖原合成关键酶GS去磷酸化活化并刺激糖原的合成[1],从而维持机体葡萄糖稳态。本研究发现,经褪黑素处理的IR HepG2细胞p-Akt和p-GSK-3β(Ser9)磷酸化水平明显升高,提示褪黑素可能通过Akt蛋白诱导GSK-3β的磷酸化,进而促进了肝细胞葡萄糖的摄取利用和糖原的合成。
FoxO1是Akt的又一靶蛋白,FoxO1蛋白为Fox转录因子O亚家族成员,是细胞内能量代谢的重要调节因子,同时也是胰岛素信号通路中的关键分子。FoxO1有多个磷酸化位点(如Ser256),胰岛素经PI3K/Akt通路使之磷酸化。磷酸化的FoxO1从细胞核外排至胞质,与受调节基因启动子的解离使其失去转录因子的活性。磷酸烯醇式丙酮酸羧激酶(PEPCK)、葡萄糖-6-磷酸酶(G6pase)是糖异生的两个关键酶,其表达即受FoxO1转录激活[2, 8-9],因此通过PI3K/Akt/FoxO1下调它们的表达是胰岛素抑制糖异生的关键。IR时因PI3K/Akt通路抑制而降低对FoxO1磷酸化的作用,使得糖异生增强,血糖升高。本研究发现MLT可以促进FoxO1蛋白的磷酸化以及FoxO1蛋白从核转出至胞质,同时磷酸化的Akt水平增高,说明MLT可能通过激活Akt/FoxO1信号通路对肝脏糖异生起到抑制作用,从而减少内源性葡萄糖的产生。
综上所述,我们认为褪黑素一方面通过Akt/GSK-3β途径促进肝细胞对葡萄糖的摄取和糖原合成,同时又通过Akt/FoxO1通路抑制肝糖异生,从而改善胰岛素抵抗和参与葡萄糖稳态的调节。
( 本文实验在南华大学医学院完成,所有作者均参与实验设计与实施、数据分析以及论文撰写工作。)
| [1] |
谭婕, 吴建华, 王江平, 等. 2型糖尿病患者糖原合成酶激酶3β的表达及活性[J]. 国际检验医学杂志, 2016, 37(20): 2831-2. Tan J, Wu J H, Wang J P, et al. The protein expression and activity of glycogen synthase kinase 3β in the peripheral blood mononuclear cells of type 2 diabetic patients[J]. Int J Lab Med, 2016, 37(20): 2831-2. doi:10.3969/j.issn.1673-4130.2016.20.011 |
| [2] |
Tsuchiya K, Ogawa Y. Forkhead box class O family member proteins: The biology and pathophysiological roles in diabetes[J]. J Diabetes Investig, 2017, 8(6): 726-34. doi:10.1111/jdi.12651 |
| [3] |
She M, Laudon M, Yin W. Melatonin receptors in diabetes: A potential new therapeutical target?[J]. Eur J Pharmacol, 2014, 744: 220-3. doi:10.1016/j.ejphar.2014.08.012 |
| [4] |
何彦峰, 李刚, 盖祥云, 等. 荭草素抑制3T3-L1前脂肪细胞分化及其改善胰岛素抵抗的作用研究[J]. 中国药理学通报, 2017, 33(9): 1221-6. He Y F, Li G, Gai X Y, et al. Effects of orientin on insulin resistance in 3T3-L1 adipocytes and its mechanism[J]. Chin pharmacol Bull, 2017, 33(9): 1221-6. |
| [5] |
金惠杰, 邱昆成, 李嘉华, 等. 药对知母-黄柏对胰岛素抵抗的改善作用[J]. 中国药理学通报, 2019, 35(7): 1020-4. Jin H J, Qiu K C, Li J H, et al. The improving effect of Zhimu-Huangbai herb pair on insulin resistance[J]. Chin pharmacol Bull, 2019, 35(7): 1020-4. doi:10.3969/j.issn.1001-1978.2019.07.025 |
| [6] |
Lin H V, Accili D. Hormonal regulation of hepatic glucose production in health and disease[J]. Cell Metab, 2011, 14(1): 9-19. doi:10.1016/j.cmet.2011.06.003 |
| [7] |
Hao J, Chen C, Huang K, et al. Polydatin improves glucose and lipid metabolism in experimental diabetes through activating the Akt signaling pathway[J]. Eur J Pharmacol, 2014, 15(745): 152-65. |
| [8] |
Mo F F, Liu H X, Zhang Y, et al. Anti-diabetic effect of loganin by inhibiting FOXO1 nuclear translocation via PI3K/Akt signaling pathway in INS-1 cell[J]. Iran J Basic Med Sci, 2019, 22(3): 262-6. |
| [9] |
Wang Y, Zhou Y, Graves D T. FOXO transcription factors: their clinical significance and regulation[J]. BioMed Res Int, 2014, 2014: 925350. |

