

2. 安徽医科大学基础医学院 生命科学学院,安徽 合肥 230032;
3. 安徽医科大学基础医学院 第一临床学院,安徽 合肥 230032;
4. 安徽医科大学基础医学院 药学院,安徽 合肥 230032
2. Dept of Pharmacology, School of Life Sciences, Hefei 230032, China;
3. Dept of Pharmacology, First Clinical Medical College, Hefei 230032, China;
4. Dept of Pharmacology, School of Pharmacy, Anhui Medical University, Hefei 230032, China
非酒精性脂肪肝病(non-alcoholic fatty liver disease,NAFLD)是一种无过量饮酒史的以肝实质细胞脂肪贮积和脂肪变性为特征的临床病理综合征,近些年文献报道,NAFLD发病率逐年增加[1],目前已成为全球慢性肝病的主要原因,其病因比较复杂,机制尚不清楚,缺少有效的防治措施。目前,NAFLD的治疗主要在抑制脂质累积和肝脏损伤,自噬(autophagy)是被认为是治疗NAFLD的新靶点,细胞自噬可以通过调节脂质代谢,减少氧化应激,改善肝细胞损伤[2]。腺苷一磷酸活化蛋白激酶(AMPK)是一种重要的细胞能量传感器,活性AMPK调控着各种代谢过程,AMPK可以通过磷酸化直接激活细胞自噬[3],在肝脏中,AMPK激活后可以调节肝脏脂质代谢[4]。
丹酚酸B(salvianolic acid B,Sal B)是丹参的根茎中提取的水溶性物质,是丹参提取物中生物活性最强的成分之一,Sal B减轻高脂饮食(high fat diet,HFD)引起的肝损伤、肝脂肪变性、炎症和氧化应激[5],改善NAFLD引起的肝损伤,有文献报道,Sal B能诱导肝癌细胞自噬,加速细胞凋亡保护肝脏[6],在糖尿病模型中,Sal B通过调节AMPK途径预防糖尿病的发生[7]。Sal B对非酒精性脂肪肝病具体机制尚不清楚。
因此,推测Sal B可能通过调控AMPK调节肝脏细胞自噬抑制NAFLD发展,保护肝脏。本实验,采用ApoE-/-小鼠给予高脂饮食建立NAFLD模型,探讨Sal B在NAFLD中对肝脏细胞自噬及其炎症和氧化应激水平的影响,观察Sal B对ApoE-/-小鼠NAFLD的保护作用。
1 材料与方法 1.1 材料 1.1.1 药品与试剂Sal B(批号:PS000276,纯度≥95%)购自成都普思生物科技股份有限公司。ApoE敲除小鼠鉴定所用引物由上海生工技术有限公司合成;Western blot用组织裂解液、蛋白酶抑制剂购自上海碧云天生物科技有限公司;兔抗Beclin1抗体(AF5128)、兔抗p62抗体(AF5384)、兔抗LC3抗体(AF4007)、兔抗AMPK抗体(AF6423)、兔抗p-AMPK抗体(AF3423)、兔抗NF-κB抗体(AF5006)、兔抗Nrf2抗体(AF0639)、山羊抗兔HRP二抗均购自Affinity公司;兔抗IL-6抗体(GB11117)、兔抗TNF-α抗体(GB13188-1)购自Servicebio公司;检测剂盒对天门冬氨酸氨基转移酶(AST)、丙氨酸氨基转移酶(ALT)、总胆固醇(TC)、甘油三酯(TG)和低密度脂蛋白胆固醇(LDL-C)试剂盒(C009-2, C010-2, A110-1, A111-1, A113-1)均购于南京建成生物公司。
1.1.2 实验动物♂,8周龄,C57BL/6J小鼠和ApoE-/-购于南京模式动物中心,许可证号:SCXK(苏)2016-010。
1.1.3 实验仪器梯度PCR仪(美国,Bio-Rad);公司石蜡切片机(RM2255,德国,徕卡);正置荧光显微镜(DM6 B, 德国,徕卡);电子天平(JA1003,上海精密仪器有限公司);酶标仪(Multiskan MK3, 美国,Thermo Labsystems);高速冷冻离心机(Mikro 200R,德国,Hettich);ChemiDocTM MP Imaging System(美国,Bio-Rad)。
1.2 方法 1.2.1 ApoE敲除小鼠基因型鉴定将实验小鼠进行剪尾(约0.3 mm)并放入EP管中,加入150 μL A液(Tab 1)后放入金属铬95 ℃变性45 min,放至室温,然后加入150 μL B液(Tab 1),上下混匀,离心,得上清为总DNA,放入4 ℃保存。之后进行反应体系配置(Tab 2),配置完成后进行PCR扩增,电泳后进行显影并拍照。
| Liquid A | NaOH (160 mg) +EDTA (12 mg)+hyperpure water (200 ml) |
| Liquid B | 1.0 mol·L-1 Tris×HCl (pH 7.5 Tris·HCl) |
| Name | Mix | ddH2O | F | R1 | R2 | DNA | Total |
| Volume | 5 μL | 2.1 μL | 0.3 μL | 0.3 μL | 0.3 μL | 2 μL | 10 μL |
| Name | Primer set |
| ApoE forward primer (F) | 5′-GCCTAGCCGAGGGAGAGCCG-3′ |
| ApoE reverse primer1 (R1) | 5′-TGTGACTTGGGAGCTCTGCAGC-3′ |
| ApoE reverse primer 2 (R2) | 5′-GCCGCCCCGACTGCATCT-3′ |
本实验采用8周龄小鼠18只,经高脂饮食饲养8周,分为3组(每组6只),分别为对照组(WT),模型组(ApoE-/-)和Sal B给药组(ApoE-/-+Sal B),第8周末给药组按照15 mg·kg-1·d-1剂量[8]腹腔注射Sal B,连续给药2周,WT和ApoE-/-组给与等剂量的生理盐水。给药结束后,麻醉小鼠,摘眼球取血液于高速冷冻离心,4 ℃,4 000 r·min-1, 10 min, 得上清;取肝脏组织,进行组织固定、病理检测、蛋白表达检测。
1.2.3 血清指标检测使用试剂盒检测血清中AST、ALT、TC、TG、LDL-C,实验方法按试剂盒(南京建成)说明操作。
1.2.4 苏木精-伊红(Hematoxylin-Eosin, HE)染色、Masson染色切取肝脏组织,4%多聚甲醛溶液固定48 h,脱水,石蜡包埋,4 μm切片,烤片,梯度酒精脱蜡,水化后进行HE染色和Masson染色,染色后常规脱水,透明,干燥,中性树胶封片,显微镜镜检,图像采集分析。
1.2.5 油红O染色切取肝脏组织,固定24 h,蔗糖脱水,OTC包埋,10 μm切片,干燥,固定15 min,自来水洗,油红染液避光浸染8~10 min,蒸馏水洗;75%酒精分化,蒸馏水洗;苏木精染3~5 min,自来水洗,分化,自来水洗,返蓝,流水冲洗,甘油明胶封片,封片后显微镜镜检,图像采集分析。
1.2.6 Western blot检测将收集保存的肝组织进行裂解,变性、电泳、转膜、封闭,兔抗一抗抗体4 ℃孵育过夜,TBST洗膜3次,山羊抗兔HRP二抗室温孵育1 h,TBST洗膜,ECL显影,Image J软件分析。
1.2.7 免疫组化肝脏组织切片,脱蜡脱水,3%H2O2室温避光孵育25 min;PBS洗涤3次,每次5 min;3%BSA室温封闭30 min,倾去封闭液;一抗4 ℃过夜;PBS洗涤3次;生物素标记二抗37 ℃孵育50 min;PBS冲洗3次;辣根酶37 ℃孵育30 min;PBS冲洗3次;DAB显色液显色;自来水充分冲洗,苏木精复染3 min,自来水充分冲洗,脱水、透明、中性树胶封片;显微镜镜检,图像采集分析。
1.2.8 免疫荧光染色肝脏组织切片,常规脱蜡脱水,PBS洗涤3次,每次5 min,免疫荧光封闭液室温封闭30min,倾去封闭液,一抗4℃过夜,PBS冲洗3次,每次5 min,山羊抗兔红色荧光二抗室温避光孵育50 min,PBS冲洗3次;DAPI染色10 min,PBS冲洗3次;滴加防荧光猝灭剂,封片,荧光显微镜镜检,图像采集分析。
1.2.9 统计学处理统计结果用x±s表示,采用SPSS16.0软件对定量资料进行统计学分析,多组之间采用One-way ANOVA进行分析,均数间两两比较采用LSD-t检验。
2 结果 2.1 PCR结果鉴定出小鼠基因型由Fig 1可见,ApoE-/-小鼠的DNA大小为245 bp,而WT小鼠的DNA大小为155 bp。由此确定实验小鼠的基因型。以便后续实验。

|
| Fig 1 Results of genotype detection of mice by PCR genotyping and gene sequencing |
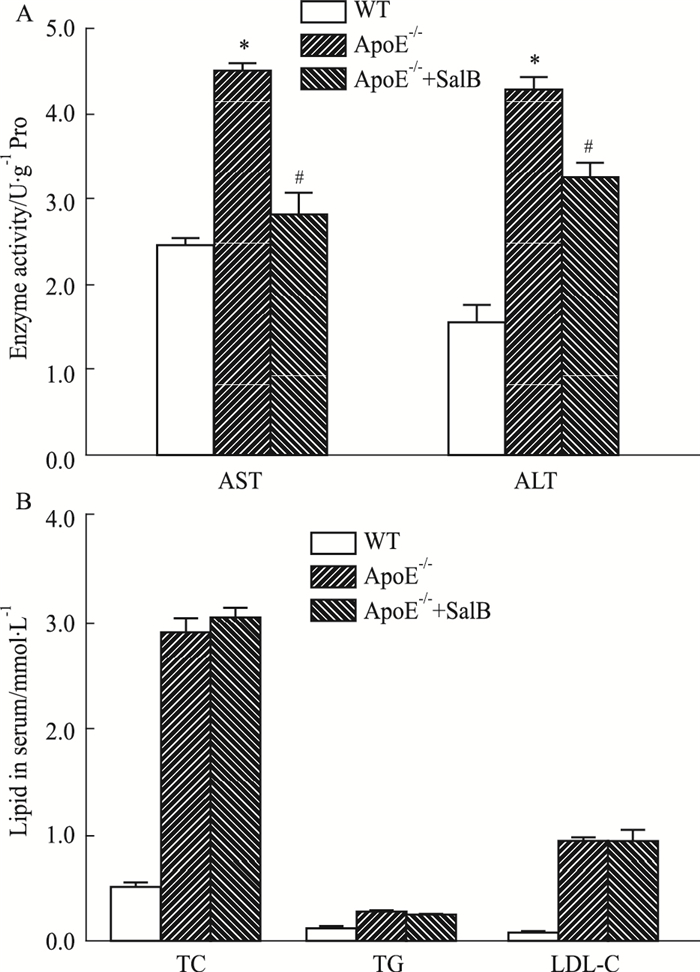
与WT组相比较,ApoE-/-组的AST与ALT指数均明显升高;而Sal B能明显降低ApoE-/-小鼠肝脏中AST与ALT水平(Fig 2A),但对于外周血中TC、TG与LDL-C血脂水平没有影响(Fig 2B)。提示Sal B降低ApoE-/-小鼠AST与ALT得水平,对血液中脂质水平无明显影响。
|
| Fig 2 Biochemical indexes in serum(n=6) A: The activity of AST, ALT in serum; B: The levels of lipid in serum. *P < 0.05 vs WT; #P < 0.05 vs ApoE-/- |
HE染色结果均可见被染成蓝色的细胞核与被染成红色的细胞质(Fig 3A),WT组小鼠肝脏组织结构正常,肝细胞大小均匀,排列规则,形态结构清晰,有少量的空泡;于WT组,ApoE-/-组小鼠肝细胞排列层次紊乱,细胞质可见大量大小不等的圆形脂肪空泡;而与ApoE-/-组相比,ApoE-/-+Sal B组小鼠肝脏的脂肪空泡明显减少,细胞排列层次较规则,形态结构较清晰。表明Sal B改善ApoE-/-小鼠肝脏的损伤。Masson染色结果可见被染成蓝色的胶原纤维与被染成红色的细胞质(Fig 3B),WT组小鼠肝脏组未发现明显的胶原纤维,ApoE-/-组小鼠中出现大量的胶原纤维,并有假小叶形成,ApoE-/-+Sal B组小鼠肝脏胶原纤维明显减少。表明Sal B减少ApoE-/-小鼠肝脏中胶原纤维的表达量。提示,在非酒精性脂肪肝病中,Sal B能够减轻肝脏的损伤,延缓纤维化的发展。

|
| Fig 3 Histological assessments of liver sections (×200, n=6) A: Hematoxylin and Eosin(H & E) staining of liver tissue; B: Oil Red O staining of liver fat; C: Masson trichrome staining of liver tissue |
油红O染色显示(Fig 3C),WT组小鼠肝脏可见少量的橘红色的脂滴,可以清晰地看到被染成蓝色的细胞核;ApoE-/-组小鼠肝脏可见明显的橘红色的脂肪沉积,细胞质内出现大量的脂滴,细胞核不明显;Sal B-ApoE-/-组与ApoE-/-组相比较,橘红色脂滴明显减少,细胞核较为清晰,说明Sal B降低ApoE-/-小鼠肝脏中沉积水平,提示在非酒精性脂肪肝病中,Sal B能够改善ApoE-/-小鼠肝脏中脂质沉积。
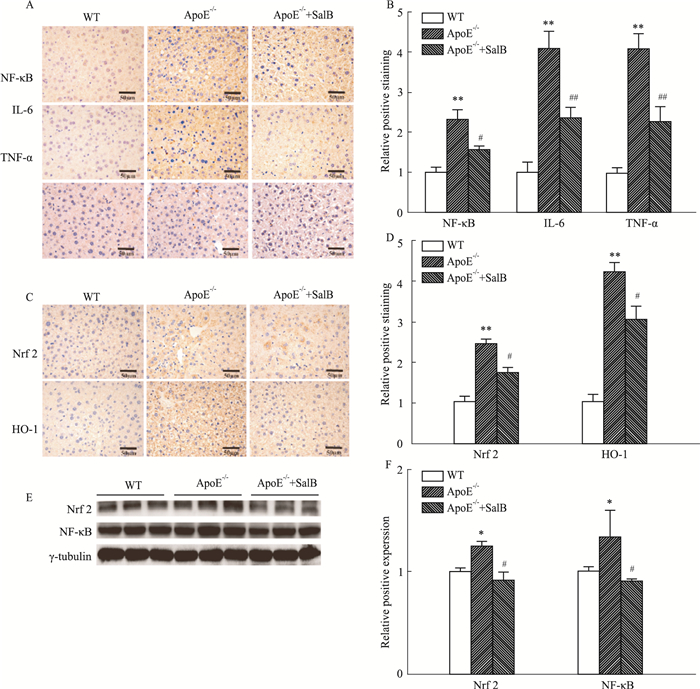
2.5 Sal B减少ApoE-/-小鼠肝脏中NF-κB、IL-6、TNF-α的表达与WT组相比,ApoE-/-组小鼠肝脏中炎症因子NF-κB、IL-6、TNF-α的表达水平明显升高,与ApoE-/-组相比,Sal B-ApoE-/-组小鼠的NF-κB p65、IL-6、TNF-α的表达水平明显降低(Fig 4A, 4B),提示Sal B能够降低ApoE-/-小鼠炎症因子水平。Fig 4E, 4F显示,与WT组相比,ApoE-/-组的NF-κB蛋白表达水平升高,与ApoE-/-组相比,Sal B-ApoE-/-组的NF-κB蛋白表达水平降低,Sal B能够降低NF-κB蛋白表达水平,提示在非酒精性脂肪肝病中,Sal B能够降低肝脏炎症水平,减轻肝脏损伤。
|
| Fig 4 Hepatic inflammation and oxidative stress(×200, n=6) A: Hepatic expression and distribution of NF-κB, IL-6, TNF-α, Nrf2 and HO-1 protein(×200); B: Protein bands of of NF-κB p65, Nrf2and γ-Tubulin; C: Relative protein levels of NF-κB p65 and Nrf2 in the liver(n=6). *P < 0.05 vs WT; **P < 0.01 vs WT; #P < 0.05 vs ApoE-/-; ##P < 0.01 vs ApoE-/-. |
免疫组化结果显示,与WT组小鼠相比,ApoE-/-组小鼠肝脏中Nrf2、HO-1的表达水平明显升高,与ApoE-/-组相比,Sal B-ApoE-/-组小鼠的Nrf2、HO-1的表达水平明显降低(Fig 4B,4C),提示Sal B能够降低ApoE-/-小鼠氧化应激水平。Fig 4E, 4F显示,与WT组相比,ApoE-/-组的Nrf2蛋白表达水平升高,与ApoE-/-组相比,Sal B-ApoE-/-组的Nrf2蛋白表达水平降低,Sal B能够降低Nrf2蛋白表达水平,提示,Sal B能够降低肝脏氧化应激水平。
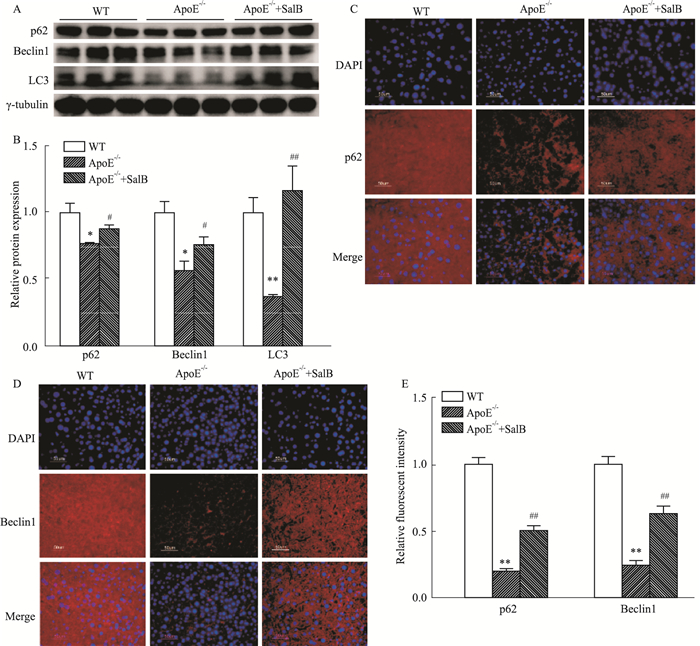
2.7 Sal B对ApoE-/-小鼠肝脏自噬水平的影响Western blot结果显示(Fig 5A, 5B),与WT组小鼠相比,ApoE-/-组小鼠肝脏Beclin1、p62、LC3表达量明显降低,Sal B-ApoE-/-组肝组织中Beclin1、p62、LC3表达量明显升高。免疫荧光显示(Fig 5C, 5D, 5E),与WT组小鼠相比,ApoE-/-组小鼠肝脏Beclin1、p62表达水平明显降低,与ApoE-/-组相比,Sal B-ApoE-/-组小鼠的Beclin1、p62的表达水平升高,Sal B能够升高Beclin1、p62、LC3表达水平,提示Sal B能够增强肝脏自噬水平。
|
| Fig 5 Hepatic autophagy(n=6) A: Protein bands of p62, Beclin-1, LC3 and γ-tubulin; B: Relative protein levels of p62, Beclin-1 and LC3 in the liver; C, D: Hepatic expression and distribution of autophagy proteins (p62 and Beclin-1) by immunofluorescence(400×); E: Relative fluorescence intensity of p62 and Beclin-1 in the liver (n=6). *P < 0.05 vs WT; **P < 0.01 vs WT; # P < 0.05 vs ApoE-/-; ##P < 0.01 vs ApoE-/-. |
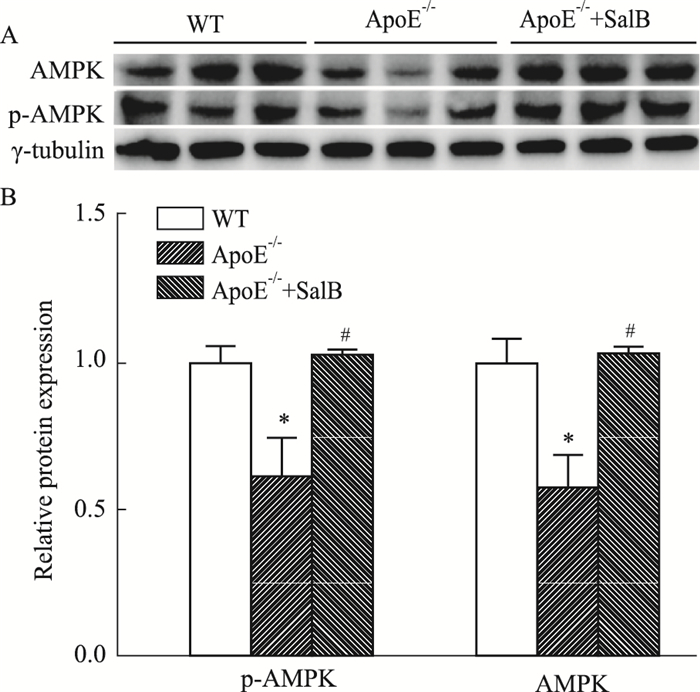
Western blot结果显示(Fig 6A, B),与WT组小鼠相比,ApoE-/-组小鼠肝脏AMPK和p-AMPK表达量明显降低,Sal B-ApoE-/-组肝组织中AMPK和p-AMPK表达量明显升高。提示Sal B能够增强AMPK的表达,促进AMPK磷酸化。
|
| Fig 6 Expression of AMPK and pAMPK(n=6) A: Protein bands of AMPK, p-AMPK and β-tubulin; B: Relative protein levels of AMPK and pAMPK in the liver. *P < 0.05 vs WT; #P < 0.05 vs ApoE-/-. |
ApoE-/-小鼠无论正常或高脂饮食均可形成严重的高脂血症、动脉粥样硬化、脂肪肝等脂质代谢疾病,研究发现高脂饮食可以加速这一过程。研究发现,ApoE-/-小鼠发生NAFLD的进程和人类NAFLD疾病谱非常相似[9],是研究NAFLD发病机制以及筛选药物的良好模型。本实验采用高脂诱导ApoE-/-小鼠,实验结果表明,高脂饮食成功ApoE-/-小鼠形成NAFLD,血清中AST、ALT明显升高,肝脏组织出现大量脂肪空泡和脂滴,脂质沉积明显,胶原纤维增生,肝脏炎症水平和氧化应激水平升高,细胞自噬水平明显降低,具有NAFLD的基本特征。
Sal B是从中药丹参根中分离出的亲水性成分,其含量最丰富、生物活性最强成分之一,具有抗氧化、抗炎、抗纤维化和抗增殖的特性[10]。Sal B能通过调节脂质代谢、抗氧化、抗炎症和抗纤维化抑制NAFLD的发展[11]。实验结果表明,Sal B可以降低ApoE-/-小鼠AST、ALT水平,明显减少肝脏空泡样病变、脂质沉积和胶原纤维,表明Sal B可以减轻小鼠NAFLD引起的肝脏损伤;Sal B明显降低ApoE-/-小鼠肝脏炎症因子(NF-κB p65、IL-6、TNF-α)、Nrf2、HO-1的表达水平,NF-κB是NAFLD损伤发展重要促炎介质,在NAFLD早期被激活,NF-κB的表达可以高效诱导炎症细胞因子(TNF-α、IL-6等)的基因表达,使炎症反应级联放大[12]。核因子NF-E2相关因子(Nrf2)是一种调节多种细胞保护基因表达的主转录因子,可产生抗氧化、解毒和代谢控制酶。当细胞氧化应激时,Nrf2从Keap解离,转移到细胞核,并结合调节几种抗氧化酶(包括HO-1)[13],因此Nrf2的表达水平可以反应细胞氧化应激的程度。Sal B降低了小鼠肝脏的炎症水平和氧化应激水平。
在体外实验中发现,Sal B可以通过AKT/mTOR信号通路诱导肝癌细胞自噬促进凋亡,从而保护肝脏[6]。Sal B可以通过诱导抑郁症大鼠细胞自噬,加强对炎症小体的清除,减轻神经炎症的发生[14]。自噬可以通过调节脂质代谢,减少氧化应激和炎症等途径改善肝细胞肝脏疾病过程中的损伤[2],肝脏富含溶酶体,并具有高水平的代谢应激诱导自噬,肝细胞自噬发生障碍可引起氧化应激和炎症的增加,导致肝脏疾病进一步发展[15]。实验结果表明,Sal B干预后,ApoE-/-小鼠肝脏中Beclin1、p62、LC3的表达水平升高,Beclin1、p62、LC3是自噬小体的生物标记蛋白,反映细胞自噬水平,实验结果表明,Sal B可以增加肝细胞的自噬水平。此外,Sal B干预后,ApoE-/-小鼠肝脏中AMPK和p-AMPK水平明显升高,Sal B可以通过调控AMPK预防糖尿病发生[7],AMPK可以通过磷酸化激活细胞自噬[3],自噬可以通过调节肝细胞脂质代谢,减少肝脏脂质沉积,从而减少脂质过氧化引起的氧化应激[2]。
综上,Sal B可能通过调节AMPK途径,增强ApoE-/-小鼠肝脏自噬水平,减弱肝脏氧化应激和炎症水平,减轻肝脏损伤,进而起到保护肝脏作用。本实验Sal B改善非酒精性脂肪肝病机制研究提供了依据,为临床治疗提供了帮助。
| [1] |
Neuschwander-Tetri B A. Non-alcoholic fatty liver disease[J]. BMC Med, 2017, 15(1): 45. doi:10.1186/s12916-017-0806-8 |
| [2] |
Li X Q, Wang W, Jia Y H, et al. Autophagy and nonalcoholic fatty liver disease[J]. Zhonghua Gan Zang Bing Za Zhi, 2016, 24(8): 632-5. |
| [3] |
Egan D F, Shackelford D B, Mihaylova M M, et al. Phosphorylation of ULK1 (hATG1) by AMP-activated protein kinase connects energy sensing to mitophagy[J]. Science, 2011, 331(6016): 456-61. doi:10.1126/science.1196371 |
| [4] |
Madiraju A K, Alves T, Zhao X, et al. Argininosuccinate synthetase regulates hepatic AMPK linking protein catabolism and ureagenesis to hepatic lipid metabolism[J]. Proc Natl Acad Sci USA, 2016, 113(24): E3423-30. doi:10.1073/pnas.1606022113 |
| [5] |
Zeng W, Shan W, Gao L, et al. Inhibition of HMGB1 release via salvianolic acid B-mediated SIRT1 up-regulation protects rats against non-alcoholic fatty liver disease[J]. Sci Rep, 2015, 5: 16013. doi:10.1038/srep16013 |
| [6] |
Gong L C., Di X. Xia, et al. AKT/mTOR signaling pathway is involved in salvianolic acid B-induced autophagy and apoptosis in hepatocellular carcinoma cells[J]. Int J Oncol, 2016, 49(6): 2538-48. doi:10.3892/ijo.2016.3748 |
| [7] |
Huang M Q, Zhou C J, Zhang Y P, et al. Salvianolic acid B ameliorates hyperglycemia and dyslipidemia in db/db mice through the AMPK pathway[J]. Cell Physiol Biochem, 2016, 40(5): 933-43. doi:10.1159/000453151 |
| [8] |
马滢, 方萌, 伍超, 等. 丹酚酸B调控pSmad3C/pSmad3L发挥抗肝纤维化-肝细胞癌作用[J]. 中国药理学通报, 2018, 34(1): 44-50. Ma Y, Fang M, Wu C, et al. Salvianolic acid B exerts anti-hepatic fibrosis-carcinoma effect via mediation of pSmad3C/pSmad3L[J]. Chin Pharmacol Bull, 2018, 34(1): 44-50. doi:10.3969/j.issn.1001-1978.2018.01.011 |
| [9] |
Schierwagen R L, Maybuchen S, Zimmer, et al. Seven weeks of Western diet in apolipoprotein-E-deficient mice induce metabolic syndrome and non-alcoholic steatohepatitis with liver fibrosis[J]. Sci Rep, 2015, 5: 12931. doi:10.1038/srep12931 |
| [10] |
Chen Y L., Hu C S, Lin F Y, et al. Salvianolic acid B attenuates cyclooxygenase-2 expression in vitro in LPS-treated human aortic smooth muscle cells and in vivo in the apolipoprotein-E-deficient mouse aorta[J]. J Cell Biochem, 2006, 98(3): 618-31. doi:10.1002/jcb.20793 |
| [11] |
Hong M, Li S, Wang N, et al. A biomedical investigation of the hepatoprotective effect of radix salviae miltiorrhizae and network pharmacology-Based prediction of the active compounds and molecular targets[J]. Int J Mol Sci, 2017, 18(3). |
| [12] |
Dela Pena A, Leclercq I, Field J, et al. NF-kappaB activation, rather than TNF, mediates hepatic inflammation in a murine dietary model of steatohepatitis[J]. Gastroenterology, 2005, 129(5): 1663-74. doi:10.1053/j.gastro.2005.09.004 |
| [13] |
Hybertson B M, Gao B. Role of the Nrf2 signaling system in health and disease[J]. Clin Genet, 2014, 86(5): 447-52. doi:10.1111/cge.12474 |
| [14] |
Jiang P Y, Guo R, Da ng, et al. Salvianolic acid B protects against lipopolysaccharide-induced behavioral deficits and neuroinflammatory response: involvement of autophagy and NLRP3 inflammasome[J]. J Neuroinflammation, 2017, 14(1): 239. doi:10.1186/s12974-017-1013-4 |
| [15] |
Ueno T, Komatsu M. Autophagy in the liver: functions in health and disease[J]. Nat Rev Gastroenterol Hepatol, 2017, 14(3): 170-84. doi:10.1038/nrgastro.2016.185 |

