

2. 中国人民解放军南部战区总医院药学部,广东 广州 510010
2. Dept of Pharmacy, General Hospital of Southern Theater Command, PLA, Guangzhou 510010, China
非小细胞肺癌(NSCLC)是最常见的肺癌类型,约占85%[1]。尽管化疗可缓解症状并提高生存率,但NSCLC患者的5年生存率仍然较低[2]。因此急需寻找NSCLC治疗新靶点及副作用较少,可提供更有效的治疗效果的新型抗癌药物。鱼藤素(Deguelin)是一种天然异黄酮类化合物,已被证明具有针对多种癌症的抗肿瘤活性,包括肺癌[3]。因此,本实验以A549细胞为研究对象研究鱼藤素对其体内外增殖的影响,以期为鱼藤素治疗肺癌及其抗肿瘤活性提供新的科学依据。
1 材料与方法 1.1 细胞株人非小细胞肺癌细胞株A549由中国科学院上海生命科学院细胞库提供。
1.2 实验动物SPF级BALB/c裸鼠(♀),3~5周龄,体质量(15~20)g,购自广东省医学实验动物中心,实验动物生产许可证号编号:SCXK(粤)2018-0002,于中国人民解放军南部战区总医院动物实验中心SPF级环境下饲养。
1.3 试剂鱼藤素(deguelin,批号D0817)、二甲基亚砜(DMSO,批号D2650)均购于Sigma公司;胎牛血清、RPMI 1640培养基均购于Gibco公司;胰酶消化液、PBS缓冲液购于Hyclone公司;CCK-8试剂盒(批号CK04)、Annexin V-FITC/PI细胞凋亡检测试剂盒(批号AD10)、细胞周期检测试剂盒(批号C543)均为日本同仁化学研究所产品;Hoechst 33258染色液(批号C1018)、苏木精伊红(HE)染色试剂盒(批号C0105)购于碧云天生物技术研究所。
1.4 实验仪器倒置荧光显微镜(IX7,日本Olympus公司);全波长酶标仪(Multiscan-GO,美国Thermo公司);低温高速离心机(RRESCO 17,美国Thermo公司);流式细胞仪(BD FACSCalibur,美国BD公司);生物组织包埋机(BM-VⅡ);灌胃针(ZC-12,北京哲成科技有限公司);石蜡切片机(CUT4060,德国MICROM);自动脱水机(HP300,深圳达科为医疗设备有限公司)。
2 方法 2.1 药物配制将鱼藤素溶于少量DMSO,配制成100 mmol·L-1母液,分装后置于-20 ℃冰箱避光保存。使用时,用培养基将母液稀释至所需浓度,现配现用。
2.2 细胞培养从细胞库中取出A549细胞,快速融解后于超净工作台中将细胞转移至离心管中,以转速1 000 r·min-1离心5 min,弃上清液,加入2~3 mL完全培养基将细胞吹打均匀,转入培养瓶中,培养于37 ℃、5% CO2的恒温箱中,待细胞密度生长至培养瓶(70~80)%时,进行传代,取对数生长期细胞进行实验。
2.3 CCK-8法将细胞以2×107·L-1接种于96孔板中,每孔100 μL,每组设5个复孔。24 h后,取出细胞已经贴壁的96孔板,弃去旧培养基,加入不同浓度鱼藤素(1.5625、3.125、6.25、12.5、25、50、100 μmol·L-1)分别作用24、48、72 h,对照组仅含细胞及培养基,空白组仅含有培养基。然后每孔加入100 μL 10% CCK-8工作液,完毕后于孵化箱中孵育4 h,于波长为450 nm处的酶标仪测定吸光度(OD)值。计算细胞存活率/% =[(OD实验组-OD空白组)/(OD对照组-OD空白组)]×100%,实验平行重复3次。
2.4 赫斯特染色实验将细胞以1×108·L-1接种于6孔板中,每孔2 mL,均匀分布。24 h后加入不同浓度的鱼藤素(5、10、20 μmol·L-1),作用24 h后将旧培养基吸出,PBS缓冲液洗涤2次,每孔加入1 mL配制好的染色液,静置7~8 min,染色完毕,吸出染色液,随后用PBS缓冲液洗涤2次,加入1 mL新的PBS,置于荧光倒置显微镜下蓝色激发光下拍照。
2.5 Annexin V-FITC/PI双染实验细胞分组给药同“2.4”,药物作用24 h后收集细胞,用冷PBS缓冲液重悬细胞,离心,弃上清液,重悬于500 μL的结合液,再加入5 μL Annexin V-FITC溶液和5 μL PI溶液,吹打混匀,避光孵育15 min,随后转移至流式管中,流式细胞仪测定细胞凋亡率。
2.6 流式细胞术检测细胞周期细胞分组给药同“2.4”,药物作用24 h后收集细胞,用冷PBS缓冲液重悬细胞,离心,弃上清液,滴加1 mL预冷的70%乙醇,置于-4 ℃固定24 h,离心,弃上清液,用冷PBS缓冲液重悬细胞,离心,弃上清液,加入500 μL按试剂盒配置好的工作液,缓慢重悬细胞,于37 ℃孵化箱中避光孵育30 min后,转移至流式管中,立即采用流式细胞仪进行检测。
2.7 裸鼠移植瘤模型裸鼠适应环境1周后,碘伏消毒裸鼠右侧腋下皮肤,注射200 μL制备好的A549细胞悬液,含有1×107个细胞,接种完后每天观察肿瘤生长情况,裸鼠的活动状况。每2 d用游标卡尺测量计算皮下肿瘤体积(V= 0.5×长径×(短径)2),待肿瘤体积达到50 mm3后,将荷瘤裸鼠随机分为4组:对照组(玉米油)、鱼藤素低剂量组(2.5 mg·kg-1)、鱼藤素中剂量组(5 mg·kg-1)、鱼藤素高剂量组(10 mg·kg-1),每组6只,并采用灌胃方式进行给药,剂量为100 kg·L-1,每两天给药1次,每次给药前测定裸鼠移植瘤体积和裸鼠体重,连续给药21 d, 颈椎脱臼处死。将剥离的肿瘤组织按组别及时放进10%的甲醛中固定,用于HE染色切片,于荧光倒置显微镜下观察移植瘤的病理形态学变化情况。
2.8 统计学分析用SPSS 22.0统计软件对数据进行分析,实验数据以x±s表示。
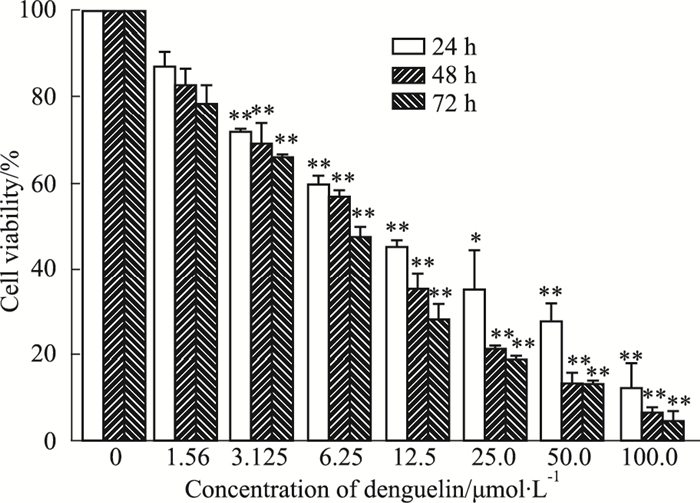
3 结果 3.1 鱼藤素对A549细胞增殖的抑制作用如Fig 1所示。与对照组相比,鱼藤素作用24 h后,随着给药浓度的增加,鱼藤素对A549细胞的增殖抑制作用明显增加,其中鱼藤素作用A549细胞24、48、72 h的半数抑制浓度(IC50),分别为(10.82±1.21)μmol·L-1、(7.11±0.82)μmol·L-1、(5.55±0.42)μmol·L-1。同时,随着鱼藤素处理时间的延长,A549细胞的细胞存活率降低(P < 0.01)。由此可见,与对照组相比,鱼藤素对A549细胞增殖具有抑制作用(P < 0.01),且呈浓度和时间依赖性。
|
| Fig 1 Effects of different concentrations of deguelin on A549 cell viability (x±s, n=3) *P < 0.05, **P < 0.01 vs 0 μmol·L-1 deguelin group |
5、10、20 μmol·L-1鱼藤素作用A549细胞24 h后,赫斯特染色观察其对细胞形态的影响。如Fig 2所示,对照组细胞密集,细胞核呈淡蓝色,少量亮蓝色荧光出现,表明少数细胞核受损,凋亡细胞数少;随着鱼藤素给药浓度的增加,亮蓝色荧光明显增强且数目增多,到达鱼藤素20 μmol·L-1高浓度时,细胞数量减少,细胞核均发出亮蓝色荧光,细胞形态皱缩,说明鱼藤素的作用下能够损伤A549细胞形态。

|
| Fig 2 Morphological effect of deguelin on A549 cells A:Control; B:5 μmol·L-1; C:10 μmol·L-1; D:20 μmol·L-1 |
5、10、20 μmol·L-1鱼藤素作用于A549细胞24 h后,Annexin-V FITC/PI双染结果如Fig 3所示,其具体的凋亡细胞百分比分布见Tab 1。与对照组相比,随着鱼藤素给药浓度的增加,细胞早期凋亡和晚期凋亡以及总凋亡的百分率升高,差异有统计学意义(P < 0.01)。说明鱼藤素能够诱导A549细胞的凋亡,并呈剂量依赖性。

|
| Fig 3 Effect of deguelin on cell apoptosis of A549 cells |
| Deguelin/μmol·L-1 | Control | 5 | 10 | 20 |
| Early apoptotic rate Q4/% | 1.2±0.10 | 2.3±0.37** | 3.2±0.79** | 7.6±0.53** |
| Late apoptotic rate Q2/% | 3.4±0.18 | 10.8±0.40** | 19.7±0.22** | 43.1±0.47** |
| Total apoptotic rate/% | 4.6±0.32 | 13.1±0.33** | 22.9±0.36** | 50.7±1.05** |
| ** P < 0.01 vs control | ||||
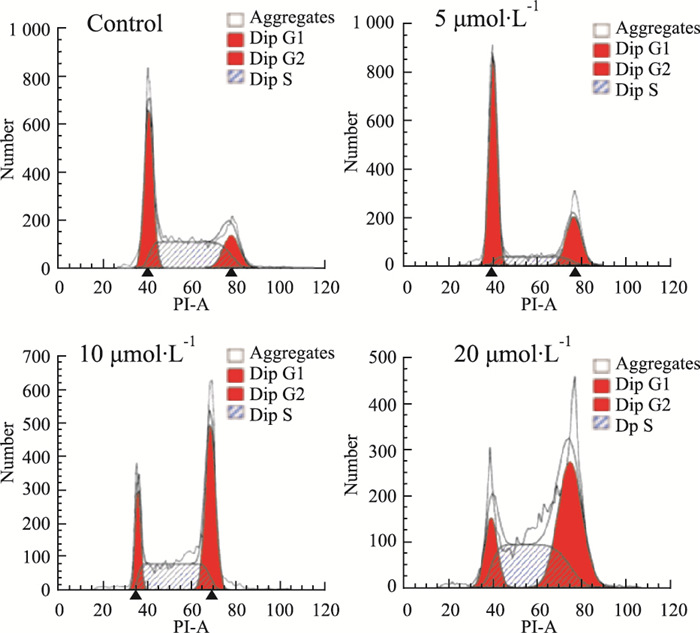
如Fig 4所示,对照组处于G2/M期的细胞百分比为(14.79±0.86)%,而5、10、20 μmol·L-1的鱼藤素处理组中处于G2/M期的细胞百分比分别为(24.91±1.35)%、(44.38±2.21)%、(45.69±1.04)%。因此,同对照组相比,鱼藤素处理组中细胞处于G2/M期的百分比增加(P < 0.01),且呈浓度依赖性,即鱼藤素使A549细胞周期阻滞于G2/M期。
| Deguelin/μmol·L-1 | G0/G1 | S | G2/M |
| Control | 38.29±0.23 | 46.92±0.49 | 14.79±0.86 |
| 5 | 56.60±1.18 | 18.49±0.83 | 24.91±1.35** |
| 10 | 15.03±1.99 | 40.59±1.20 | 44.38±2.21** |
| 20 | 13.37±0.64 | 40.94±1.43 | 45.69±1.04** |
| ** P < 0.01 vs control | |||
|
| Fig 4 Effect of deguelin on cell cycle of A549 cells by flow cytometry |
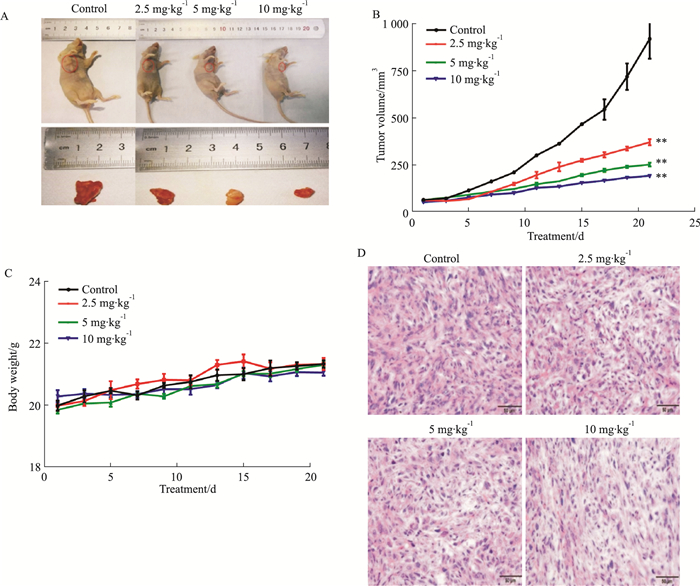
鱼藤素可以抑制A549异种移植模型中的肿瘤生长(Fig 5A),给药21 d后,对照组的肿瘤体积已达到约920 mm3,但在2.5、5、10 mg·kg-1鱼藤素给药组中,平均肿瘤体积分别约为369、251、190 mm3(Fig 5B)。同时,与对照组相比,经过鱼藤素处理的组之间荷瘤小鼠的体质量没有变化,表明鱼藤素没有明显的毒性作用(Fig 5C)。由Fig 5D可知,在空白对照组中,可见细胞密集成片排列,细胞体积较大且不规则、细胞核颜色较深,并且有核分裂。而鱼藤素处理组中可以观察到细胞体积皱缩,排列稀疏,细胞核出现固缩,且随着给药量的增加,变化越明显。由此从肿瘤细胞形态上验证了鱼藤素可抑制移植瘤的增长。
|
| Fig 5 Tumor growth in vivo suppressed by deguelin (n=6) A: Effect of each group of drugs on the gross morphology; B: Tumor volume changes with treatment; C: Tumor weight of each group; D: HE staining of transplanted tumor (×400). *P<0.05, **P < 0.01 vs control. |
鱼藤素是一种天然产物,存在于多种植物物种中,如鱼藤(Derris trifoliata),栓皮豆(Mundulea sericea),毒灰叶(Tephrosia toxicaria),浮氏灰叶(Tephrosia vogelii)和毕澄茄(Pipe cubeba)。近年来研究发现,鱼藤素或通过诱导细胞凋亡,阻滞细胞周期和抗血管生成等方面达到抑制肿瘤增殖的作用[4-6]。本研究以A549细胞为模型,发现鱼藤素能明显提高A549细胞凋亡率,抑制细胞增殖,这与Hsu等[7]研究鱼藤素对肺癌细胞H460的作用结果相似,表明鱼藤素能促进细胞凋亡作用。此外,研究表明鱼藤素可以通过下调H1299细胞中CDK4、CDK6、CCND1基因表达使细胞阻滞在G0/G1期,达到抗肿瘤作用[8],而CDC2与cyclin B复合体正调控G2/M期检查点,促进细胞进入有丝分裂,是推动细胞有丝分裂的关键调节因子[9],因此进一步探讨鱼藤素是否通过调节CDC2与cyclin B复合体相关机制使A549细胞阻滞在G2/M期,相关研究正在进行中。
人体肿瘤裸鼠移植瘤模型可用于研究人类疾病发生机制和生理学特性。Rygaard[10]于1969年首次建立了人结肠癌裸鼠移植瘤模型。目前,裸鼠移植瘤模型已被广泛应用于抗肿瘤药物的筛选中,包括肺癌、乳腺癌、前列腺癌、肝癌、胃癌和结肠癌等[11-13]。近年来,也有通过建立裸鼠移植瘤模型来研究鱼藤素的体内活性的相关报道。Li等[14]于6周龄无胸腺裸鼠右侧皮下接种肺癌细胞(NCI‐H1299)建立模型,肿瘤体积达到100 mm3后,鱼藤素(3 mg·kg-1)给药21 d处死裸鼠。结果表明鱼藤素可通过部分抑制Bmi1和诱导Noxa表达而对移植瘤的生长具有抑制作用。Li等[15]将HepG2细胞(3×106)接种于6周龄♀无胸腺裸鼠右侧皮下,当肿瘤体积接近100 mm3时,随机分组给药,鱼藤素(4 mg·kg-1)每3 d腹腔注射给药1次,接种细胞34 d后采用安乐死并提取肿瘤块,通过平均肿瘤体积和质量对鱼藤素药效进行评价,结果表明同空白对照组相比,鱼藤素明显抑制体内肿瘤生长。本研究通过接种A549细胞建立裸鼠移植瘤模型来评估鱼藤素对非小细胞肺癌细胞的体内抗肿瘤活性,结果表明:鱼藤素可以明显抑制A549细胞裸鼠移植瘤的生长,而对裸鼠没有明显的毒副作用。
综上所述,体内外实验表明,鱼藤素对A549细胞存在抗肿瘤活性,并与诱导细胞凋亡及细胞阻滞相关,为加速开发鱼藤素作为临床抗癌制剂提供理论基础。
( 致谢: 本实验在中国人民解放军南部战区总医院医学实验科和动物实验中心完成,特别感谢实验室老师的指导与帮助。)
| [1] |
Popat S, Mok T, Yang J C, et al. Afatinib in the treatment of EGFR mutation-positive NSCLC——a network meta-analysis[J]. Lung Cancer, 2014, 85(2): 230-8. doi:10.1016/j.lungcan.2014.05.007 |
| [2] |
Goldstraw P, Crowley J, Chansky K, et al. The IASLC Lung Cancer Staging Project: proposals for the revision of the TNM stage groupings in the forthcoming (seventh) edition of the TNM Classification of malignant tumours[J]. J Thorac Oncol, 2007, 2(8): 706-14. doi:10.1097/JTO.0b013e31812f3c1a |
| [3] |
Xu H, Li X, Ding W, et al. Deguelin induces the apoptosis of lung cancer cells through regulating a ROS driven Akt pathway[J]. Cancer Cell Int, 2015, 15(25): 1-9. |
| [4] |
Wang Y, Ma W, Zheng W. Deguelin, a novel anti-tumorigenic agent targeting apoptosis, cell cycle arrest and anti-angiogenesis for cancer chemoprevention[J]. Mol Clin Oncol, 2013, 1(2): 215-9. doi:10.3892/mco.2012.36 |
| [5] |
Suh Y A, Kim J H, Sung M A, et al. A novel antitumor activity of deguelin targeting the insulin-like growth factor (IGF) receptor pathway via up-regulation of IGF-binding protein-3 expression in breast cancer[J]. Cancer Lett, 2013, 332(1): 102-9. doi:10.1016/j.canlet.2013.01.022 |
| [6] |
Nguyen M P, Lee D, Lee S H, et al. Deguelin inhibits vasculogenic function of endothelial progenitor cells in tumor progression and metastasis via suppression of focal adhesion[J]. Oncotarget, 2015, 6(18): 16588-600. |
| [7] |
Hsu Y C, Chiang J H, Yu C S, et al. Antitumor effects of deguelin on H460 human lung cancer cells in vitro and in vivo: Roles of apoptotic cell death and H460 tumor xenografts model[J]. Environ Toxicol, 2017, 32(1): 84-98. doi:10.1002/tox.22214 |
| [8] |
陈彦洁, 柳传毅, 吕满霞, 等. 鱼藤素诱导肺癌细胞凋亡和细胞周期阻滞的分子机制[J]. 中国药理学通报, 2019, 35(8): 1109-14. Chen Y J, Liu C Y, Lyu M X, et al. Molecular mechanism of deguelin-induced apoptosis and cell cycle arrest in lung cancer cells in vitro[J]. Chin Pharmacol Bull, 2019, 35(8): 1109-14. doi:10.3969/j.issn.1001-1978.2019.08.015 |
| [9] |
孙燕, 冯琳迤, 雷蕾, 等. 氯氧喹对不同类型乳腺癌细胞系的抑制作用及机制[J]. 中国药理学通报, 2019, 35(3): 347-52. Sun Y, Feng L Y, Lei L, et al. Inhibitory effect of chloroxoquinoline in different breast cancer cells[J]. Chin Pharmacol Bull, 2019, 35(3): 347-52. doi:10.3969/j.issn.1001-1978.2019.03.011 |
| [10] |
Rygaard J. Immunobiology of the mouse mutant "nude"[J]. Acta Patholo Microbiol Scandinav, 1969, 77(4): 761-2. |
| [11] |
Walsh N C, Kenney L L, Jangalwe S, et al. Humanized mouse models of clinical disease[J]. Annu Rev Pathol, 2017, 12: 187-215. doi:10.1146/annurev-pathol-052016-100332 |
| [12] |
Duan Z, Wei B, Deng J, et al. The anti-tumor effect of ginsenoside Rh4 in MCF-7 breast cancer cells in vitro and in vivo[J]. Biochem Biophys Res Commun, 2018, 499(3): 482-7. doi:10.1016/j.bbrc.2018.03.174 |
| [13] |
Wu Y W, Hsu K C, Lee H Y, et al. A novel dual HDAC6 and tubulin inhibitor, MPT0B451, displays anti-tumor ability in human cancer cells in vitro and in vivo[J]. Front Pharmacol, 2018, 9: 205. doi:10.3389/fphar.2018.00205 |
| [14] |
Li W, Yu X, Xia Z, et al. Repression of Noxa by Bmi1 contributes to deguelin‐induced apoptosis in non-small cell lung cancer cells[J]. J Cell Mol Med, 2018, 22(12): 6213-27. doi:10.1111/jcmm.13908 |
| [15] |
Li M, Yu X, Li W, et al. Deguelin suppresses angiogenesis in human hepatocellular carcinoma by targeting HGF-c-Met pathway[J]. Oncotarget, 2017, 9(1): 152-66. |

