


2. 湖南中医药大学中医药防治眼耳鼻咽喉疾病湖南省重点实验室,湖南 长沙 410208;
3. 湖南中医药大学医学院,湖南 长沙 410208;
4. 湖南中医药大学湖南省中医药防治眼耳鼻咽喉疾病与视功能保护工程技术研究中心,湖南 长沙 410208;
5. 长沙医学院中医学院,湖南 长沙 410219
何迎春(1972-),女,博士,教授,博士生导师,研究方向:中西医结合防治耳鼻咽喉疾病和肿瘤,E-mail:yingchunhe@aliyun.com。
 ,
LIU Jie1,2,
XU Bing-yan1,2,
DAI Na1,2,
HU Mei3,
ZHOU Fang-liang3,4,
SHI Hong-jian2,4,
LUO Jing-jing2,3,
LIN Ting2,4,
HE Ying-chun2,3,4
,
LIU Jie1,2,
XU Bing-yan1,2,
DAI Na1,2,
HU Mei3,
ZHOU Fang-liang3,4,
SHI Hong-jian2,4,
LUO Jing-jing2,3,
LIN Ting2,4,
HE Ying-chun2,3,4
2. Hunan Provincial Key Lab for the Prevention and Treatment of Ophthalmology and Otolaryngology Diseases with Traditional Chinese Medicine, Hunan University of Chinese Medicine, Changsha 410208, China;
3. College of Medicine, Hunan University of Chinese Medicine, Changsha 410208, China;
4. Hunan Provincial Research Engineering Technology Center for the Prevention and Treatment of Ophthalmology and Otolaryngology Diseases with Traditional Chinese Medicine and Visual Function Protection, Hunan University of Chinese Medicine, Changsha 410208, China;
5. College of traditional Chinese Medicine, Changsha Medical University, Changsha 410219, China
益气解毒方是本课题组长期研究的一个复方,由黄芪、黄连、白花蛇舌草、党参、天花粉、茯苓、甘草组成,能够明显改善鼻咽癌患者的气虚体质,有效缓解放化疗带来的不良反应。大量研究表明,益气解毒方水提物能有效抑制鼻咽癌细胞增殖、迁移,诱导细胞凋亡,但其作用机制尚待进一步探讨。研究表明,MAPK/ERK信号通路参与肿瘤细胞多种生物学行为,呈现异常高表达状态[1]。我们前期的研究表明,益气解毒方水提物可以通过下调MAPK/ERK信号通路关键蛋白的表达,阻滞细胞周期,抑制人鼻咽癌CNE2细胞的增殖[2]。那么,它是否能够抑制MAPK/ERK信号通路的活化,从而发挥诱导鼻咽癌细胞凋亡的效应,是本课题研究的重点。本实验以人鼻咽癌CNE1、CNE2细胞为研究对象,用不同浓度益气解毒方水提物干预,观察细胞增殖和凋亡情况,检测CNE1、CNE2细胞中生存凋亡相关蛋白Survivin、XIAP、Bcl-2、Bax及MAPK/ERK信号通路关键蛋白的表达,初步探讨益气解毒方水提物诱导人鼻咽癌细胞凋亡的分子机制,以期为扩大其临床应用提供理论依据。
1 材料 1.1 细胞株人鼻咽癌细胞CNE1(高分化)、CNE2(低分化),购自北京北纳创联生物技术研究院,本实验室传代培养。
1.2 药物与试剂益气解毒方药物组成及水提物的制备主要参考廖雪等[3]的制备方法。RPMI 1640培养基(HyClone公司);胎牛血清(Gibco公司);DMSO(Amresco公司);CCK-8试剂盒(日本同仁公司);Hoechst 33342(翊圣生物科技有限公司);线粒体膜电位检测试剂盒(JC-10)(北京索莱宝);Annexin V-FITC/PI凋亡检测试剂盒(BD公司);MAPK/ERK信号通路蛋白检测盒(CST公司);抗体Survivn、XIAP、Bax、Bcl-2(CST公司)。
1.3 仪器CO2培养箱贺利氏HERAcell 150i(赛默飞世尔公司);ELX800全自动酶标分析仪、CytationTM5细胞成像多功能检测系统(BioTek公司);5415R高速冷冻离心机(Eppendorf公司);荧光倒置光学显微镜及图像采集系统(OLYMPUS公司);荧光双染流式细胞仪Cellometer Image Cytometer(K2)(Nexcelom公司);Odyssey-CLX双色红外荧光成像系统(Gene有限公司)。
2 方法 2.1 细胞培养鼻咽癌CNE1、CNE2细胞用含10%胎牛血清的RPMI 1640培养基培养,置于37 ℃、5% CO2的培养箱内培养,适时传代,取对数生长期的细胞用于实验[2]。
2.2 CCK-8法检测细胞活性分组如下:对照组(Control)、益气解毒方提取物(Yiqi Jiedu Formula extract, YQ)组(0.125、0.25、0.5、1.0 g·L-1)、顺铂组(cisplatin,Cis) 4.0 mg·L-1。取对数生长期的细胞,常规消化,制成每100 μL含3 000个细胞的悬液,种于96孔板中,待细胞贴壁后,弃原培养基,每孔加入200 μL含不同浓度药物的培养基,每个浓度设5个复孔。分别于24、48、72 h后,弃原培养液,每孔加入100 μL CCK-8溶液,孵育1.5 h后,于酶标仪测450 nm处检测吸光度[2]。重复3次。
2.3 Hoechst 33342染色法观察细胞凋亡形态分组如下:Control、YQ(0.25、0.5、1.0 g·L-1)、Cis 4.0 mg·L-1。取对数生长期CNE1、CNE2细胞,常规消化后,种于6孔板中,待细胞贴壁后,加入不同浓度益气解毒方水提物,每个浓度设置3次复孔。处理48 h后,用PBS洗涤2次,每孔加入1 mL 10 mg·L-1的Hoechst 33342染色液,置于培养箱中避光孵育20 min,再用PBS洗涤3次,于荧光倒置显微镜下观察拍照。重复3次。
2.4 线粒体膜电位检测试剂盒(JC-10)检测细胞凋亡分组同“2.3”。取对数生长期CNE1、CNE2细胞,常规消化后种于6孔板中,待细胞贴壁后,加入不同浓度益气解毒方水提物,每个浓度设置3次复孔。处理48 h后,用PBS洗涤2次,吸净残留的PBS后,加入1 mL细胞培养液,再加入1 mL JC-10染色工作液,充分混匀后,在细胞培养箱中静置孵育20 min;同时配制一定体积的JC-10染色缓冲液,置于冰浴盒中;培养箱孵育完成后,用配制好的JC-10染色缓冲液清洗2次,吸净残留的染色缓冲液后,加入2 mL细胞培养液,于Cytation 5观察拍照。重复3次。
2.5 流式细胞术检测细胞凋亡率分组同“2.3”。取对数生长期CNE1、CNE2细胞,常规消化后种于25 cm2培养瓶中,待细胞贴壁长至50%后,加入不同浓度益气解毒方水提物,每个浓度设置3个重复。处理48 h后,用PBS洗涤2次,吸净残留的PBS后,胰蛋白酶(不含EDTA)消化,制成单细胞悬液,收集细胞离心,用PBS洗涤2次,将约1×106个细胞移入离心管中,再次离心收集细胞,加入100 μL 1×Binding Buffer重悬细胞,分别加入5 μL FITC和PI,混匀后避光染色15 min,再加100 μL 1×Binding Buffer终止;取20 μL细胞悬液上机检测。30 min内用流式细胞仪检测凋亡。重复3次。
2.6 Western blot检测相关蛋白表达分组同“2.3”。取对数生长期CNE1、CNE2细胞,常规消化后种于培养皿中,待细胞贴壁后,加入不同浓度益气解毒方水提物,每个浓度设置3个重复。处理48 h后,用PBS洗涤2次,吸净残留的PBS后加入细胞裂解液,冰上裂解30 min。并测定药物组蛋白浓度,取50 μg蛋白上样,电泳、转膜、封闭、敷抗体、显影[2]。检测β-actin、Survivin、XIAP、Bcl-2、Bax、p-c-Raf、p-MEK、p-ERK1/2的表达情况。目的蛋白相对表达量=目的蛋白/β-actin,重复3次。
2.7 统计方法采用SPSS 22.0统计软件处理,计量资料实验数据服从正态分布,用x±s表示,单因素设计,多组间计量资料比较采用单因素方差分析,满足方差齐性,多重比较用LSD检验,方差不齐用Dunnet T3检验。计量资料不服从正态分布的,则采用秩和检验。所有的结果分析图由GraphPad Prism7.0软件制作完成。
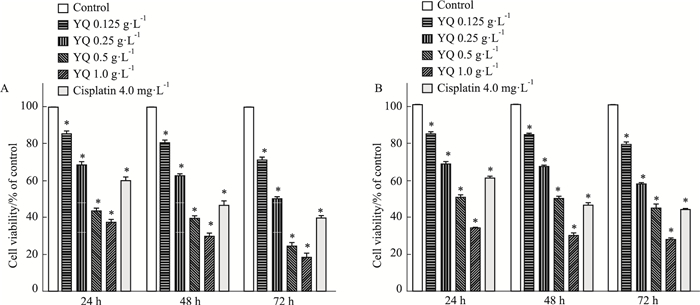
3 结果 3.1 益气解毒方对鼻咽癌细胞活性的影响Fig 1的CCK-8检测结果显示,不同浓度益气解毒方水提物分别处理CNE1、CNE2细胞24、48、72 h后,与对照组相比,CNE1、CNE2细胞的增殖均受到抑制,且随着浓度和时间的增加,其抑制作用更加明显(P<0.05)。
|
| Fig 1 Inhibition of YQ on proliferation of CNE1(A) and CNE2(B) cells by CCK-8 (x±s, n=3) *P < 0.05 vs control |
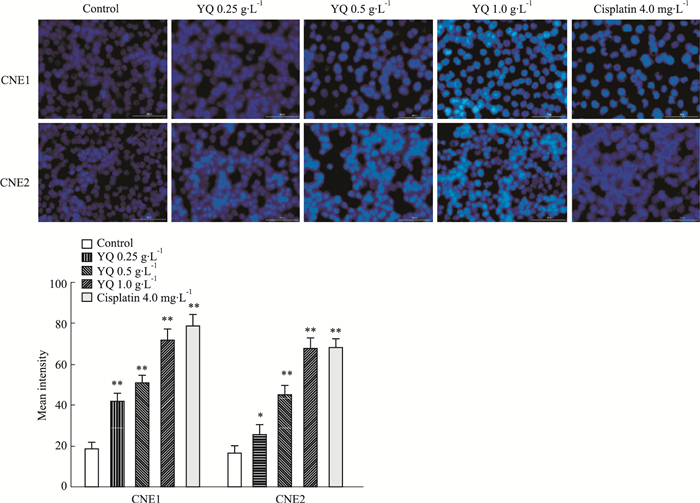
如Fig 2所示,对照组的细胞核呈均匀一致的淡蓝色;不同浓度益气解毒方水提物处理后的细胞出现明显的凋亡特征,即部分细胞核呈颗粒状亮蓝色,同时伴有细胞核的边集、碎裂、皱缩等,且荧光强度逐渐增加;顺铂处理后,细胞核荧光强度增强,有明显的凋亡。对各组荧光强度进行半定量分析,与对照组相比,不同浓度药物组的荧光强度明显增加。
|
| Fig 2 Effect of YQ on apoptosis morphology of CNE1 and CNE2 cells by Hoechst 33342 (scale bar=100 μm) *P < 0.05, **P < 0.01 vs control |
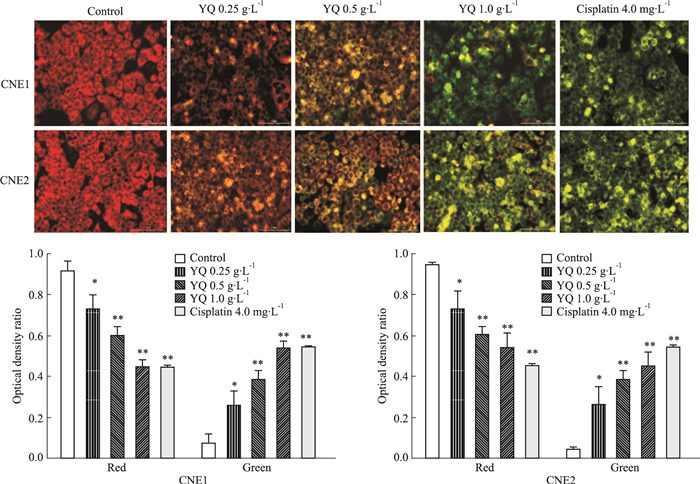
如Fig 3所示,对照组CNE1、CNE2细胞经JC-10染色后,显示红色荧光;不同浓度益气解毒方水提物处理后,CNE1、CNE2细胞出现不同程度的绿色荧光,说明细胞线粒体膜电位下降。用ImageJ对红绿荧光进行光密度分析,并计算各自所占总光密度的比值,结果显示,益气解毒方水提物可以诱导鼻咽癌细胞凋亡。
|
| Fig 3 Effect of YQ on apoptosis of CNE1 and CNE2 cells by JC-10 (scale bar=100 μm) *P < 0.05, **P < 0.01 vs control |
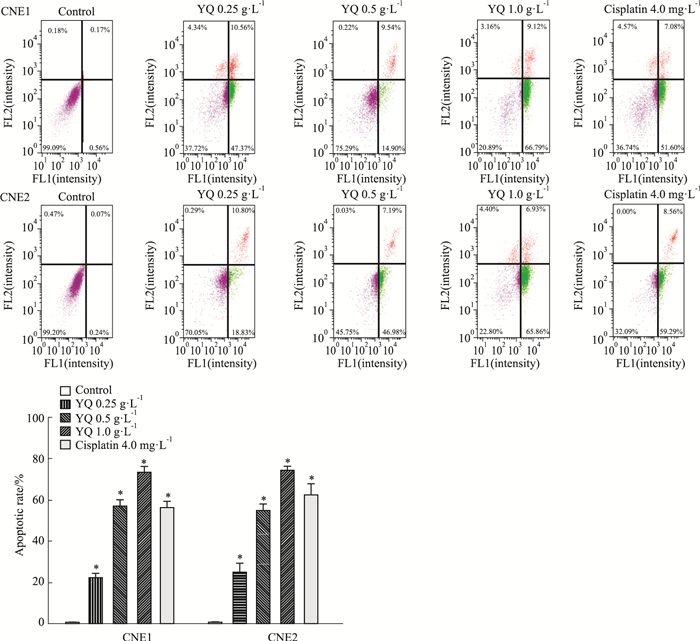
经荧光双染流式细胞仪检测发现(Fig 4),不同浓度益气解毒方水提物作用于CNE1、CNE2细胞48 h后,与对照组相比,益气解毒方水提物各浓度组,CNE1、CNE2细胞凋亡率明显增加(P<0.05),提示益气解毒方水提物可以明显促进CNE1、CNE2细胞凋亡。
|
| Fig 4 Effect of YQ on apoptosis rate of CNE1 and CNE2 cells (x±s, n=3) *P < 0.05 vs control |
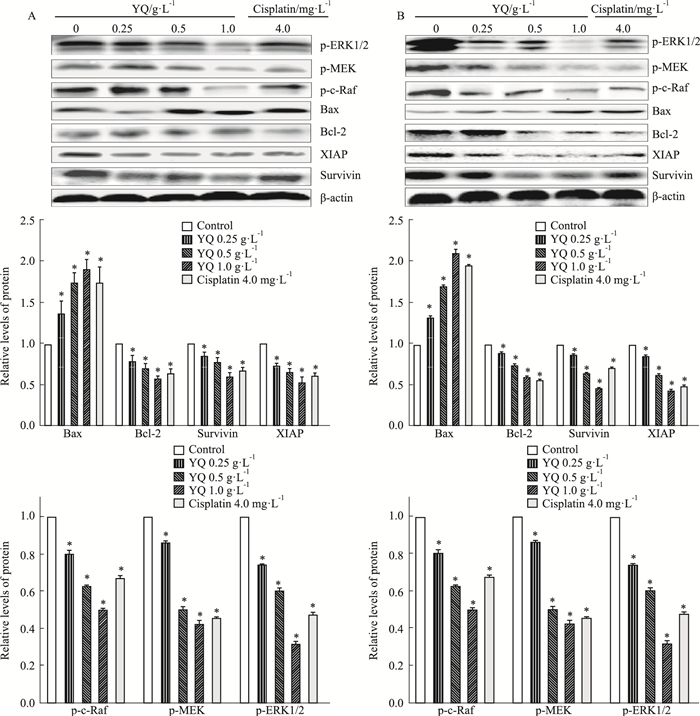
如Fig 5所示,与对照组比较,益气解毒方水提物各浓度组CNE1和CNE2细胞的生存蛋白Survivin、XIAP、抗凋亡蛋白Bcl-2表达均降低,促凋亡蛋白Bax表达上升,MAPK/ERK信号通路关键蛋白p-c-Raf、p-MEK、p-ERK1/2表达明显下降,且差异都具有统计学意义(P<0.05)。
|
| Fig 5 Survival and apoptotic protein and MAPK/ERK signaling pathway key protein expression level in CNE1 (A) and CNE2 (B) cells (x±s, n=3) *P < 0.05 vs control |
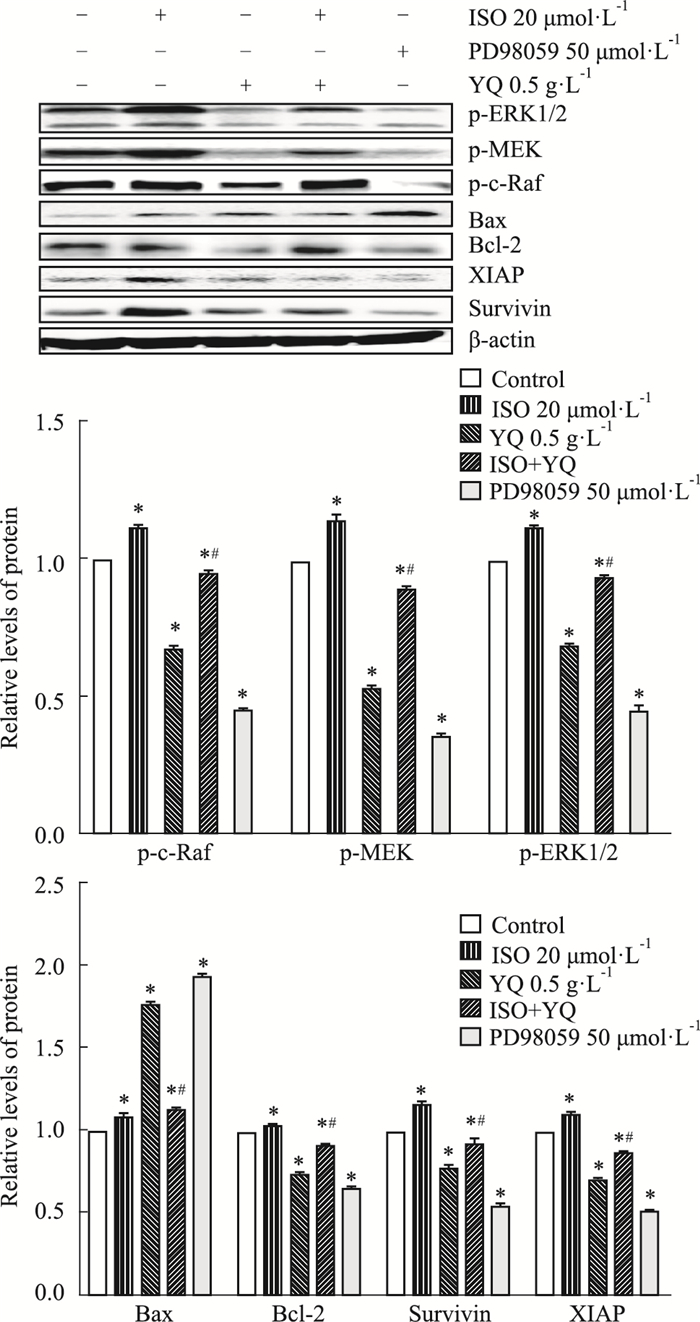
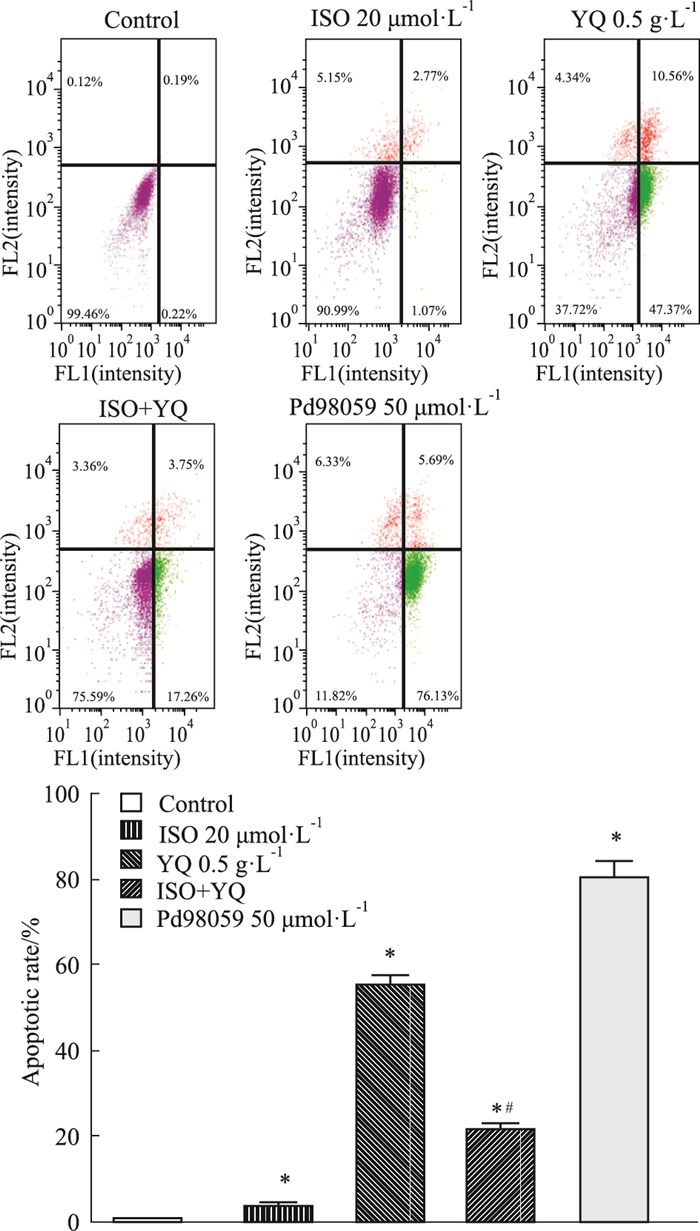
在以上结果的基础上,为了进一步验证益气解毒方水提物是否通过干预MAPK/ERK信号通路发挥诱导凋亡作用,课题组选择鼻咽癌CNE2细胞,加入该通路的激活剂和抑制剂。Fig 6结果显示,与单用益气解毒方水提物组相比,加入激活剂ISO处理CNE2细胞48 h,特异性激活MAPK/ERK信号通路后,关键蛋白p-c-Raf、p-MEK、p-ERK1/2的表达量相对上升;而加入该通路抑制剂PD98059处理CNE2细胞48 h后,该信号通路受到抑制,关键蛋白的表达量均相对下降。同时,加入激活剂ISO和益气解毒方水提物处理CNE2细胞48 h后,与单用益气解毒方水提物相比,其诱导细胞CNE2凋亡的效应降低(Fig 7)。
|
| Fig 6 Related protein expression level in CNE2 by MAPK/ERK signaling pathway activator and inhibitor (x±s, n=3) *P < 0.05 vs control; #P < 0.05 vs YQ group |
|
| Fig 7 Effect of MAPK/ERK signaling pathway activator and inhibitor on YQ induced apoptosis (x±s, n=3) *P < 0.05 vs control; #P < 0.05 vs YQ group |
鼻咽癌是耳鼻咽喉科常见的恶性肿瘤,多发生在我国南方地区[4],其病因可能与EB病毒感染、环境、遗传等因素有关[5-6]。目前治疗以放化疗为主[7],患者5年生存率为40%~60%,并且存在放疗不敏感、化疗耐药等不良反应,所以如何减轻不良反应,是临床治疗中面临的较为棘手的问题。而我国有采用中药治疗鼻咽癌的案例,中药及复方可明显减轻放化疗后副作用,提高机体免疫功能,起到增效减毒的作用[8-10]。实验研究发现,益气解毒方联合同期的放化疗可以明显提高鼻咽癌患者的免疫力和生存率,减轻放化疗毒副反应[11-12]。
细胞的生长情况决定于细胞增殖与凋亡之间的动态平衡,MAPK/ERK信号通路是细胞内重要的促进细胞增殖和抑制细胞凋亡的经典通路,主要是通过调控该通路下游的细胞周期调节相关蛋白和细胞生存凋亡相关蛋白的活性,调节细胞的增殖、分化、凋亡。该通路的异常激活与鼻咽癌、乳腺癌、肝癌等多种肿瘤的发生、发展密切相关[13]。我们前期的研究显示,益气解毒方可以明显抑制鼻咽癌细胞的增殖,可以阻滞细胞于G2/M期,发挥抑瘤作用。MAPK/ERK信号通路在益气解毒方抑制CNE2细胞增殖过程中发挥重要作用,而诱导细胞凋亡也是药物发挥抗肿瘤作用的重要途径,那么益气解毒方是否通过抑制该通路的活化诱导细胞凋亡,值得进一步研究。随着对肿瘤发生机制的进一步研究,发现凋亡在肿瘤疾病中非常关键。从某种角度来说,凋亡不正常可以导致细胞的增殖异常[14]。所以,如何促使细胞凋亡是肿瘤防治的热点和难点,能否有效地促进细胞凋亡,也是抗肿瘤能力评价的关键指标。目前,针对细胞凋亡的检测方法主要有细胞的形态观察、Hoechst 33342细胞核染色法、TUNEL染色法、线粒体膜电位检测、AnnexinV-FITC/PI染色法、电镜等[15]。本研究主要选取了CNE1、CNE2两株细胞,分别采用Hoechst 33342染色法观察细胞核的形态、线粒体膜电位检测试剂盒(JC-10)检测细胞凋亡、Annexin V-FITC/PI双染法检测凋亡情况。Hoechst 33342染色法、JC-10染色法和流式细胞术的结果均显示益气解毒方能诱导鼻咽癌细胞凋亡。
有研究表明,异常活化的ERK可以上调Bcl-2家族抗凋亡成员Bcl-2、Bcl-XL、Mcl-1的表达,从而达到抑制凋亡,促进肿瘤细胞生存的作用;并且ERK还可以通过抑制促凋亡蛋白Bad和Bim的表达,发挥抗凋亡作用。Korfi等[16]运用MEK抑制剂联合Bcl-2家族抑制剂诱导细胞凋亡,发现这种联合效果主要是促凋亡因子Bim磷酸化介导的。本实验主要观察验证益气解毒方作用于人鼻咽癌细胞后,MAPK/ERK信号通路在细胞凋亡中的作用。研究发现,益气解毒方作用于人鼻咽癌细胞后,细胞增殖受到抑制,且作用48 h细胞出现明显凋亡,细胞生存蛋白Survivin、XIAP、抗凋亡蛋白Bcl-2表达均降低,而促凋亡蛋白Bax表达上升,MAPK/ERK信号通路关键蛋白p-c-Raf、p-MEK、p-ERK1/2的表达均明显下调,即抑制MAPK/ERK信号通路活化。益气解毒方对人鼻咽癌CNE1、CNE2细胞的增殖抑制效应和凋亡诱导效果基本平行。在此基础上,为了进一步明确MAPK/ERK信号通路在益气解毒方诱导人鼻咽癌细胞凋亡中的作用,我们选择CNE2细胞株,加入该通路的激活剂和抑制剂,活化和阻断通路。加入激活剂后,p-c-Raf、p-MEK、p-ERK1/2的表达量相对上升,而加入抑制剂后,关键蛋白的表达量相对下降。同时,在该信号通路活化后,生存蛋白Survivin、XIAP、抗凋亡蛋白Bcl-2表达量上升,促凋亡蛋白Bax表达下降,而通路阻断后,生存蛋白Survivin、XIAP、抗凋亡蛋白Bcl-2表达量则下降,促凋亡蛋白Bax表达上升。与直接加水提物比较,先加激活剂ISO再加水提物组p-c-Raf、p-MEK、p-ERK1/2的表达量明显升高,XIAP、Survivn和Bcl-2表达量亦升高,而Bax表达量则相对降低。根据Western blot结果,课题组再次验证其凋亡效应,用流式细胞术检测分别加入MAPK/ERK信号通路激活剂、抑制剂、先加激活剂再加水提物、只加YQ水提物0.5 g ·L-1干预CNE2细胞48 h后,CNE2细胞的凋亡率。结果显示,加入激活剂后,CNE2细胞存在生理情况下的凋亡,加入抑制剂后,CNE2细胞的凋亡率接近80%,YQ水提物组凋亡率在50%左右,而先加激活剂再加水提物组,CNE2细胞凋亡率明显降低(P<0.05),即益气解毒方诱导凋亡的效应被明显削弱,表明MAPK/ERK信号通路在益气解毒方诱导凋亡中发挥重要的作用。抑制MAPK/ERK信号通路的活化,下调Survivin、XIAP、Bcl-2的表达,上调Bax的表达,是益气解毒方诱导人鼻咽癌细胞凋亡效应的重要机制之一。
综上所述,本实验证实了益气解毒方水提物能够诱导人鼻咽癌细胞凋亡,抑制增殖。研究结果表明,益气解毒方水提物主要通过抑制MAPK/ERK信号通路,抑制关键蛋白p-c-Raf、p-MEK、p-ERK1/2的表达,下调Survivin、XIAP、Bcl-2的表达,上调Bax的表达,来诱导人鼻咽癌细胞凋亡。所以,抑制MAPK/ERK信号通路的活化,是益气解毒方发挥抗鼻咽癌作用的重要机制之一,MAPK/ERK信号通路在益气解毒方诱导鼻咽癌细胞凋亡过程中发挥重要作用。
| [1] |
刘伟, 黄玮, 李瑞琴. MAPK/ERK信号传导通路与肿瘤发生的相关机制研究进展[J]. 中国现代医药杂志, 2016, 18(8): 97-100. Liu W, Huang W, Li R Q. Advances in the study of the mechanism of MAPK/ERK signal transduction pathway and tumorogenesis[J]. Med J Chin, 2016, 18(8): 97-100. doi:10.3969/j.issn.1672-9463.2016.08.0033 |
| [2] |
胡晶, 戴娜, 徐冰雁, 等. 益气解毒方通过MAPK/ERK信号通路抑制鼻咽癌细胞增殖[J]. 中国中药杂志, 2018, 43(5): 19-25. Hu J, Dai N, Xu B Y. Effect of Yiqi Jiedu formula on MAPK/ERK signaling pathway of human nasopharyngeal carcinoma CNE2 cells[J]. China J Chin Mater Med, 2018, 43(5): 19-25. |
| [3] |
廖雪, 蔺婷, 罗晶婧, 等. 益气解毒方水提物对RAW264.7细胞免疫功能的影响[J]. 肿瘤基础与临床, 2015(6): 473-6. Liao X, Lin T, Luo J J. Immunomodulating effects of Yiqi Jiedu formula on RAW264.7 cells[J]. J Basic Clin Oncol, 2015(6): 473-6. doi:10.3969/j.issn.1673-5412.2015.06.004 |
| [4] |
Wei K R, Zheng R S, Zhang S W, et al. Nasopharyngeal carcinoma incidence and mortality in China, 2013[J]. Chin J Cancer, 2017, 36(1): 90. doi:10.1186/s40880-017-0257-9 |
| [5] |
Liu Z, Chang E T, Liu Q, et al. Quantification of familial risk of nasopharyngeal carcinoma in a high-incidence area[J]. Cancer, 2017, 123(14): 2716-25. doi:10.1002/cncr.30643 |
| [6] |
Baizig N M, Morand P, Seigneurin J M, et al. Complementary determination of Epstein-Barr virus DNA load and serum markers for nasopharyngeal carcinoma screening and early detection in individuals at risk in Tunisia[J]. Eur Arch Otorhinolaryngol, 2012, 269(3): 1005-11. doi:10.1007/s00405-011-1717-5 |
| [7] |
De A C H. Intensity-modulated radiation therapy for head and neck cancer: systematic review and meta-analysis[J]. Radiotherapy Oncology, 2014, 110(1): 9-15. doi:10.1016/j.radonc.2013.11.010 |
| [8] |
吴新正, 何迎春, 田道法, 等. 中药防治癌前病变现状及其机制[J]. 中草药, 2006, 37(7): 1101-4. Wu X Z, He Y C, Tian D F. Status and mechanism of controlling precancerous lesions with Chinese materia medica[J]. Chin Tradit Herb Drugs, 2006, 37(7): 1101-4. doi:10.3321/j.issn:0253-2670.2006.07.058 |
| [9] |
朱道琦, 黄沐, 刘钊汝, 等. 姜黄素对鼻咽癌抗拒株的放射增敏作用及其机制研究[J]. 中国药理学通报, 2017, 33(8): 1086-91. Zhu D Q, Huang M, Liu Z R, et al. Effect of curcumin on radiosensitization of radioresistant nasopharyngeal carcinoma cell line CNE-2R and its mechanism[J]. Chin Pharmacol Bull, 2017, 33(8): 1086-91. doi:10.3969/j.issn.1001-1978.2017.08.010 |
| [10] |
王磊, 梁杰, 阿提坎·卡吾力, 等. 复方苦参注射液治疗鼻咽癌放射性口腔黏膜损伤疗效观察[J]. 中草药, 2015, 46(6): 875-7. Wang L, Liang J, ATIKAN Kwuli, et al. Observation of curative effect of Compound Sophorae Injection on treatment of radioactive oral mucosa injury with nasopharyngeal carcinoma[J]. Chin Tradit Herb Drugs, 2015, 46(6): 875-7. |
| [11] |
李梅芳, 余丽亚, 吴新正, 等. 益气养阴解毒方影响鼻咽癌患者放化疗后康复过程的临床疗效观察[J]. 中国中西医结合耳鼻咽喉科杂志, 2013, 21(1): 29-32. Li M F, Yu Y L, Wu X Z, et al. Effect of Yiqi Yangyin Jiedu Recipe on the rehabilitation of nasopharyngeal carcinoma patients after radiotherapy and chemotherapy[J]. Chin J Otorhinolaryngol Integr Med, 2013, 21(1): 29-32. doi:10.3969/j.issn.1007-4856.2013.01.007 |
| [12] |
穆光锐. 益气解毒方联合同期放化疗对局部晚期鼻咽癌患者T淋巴细胞亚群及生存率的影响[J]. 现代中西医结合杂志, 2016, 25(24): 2701-3. Mu G R. Effect of Yiqi Jiedu Recipe combined with concurrent radiotherapy and chemotherapy on T lymphocyte subsets and survival rate in patients with locally advanced nasopharyngeal carcinoma[J]. Mod J Integr Tradit Chin West Med, 2016, 25(24): 2701-3. doi:10.3969/j.issn.1008-8849.2016.24.029 |
| [13] |
Wang L H, Li Y, Yang S N, et al. Gambogic acid synergistically potentiates cisplatin-induced apoptosis in non-small-cell lung cancer through suppressing NF-κB and MAPK/HO-1 signalling[J]. Br J Cancer, 2014, 110(2): 341. doi:10.1038/bjc.2013.752 |
| [14] |
Goldar S, Khaniani M S, Derakhshan S M, et al. Molecular mechanisms of apoptosis and roles in cancer development and treatment[J]. Asian Pac J Cancer Prev, 2015, 16(6): 2129-44. doi:10.7314/APJCP.2015.16.6.2129 |
| [15] |
吕莹, 张德禄, 张宏, 等. 细胞凋亡检测方法研究进展[J]. 西北师范大学学报(自然科学版), 2007, 43(2): 82-7. Lyu Y, Zhang D L, Zhang H, et al. Progress on research method of cell apoptosis[J]. J Northwest Normal Univ (Natural Sci), 2007, 43(2): 82-7. doi:10.3969/j.issn.1001-988X.2007.02.020 |
| [16] |
Korfi K, Smith M, Swan J, et al. BIM mediates synergistic killing of B-cell acute lymphoblastic leukemia cells by BCL-2 and MEK inhibitors[J]. Cell Death Dis, 2016, 7(7): e2177. |