


2. 河北医科大学基础医学院病理学教研室,河北 石家庄 050017
2. Dept of Pathology, Hebei Medical University, Shijiazhuang 050017, China
系膜细胞增殖及细胞外基质增生是肾小球疾病进展的主要原因,目前血小板衍生生长因子(platelet-derived growth factor,PDGF)与增殖性肾炎发病的关系已经被广泛证实[1-2]。新近的研究显示,在血管平滑肌细胞中,PDGF可以诱导periostin表达[3],而细胞间基质蛋白periostin与细胞增殖关系密切[4],并在细胞外基质代谢中发挥重要作用[5]。PDGF促进系膜细胞增殖及细胞外基质增生的作用是否通过periostin起作用,目前未见报道。
本研究以小鼠系膜细胞(mouse mesangial cell,MMC)为研究对象,PDGF为刺激物,以增殖细胞核抗原(proliferating cell nuclear antigen,PCNA)作为细胞的增殖指标,以纤连蛋白(fibronectin,FN)和转化生长因子-β1(transforming growth factor-β1,TGF-β1)作为细胞外基质合成的指标,通过观察PDGF刺激下periostin的表达及其与系膜细胞增殖、细胞外基质合成的关系,并构建periostin沉默质粒转染至小鼠系膜细胞内,观察转染periostin沉默质粒能否起到干预作用,为肾小球疾病进展的病因研究和靶向治疗提供新的思路。
1 材料 1.1 细胞株MMC购自中国科学院上海生科院细胞资源中心。
1.2 试剂兔抗periostin多克隆抗体(ab152099),购自英国Abcam公司;兔抗FN多克隆抗体(15613-1-AP)、兔抗PCNA多克隆抗体(10205-2-AP)、TRITC-猴抗兔IgG,均购自美国Proteintech公司;兔抗TGF-β1多克隆抗体、兔抗β-actin单克隆抗体,均购自美国Epitomics公司,pYr-adshuttle-4empty vector、pYr-ads-4-POSTON vector,购自长沙赢润生物有限公司;重组鼠PDGF-BB(315-18),购自美国PeproTech公司。
1.3 仪器高速低温离心机(德国Eppendorf公司);相差倒置显微镜、荧光显微镜(日本Olympus公司);CO2培养箱(日本SANYO公司)。
2 方法 2.1 MMC细胞培养与实验分组用含10%胎牛血清的DMEM/F12(3:1)培养基常规培养小鼠系膜细胞。①细胞以6孔板培养24 h后,换含10 μg·L-1 PDGF刺激物的培养基,孵育细胞0、2、4、6、12 h,收集细胞进行免疫荧光化学染色和细胞总蛋白提取。② Lipofectamine 2000分别转染pYr-ads-4-POSTON vector及pYr-adshuttle-4empty vector空质粒,转染后的细胞进行G418(800 mg·L-1)抗性筛选,传代培养筛选出阳性克隆细胞。同步化后的细胞随机分为control组、PDGF组、PDGF+空质粒转染(PDGF+sh-nc)组和PDGF+ periostin沉默质粒(PDGF+sh-periostin)组。后3组细胞以10 μg·L-1 PDGF孵育6 h后终止培养,收集细胞,分别提取细胞总蛋白,进行免疫荧光化学染色。
2.2 Western blot检测蛋白表达收集各组细胞并加入冰冷的裂解液200 μL,提取总蛋白。采用考马斯亮蓝法测定蛋白浓度,分装后-80 ℃保存。50 μg蛋白样品,加入加样缓冲液,沸水变性5 min,10% SDS-PAGE凝胶电泳湿转至PVDF膜;5%脱脂奶粉37 ℃封闭2 h;5%脱脂奶粉稀释一抗,periostin、PCNA、FN、TGF-β1及β-actin抗体(稀释比例1:1 000)4 ℃过夜。TBST洗膜后,加辣根过氧化物酶标记的羊抗兔IgG(1:5 000稀释),37 ℃孵育1 h;TBST洗膜,滴加ECL增强化学发光试剂,Odyssey FC成像系统显像。用美国UVP公司LabWorks 4.5软件对条带进行分析,读取积分光密度值(integrated option density,IOD),目的蛋白条带的IOD值除以β-actin条带的IOD值,进行统计学分析。
2.3 荧光细胞化学检测细胞采用6孔板爬片,培养终止后,细胞用4 ℃生理盐水冲洗2次,4%多聚甲醛固定10 min,PBS冲洗3次,每次5 min;0.5% Triton X-100 37 ℃打孔10 min,PBS冲洗,每次5 min,共3次;正常山羊血清封闭,37 ℃孵育1 h;弃封闭液,滴加1:200稀释的periostin一抗,4 ℃过夜;PBS冲洗,每次5 min,共3次; 滴加TRITC标记猴抗兔IgG,37 ℃孵育1 h;PBS冲洗,每次5 min,共5次; 滴加DAPI(1:100配制),37 ℃孵育10 min;PBS冲洗,每次5 min,共5次;荧光显微镜下观察并摄取图像。
2.4 统计学分析计量资料以x±s表示,采用SPSS 13.0统计软件进行分析,组间比较采用方差分析。
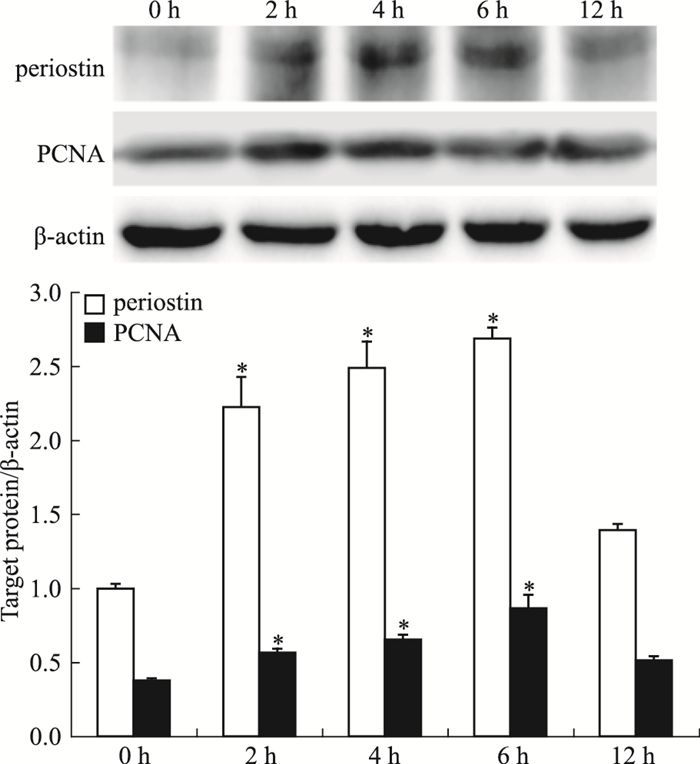
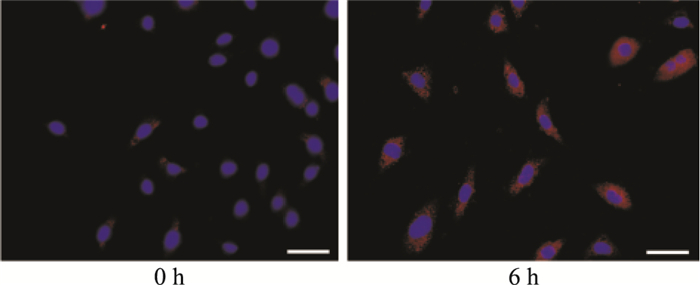
3 结果 3.1 PDGF诱导periostin蛋白高表达10 μg·L-1 PDGF刺激MMC后,periostin蛋白表达明显升高。Fig 1的Western blot结果显示,刺激2 h后periostin水平开始升高,6 h达到高峰,表达上调2.69倍,12 h明显回落。同样Fig 2的细胞免疫荧光结果显示,PDGF刺激后periostin的表达明显增强,主要定位在胞质,而在0 h组,periostin仅在胞质有微弱表达。
|
| Fig 1 1 Expression of periostin and PCNA protein in MMC stimulated by PDGF detected by Western blot (x±s, n=3) *P < 0.05 vs 0 h group |
|
| Fig 2 Expression of periostin protein in MMC stimulated by PDGF detected by immunofluorescence (scale bar: 50 μm) Blue: DAPI staining. |
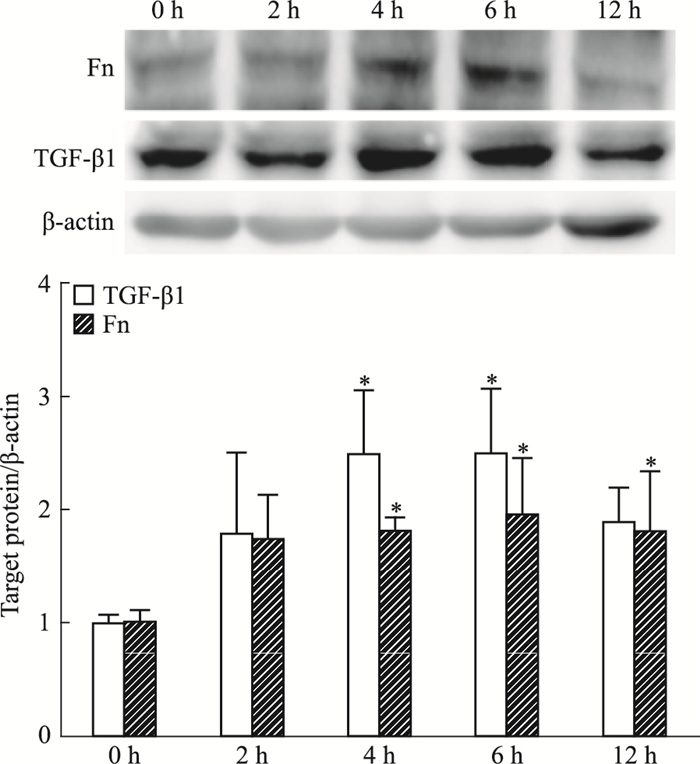
10 μg·L-1 PDGF刺激MMC后,PCNA蛋白表达明显升高,Fig 1的Western blot结果显示,刺激2 h后PCNA开始升高,6 h达到高峰,表达上调2.31倍,12 h明显回落。Fig 3结果显示,PDGF刺激后,FN、TGF-β1蛋白的表达明显上调,刺激4 h后,FN、TGF-β1蛋白的表达明显增加,6 h达高峰,分别较0 h组升高2.31、2.50倍。
|
| Fig 3 Expression of FN, TGF-β1 protein in MMC stimulated by PDGF detected by Western blot (x±s, n=3) *P < 0.05 vs 0 h group |
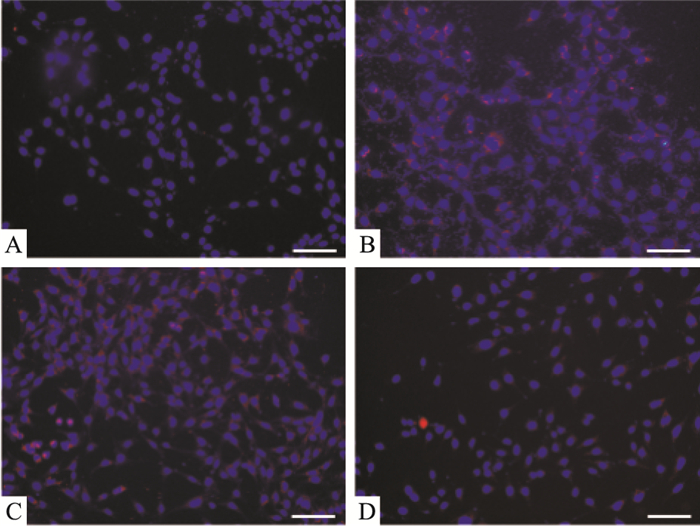
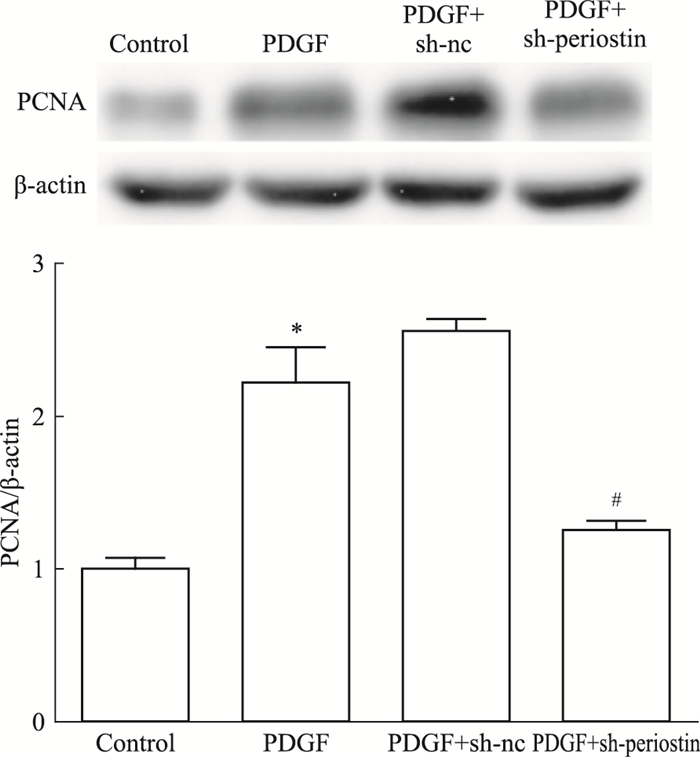
质粒转染后,Fig 4的Western blot结果显示,与PDGF刺激的未转染组和转染空质粒组比较,转染sh-periostin沉默质粒(pYr-ads-4-POSTON vector)使periostin的蛋白表达明显下降,较空质粒组下降60.40%。同样Fig 5细胞免疫荧光结果显示,与转染空质粒组比较,转染sh-periostin沉默质粒组periostin蛋白的胞质表达明显减少。Western blot进一步检测了质粒转染并给予PDGF刺激后PCNA的蛋白表达,结果PCNA表达明显下降,较空质粒组降低47.74%(Fig 6)。

|
| Fig 4 Expression of periostin protein in transfected sh-periostin vector MMC stimulated by PDGF detected by Western blot (x±s, n=3) *P < 0.05 vs control group; #P < 0.05 vs PDGF+sh-nc group |
|
| Fig 5 Expression of periostin protein in transfected sh-periostin vector MMC stimulated by PDGF detected by immunofluorescence (scale bar: 100 μm) A:Control; B: PDGF; C: PDGF+sh-nc; D: PDGF+sh-periostin. Blue: DAPI staining. |
|
| Fig 6 Expression of PCNA protein in transfected sh-periostin vector MMC stimulated by PDGF detected by Western blot (x±s, n=3) *P < 0.05 vs control group; #P < 0.05 vs PDGF+sh-nc group |
Western blot进一步检测了质粒转染并给予PDGF刺激后FN和TGF-β1的蛋白表达。如Fig 7所示,与PDGF刺激的未转染组和转染空质粒组比较,FN、TGF-β1的蛋白表达明显降低,分别下降57.77%、50.41%。

|
| Fig 7 Expression of FN, TGF-β1 protein in transfected sh-periostin vector MMC stimulated by PDGF detected by Western blot (x±s, n=3) *P < 0.05 vs control group; #P < 0.05 vs PDGF+sh-nc group |
PDGF作为目前已知多肽生长因子中最强的有丝分裂原,与多种细胞增殖密切相关[6-7],其过度表达与肾脏疾病的关系已被大量的实验所证实。PDGF可以刺激系膜细胞及单核巨噬细胞增殖、转型,并进一步刺激细胞外基质的产生[1-2]。近来的研究显示,PDGF可以诱导periostin在血管平滑肌细胞中的表达[3],在系膜细胞中,PDGF能否诱导periostin的表达少见研究。最近,periostin在肾脏疾病中的作用受到越来越多的关注,PDGF促进系膜细胞增殖及细胞外基质增生的作用是否与periostin有关,尚未见报道。本实验Western blot与免疫荧光的结果显示,PDGF上调periostin蛋白表达,同时使PCNA和FN、TGF-β1的蛋白表达明显升高,表明PDGF上调系膜细胞增殖和细胞外基质合成水平,可能与上调periostin蛋白表达有关。
Periostin是细胞间基质蛋白的一种[8],是αvβ1、β3、β4和β5整合素的配体。大量研究显示,periostin与细胞增殖、分化、黏附等关系密切,periostin在多囊肾的囊壁上皮细胞过表达,能够促进囊壁上皮细胞增殖,periostin敲除鼠与periostin(+/+)鼠相比,肾细胞增殖减轻,肾囊数目和总的囊面积减少,生存期明显延长[9]。periostin在细胞外基质的代谢中也发挥重要作用,与多种组织纤维化有关[10-11]。肾小管上皮细胞给予periostin刺激后,Ⅰ型胶原表达增加[12]。野生型单侧输尿管闭塞模型鼠梗阻侧肾脏periostin的表达、合成和肾损伤进行性增加,periostin敲除鼠则显示肾脏纤维化减轻,结构改善[13]。由缺氧或缺血引发的急性肾损伤小鼠,periostin通过p38 MAPK途径促进肾脏纤维化[14]。
为了进一步探讨PDGF引起的系膜细胞增殖和细胞外基质合成增加是否确实与上调periostin相关,我们转染了periostin沉默质粒,发现与PDGF刺激的未转染组和转染空质粒组比较,转染sh-periostin质粒组periostin的蛋白表达下降,同时PCNA、FN、TGF-β1蛋白表达明显减弱,提示periostin沉默质粒能够逆转PDGF引起的系膜细胞PCNA、FN、TGF-β1蛋白表达,PDGF引起的系膜细胞增殖和细胞外基质产生通过periostin起作用。
我们下一步的研究将在体外实验的基础上,将periostin沉默质粒转染至增殖性肾炎小鼠体内,从整体水平上探讨periostin在增殖性肾炎中的作用,为肾脏疾病进展的防治提供思路。
( 致谢: 本实验于河北医科大学病理学实验室完成,感谢实验室全体老师的帮助。)
| [1] |
Wang Y, Liu D, Zhao H, et al. Cordyceps sinensis polysaccharide CPS-2 protects human mesangial cells from PDGF-BB-induced proliferation through the PDGF/ERK and TGF-beta1/Smad pathways[J]. Mol Cell Endocrinol, 2014, 382(2): 979-88. doi:10.1016/j.mce.2013.11.018 |
| [2] |
Kok H M, Falke L L, Goldschmeding R, et al. Targeting CTGF, EGF and PDGF pathways to prevent progression of kidney disease[J]. Nat Rev Nephrol, 2014, 10(12): 700-11. doi:10.1038/nrneph.2014.184 |
| [3] |
Chen Z, Xie J, Hao H, et al. Ablation of periostin inhibits post-infarction myocardial regeneration in neonatal mice mediated by the phosphatidylinositol 3 kinase/glycogen synthase kinase 3β/cyclin D1 signallingpathway[J]. Cardiovasc Res, 2017, 113(6): 620-32. doi:10.1093/cvr/cvx001 |
| [4] |
Nuzzo P V, Rubagotti A, Zinoli L, et al. The prognostic value of stromal and epithelial Periostin in expression in human breast cancer: correlation with clinical pathological features and mortality outcome[J]. BMC Cancer, 2016, 16: 95. doi:10.1186/s12885-016-2139-y |
| [5] |
Sidhu S S, Yuan S, Innes A L, et al. Roles of epithelial cell-derived periostin in TGF-beta activation, collagen production, and collagen gel elasticity in asthma[J]. Proc Natl Acad Sci USA, 2010, 107(32): 14170-5. doi:10.1073/pnas.1009426107 |
| [6] |
由淑萍, 赵军, 马龙, 等. 肉苁蓉苯乙醇总苷对血小板衍生生长因子诱导的肝星状细胞增殖的影响及机制[J]. 中国药理学通报, 2016, 32(9): 1231-5. You S P, Zhao J, Ma L, et al. Effect and mechanism of total glucosides of Cistanche tubulosa on proliferation of hepatic stellate cells induced by platelet-derived growth factor[J]. Chin Pharmacol Bull, 2016, 32(9): 1231-5. doi:10.3969/j.issn.1001-1978.2016.09.009 |
| [7] |
张伟云, 王晓禹, 王丽荣, 等. 萘醌衍生物抗血管平滑肌细胞增殖的活性研究[J]. 中国药理学通报, 2019, 35(3): 359-64. Zhang W Y, Wang X Y, Wang L R, et al. Activity of naphthoquinone derivatives against proliferation of vascular smooth muscle cells[J]. Chin Pharmacol Bull, 2019, 35(3): 359-64. doi:10.3969/j.issn.1001-1978.2019.03.013 |
| [8] |
Horiuchi K, Amizuka N, Takeshita S, et al. Identification and characterization of a novel protein, periostin, with restricted expression to periosteum and periodontal ligament and increased expression by transforming growth factor beta[J]. J Bone Miner Res, 1999, 14(7): 1239-49. doi:10.1359/jbmr.1999.14.7.1239 |
| [9] |
Wallace D P, White C, Savinkova L, et al. Periostin promotes renal cyst growth and interstitial fibrosis in polycystic kidney disease[J]. Kidney Int, 2014, 85(4): 845-54. doi:10.1038/ki.2013.488 |
| [10] |
Tajiri M, Okamoto M, Fujimoto K, et al. Serum level of periostin can predict long-term outcome of idiopathic pulmonary fibrosis[J]. Respir Investig, 2015, 53(2): 73-81. doi:10.1016/j.resinv.2014.12.003 |
| [11] |
Huang Y, Liu W, Xiao H, et al. Matricellular protein periostin contributes to hepatic inflammation and fibrosis[J]. Am J Pathol, 2015, 185(3): 786-97. doi:10.1016/j.ajpath.2014.11.002 |
| [12] |
Sen K, Lindenmeyer M T, Gaspert A, et al. Periostin is induced in glomerular injury and expressed de novo in interstitial renal fibrosis[J]. Am J Pathol, 2011, 179(4): 1756-67. doi:10.1016/j.ajpath.2011.06.002 |
| [13] |
Hwang J H, Yang S H, Kim Y C, et al. Experimental inhibition of periostin attenuates kidney fibrosis[J]. Am J Nephrol, 2017, 46(6): 501-17. doi:10.1159/000485325 |
| [14] |
An J N, Yanq S H, Kim Y C, et al. Periostin induces kidney fibrosis after acute kidney injury via the p38 MAPK pathway[J]. Am J Physiol Renal Physiol, 2019, 316(3): 426-37. doi:10.1152/ajprenal.00203.2018 |

