

2. 锦州医科大学附属第一医院外科重点实验室,辽宁 锦州 121000
2. Key Lab of Surgery, the First Affiliated Hospital of Jinzhou Medical University, Jinzhou, Liaoning 121000, China
舌鳞状细胞癌(tongue squamous cell carcinoma,TSCC)是口腔癌中最常见的恶性肿瘤之一, 与其他口腔恶性肿瘤相比,其恶性程度高,生长快,浸润性强[1]。在过去的几十年中,尽管对TSCC的诊断和治疗取得了进展,但发病率和死亡率并没有降低。舌癌的主要治疗策略是彻底的外科手术和放化疗,由于其早期症状不明显,不易被发现,失去了最佳的手术治疗时期,而化疗药的毒副作用较大,因此,寻找毒副作用少且对舌癌有抑制作用的药物尤为重要。积雪草酸(asiatic acid,AA)属于五环三萜酸,结构见Fig 1, 主要来源于伞形科植物积雪草(Centella asiatica),最早常用于促进伤口愈合。近年来,已发现AA具有许多生物活性,如抗炎护肤、保肝、降血糖、抗氧化、神经保护、心肌保护,引起了人们极大的研究兴趣[2-3]。近年来一些研究显示,AA也是促进肿瘤细胞凋亡且毒副作用小的天然产物。Wu等[4]在裸鼠成瘤模型上证实,AA可以抑制肺癌肿瘤的生长,而对正常细胞无明显影响。AA对舌癌TCA-8113细胞的抗肿瘤作用尚未有报道,因此,本研究观察了AA体外对舌癌TCA-8113细胞增殖、凋亡和细胞周期阻滞的影响,并探讨了其可能的作用机制。

|
| Fig 1 Chemical structural of asiatic acid |
人舌癌TCA-8113细胞,由锦州医科大学附属第一医院外科重点实验室赠予。
1.1.2 药物与试剂AA(货号:464-92-6, 批号:JZ18030112),购自南京景竹生物科技有限公司,纯度>98%,分子式C30H48O5,分子质量488.7,溶于DMSO,DMSO终浓度小于0.1%。MTT、Hoechst 33342、二甲基亚砜(DMSO)、结晶紫(北京Solarbio公司);胎牛血清(FBS)、RPMI 1640培养基(美国HyClone公司);细胞凋亡试剂盒(北京四正柏生物科技有限公司);细胞周期检测试剂盒(沈阳万类生物科技公司);Bcl-2、Bax、cleaved caspase-3、β-actin抗体(美国Cell Signaling Technology公司);ECL Plus试剂盒(美国Thermo公司)。
1.1.3 仪器CO2培养箱(Thermo Fisher Scientific公司);倒置显微镜(日本Olympus);倒置荧光显微镜(德国Leica);流式细胞仪(美国BD Biosciences);全自动酶标仪(美国Biotek);MINIVE垂直蛋白电泳(美国Amersham Biosciences)。
1.2 方法 1.2.1 细胞培养舌癌TCA-8113细胞用含10% FBS、100 kU·L-1青霉素和100 mg·L-1链霉素的RPMI 1640, 放在37 ℃、5% CO2培养箱中培养,每2~3 d换1次液,细胞生长到皿底80%~90%时,进行传代培养或实验。
1.2.2 MTT检测TCA-8113细胞活力取对数生长期TCA-8113细胞,将每孔约8×103个细胞置于96孔板中至细胞贴壁,弃旧培养液,每孔加入含不同浓度AA(0、20、30、40、50 μmol·L-1)的100 μL培养基,每组设6个复孔,培养24 h后,每孔加入20 μL MTT(5 g·L-1)继续培养4 h后,每孔加150 μL DMSO,酶标仪检测490 nm处的OD值。细胞活力/%=(OD给药组-OD空白组/OD对照组-OD空白组)×100%。
1.2.3 克隆形成实验检测TCA-8113细胞克隆形成取对数生长期细胞,铺6孔培养板,每孔细胞约1×103个,设置对照组、AA(20、30、40、50 μmol·L-1)处理组,作用时间为1周,每2 d换液1次,药物浓度保持不变。然后用PBS轻轻漂洗2次;甲醇固定30 min,PBS轻轻漂洗3次;结晶紫染色25 min,PBS漂洗4~5次;晾干,相机拍照。
1.2.4 Hoechst 33342染色观察TCA-8113细胞凋亡形态取对数生长期的TCA-8113细胞,6孔板中每孔约铺1×104个细胞,培养至细胞长满孔底80%,设对照组、AA(20、30、40、50 μmol·L-1)处理组,加入10 mg·L-1 Hoechst 33342染色液(1 000:1),染色15 min后,PBS洗3次,用荧光显微镜(×200)观察细胞形态,并记录图像。
1.2.5 流式细胞术(flow cytometry,FCM)检测TCA-8113细胞的凋亡率培养细胞至对数生长期,设空白对照组、AA(20、30、40、50 μmol·L-1)处理组,作用24 h后,用不含EDTA的胰蛋白酶消化细胞,取约4×105~5×105个细胞,并在离心管中1 200 r·min-1离心5 min。用预冷PBS混匀,冲洗,取100 μL流式缓冲液重悬细胞,加入5 μL的Annexin V-FITC和10 μL的PI,避光4 ℃孵育15 min,再加400 μL的PBS,移入流式管中,通过流式细胞术检测细胞凋亡率。Q1区表示坏死细胞及机械损伤细胞,Q2表示晚期凋亡细胞,Q3表示活细胞,Q4表示早期凋亡细胞。
1.2.6 流式细胞术分析TCA-8113细胞周期收集用AA处理24 h的细胞及对照组细胞,根据细胞周期检测试剂盒的说明调整细胞密度,固定,添加RNaseA,并添加碘化丙啶染色溶液,转移到流式管中,上机分析细胞周期。
1.2.7 Western blot检测相关蛋白表达用AA(0、20、30、40、50 μmol·L-1)作用TCA-8113细胞24 h,细胞刮刀收集细胞,在冰盒上用细胞裂解液(裂解液:PMSF=100:1)将细胞裂解30 min,每8 min摇动1次,4 ℃、12 000 r·min-1离心25 min。BCA蛋白试剂盒测定蛋白质浓度,制样并在沸水中变性10 min。取蛋白样品,行SDS-PAGE电泳,电湿转至PVDF膜,用3% BSA封闭液封闭1.5 h后,加入一抗(1:1 000)4 ℃过夜,以TBST漂洗后,加入二抗(1:1 000)室温孵育1 h,用TBST冲洗3次,最后用ECL显色试剂盒显色。
1.3 统计学分析所有数据表示为x±s,两独立样本采用t检验,进行正态性检验和方差齐性检验的多组间比较用单因素方差分析,统计分析由SPSS 22.0软件完成。
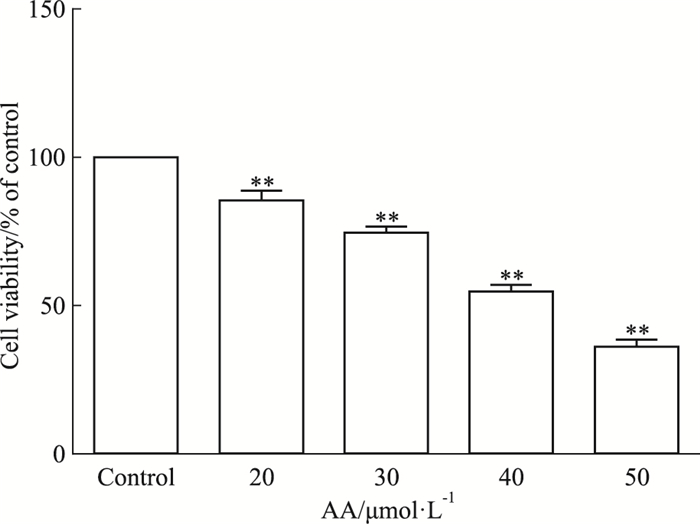
2 结果 2.1 AA抑制TCA-8113细胞的增殖Fig 2的MTT结果显示,随着AA浓度的增加,人舌癌TCA-8113细胞的活力明显降低,其作用24 h的IC50值为42.13 μmol·L-1。
|
| Fig 2 Effect of AA on viability of TCA-8113 cell (x±s, n=6) **P < 0.01 vs control |
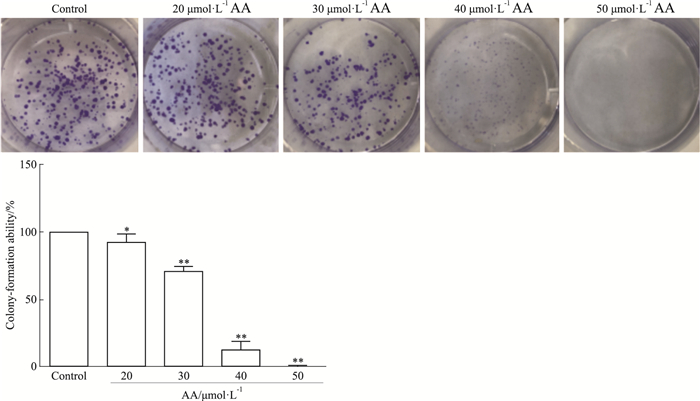
如Fig 3所示,对照组细胞克隆形成能力为100%,随着AA浓度的增大,克隆形成能力明显降低(P<0.01)。
|
| Fig 3 Effect of AA on colony-formation ability of TCA-8113 cells (x±s, n=5) *P < 0.05, **P < 0.01 vs control |

|
| Fig 4 Effect of AA on nuclear morphology change of TCA-8113 cells (×200) |
Hoechst 33342染色时,在荧光显微镜下观察到正常细胞核显示出弱的蓝光,而凋亡细胞核显示出致密的亮蓝色荧光。如Fig 4所示,对照组TCA-8113细胞核呈微弱荧光,随着AA浓度的增大,细胞核的蓝色荧光致密且亮,与AA浓度呈正比。流式细胞仪结果如Fig 5所示,AA(20、30、40、50 μmol·L-1)逐渐诱导TCA-8113细胞的凋亡。

|
| Fig 5 Effect of AA on apoptosis of TCA-8113 cells (x±s, n=5) *P < 0.05, **P < 0.01 vs control |
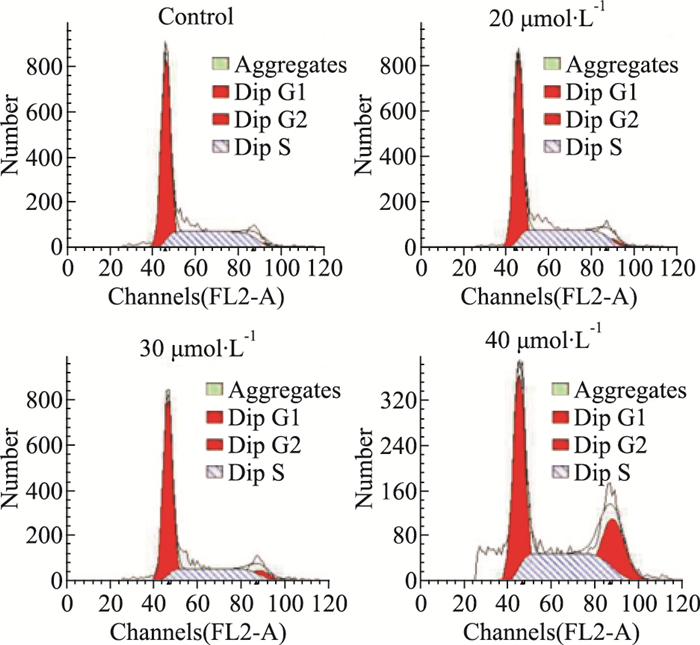
流式分析细胞周期分布情况,检测细胞周期改变是否参与AA诱导TCA-8113细胞凋亡的过程。Fig 6、Tab 1结果显示,不同浓度AA作用24 h后,TCA-8113细胞在G2/M期明显停滞(P<0.05)。
|
| Fig 6 Cell cycle distribution of TCA-8113 cells after treatment with AA for 24 h (x±s, n=5) |
| AA/μmol·L-1 | Cell cycle/% | ||
| G0/G1 | S | G2/M | |
| 0 | 58.6±0.9 | 37.8±0.8 | 3.7±0.3 |
| 20 | 54.4±1.5* | 38.7±0.9 | 5.3±0.6* |
| 30 | 53.6±0.5* | 35.3±0.4 | 11.3±0.7* |
| 40 | 40.8±0.7* | 34.3±0.6 | 24.2±1.0* |
| *P<0.05 vs control group | |||
如Fig 7所示,与对照组相比,AA组Bcl-2表达降低,而Bax、cleaved caspase-3蛋白水平均明显增加,具有一定程度的浓度依赖性(P<0.01)。

|
| Fig 7 Effect of AA on expression of Bax, Bcl-2 and cleaved caspase-3 in TCA-8113 cells (x±s, n=3) *P < 0.05, **P < 0.01 vs control |
如Fig 8所示,AA呈浓度依赖性增加p53、p21蛋白的表达(P<0.05)。

|
| Fig 8 Effect of AA on expression of p53 and p21 in TCA-8113 cells (x±s, n=3) *P < 0.05, **P < 0.01 vs control |
TSCC是全球口腔癌中发病率和死亡率的主要原因,全世界约50%的舌癌患者存在晚期疾病, 经手术完整切除后,癌症仍有复发和转移的可能性,严重影响了患者的生活质量。因此,如何抑制舌鳞癌的增殖、诱导其凋亡,是目前抗肿瘤治疗的热点问题。AA可抑制各种肿瘤细胞,如乳腺癌、卵巢癌、结肠癌和肺癌的增殖和分化。然而,特异性抗癌机制非常复杂,涉及线粒体凋亡和细胞周期分布。Aktarul等[5]研究表明,在大鼠结肠癌模型中,AA能抑制癌前病变、炎症、细胞增殖和诱导细胞凋亡,而对结肠黏膜细胞无毒性作用。Chen等[6]研究表明,AA能抗顺铂引起的急性肾损伤,对小鼠的正常细胞无影响。以上研究结果说明,AA有可能作为低毒高效的抗肿瘤药物应用。本研究利用不同浓度的AA处理人舌癌TCA-8113细胞,MTT结果显示,其IC50值为42.13 μmol·L-1,确定了后续实验所用AA浓度(20、30、40、50 μmol·L-1),即达到了抑制肿瘤细胞增殖和促进凋亡的效果,又不会产生毒副作用。此外,AA处理的舌癌细胞的克隆生长被阻断,进一步证实了AA的抗肿瘤活性,但其作用机制不明。
Hoechst 33342染色是观察AA诱导细胞凋亡变化的最直观方法。随着AA浓度的增高,舌癌TCA-8113细胞体积大小不一,细胞核或细胞质呈致密浓染的颗粒状荧光,在凋亡细胞中,清楚地观察到具有高蓝色荧光强度的凋亡小体。通过流式细胞术检测AA作用于舌癌TCA-8113细胞后荧光强度,反映凋亡情况,实验结果显示,AA处理TCA-8113细胞24 h后,细胞凋亡率逐渐增加,最高可达79.42%。
细胞凋亡主要表现为核凝聚和碎裂,凋亡小体出现,未见质膜破裂。目前,已知肿瘤细胞凋亡通路有多种,主要依赖线粒体通路和凋亡受体通路两种方式。在细胞凋亡过程中,许多凋亡信号汇聚于线粒体,Bcl-2家族成员通过整合凋亡信号,使细胞色素C释放,协调caspase-3激活,从而使线粒体外膜的通透性增加[7]。p53蛋白分子作为转录因子,能够上调Bax的表达,从而对抗Bcl-2的抗凋亡作用[8]。Bcl-2族系的凋亡相关蛋白,如Bcl-2、Bax、Bcl-xl都锚定于线粒体膜中,它们能阻止或促进细胞色素C的释放,进而影响细胞的程序性死亡[9-10]。Bax表达增加能够促进细胞色素C释放到细胞质中,而Bcl-2抗凋亡蛋白能够保持线粒体完整性来阻止细胞色素C的释放。因此,Bcl-2蛋白表达降低有利于细胞色素C从线粒体中释放出来,有助于caspase-3激活,活化的caspase-3被认为是细胞凋亡的生物标记物[11]。本研究Western blot结果显示,AA抑制Bcl-2表达的同时,增加Bax的表达,导致caspase-3表达增加,且呈浓度依赖性。
细胞周期控制是一个高度调控的过程,涉及一系列复杂的信号,大多数癌细胞在G1检查点发生分裂,导致依赖G2检查点来调节细胞复制。正常细胞依靠G1检查点来保护自己免受DNA损伤。因此,影响G2/M细胞周期的药物对正常细胞的危害较小[12]。p53作为一种肿瘤抑制蛋白,通过诱导p21依赖性细胞周期阻滞或凋亡,来控制细胞对刺激因素应激的长期反应[13]。本实验通过流式细胞术分析舌癌TCA-8113细胞的细胞周期,不同浓度的AA作用TCA-8113细胞24 h后,细胞周期在G2/M期逐渐被阻断,且呈浓度依赖性。此外,我们检测了p53及p21的表达,发现在AA处理后p53和p21上调。这些数据表明,AA诱导的G2/M期阻滞与p53、p21上调有关。这与Hsu等[14]报道的AA可以诱导人乳腺癌细胞阻滞在S-G2/M期,以及Zhang等[15]发现在多发性骨髓瘤RPMI 8226细胞中,AA处理也导致G2/M期阻滞相一致。
综上所述,本研究表明,AA抑制舌癌TCA-8113细胞的增殖作用主要通过诱导细胞凋亡和细胞周期阻滞在G2/M期来完成。AA诱导TCA-8113细胞凋亡的机制可能与调控p53通路相关蛋白p53、p21、Bax及抑制Bcl-2有关。随后的实验将探索AA抑制细胞增殖和动物实验的更多分子机制。
| [1] |
史毅, 吴伟忠, 霍安, 等. 补骨脂乙素对Tca8113细胞迁移及侵袭的抑制作用及其机制[J]. 中国药理学通报, 2015, 31(12): 1741-5. Shi Y, Wu W Z, Huo A, et al. Inhibitory effect of isobavachalcone on migration and invasion of Tca8113 cells and its mechanism[J]. Chin Pharmacol Bull, 2015, 31(12): 1741-5. doi:10.3969/j.issn.1001-1978.2015.12.022 |
| [2] |
刘华清, 许青云, 王天麟. 积雪草酸的研究进展[J]. 中国野生植物资源, 2014, 33(4): 30-3. Liu H Q, Xu Q T, Wang T L. Progress of study on asiatic acid[J]. Chin Wild Plant Resources, 2014, 33(4): 30-3. doi:10.3969/j.issn.1006-9690.2014.04.009 |
| [3] |
孟哲, 腾帅, 王琛, 等. 积雪草酸通过激活Nrf2抗氧化通路抑制自发性高血压大鼠心肌纤维化[J]. 中国药理学通报, 2018, 34(8): 1073-8. Meng Z, Teng S, Wang C, et al. Asiatic acid inhibits cardiac fibrosis via activating Nrf2-mediated anti-oxidant signaling pathway in spontaneous hypertensive rats[J]. Chin Pharmacol Bull, 2018, 34(8): 1073-8. doi:10.3969/j.issn.1001-1978.2018.08.009 |
| [4] |
Wu T, Geng J, Guo W, et al. Asiatic acid inhibits lung cancer cell growth in vitro and in vivo by destroying mitochondria[J]. Acta Pharm Sin B, 2017, 7(1): 65-72. doi:10.1016/j.apsb.2016.04.003 |
| [5] |
Aktarul I S, Vijay M, Senbagarani R, et al. Asiatic acid abridges pre-neoplastic lesions, inflammation, cell proliferation and induces apoptosis in a rat model of colon carcinogenesis[J]. Chem Biol Interact, 2017, 27(8): 197-211. |
| [6] |
Chen Y, Yun G, Huang T S, et al. Asiatic acid protects against cisplatin-induced acute kidney injury via anti-apoptosis and anti-inflammation[J]. Biomed Pharmacother, 2018, 10(7): 1354-62. |
| [7] |
Desagher S, Martinou J C. Mitochondria as the central control point of apoptosis[J]. Trends Cell Biol, 2000, 10(9): 369-77. doi:10.1016/S0962-8924(00)01803-1 |
| [8] |
Wang L, Peng Y, Shi K, et al. Osthole inhibits proliferation of human breast cancer cells by inducing cell cycle arrest and apoptosis[J]. J Biomed Res, 2015, 29(2): 132-8. |
| [9] |
Jemal A, Siegel R, Xu J, et al. Cancer statistics, 2010[J]. CA Cancer J Clin, 2010, 60(5): 277-300. doi:10.3322/caac.20073 |
| [10] |
Kalkavan H, Green D R. MOMP, cell suicide as a BCL-2 family business[J]. Cell Death Differ, 2018, 25(1): 46-55. doi:10.1038/cdd.2017.179 |
| [11] |
Ren L, Cao Q X, Zhai F R, et al. Asiatic acid exerts anticancer potential in human ovarian cancer cells via suppression of PI3K/Akt/mTOR signalling[J]. Pharm Biol, 2016, 54(11): 2377-82. doi:10.3109/13880209.2016.1156709 |
| [12] |
Kawabe T. G2 checkpoint abrogators as anticancer drugs[J]. Mol Cancer Ther, 2004, 3(4): 513-9. |
| [13] |
郭珮, 冉建华, 李静, 等. 注射用核糖核酸Ⅱ上调p53诱导人白血病细胞凋亡[J]. 中国药理学通报, 2016, 32(12): 1729-34. Guo P, Ran J H, Li J, et al. Ribonucleic acid Ⅱ induces apoptosis in human leukemia cells by up-regulating p53[J]. Chin Pharmacol Bull, 2016, 32(12): 1729-34. doi:10.3969/j.issn.1001-1978.2016.12.018 |
| [14] |
Hsu Y L, Kuo P L, Lin L T, et al. Asiatic acid, a triterpene, induces apoptosis and cell cycle arrest through activation of extracellular signal-regulated kinase and p38 mitogen-activated protein kinase pathways in human breast cancer cells[J]. J Pharmacol Exp Ther, 2005, 313(1): 333-44. doi:10.1124/jpet.104.078808 |
| [15] |
Zhang J, Ai L, Lv T, et al. Asiatic acid, a triterpene, inhibits cell proliferation through regulating the expression of focal adhesion kinase in multiple myeloma cells[J]. Oncol Lett, 2013, 6(6): 1762-6. doi:10.3892/ol.2013.1597 |

