


2. 安东国立大学食品科学与生物技术学院,韩国 安东 760749
2. Dept of Food Science and Biotechnology, Andong National University, Andong 760749, Korea
随着人们生活质量的不断提高,全球肥胖率呈直线增长趋势,中国现已成为肥胖超级大国。肥胖是一种慢性疾病,可引发Ⅱ型糖尿病、血脂异常症、心血管疾病和高血压等疾病,严重危害公众的身体健康[1]。脂肪细胞分化与调控的失常,可导致脂肪细胞体积的增大、脂肪组织的沉积以及脂肪细胞调控因子分泌的紊乱,继而引起肥胖代谢性疾病[2]。因此,研究脂肪细胞分化的抑制作用有助于寻找抗肥胖代谢性疾病的新原料,对于探索预防与治疗代谢性疾病具有重要的理论意义和应用价值。蕨菜(Pteridium aquilinum (Linn.) Kuhn var. Latiusculum (Desv) Underw)作为药食两用植物,有很高的药用价值,有清热解毒、消肿、利水、安神、润肠通便等功效,可用于治疗高血压、糖尿病、风湿性关节炎等症状[3]。现代药理研究表明:蕨菜含有多酚、多糖、黄酮、萜类等多种生物活性物质,具有抗氧化、降血糖及增强机体免疫等功效[4]。本课题组前期研究发现[5],不同真菌固体发酵前后蕨菜醇提取物具有明显体外抗氧化和抗炎症活性。蕨菜水提取物对高血脂小鼠的血脂代谢紊乱具有良好调节作用[6],但蕨菜超临界萃取物对3T3-L1脂肪细胞分化的抑制作用及其分子机制尚不明确。
超临界CO2萃取是一种低温绿色环保萃取分离技术,与溶剂提取法、酶解辅助法和超声提取法等传统工艺相比,具有萃取高效、时间短、无溶剂残留等优点,且更大程度上保留了天然植物热敏性和易氧化等生物活性成分。顾仁勇等[7]采用超临界CO2萃取技术提取八月瓜多酚,多酚含量提高2.45倍,产品纯度提高15.46%。Tohar等[8]采用超临界CO2萃取美丽帽柱木叶的活性成分,明显增加了其抗炎症作用。然而,目前尚鲜有关于蕨菜超临界萃取及其化学成分的研究。为此,本研究采用超临界CO2技术萃取蕨菜活性成分,通过GC-MS对萃取物进行化学成分分析,并探究蕨菜萃取物对3T3-L1前脂肪细胞分化的抑制作用及分子机制,以期为蕨菜进一步的开发利用提供科学依据。
1 材料 1.1 细胞株3T3-L1前脂肪细胞株购自美国模式培养物集存库(American Type Culture Collection, ATCC)。
1.2 药品与试剂四甲基偶氮唑蓝(MTT;批号:M2128,规格:1 g)、胰岛素(insulin;批号:I9278,规格:5 mL)、3-异丁基-1-甲基黄嘌呤(3-Isobutyl-l-methylxanthine,IBMX;批号:17018,规格:100 mg)、地塞米松(dexamethasone,Dex;批号:D4902,规格:100 mg)、油红O(批号:O0625,规格:25 g),均购自美国Sigma公司;DMEM培养基(批号:88425,规格:135 g)、胰蛋白酶(批号:A40009,规格:100 μg)、胎牛血清(批号:26400044,规格:500 mL)、小牛血清(批号:16010159,规格:500 mL)及其它细胞培养试剂购自美国Gibco公司;cDNA合成试剂盒(批号:6110B,规格:200 rxns)购自日本TaKaRa公司。
1.3 仪器Waters MV-10型超临界萃取系统(美国Waters公司);Agilent HP7890-5975C型气相色谱-质谱联用仪(美国Agilent公司);SpectraMax-190型全波长酶标仪(美国Molecular Devices公司);IX51型倒置显微镜(日本Olympus公司);ECOTM实时荧光定量PCR仪(美国Illumina公司)。
2 方法 2.1 蕨菜超临界萃取物的制备将蕨菜洗净晾干,于60 ℃烘干至恒重,粉碎过40目筛,得蕨菜粉末。准确称取原料5.0 g,采用超临界CO2流体萃取方法提取蕨菜活性成分。萃取条件为:萃取压力20 Mpa,温度30 ℃,动态萃取时间10 min,静态萃取时间10 min,CO2流量10 mL·min-1,夹带剂为75%乙醇1 mL·min-1,循环萃取2次。萃取后采用旋转蒸发仪浓缩至恒重,得到粘稠状萃取物。
2.2 蕨菜萃取物化学成分的GC-MS分析将超临界萃取得到的蕨菜萃取物用甲醇配制成1 000 mg·L-1溶液,利用GC-MS对试样进行分析。色谱条件:选用HP-5MS弹性石英毛细管柱(30 m×0.25 mm×0.25 μm);进样量为0.5 μL,进样口模式为不分流,进样口温度为280 ℃;柱箱程序为40 ℃保持3 min,以4 ℃·min-1升至160 ℃保持3 min,以4 ℃·min-1升至285 ℃保持10 min;运行时间为70 min。质谱条件:电离方式为电子轰击(EI),电子能量为70 eV,离子源温度为230 ℃;扫描范围m/z为35~450 amu全离子扫描;质谱数据库为NIST08标准谱库。
2.3 3T3-L1前脂肪细胞的培养与诱导分化将3T3-L1前脂肪细胞置于含10%小牛血清的DMEM培养基中,在37 ℃、5% CO2、95%湿度的培养箱内培养。待细胞生长至80%时,传代培养。
取对数生长期的3T3-L1前脂肪细胞,以1×108·L-1细胞密度接种于24孔板中,每孔加入500 μL细胞悬浮液。待细胞融合后接触抑制48 h(记为分化d 0),加含0.5 mmol·L-1 IBMX、5 mg·L-1胰岛素、1 μmol·L-1 Dex及10%胎牛血清的DMEM培养基培养48 h(d 2),更换为含5 mg·L-1胰岛素的10%胎牛血清的DMEM培养基培养48 h(d 4)。以后每48 h更换一次10%胎牛血清的DMEM培养基,直至90%的前脂肪细胞分化为脂肪细胞,并于d 8检测脂肪的含量[2]。在0~8天中,同时加入不同浓度的蕨菜超临界萃取物(50、100、200 mg·L-1)。实验设置未诱导分化的细胞为对照组(Control)、诱导分化的脂肪细胞为模型组(Model)、SFE-PA组(诱导分化+ SFE-PA 50、100、200 mg·L-1)。每组平行3个复孔,重复3次。
2.4 MTT法检测3T3-L1前脂肪细胞的活性取对数生长期的3T3-L1前脂肪细胞,以1×108·L-1细胞密度接种于96孔板中,每孔加入100 μL。待细胞完全贴壁良好后(约48 h),更换含不同浓度蕨菜超临界萃取物(50、100、200 mg·L-1)的10%胎牛血清的DMEM培养基。培养48 h后,每孔加入MTT溶液20 μL,继续培养3 h, 然后去除孔内的液体,每孔中加入200 μL DMSO使紫色结晶充分溶解,于570 nm波长处测各孔的OD值[9]。
2.5 油红O染色比色法分析3T3-L1前脂肪细胞的分化程度诱导分化d 8,移去培养液,用PBS清洗3次,然后用4%多聚甲醛固定30 min,PBS清洗3次,加入油红O染液。染色60 min后去除染液,PBS清洗3次,倒置显微镜下观察并拍摄照片,之后加入200 μL异丙醇使其充分溶解染色脂肪细胞内的油红O,于520 nm波长处测定吸光值[2]。
2.6 qRT-PCR法检测脂肪细胞分化转录调控因子和脂质合成相关基因mRNA的表达采用不同浓度蕨菜超临界萃取物(50、100、200 mg·L-1)处理3T3-L1细胞,利用TRIzol试剂提取总RNA,然后采用PrimeScriptTM RT试剂将RNA逆转录为cDNA。加入SYBR Green、引物及cDNA模板,进行实时荧光定量PCR反应。引物序列见表Tab 1。
| Gene | Sequence |
| PPARγ | Forward 5′-TCGCTGATGCACTGCCTATG-3′ |
| Reverse 5′-GAGAGGTCCACAGAGCTGATT-3′ | |
| CEBPα | Forward 5′-CCTTCAACGACGAGTTCCTG-3′ |
| Reverse 5′-TGGCCTTCTCCTGCTGTC-3′ | |
| SREBP-1c | Forward 5′-GGAGACATCGCAAACAAGCTGA-3′ |
| Reverse 5′-CAGACTGCAGGCCAGATCCA-3′ | |
| FAS | Forward 5′-ATCCTGGAACGAGAACACGATCT-3′ |
| Reverse 5′-AGAGACGTGTCACTCCTGGACCT-3′ | |
| ACC | Forward 5′-GAGTGACTGCCGAAACATCTCTG-3′ |
| Reverse 5′-GCCTCTTCCTGACAAACGAGT-3′ | |
| β-actin | Forward 5′-GTTGGACCTGACAGACTACCTCA-3′ |
| Reverse 5′-GTTGCCAATAGTGATGACCT-3′ |
所得数据用x±s表示,应用SPSS 18.0软件进行统计分析,利用单因素方差分析(One-way ANOVA)中的LSD法进行两两比较。
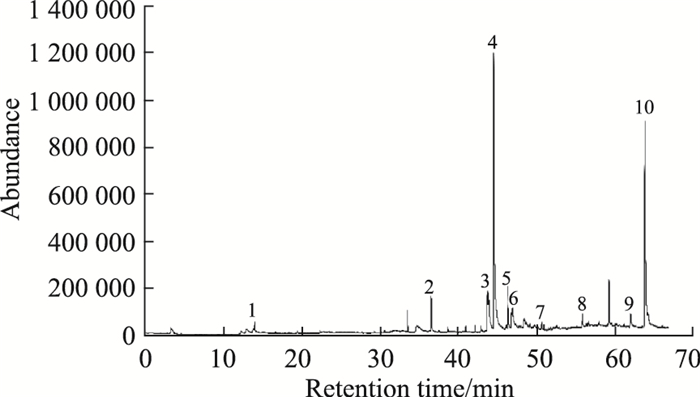
3 结果 3.1 蕨菜超临界萃取物的化学成分分析对蕨菜超临界萃取物的主要化学成分进行了GC-MS定性分析,总离子流图谱如Fig 1所示。运用NIST08质谱库对照,从SFE-PA中鉴定出10种化合物,占总峰面积量的87.17%。由Tab 2可知,SFE-PA含有酚类、酯类、有机酸类、醇类等化合物,以酚类、醇类化合物为主,其中含有2种酚类化合物(44.33%)、4种醇类化合物(32.08%)、2种有机酸类化合物(9.46%)、2种酯类化合物(1.30%)。SFE-PA的主要化学成分为4, 4, 5, 7, 8-五甲基-二氢香豆素(36.07%)、β-谷甾醇(25.66%)、4-氨基-7-二乙氨基-香豆素(8.26%)、棕榈酸(5.05%)、亚油酸(4.41%)、植醇(3.31%)、菜油甾醇(2.06%)等。
|
| Fig 1 Total ion chromatogram of supercritical extract from Pteridium aquilinum |
| No | Retention time (min) | Compounds | Formula | Molecule mass | Relative content (%) |
| 1 | 13.967 4 | Eucalyptol | C10H18O | 154.25 | 1.05 |
| 2 | 36.532 8 | Palmitic acid | C16H32O2 | 256.42 | 5.05 |
| 3 | 43.859 1 | 4-Amino-7-diethylamino-chromen-2-one | C13H16N2O2 | 232.12 | 8.26 |
| 4 | 44.533 7 | 4, 4, 5, 7, 8-Pentamethyl- dihydrocoumarin | C14H18O2 | 218.29 | 36.07 |
| 5 | 46.318 5 | Phytol | C20H40O | 296.53 | 3.31 |
| 6 | 46.894 5 | Linoleic acid | C18H32O2 | 280.45 | 4.41 |
| 7 | 50.6355 | Bis(2-ethylhexyl) adipate | C22H42O4 | 370.57 | 0.44 |
| 8 | 55.870 8 | Dioctyl sebacate | C26H50O4 | 426.67 | 0.86 |
| 9 | 62.014 2 | Campasterol | C28H48O | 400.69 | 2.06 |
| 10 | 63.866 5 | β-Sitosterol | C29H50O | 414.71 | 25.66 |
由Fig 2可知,在50 ~ 200 mg·L-1浓度下,蕨菜超临界萃取物对3T3-L1前脂肪细胞活性无明显影响,且无剂量效应。当浓度达到200 mg·L-1时,3T3-L1前脂肪细胞活力为99.39%,与空白对照组相比(Control),差异无统计学意义。以上说明,SFE-PA在200 mg·L-1浓度内,对3T3-L1前脂肪细胞无明显毒性作用。

|
| Fig 2 Effect of SFE-PA on cell viability of 3T3-L1 preadipocytes (x±s, n=3) |
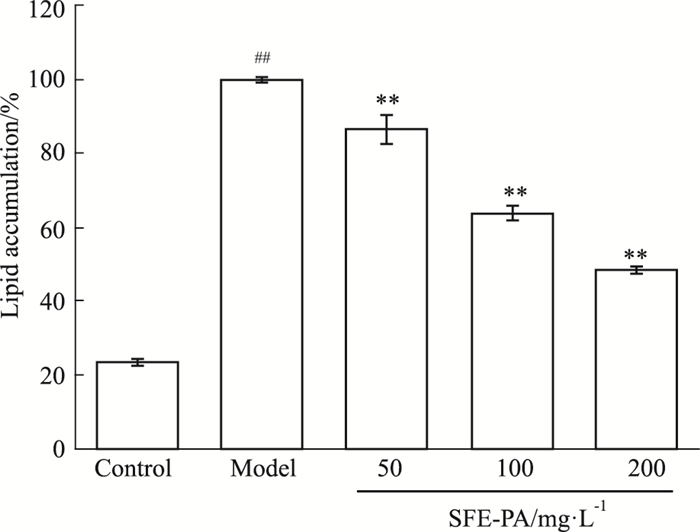
由Fig 3可知,蕨菜超临界萃取物可以明显抑制3T3-L1前脂肪细胞的分化,明显减少成熟脂肪细胞中的脂肪积累。采用油红O染色比色进行分析,SFE-PA在浓度50、100、200 mg·L-1处理条件下,其脂肪含量分别是模型组(Model)的86.73%、64.01%、48.54%,呈剂量依赖性降低,且差异具有显著性(P<0.01)。
|
| Fig 3 Effect of SFE-PA on differentiation of 3T3-L1 preadipocytes (x±s, n=3) ##P < 0.01 vs control group, **P < 0.01 vs model group |
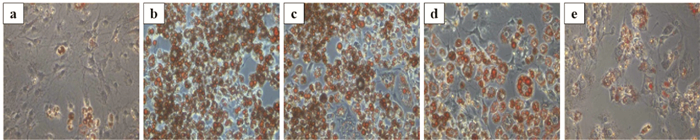
Fig 4所示为3T3-L1前脂肪细胞分化前后的形态变化,在显微镜下观察,未诱导分化的3T3-L1前脂肪细胞为长梭形,细胞内无脂滴。采用鸡尾酒式诱导分化后,细胞形态变大变圆,体积增大,细胞质内出现脂滴,8 d后90%以上的细胞分化为成熟的脂肪细胞。通过油红O染色,可见胞质中含有的大量脂滴被染成红色,在核周围形成“戒指环”结构。经蕨菜超临界萃取物干预后,脂肪细胞中被染成红色的脂滴减少,且呈剂量效应。
|
| Fig 4 Morphological micrographs of 3T3-L1 preadipocytes after incubation with SFE-PA (×200) a: Control; b: Model; c: SFE-PA 50 mg·L-1; d: SFE-PA 100 mg·L-1; e: SFE-PA 200 mg·L-1. |
过氧化物酶体增殖物激活受体γ(peroxisome proliferator-activated receptor γ,PPARγ)和CCAAT/增强子结合蛋白α(CCAAT/enhancer-binding protein α,C/EBPα)是3T3-L1前脂肪细胞分化的关键转录调控因子。由Fig 5可知,与对照组(Control)相比,随着脂肪细胞分化过程的进行,模型组PPARγ和CEBPα的mRNA相对表达量明显增加(P<0.01)。SFE-PA可以明显下调PPARγ和CEBPα mRNA表达量,其中200 mg·L-1 SFE-PA处理组分别下降为模型组(Model)的18.21%和15.54%,差异有显著性(P<0.01)。SFE-PA还明显降低了固醇调节元件结合蛋白-1c(sterol regulatory element-binding protein 1c, SREBP-1c)mRNA表达水平,其中100、200 mg·L-1 SFE-PA处理组分别下降为模型组(Model)的52.65%、27.16%,呈剂量依赖性降低,差异具有统计学意义(P<0.01)。

|
| Fig 5 Effect of SFE-PA on mRNA expression of PPARγ, CEBPα, SREBP-1c in adipocytes (x±s, n=3) ##P < 0.01 vs control group, *P < 0.05, **P < 0.01 vs model group |
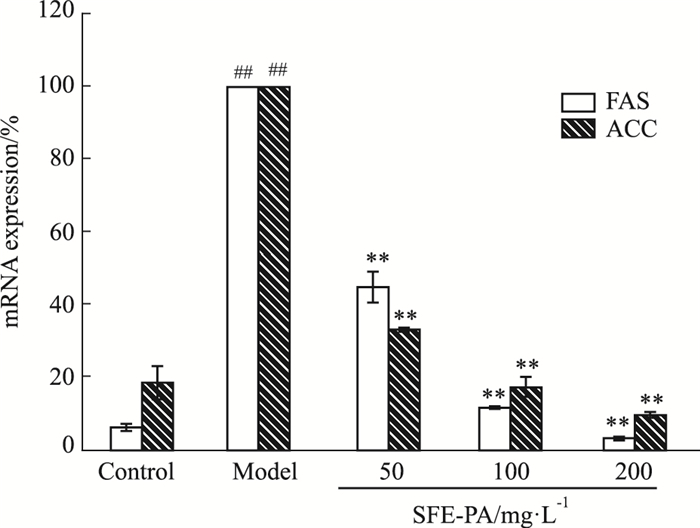
乙酰辅酶A羧化酶(acetyl CoA carboxylase,ACC)和脂肪酸合成酶(fatty acid synthase,FAS)是脂质合成途径中关键酶,在脂肪沉积中发挥了重要作用。由Fig 6可知,与对照组(Control)相比,随着脂肪细胞分化过程的进行,模型组(Model)FAS和ACC的mRNA相对表达量明显增加(P<0.01),分别是对照组的15.76、5.35倍。SFE-PA明显抑制了脂肪细胞分化中脂质合成基因FAS、ACC mRNA的表达水平,随着SFE-PA浓度的增加,抑制效果呈浓度依赖性增加,差异且有统计学意义(P<0.01)。与模型组(Model)相比,当SFE-PA浓度为200 mg·L-1时,对细胞内FAS、ACC mRNA表达的抑制率分别96.54%、90.11%。
|
| Fig 6 Effect of SFE-PA on mRNA expression of FAS, ACC in adipocytes (x±s, n=3) ##P < 0.01 vs control group, **P < 0.01 vs model group |
肥胖作为一种慢性代谢性疾病已成为危害全球公众健康的主要问题之一,它与血脂异常症、心血管疾病和Ⅱ型糖尿病等多种疾病的发生密切相关[1]。治疗肥胖的药物主要有奥利司他(orlistat)和西布曲明(sibutramine),但长期服用效果不理想,而且存在严重的副作用,如头疼、胃疼、腹泻等,甚至可能增加患心血管疾病的风险,因此,人们急需一种安全并高效的治疗药物[10]。酚类、黄酮、多糖、醇类等生物活性物质是近年来各领域研究的热点,大多数体外研究表明[2, 4, 10],天然植物资源来源的酚类、黄酮、多糖等具有抗氧化、抗肥胖、降血糖及增强机体免疫等生物学作用。本研究采用超临界CO2萃取蕨菜活性物质,通过GC-MS分析其主要化学成分,并以3T3-L1前脂肪细胞为研究对象,研究蕨菜超临界萃取物对3T3-L1前脂肪细胞分化的影响,探讨蕨菜在抗肥胖代谢性疾病方面的功效。共鉴定出10种化合物,占总峰面积量的87.17%,主要化学成分为4, 4, 5, 7, 8-五甲基-二氢香豆素(36.07%)、β-谷甾醇(25.66%)、4-氨基-7-二乙氨基-香豆素(8.26%)等。姚元发[11]研究表明,香豆素类化合物能改善高脂小鼠的血脂水平,并明显减轻肥胖小鼠体重。Yang等[12]从鲁桑中分离鉴定出β-谷甾醇等活性成分,并发现β-谷甾醇能明显抑制3T3-L1脂肪细胞的分化。从本试验中我们得出蕨菜超临界萃取物显著性的抑制脂肪细胞的分化,而高含量的酚类、醇类可能是其潜在的抑制3T3-L1脂肪细胞分化的活性物质基础。
为了阐明其中的分子机制,本研究检测了脂肪细胞分化过程中细胞分化转录调控因子和脂质合成相关基因的表达水平。目前研究认为调节脂肪细胞分化的主要调控因子包括PPARγ、CEBPα和SREBP-1c。PPARγ和CEBPα具有调节脂肪形成、糖脂代谢和细胞增殖分化等生物学功能,它们的过度表达可以诱导并加快脂肪细胞分化,并激活众多脂肪细胞分化相关基因的转录表达,促进细胞内脂肪的累积[13]。SREBP-1c在前脂肪细胞分化早期发挥着重要作用,并能够在脂肪细胞分化过程中增加PPARγ的活性[14]。本研究中,蕨菜超临界萃取物可以明显抑制脂肪细胞中PPARγ、CEBPα和SREBP-1c的mRNA表达,从而一定程度上抑制了前脂肪细胞的分化,减少成熟脂肪细胞中的脂肪积累。研究表明脂肪细胞分化也与脂质合成酶基因密切相关。FAS和ACC是脂质合成途径中的关键酶,在脂肪沉积中发挥着重要作用,当脂肪细胞分化时,脂滴增多,即FAS和ACC表达增加[15]。本研究结果表明,蕨菜超临界萃取物在mRNA水平对FAS和ACC表达下调明显,从而明显减少了细胞内三酰甘油脂滴生成。
综上所述,蕨菜超临界萃取物能够明显抑制3T3-L1细胞分化,减少细胞脂肪沉积,可能是通过减少脂肪细胞分化转录调控因子PPARγ、CEBPα和SREBP-1c的mRNA表达量,下调脂质合成相关基因FAS和ACC的mRNA表达实现的。经GC-MS分析萃取物中的主要化学成分,共鉴定出10种化合物,其中高含量的酚类、醇类可能是其潜在的抑制3T3-L1脂肪细胞分化的活性物质基础。本研究揭示了蕨菜在肥胖的预防治疗中具有潜在的价值。
( 致谢: 本实验主要在安徽省黄山学院生态与健康技术中心和韩国安东国立大学食品科学与生物技术国家重点实验室完成,感谢胡长玉老师、耿玉闯、武梦雪、王雅莉等同学的帮助,在此致以真诚的感谢。)
| [1] |
Kowalska K, Olejnik A, Rychlik J, et al. Cranberries (Oxycoccus quadripetalus) inhibit adipogenesis and lipogenesis in 3T3-L1 cells[J]. Food Chem, 2014, 148: 246-52. doi:10.1016/j.foodchem.2013.10.032 |
| [2] |
Kwon T H, Wu Y X, Kim J S, et al. 6, 6'-bieckol inhibits adipocyte differentiation through down -regulation of adipogenesis and lipogenesis in 3T3-L1 cells[J]. J Sci Food Agric, 2015, 95(9): 1830-7. doi:10.1002/jsfa.6881 |
| [3] |
宋广磊, 王奎武, 张虹, 等. 蕨菜多糖的分离纯化单糖组分及免疫调节活性研究[J]. 药物分析杂志, 2016, 36(12): 2107-12. Song G L, Wang K W, Zhang H, et al. Purification, characterization and immunomodulating activity of polysaccharides from Pteridium aquilinum (Linn.) Kuhn[J]. Chin J Pharm Anal, 2016, 36(12): 2107-12. |
| [4] |
Song G, Wang K, Zhang H, et al. Structural characterization and immunomodulatory activity of a novel polysaccharide from Pteridium aquilinum[J]. Int J Biol Macromol, 2017, 102: 599-604. doi:10.1016/j.ijbiomac.2017.04.037 |
| [5] |
吴永祥, 吴丽萍, 胡晓倩, 等. 不同真菌固体发酵对蕨菜主要活性成分及其体外抗氧化和抗炎症作用的影响[J]. 食品科学, 2018, 39(24): 168-74. Wu Y X, Wu L P, Hu X Q, et al. Effect of solid-state fermentation with various fungi on main bioactive components of Pteridium aquilinum and their antioxidant and anti-inflammatory activities in vitro[J]. Food Sci, 2018, 39(24): 168-74. doi:10.7506/spkx1002-6630-201824026 |
| [6] |
杨辉, 曾春萍. 三种野菜水提液对高脂小鼠血脂代谢的影响[J]. 食品研究与开发, 2015, 36(6): 11-3. Yang H, Zeng C P. Effects of water extract from Scorzonera sinensis lipsch, Pteridium aquilinum and Sonchus oleraceus L. on plasma-lipids metabolism in mice fed high fats diet[J]. Food Res Dev, 2015, 36(6): 11-3. doi:10.3969/j.issn.1005-6521.2015.06.003 |
| [7] |
顾仁勇, 杨万根, 余佶. 响应面优化超临界CO2萃取八月瓜幼果多酚工艺[J]. 食品科学, 2015, 36(10): 76-80. Gu R Y, Yang W G, Yu J. Optimization of supercritical CO2 extraction conditions of polyphenols from young fruits of Holboellio latifolia by response surface methodology[J]. Food Sci, 2015, 36(10): 76-80. doi:10.7506/spkx1002-6630-201510015 |
| [8] |
Tohar N, Shilpi J A, Sivasothy Y, et al. Chemical constituents and nitric oxide inhibitory activity of supercritical carbon dioxide extracts from Mitragyna speciosa leaves[J]. Arab J Chem, 2019, 12(3): 350-9. doi:10.1016/j.arabjc.2016.09.005 |
| [9] |
吴永祥, 毕淑峰, 姜薇, 等. 桑白皮多酚对B16细胞内黑色素生成的影响及其机制[J]. 中国药理学通报, 2018, 34(9): 1296-301. Wu Y X, Bi S F, Jiang W, et al. Effect of polyphenol from Cortex Mori on melanogenesis of B16 cells and its mechanism[J]. Chin Pharmacol Bull, 2018, 34(9): 1296-301. doi:10.3969/j.issn.1001-1978.2018.09.021 |
| [10] |
Chyau C C, Chu C C, Chen S Y, et al. The inhibitory effects of Djulis (Chenopodium formosanum) and its bioactive compounds on adipogenesis in 3T3-L1 adipocytes[J]. Molecules, 2018, 23(7): 1780-95. doi:10.3390/molecules23071780 |
| [11] |
姚元发.香豆素类化合物对小鼠2型糖尿病的干预作用及机制研究[D].杭州: 浙江工业大学, 2017. Yao Y F. Study on intervention effects and mechanisms of coumarins on type 2 diabetes in mice[D]. Hangzhou: Zhejiang University of Technology, 2017. http://cdmd.cnki.com.cn/Article/CDMD-10337-1017252960.htm |
| [12] |
Yang Z G, Matsuzaki K, Takamatsu S, et al. Inhibitory effects of constituents from Morus alba var. multicaulis on differentiation of 3T3-L1 cells and nitric oxide production in RAW264.7 cells[J]. Molecules, 2011, 16: 6010-22. doi:10.3390/molecules16076010 |
| [13] |
李吉萍, 张文友, 孙婷婷, 等. 板蓝根水提物对3T3-L1前脂肪细胞增殖和分化的影响[J]. 中国药理学通报, 2017, 33(8): 1159-64. Li J P, Zhang W Y, Sun T T, et al. Effects of water extract of Radix Isatidis on proliferation and differentiation of 3T3-L1 preadipocytes[J]. Chin Pharmacol Bull, 2017, 33(8): 1159-64. doi:10.3969/j.issn.1001-1978.2017.08.023 |
| [14] |
Shen S, Liao Q, Feng Y, et al. Myricanol mitigates lipid accumulation in 3T3-L1 adipocytes and high fat diet-fed zebrafish via activating AMP-activated protein kinase[J]. Food Chem, 2019, 270: 305-14. doi:10.1016/j.foodchem.2018.07.117 |
| [15] |
何彦峰, 李刚, 盖祥云, 等. 荭草素抑制3T3-L1前脂肪细胞分化及其改善胰岛素抵抗的作用研究[J]. 中国药理学通报, 2017, 33(9): 1221-5. He Y F, Li G, Gai X Y, et al. Effects of orientin on insulin resistance in 3T3-L1 adipocytes and its mechanism[J]. Chin Pharmacol Bull, 2017, 33(9): 1221-5. |

