

2. 南方医科大学南方医院中医科,广东 广州 510515;
3. 广东省传统医学与运动伤害康复研究所,广东 广州 510317
2. Dept of Traditional Chinese Medicine, Nanfang Hospital, Southern Medical University, Guangzhou 510515, China;
3. Guangdong Institute of Traditional Medicine and Sports Injury Rehabilitation, Guongzhou 510317, China
重型再生障碍性贫血(severe aplastic anemia,SAA)是以全血细胞减少、骨髓增生重度减低为特征的骨髓衰竭综合征,目前发病机制尚不完全清楚[1]。国内外大量实验研究证实,免疫介导骨髓衰竭小鼠模型是一个最接近SAA发病机制的动物模型[2]。在建立免疫介导的骨髓衰竭(bone marrow failure,BMF)小鼠模型过程中,亚致死剂量射线辐照是必需条件[3-4]。我们在处理模型小鼠时发现,肾、肝脏等多脏器苍白,与文献报道一致[4-5]。相关研究证实辐射会导致肾脏氧化应激反应[6],而贫血可进一步加重肾脏氧化应激损伤[7],但在建立免疫介导的BMF模型过程中诱导的肾脏氧化应激尚未见报道。
川芎嗪((tetramethylpyrazine,TMP)是从中药川芎中提取出来的活性生物碱,具有抑制血小板聚集、清除自由基、扩张血管、改善微循环等作用[8],并能减轻辐射诱导的DNA损伤、氧化应激反应及细胞凋亡[9],临床上广泛应用于心脑血管、呼吸系统、肾脏等疾病治疗,实验研究也证实了其治疗肾缺血/再灌注损伤及膜性肾病的有效性[10-11]。然而,TMP是否对BMF小鼠肾脏氧化应激具有保护作用尚不清楚。本研究旨在探讨川芎嗪对BMF小鼠肾脏氧化应激的影响及潜在机制。
1 材料与方法 1.1 材料 1.1.1 实验动物C57BL/6 ♀小鼠,SPF级,6周龄,体质量(15~18) g,共60只,购自南方医科大学实验动物中心,合格证号:SYXK(粤)2016-0167,在SPF级动物房内饲养。DBA/2 ♀小鼠14只,6周龄,购自北京维通利华实验动物技术有限公司,动物合格证号:SCXK(京)2016-0006。
1.1.2 药物与试剂川芎嗪单体(生产批号:18101001,成都曼思特生物科技有限公司);微量还原型谷胱甘肽(glutathione,GSH)测试盒、超氧化物歧化酶(superoxide dismutase,SOD)试剂盒、谷胱甘肽过氧化物酶(glutathione peroxidase,GSH-Px)试剂盒、丙二醛(malondialdehyde,MDA)试剂盒(南京建成生物工程研究所,货号分别为:A006-2、A001-1、A005、A003-1);HIF-1α抗体(ab1,Abcam);VEGFA抗体(A17877,ABclonal Technology)。
1.1.3 仪器辐照仪(MultiRad);轮转石蜡切片机(Leica);血细胞计数仪(迈瑞BC-5000全自动血细胞分析仪);光学显微照相系统(日本Olympus)。
1.2 动物分组与处理按随机数字表法,将受体C57BL/6小鼠分为正常对照组、单纯辐照组、模型组、TMP低、中、高剂量组,每组10只。颈椎脱位法处死供体DBA/2小鼠,于体积分数75%乙醇中浸泡5 min,无菌操作取其颈部、腋下、肠系膜淋巴结及胸腺,加PBS缓冲液,轻轻研磨后,用200目筛网过滤,按胸腺细胞:淋巴结细胞=1 :2制成淋巴细胞混悬液,配成细胞悬液浓度为2×1010·L-1。
1.3 免疫介导的BMF模型的建立受体C57BL/6小鼠经5.0 Gy X射线全身均匀照射后,4 h内经尾静脉输入DBA/2小鼠淋巴细胞混悬液0.2 mL,含4×106个淋巴细胞。14 d后处理各组小鼠,模型成功判定标准:①血细胞计数:全血细胞减少;②骨髓活检:骨髓多部位增生不良或低下,巨核细胞缺如,非造血细胞比例增多。
1.4 观察指标 1.4.1 血细胞检测与骨髓有核细胞计数在小鼠濒死状态或存活14 d后,采用摘眼球取血法采血, 置于EDTA抗凝管中,检测各组小鼠血细胞计数。取右侧股骨,用PBS缓冲液反复冲洗骨髓腔直至股骨发白,留取骨髓细胞悬液,裂解红细胞后,计数骨髓有核细胞数量。
1.4.2 骨髓与肾脏病理学检查取左侧股骨,浸泡于脱钙液中至股骨软化后,用自来水浸泡2 h,置于10%中性甲醛固定72 h;取各组肾脏置于10%中性甲醛固定72 h。以上组织经乙醇梯度脱水、石蜡包埋、半薄切片及苏木精-伊红染色后,光学显微镜下观察正常对照组、单纯辐照组、模型组和给药组之间骨髓与肾脏病理学变化。
1.4.3 肾脏氧化应激检测取肾脏组织100 mg, 经冰冷PBS漂洗和裂解液匀浆后,于4 ℃、10 000×g离心15 min,取上清液,采用BCA蛋白定量试剂盒测定蛋白浓度。采用试剂盒检测MDA、SOD、GSH和GSH-Px活性水平,按照说明书操作。
1.4.4 免疫组织化学法检测肾脏HIF-1α、VEGF蛋白表达将肾组织石蜡切片经烤片和常规脱蜡至水后,经热修复抗原,于3%过氧化氢溶液中灭活内源性过氧化物酶及BSA封闭后,滴加一抗HIF-1α、VEGF,37 ℃烤箱中孵育0.5 h;室温下复温5 min,滴加二抗,37 ℃烘箱中孵育20 min,DAB显色2~5 min,于显微镜下观察显色情况,经苏木精复染和中性树胶封片,PBS代替一抗作阴性对照。结果判定:胞质呈棕黄色为阳性表达。应用ImageJ图像处理软件计算平均光密度来分析表达情况。
1.5 统计学处理使用SPSS 20.0分析数据,计量资料用x±s来表示, 采用单向方差分析检验(one-way ANOVA)进行组间比较;用GraphPad Prism 5软件作图。
2 结果 2.1 外周血细胞检测与骨髓有核细胞计数Tab 1结果显示,与正常对照组相比,模型小鼠在濒死状态或存活14 d后,外周血三系红细胞、白细胞、血小板和骨髓有核细胞数量都明显下降(P < 0.01),尤其白细胞下降最明显;与模型组相比,TMP给药组红细胞出现上升趋势,其中TMP高剂量组上升最明显(P < 0.05);与模型组相比,TMP给药组血小板出现上升,其中TMP低剂量组增加最明显(P < 0.01);与模型组相比,TMP高剂量组有核细胞明显上升(P < 0.05)。
| Group | WBC(×109·L-1) | RBC(×1012·μL-1) | PLT(×109·L-1) | Nucleated cell(×106) |
| Control | 7.19±0.96 | 10.82±0.49 | 421.50±101.36 | 12.75±2.42## |
| TBI | 0.36±0.17## | 8.18±1.06## | 151.00±39.05## | 2.30±1.04## |
| Model | 0.19±0.07## | 6.53±0.64## | 78.00±22.8## | 1.94±0.53## |
| TMP(5 g·L-1) | 0.87±0.37## | 8.21±0.82## | 300.50±106.12* | 2.28±0.41## |
| TMP(10 g·L-1) | 0.51±0.21## | 9.16±0.62#* | 138.50±83.26 | 3.14±0.62## |
| TMP(20 g·L-1) | 0.46±0.22## | 9.86±0.71** | 231.67±141.82 | 4.51±4.01##* |
| *P < 0.05, **P < 0.01 vs model; #P < 0.05, ##P < 0.01 vs control | ||||
Fig 1的骨髓病理可见,正常对照组造血组织结构完整,造血细胞分布均匀,造血细胞增殖旺盛;而模型组有核细胞明显减少,巨核细胞缺如,大量脂肪空泡代替造血细胞。TMP给药各组骨髓有核细胞增加,随TMP给药剂量的增加,骨髓有核细胞增加越明显。

|
| Fig 1 Bone marrow pathology of each group (HE ×200) A: Control group; B: TBI group; C: Model group; D: TMP low dose group; E: TMP medium dose group; F: TMP high dose group. |
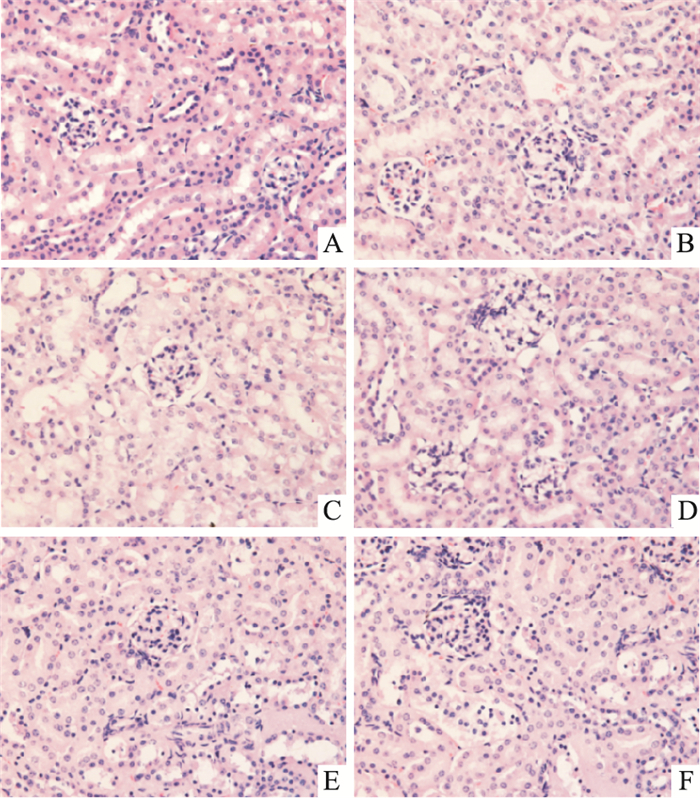
Fig 2的肾脏病理可见,模型组小鼠肾小管上皮细胞水肿,但无明显的淋巴细胞浸润;TMP给药各组未见明显的肾脏病理学改变。
|
| Fig 2 Renal pathology of each group (HE×400) A: Control group; B: TBI group; C: Model group; D: TMP low dose group; E: TMP medium dose group; F: TMP high dose group. |
Tab 2结果显示,与正常对照组相比,模型组肾脏MDA含量明显升高(P < 0.05);TMP中、高剂量组及单纯辐照组肾脏中MDA含量与模型组相比明显降低(P < 0.05, P < 0.01)。相比于正常对照组,模型组的SOD活力明显降低(P < 0.05);TMP高剂量组SOD活力与模型组相比明显升高(P < 0.05)。与正常对照组相比,单纯辐照组、模型组、TMP低剂量组肾脏GSH含量明显下降(P < 0.01);TMP中、高剂量组GSH含量与模型组相比明显升高(P < 0.01)。与正常对照组相比,模型组GSH-Px活力明显下降(P < 0.05),而单纯辐照组、TMP给药各组无明显统计学差异(P>0.05)。
| Group | MDA | SOD | GSH | GSH-Px |
| Control | 0.47±0.04 | 522.13±46.40 | 4.34±0.18 | 1 459.73±77.70 |
| TBI | 0.54±0.10* | 419.47±40.88 | 2.26±0.30## | 1 025.20±278.77 |
| Model | 0.89±0.13# | 337.46±97.52# | 1.90±0.25## | 945.64±161.69# |
| TMP(5 mg·mL-1) | 0.68±0.16 | 410.82±63.58 | 2.47±0.44## | 1 274.34±149.80 |
| TMP(10mg·mL-1) | 0.50±0.11** | 477.23±71.80 | 3.54±0.71** | 1 237.80±222.05 |
| TMP(20mg·mL-1) | 0.48±0.10** | 500.30±48.64* | 3.69±0.52** | 1 325.01±142.80 |
| *P < 0.05, **P < 0.01 vs model; #P < 0.05, ##P < 0.01 vs control | ||||
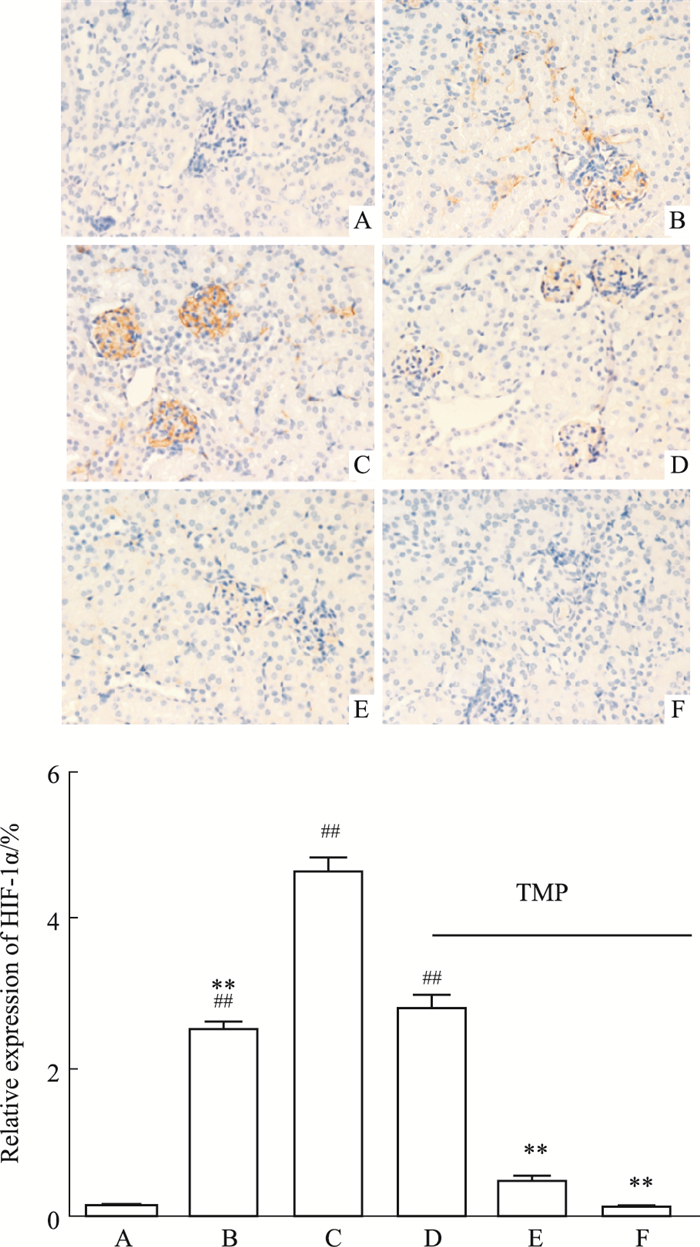
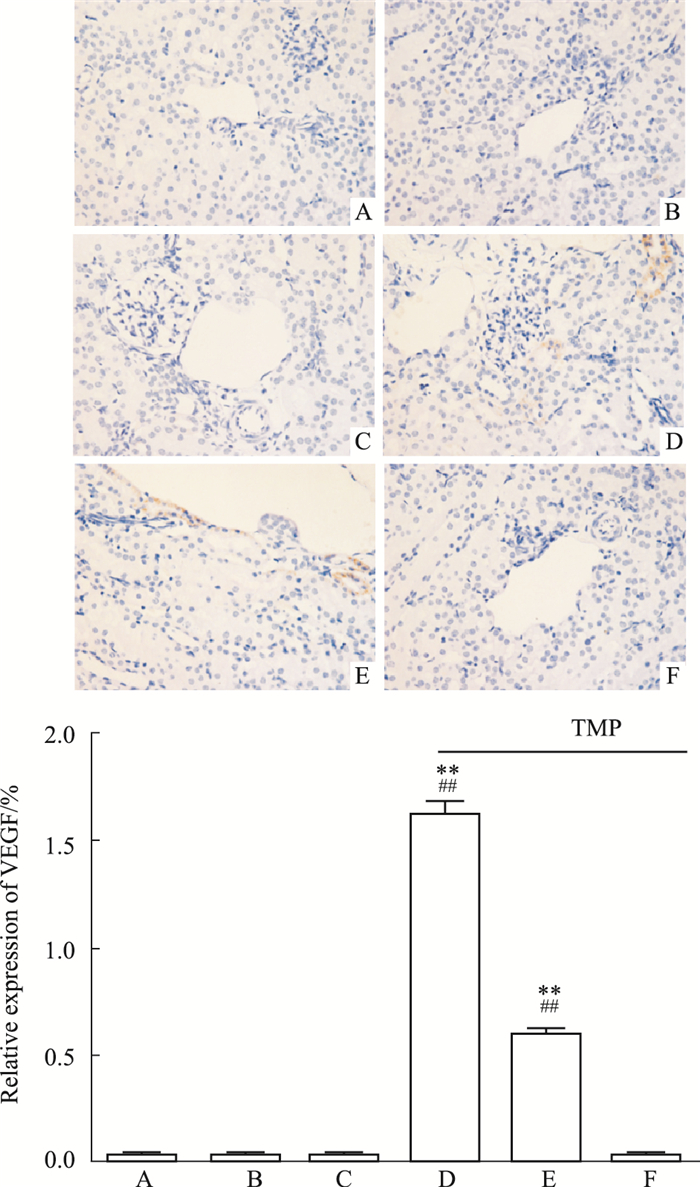
经免疫组化检测,正常对照组未见HIF-1α表达,单纯辐照组小鼠肾小球基底膜区可见少量棕黄色的阳性颗粒表达,模型组HIF-1α阳性表达量明显增多;经TMP治疗后,与模型组相比,TMP中、高剂量组HIF-1α明显下降(P < 0.01),TMP高剂量组几乎未见HIF-1α表达,见Fig 3。正常对照组、单纯辐照组、模型组小鼠未见VEGF表达,但经川芎嗪干预后,TMP低、中剂量组肾血管旁肾小管出现VEGF表达(Fig 4)。
|
| Fig 3 Expression of HIF-1α in renal tissues by immunohistochemical staining (×400) A: Control group; B:TBI group; C: Model group; D:TMP low dose group; E: TMP medium dose group; F: TMP high dose group.**P < 0.01 vs model; ##P < 0.01 vs control |
|
| Fig 4 Expression of VEGF in renal tissues by immunohistochemical staining (×400) A: Control group; B:TBI group; C: Model group; D:TMP low dose group; E: TMP medium dose group; F: TMP high dose group. **P < 0.01 vs model; ##P < 0.01 vs control |
免疫介导的BMF模型作为最接近SAA患者发病机制的动物模型[2],目前国内外大多采用辐照结合淋巴细胞输注的方法建立免疫介导的BMF动物模型。本实验中,我们通过X射线辐照结合淋巴细胞输注造模14 d后,模型组小鼠外周血三系和骨髓有核细胞均明显减少,骨髓病理可见脂肪空泡、巨核细胞缺如,说明成功建立免疫介导的BMF小鼠模型。既往研究表明,多种致病因素如辐照、缺血缺氧、炎症等都可导致肾脏氧化应激反应[6-7]。本实验肾脏病理切片显示,模型组小鼠肾小管水肿,检测肾脏氧化应激反应相关指标发现,与正常对照组相比,模型组小鼠肾脏氧化应激指标MDA明显上升,而抗氧化应激指标SOD、GSH、GSH-Px出现明显下降,单纯辐照组小鼠肾脏GSH明显下降,提示单纯辐照及造模都可导致小鼠肾脏氧化应激反应。
缺氧诱导因子HIF-1α是一种细胞应对缺氧的反应元件,已被证明在辐射损伤后被激活和上调表达[12],并参与多种应激反应。TMP作为一种有效的抗氧化剂,能够降低多种原因诱导的氧化应激反应,还能降低HIF-1α的表达[13]。并且HIF-1α参与调节VEGF的表达,而VEGF能通过诱导新血管的形成来重塑肾血流动力学[14]。那么,TMP能否通过HIF-1α/VEGF信号通路来减轻BMF小鼠肾脏因辐照与严重贫血诱导的氧化应激,值得深入探讨。
在本实验中,单纯辐照及造模后小鼠肾脏都存在氧化应激反应,并且HIF-1α蛋白表达增加,说明单纯辐照及造模后肾脏氧化应激可能与HIF-1α表达有关。给予TMP干预后,BMF小鼠肾脏无明显的病理学改变,TMP中、高剂量组肾脏MDA下降,而SOD、GSH上升,氧化与抗氧化系统恢复平衡,肾小球中HIF-1α蛋白表达明显下降、肾小管中出现VEGF蛋白表达,相关文献也证实,在HIF-1α降解的条件下,VEGF能被连续合成和持续表达[14],表明TMP可能通过抑制HIF-1α及上调VEGF蛋白表达,即通过调节HIF-1α/VEGF信号通路,从而减少模型小鼠肾脏氧化应激反应,达到保护小鼠肾脏的作用。
综上所述,TMP对免疫介导的骨髓衰竭C57BL/6小鼠模型肾脏氧化应激具有良好保护作用,其作用机制可能涉及HIF-1α/VEGF信号通路调控。
| [1] |
Young N S, Calado R T, Scheinberg P. Current concepts in the pathohysiology and treatment of aplastic anemia[J]. Blood, 2006, 108(8): 2509-19. doi:10.1182/blood-2006-03-010777 |
| [2] |
Li J, Chen H, Lyu Y B, et al. Intraperitoneal injection of multiplacentas pooled cells treatment on a mouse model with aplastic anemia[J]. Stem Cells Int, 2016, 2016: 3279793. |
| [3] |
Feng X, Lin Z, Sun W, et al. Rapamycin is highly effective in murine models of immune-mediated bone marrow failure[J]. Haematol, 2017, 102(10): 1691-703. doi:10.3324/haematol.2017.163675 |
| [4] |
Chen J, Desierto M J, Feng X, et al. Immune-mediated bone marrow failure in C57BL/6 mice[J]. Exp Hematol, 2015, 43(4): 256-67. doi:10.1016/j.exphem.2014.12.006 |
| [5] |
王洋, 肖扬, 李力, 等. 氯甲基苯甲酰氨标记骨髓间充质干细胞在免疫介导骨髓衰竭小鼠模型体内的归巢[J]. 中国组织工程研究, 2012, 16(10): 1716-20. Wang Y, Xiao Y, Li L, et al. In vivo homing of chloromethyl-benzamidodialkylcarbocyanine-labeled bone marrow mesenchymal stem cells after transplantation into a mouse model of immune-mediated bone marrow failure[J]. Chin J Tissue Engin Res, 2012, 16(10): 1716-20. doi:10.3969/j.issn.1673-8225.2012.10.002 |
| [6] |
Bellés M, Gonzalo S, Serra N, et al. Environmental exposure to low-doses of ionizing radiation. Effects on early nephrotoxicity in mice[J]. Environ Res, 2017, 156: 291-6. doi:10.1016/j.envres.2017.03.034 |
| [7] |
Nuhu F, Bhandari S. Oxidative stress and cardiovascular complications in chronic kidney disease, the impact of anaemia[J]. Pharmaceuticals (Basel), 2018, 11(4): 103. doi:10.3390/ph11040103 |
| [8] |
舒冰, 周重建, 马迎辉, 等. 中药川芎中有效成分的药理作用研究进展[J]. 中国药理学通报, 2006, 22(9): 1043-7. Shu B, Zhou C J, Ma Y H, et al. Research progress on pharmacological activities of the available compositions in Chinese medicinal herb Ligusticum chuanxiong[J]. Chin Pharmacol Bull, 2006, 22(9): 1043-7. doi:10.3321/j.issn:1001-1978.2006.09.005 |
| [9] |
Zheng H, Wang S, Zhou P, et al. Effects of ligustrazine on DNA damage and apoptosis induced by irradiation[J]. Environ Toxicol Pharmacol, 2013, 36(3): 1197-206. doi:10.1016/j.etap.2013.09.023 |
| [10] |
Fengb L, Ke N, Cheng F, et al. The protective mechanism of ligustrazine against renal ischemia/reperfusion injury[J]. J Surg Res, 2011, 166(2): 298-305. doi:10.1016/j.jss.2009.04.005 |
| [11] |
程闰, 夏梁静, 刘刚, 等. 川芎嗪对膜性肾病模型大鼠肾脏的保护作用[J]. 中国组织工程研究, 2019, 23(11): 1730-7. Cheng R, Xia L J, Liu G, et al. Protective effect of tetramethylpyrazine on kidney in rats with membranous nephropathy[J]. Chin J Tissue Engin Res, 2019, 23(11): 1730-7. doi:10.3969/j.issn.2095-4344.1100 |
| [12] |
Rabbani Z N, Mi J, Zhang Y, et al. Hypoxia inducible aactor 1α signaling in fractionated radiation-induced lung injury:role of oxidative stress and tissue hypoxia[J]. Radiation Res, 2010, 173(2): 165-74. doi:10.1667/RR1816.1 |
| [13] |
Zhang F, Lu S, He J, et al. Ligand activation of PPARγ by ligustrazine suppresses pericyte functions of hepatic stellate cells via SMRT-mediated transrepression of HIF-1α[J]. Theranostics, 2018, 8(3): 610-26. doi:10.7150/thno.22237 |
| [14] |
Neelam S, Brooks M M, Cammarata P R. Lenticular cytoprotection. Part 1:The role of hypoxia inducible factors-1α and -2α and vascular endothelial growth factor in lens epithelial cell survival in hypoxia[J]. Mol Vis, 2013, 19: 1-15. |

