

2. 广东天然药物研究与开发重点实验室,广东 湛江 524023;
3. 广东医科大学·广东润和生物科技有限公司辅酶Q10联合研究中心,广东 东莞 523808
吴铁(1955-),男,硕士,教授,硕士生导师,研究方向:抗炎免疫与骨质疏松药理学,通讯作者,E-mail:wutie2@163.com
 ,
CHEN Cai-ling1,
ZHENG Xiao-yan1,
LIU Cui-juan1,
CUI Liao1,2,
XU Bi-lian1,2
,
CHEN Cai-ling1,
ZHENG Xiao-yan1,
LIU Cui-juan1,
CUI Liao1,2,
XU Bi-lian1,2
 ,
WU Tie1,2,3
,
WU Tie1,2,3

2. Key Lab of Nature Drug Research and Development, Zhanjiang, Guangdong 524023, China;
3. Guangdong Medical University & Guangdong Runhe Biological Technology Co., Ltd. Coenzyme Q10 Research Institute, Dongguan, Guangdong 523808, China
随着社会人口老龄化的到来,与增龄相关的肌肉骨骼系统疾病日益受到关注。骨质疏松症(osteoporosis,OP)是指骨质减少和骨组织微结构恶化导致骨脆性增加和易感性骨折的疾病[1]。而肌少症(sarcopenia,SP)则被认为能影响机体平衡增加跌倒风险,从而使老年人功能受限[2]。两种疾病相互影响,紧密关联,如何解决老年性肌少症伴随而来的骨质疏松骨折风险,是一个不容忽视的问题。辅酶Q10是生物体内广泛存在的一类脂溶性醌类物质,具有较强抗氧化和清除氧自由基的的能力,还能改善线粒体的功能障碍[3]。随着年龄增长,辅酶Q10合成能力下降,老年人体内辅酶Q10含量降低,因此通过外源性补充十分必要[4]。一方面[5],辅酶Q10能促进成骨细胞的分化,并抑制破骨细胞的分化,从而使骨量增加。另一方面[6],辅酶Q10对缺血/再灌注造成的骨骼肌损伤具有保护作用,该损伤是由于氧自由基的产生和促炎细胞因子的合成与释放造成。因此,本研究建立D-半乳糖小鼠的亚急性衰老模型,观察辅酶Q10是否能够同时作用于肌肉骨骼系统,为临床上治疗“骨质疏松症-肌少症”的难题提供参考依据。
1 材料与方法 1.1 实验动物40只SPF级8周龄雄性KM小鼠,体质量(30±5) g,购自广东省医学实验动物中心,合格证号:SYXK(粤)2013-0002。
1.2 药物与试剂骨化三醇,购于Hoffmann-La Roche AG,批号:B4208。D-半乳糖,购于索莱宝,批号:129G051。生理盐水,购于石家庄四药有限公司,批号1703032103。
1.3 仪器PTY-224-423电子天平(福州华志科学仪器有限公司);数控超声波清洗器KQ5200DB(昆山超声仪器有限公司);858 Mini Bionix型材料测试系统(美国MST公司);Viva Micro CT 40(SCANCO Medical AG);ZTS-20N拉力检测仪(日本IMADA);JEM 1400(日本JEOL)
1.4 实验动物分组与给药根据体质量按随机区组法,将小鼠平均分配到4组,每组10只,具体分组及给药为:(1)正常对照组(Control):皮下注射及灌胃给予生理盐水;(2)D-半乳糖模型组(Model):皮下注射500 mg·kg-1·d-1 D-半乳糖(生理盐水溶解D-半乳糖,浓度为0.28 mol·L-1),并灌胃给予生理盐水;(3)骨化三醇组(Calcitriol):造模方法同模型组,然后按0.076 μg·kg-1·d-1灌胃骨化三醇混悬液(取一粒含0.25 μg骨化三醇的胶囊,加入33.3 mL生理盐水,室温超声60 min,超声功率为70%)。(4)辅酶Q10组(CoQ10):造模方法同模型组,然后按250 mg·kg-1·d-1灌胃辅酶Q10紫苏籽油溶液(将1 250 mg辅酶Q10加入到50 ml紫苏籽油中,搅拌溶解即得)。所有小鼠连续给药12周。每周称体质量1次,从第8周开始,每7 d测一次双前肢肌力。实验结束时,取左侧股骨进行micro-CT及骨生物力学检测,取腓肠肌做超微透射电子显微镜检查。
1.5 观察指标及测定方法 1.5.1 体质量的检测每周称体质量1次,实验结束取材前称体质量,作为实验结束时的体质量。实验开始前和实验结束时的体质量的差值,即为体质量净增长值(△W)。
1.5.2 股骨质量和质量指数的检测取股骨,除净表面附着组织,用滤纸吸干表面体液,电子天平称重,即得股骨质量。股骨质量/实验结束时体质量,即为股骨质量指数。
1.5.3 双前肢肌力的检测将小鼠双前肢放在拉力计的感应网处,待小鼠适应1 min后轻轻提起尾部使之与身体平行,向小鼠前倾的相反方向缓慢用力拖拽,0.5~1 min读数,每只小鼠测定3次,取拉力读数最大的数值。
1.5.4 骨生物力学的检测用858 Mini Bionix型材料测试系统进行三点弯曲实验,分析股骨生物力学性能。把股骨放在MTS实验机上,加载速度为0.155 mm·s-1,跨距5 mm。绘制载荷-形变曲线,从曲线上读取数据,根据相应的公式计算参数指标:最大载荷(maximum load)、断裂载荷(break load)、弹性载荷(elastic load)、刚性系数(stiffness)。
1.5.5 micro-CT的检测将股骨沿着长轴放在固定器内,用viva CT40对股骨干骺端进行扫描。viva CT40选择扫描参数:能量/强度为70 kVP,114 μA,8 W,扫描时间为29.7 min,片数Slice为505。扫描完成后,选取距生长板远端1.0 mm、层厚2.0 mm的骨组织为松质骨感兴趣区域(region of interest,ROI)行三维重建,以最低阈值为148提取图像信息。使用其软件(SCANCO Medical AG)进行重建定量分析。参数如下:连接密度(connectivity density,Conn.D.)、结构模型指数(structure model index,SMI)、骨密度(bone mineral density,BMD)、骨体积分数(bone volume/tissue volume,BV/TV)、骨小梁数量(trabecular number,Tb.N)、骨小梁厚度(trabecular thickness,Tb.Th)、骨小梁分离度(trabecular separation,Tb.Sp)。
1.5.6 腓肠肌透射电子显微镜的检测将新鲜组织沿纵轴用锋利手术刀片切成宽为1 mm,长为2~3 mm的组织块,投入质量浓度为30 g·L-1的戊二醛溶液中,4 ℃固定24 h。依次经磷酸缓冲溶液漂洗、质量浓度为10 g·L-1的锇酸溶液固定、逐级乙醇和丙酮脱水、包埋剂浸透与聚合,1~2 μm半薄切片定位后,切60 nm超薄切片,染色后干燥并在透射电子显微镜下观察。
使用Gantan832软件,随机视野拍10张,放大倍数分别为15 000倍和40 000倍。画出并统计肌原纤维中的肌小节(sarcomere,S)、明带(I-band, I)、暗带(A-band,A)、H带(H-zone, H)、M线(M-line, M)、Z线(Z-line, Z)和重叠肌动蛋白和肌球蛋白肌丝(overlapped actin and myosin myofilaments,O)长度。
1.6 统计学分析实验数据均用x±s表示,采用SPSS 22.0软件进行单因素方差分析(ANOVA),若Levene检验方差齐性,则组间采用LSD检验;若方差不齐则采用welch校正后做方差分析,组间采用Dunnett’s T3多重检验。
2 结果 2.1 各组小鼠体质量变化和体质量净增长比较由Tab 1可见,各组间小鼠体质量差异无统计学意义(P>0.05)。由Tab 2可见,与正常对照组相比,模型组体质量净增长明显减少(P < 0.01)。与模型组相比,骨化三醇组和辅酶Q10组体质量增长均明显增加(P < 0.05)。
| Group | 0 W | 2 W | 4 W | 6 W | 8 W | 10 W | 12 W |
| Control | 29.9±4.6 | 32.5±5.4 | 34.5±5.6 | 37.2±5.7 | 39.0±5.5 | 40.0±5.2 | 40.8±5.2 |
| Model | 31.8±4.9 | 32.8±4.3 | 33.3±3.5 | 34.5±3.9 | 36.9±4.6 | 36.7±3.9 | 37.2±3.7 |
| Calcitriol | 29.5±3.9 | 32.0±4.9 | 32.5±4.7 | 34.7±5.2 | 37.1±5.4 | 37.5±5.4 | 38.6±5.4 |
| CoQ10 | 31.0±4.8 | 33.0±5.2 | 34.3±5.2 | 36.5±5.9 | 38.6±5.0 | 38.5±5.8 | 39.8±6.0 |
| Group | △W/g |
| Control | 11.41±2.77 |
| Model | 5.85±3.97** |
| Calcitriol | 9.07±3.70# |
| CoQ10 | 9.38±3.36# |
| **P < 0.01 vs control; #P < 0.05 vs model | |
由Tab 3可见,与正常对照组相比,模型组股骨质量明显减少(P < 0.05),股骨质量指数有下降的趋势,但差异无统计学意义。与模型组相比,骨化三醇组和辅酶Q10组股骨质量及质量指数均明显增加(P < 0.05)。
| Group | Femur mass/mg | Femur mass index/ mg·g-1 |
| Control | 87.4±13.1 | 2.10±0.16 |
| Model | 74.9±11.9* | 1.97±0.28 |
| Calcitriol | 86.9±13.3# | 2.27±0.43# |
| CoQ10 | 89.1±10.4# | 2.28±0.14# |
| *P < 0.05 vs control; #P < 0.05 vs model | ||
由Tab 4可见,第8周开始,与正常对照组相比,模型组双前肢肌力有下降趋势。与模型组相比,用药组双前肢肌力无明显改变。
| Group | 8W | 9W | 10W | 11W | 12W |
| Control | 1.43±0.18 | 1.40±0.18 | 1.41±0.25 | 1.67±0.34 | 1.80±0.22 |
| Model | 1.30±0.18 | 1.32±0.21 | 1.39±0.12 | 1.65±0.16 | 1.72±0.14 |
| Calcitriol | 1.43±0.29 | 1.40±0.14 | 1.57±0.26 | 1.64±0.29 | 1.75±0.19 |
| CoQ10 | 1.55±0.27 | 1.40±0.21 | 1.55±0.18 | 1.70±0.13 | 1.86±0.13 |
由Tab 5可见,与正常对照组相比,模型组股骨最大载荷、刚性系数分别下降19.8%、23.7%(P < 0.01)。与模型组相比,骨化三醇组最大载荷、刚性系数分别增加26.9%(P < 0.05)、13.2%(P < 0.01);辅酶Q10组最大载荷增加26.5%(P < 0.01)。
| Group | Break load/N | Maximum load/N | Elastic load/N | Stiffness/N·mm-1 |
| Control | 24.77±3.39 | 28.74±3.74 | 14.14±1.54 | 234.45±55.24 |
| Model | 21.50±5.00 | 23.06±4.86** | 12.65±1.18 | 178.96±36.79** |
| Calcitriol | 25.25±4.02 | 27.88±3.79# | 13.24±2.29 | 202.59±31.88* |
| CoQ10 | 26.20±6.69 | 29.18±6.04## | 13.34±2.48 | 206.25±35.29 |
| *P < 0.05, **P < 0.05 vs control; #P < 0.05, ##P < 0.01 vs model | ||||
由Tab 6可见,与正常对照组相比,模型组micro-CT参数Conn.D、BMD降低(P < 0.05),而Tb.Sp增加(P < 0.05)。与模型组相比,骨化三醇组BMD、Tb.Th增加(P < 0.05),而Tb.Sp降低(P < 0.05);辅酶Q10组Conn.D.、BMD、Tb.Th均增加(P < 0.05),而SMI、Tb.Sp明显下降(P < 0.01)。
| Parameter | Control | Model | Calcitriol | CoQ10 |
| Conn.D./ 1·mm-3 | 28.050±12.290 | 7.180±4.250* | 36.630±22.170 | 38.640±22.280# |
| SMI | 2.650±0.340 | 2.890±0.260 | 2.500±0.430 | 2.050±0.730*## |
| BMD/mg HA /ccm | 71.950±43.290 | 25.330±16.600* | 78.840±47.210# | 84.640±47.300## |
| BV/TV/ % | 0.076±0.045 | 0.037±0.012 | 0.103±0.058 | 0.140±0.097 |
| Tb.N/ mm-1 | 1.480±0.700 | 0.810±0.280 | 1.880±0.980 | 2.300±1.110 |
| Tb.Th/mm | 0.049±0.008 | 0.046±0.004 | 0.053±0.005# | 0.057±0.011*## |
| Tb.Sp/mm | 0.770±0.410 | 1.310±0.420* | 0.680±0.490# | 0.460±0.210## |
| *P < 0.05 vs control; #P < 0.05, ##P < 0.01 vs model | ||||
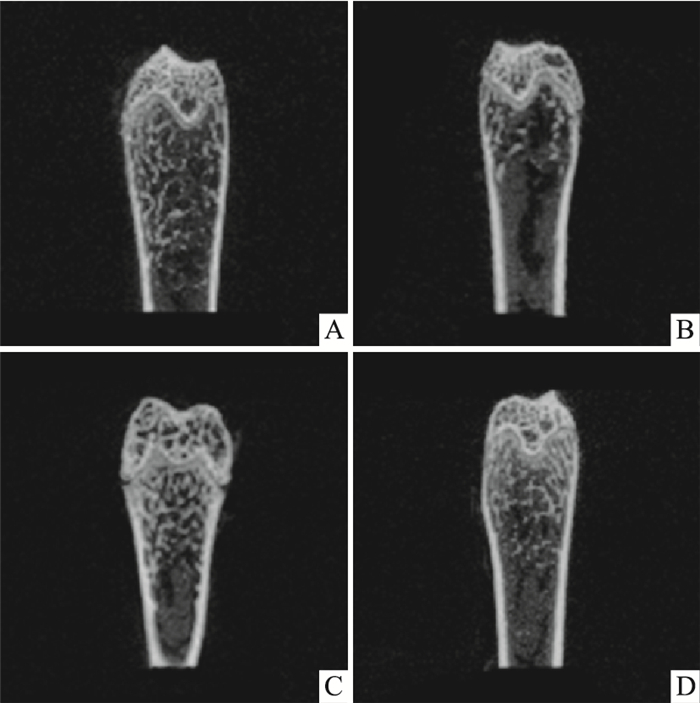
由Fig 1可见,正常对照组股骨骨小梁数量丰富而致密。与正常对照组相比,模型组骨小梁数量较少,排列稀疏。与模型组相比,骨化三醇组和辅酶Q10组骨小梁数量丰富而密集,连续性好。
|
| Fig 1 2D reconstruction of micro-CT of mouse femur from control mice(A), model mice(B), calcitriol mice(C) and CoQ10 mice(D) |
由Fig 2可见,正常对照组股骨骨小梁较粗,空隙较小,网状结构明显。与正常对照组相比,模型组骨小梁缺失明显,网状结构退化。与模型组相比,骨化三醇组和辅酶Q10组骨小梁较粗,网状结构明显。

|
| Fig 2 ROI region 3D reconstruction of micro-CT of mouse femur from control group(A), model group(B), calcitriol group(C) and CoQ10 group(D) |
由Fig 3A和Fig 4A可见,正常组腓肠肌肌纤维排列有序,肌丝排列整齐,肌纤维间可见卵圆形线粒体,线粒体嵴较为清晰。由Fig 3B和Fig 4B可见,模型组腓肠肌肌纤维和肌丝排列不够紧密,肌丝或肌原纤维间存在缝隙和空洞,A带出现断裂,肌原纤维间出现数量丰富且异常增大的线粒体,其形状不规则,有的长度可超过一个肌小节。Fig 3C和Fig 4C可见,骨化三醇组的肌丝排列整齐,可见丰富的肌质网和横管系统,肌原纤维间存在少量卵圆形线粒体。Fig 3D和Fig 4D可见,辅酶Q10组的肌原纤维束排列有序而紧凑,可见卵圆形线粒体,线粒体嵴较为清晰。

|
| Fig 3 Electron micrographs of longitudinal sections of gastrocnemius myofibers from control group(A), model group(B), calcitriol group(C) and CoQ10 group(D)(15 000×) S, sarcomeres; A, A-band; I, I-band; white arrowheads, intermyofibrillar mitochondria |

|
| Fig 4 Electron micrographs of longitudinal sections of gastrocnemius myofibers from control group(A), model group(B), calcitriol group(C) and CoQ10 group(D)(40 000×) H, H-zone; M, M-line; white arrowheads, intermyofibrillar mitochondria; black arrowheads, cavity |
由Tab 7可见,与正常对照组相比,模型组腓肠肌纤维的肌小节、I带、H带、M线和Z线长度明显增加(P < 0.01),重叠肌动蛋白和肌球蛋白肌丝长度明显缩短(P < 0.01)。与模型组相比,骨化三醇组和辅酶Q10组腓肠肌肌纤维的I带、H带、M线和Z线均明显缩短(P < 0.01),而重叠肌动蛋白和肌球蛋白肌丝长明显增长(P < 0.01)。
| Parameter | Control | Model | Calcitriol | CoQ10 |
| S/μm | 1.73±0.10 | 1.86±0.18** | 1.77±0.14 | 1.85±0.10 |
| I/μm | 0.372±0.062 | 0.521±0.096** | 0.411±0.108## | 0.408±0.034## |
| A/μm | 1.35±0.08 | 1.41±0.19 | 1.44±0.08 | 1.39±0.06 |
| O/μm | 0.593±0.030 | 0.431±0.141** | 0.627±0.027## | 0.594±0.047## |
| H/μm | 0.156±0.015 | 0.345±0.172** | 0.176±0.022## | 0.171±0.022## |
| M/μm | 0.055±0.010 | 0.083±0.023** | 0.054±0.008## | 0.053±0.006## |
| Z/μm | 0.037 9±0.009 8 | 0.091 4±0.018 2** | 0.045 8±0.009 6## | 0.045 0±0.008 9## |
| **P < 0.01 vs control; ##P < 0.01 vs model | ||||
与正常对照组相比,D-半乳糖模型组小鼠体质量净增长值明显下降,说明D-半乳糖能导致小鼠体质量减轻。micro-CT定量参数的结果显示,与正常对照组相比,D-半乳糖组的Conn.D.和BMD降低,而Tb.Sp增加。micro-CT的三维重建图中可见,模型组骨小梁排列稀疏,存在较大空洞,网状结构明显退化。结果表明,连续12周皮下注射500 mg·kg-1·d-1 D-半乳糖,能致雄性小鼠骨量减少及骨微结构损伤。本次研究结果与课题组前期研究[7]相一致。D-半乳糖代谢过程中产生的自由基能破坏胶原蛋白,引起骨矿物质流失,加速雄鼠衰老,导致骨量丢失[8],同时D-半乳糖转化为晚期糖基化终产物(AGEs)在组织中累积,增加成骨细胞中蛋白水解酶的活性,从而诱导成骨细胞凋亡。
通过超微透射电子显微镜观察发现,模型组肌小节、I带、H带、M线和Z线长度显著性增长,重叠肌动蛋白和肌球蛋白的肌丝长度明显减少,且肌原纤维间存在大量形状不一的庞大线粒体。该发现与Sayed等[9]报道类似,老年鼠的肌原纤维中肌小节,I带和H带长度随着年龄增长而增加,而A带没有变化,并且肌原纤维间线粒体数量和横截面积明显增加。
肌原纤维是骨骼肌细胞的收缩单位,肌原纤维的成分直接影响着肌肉的生物学性能。当肌纤维被拉伸时,肌纤维伴随着I带延长而变长,而当肌纤维收到刺激而收缩并重叠时,肌纤维和I带会变短。通过拉伸和收缩,A带保持恒定长度,根据延长或缩短肌小节和I带,H带长度也发生改变[10]。本研究发现D-半乳糖诱导的衰老小鼠腓肠肌收缩性能下降,与老年小鼠的骨骼肌老化相似。这是由于D-半乳糖可以诱导线粒体DNA的缺失增加,导致三磷酸腺苷(ATP)水平下降,电子传递链复合物水平下降,最终诱导线粒体功能障碍[11]。模型组出现的大量庞大的线粒体,可能由于线粒体损伤,骨骼肌需要更多的能量,从而引发线粒体代偿性增加,以此供应氧化磷酸化障碍所致的能量缺乏[12]。
本研究还发现,与模型组相比,辅酶Q10组小鼠体质量净增长值明显增加,说明外源性补充辅酶Q10能保护D-半乳糖导致的小鼠体质量减轻。与模型组相比,辅酶Q10组小鼠股骨质量和股骨质量分数明显增加。此外,与模型组相比,辅酶Q10能明显增加股骨最大载荷、BMD和Tb.Th,并降低Tb.Sp。股骨micro-CT三维重建图可见,辅酶Q10组骨小梁较粗而厚且数量丰富。结果提示,辅酶Q10能增加股骨质量,改善D-半乳糖所致的骨微结构损伤,从而使骨骼的质量和功能上得到保护。
超微透射电子显微镜检查的结果显示,与模型组相比,辅酶Q10组的腓肠肌肌原纤维排列更为整齐,肌丝排列紧凑,线粒体形状规则且清晰。辅酶Q10组I带、H带、M线和Z线长度明显缩短,而重叠肌动蛋白和肌球蛋白肌丝长度明显增加,同时,辅酶Q10组并无观察到庞大线粒体。研究结果提示,辅酶Q10能够改善D-半乳糖造成的小鼠肌纤维收缩性能下降,维持肌原纤维结构的完整。进一步说明辅酶Q10对肌肉有保护作用。
辅酶Q10是人体重要的抗氧化剂和非特异性免疫增强剂,其生理功能广泛,除具有较强清除自由基和抗氧化功能、增强心脏动力和调节血脂等功能[3],还在抗骨质疏松作用方面有良好效果。研究表明[13],辅酶Q10既是成骨细胞生成核因子κB受体活化因子配体(RANKL)诱导的破骨细胞分化的抑制剂,也是成骨细胞分化的促进剂,其能明显抑制破骨细胞NFATc 1、TRAP和破骨细胞相关免疫球蛋白样受体的基因表达,并通过转录因子活性促进骨分化过程中的再生。
辅酶Q10能改善D-半乳糖致雄性小鼠腓肠肌肌原纤维超微结构,主要原因可能是一方面外源性补充辅酶Q10能加速清除D-半乳糖代谢产生的自由基堆积,降低氧化应激的水平,抑制线粒体的过氧化保护生物膜结构的完整性[14],使线粒体中氧化磷酸化活动得以维持,因而机体的能量负荷减轻。另一方面,辅酶Q10弥补了D-半乳糖致衰老小鼠体内辅酶Q10的缺失,辅助线粒体中ATP的磷酸还原作用,让细胞能量供应系统快速活化,从而增强老年机体的体能和精力[4]。此外,辅酶Q10还能通过复杂的分子机制作用于骨骼肌细胞。Boroujeni等[6]发现,辅酶Q10能通过抑制核因子κB(NF-κB)的活化作用,减少骨骼肌缺血再灌注模型大鼠腓肠肌中肿瘤坏死因子(TNF-α)和NF-κB的表达,从而减轻肌纤维变性和肥大细胞浸润。
本研究中还同时观察了骨化三醇对D-半乳糖致雄性小鼠骨骼和肌肉的影响,发现骨化三醇对改善骨微结构破坏和肌肉肌原纤维的损坏也有益处。已有证据表明[15],维生素D能增加肌肉内蛋白质合成及肌质网内钙的吸收,并且可以调节骨钙蛋白和相关炎症因子从而影响肌肉系统的生长发育过程。
本研究发现,连续12周皮下注射500 mg·kg-1·d-1D-半乳糖可致小鼠发生骨微结构破坏,并引起肌原纤维结构损伤。本研究创新之处在于首次观察辅酶Q10对这种D-半乳糖致亚急性衰老小鼠骨骼和肌原纤维损伤有明显的保护作用,提示了辅酶Q10能够同时作用于肌肉系统和骨骼系统,为临床上预防和治疗男性骨质疏松合并肌肉减少的患者提供了实验研究数据,为临床解决“骨质疏松症-肌少症”的治疗难题提供参考依据。但辅酶Q10究竟如何作用于D-半乳糖诱导的亚急性衰老小鼠的骨骼肌细胞仍需进一步地探讨。
( 致谢: 本实验在广东医科大学药理学实验室完成,感谢各位老师和同学的帮助 )
| [1] |
Lambert J K, Zaidi M, Mechanick J I. Male osteoporosis: Epidemiology and the pathogenesis of aging bones[J]. Curr Osteopor Rep, 2011, 9(4): 229-36. doi:10.1007/s11914-011-0066-z |
| [2] |
杨丽君, 吴永华, 张俐. 肌少症、骨质疏松症的关系及研究进展[J]. 中国骨质疏松杂志, 2017, 23(8): 1112-6. Yang L J, Wu Y H, Zhang L. Sarcopenia and osteoporosis: the connections and research progress[J]. Chin J Osteopor, 2017, 23(8): 1112-6. doi:10.3969/j.issn.1006-7108.2017.08.028 |
| [3] |
万艳娟, 吴军林, 吴清平. 辅酶Q10生理功能及应用研究进展[J]. 食品工业科技, 2014, 35(14): 390-5. Wan Y J, Wu J L, Wu Q P. Research progress in physiological functions and application of coenzyme Q10[J]. Sci Technol Food Ind, 2014, 35(14): 390-5. |
| [4] |
薛茂云. 辅酶Q10的营养作用及应用[J]. 江苏调味副食品, 2010, 27(1): 13-6. Xue M Y. Nutrition of coenzyme Q10 and its application[J]. Jiangsu Cond Subs Food, 2010, 27(1): 13-6. doi:10.3969/j.issn.1006-8481.2010.01.004 |
| [5] |
Zheng D, Cui C, Yu M, et al. Coenzyme Q10 promotes osteoblast proliferation and differentiation and protects against ovariectomy-induced osteoporosis[J]. Mol Med Rep, 2018, 17(1): 400-7. |
| [6] |
Boroujeni M B, Khayat Z K, Anbari K, et al. Coenzyme Q10 protects skeletal muscle from ischemia-reperfusion through the NF-kappa B pathway[J]. Perfusion, 2017, 32(5): 372-7. doi:10.1177/0267659116683790 |
| [7] |
梁美婷, 吕思敏, 王可欣, 等. 用Micro CT评价D-半乳糖致雄性小鼠骨质疏松模型及骨化三醇的防治作用[J]. 中国药理学通报, 2019, 35(3): 391-5. Liang M T, Lyu S M, Wang K X, et al. Evaluation of D-galactose induced osteoporosis in male mice by Micro CT and the preventive effect of calcitriol[J]. Chin Pharmacol Bull, 2019, 35(3): 391-5. doi:10.3969/j.issn.1001-1978.2019.03.019 |
| [8] |
Rehman S U, Shah S A, Ali T. Anthocyanins Reversed D-Galactose-Induced Oxidative Stress and Neuroinflammation Mediated Cognitive Impairment in Adult Rats[J]. Mol Neurobiol, 2017, 54(1): 255-71. |
| [9] |
Sayed R K, de Leonardis E C, Guerrero-Martínez J A, et al. Identification of morphological markers of sarcopenia at early stage of aging in skeletal muscle of mice[J]. Exp Gerontol, 2016, 83: 22-30. doi:10.1016/j.exger.2016.07.007 |
| [10] |
Huxley H E. The double array of filaments in cross-striated muscle[J]. J Biophys Biochem Cytol, 1957, 3(5): 631-48. doi:10.1083/jcb.3.5.631 |
| [11] |
刘建亚, 冯文静, 王仁萍. D-半乳糖致衰老动物模型及其机制研究进展[J]. 中华老年多器官疾病杂志, 2018, 17(3): 224-7. Liu J Y, Feng W J, Wang R P. Research progress in D-galactose-induced aging animal model and its mechanisms[J]. Chin J Mult Organ Dis Eld, 2018, 17(3): 224-7. |
| [12] |
武忠弼, 周晓军. 超微病理诊断学[M]. 上海: 上海科学技术出版社, 2003: 90-4. Wu Z B, Zhou X J. Ultramicro pathological diagnosis[M]. Shanghai: Shanghai Scientific & Technical Publishers, 2003: 90-4. |
| [13] |
Moon H, Ko W, Jung M, et al. Coenzyme Q10 regulates osteoclast and osteoblast differentiation[J]. J Food Sci, 2013, 78(5): H 785-891. doi:10.1111/1750-3841.12116 |
| [14] |
Garrido-Maraver J, Cordero M D, Oropesa-Avila M, et al. Clinical applications of coenzyme Q10[J]. Front Biosci, 2014, 19: 619-33. doi:10.2741/4231 |
| [15] |
姜宇, 宣文华, 任天丽. 维生素D对肌少症的影响及其作用[J]. 中国骨质疏松杂志, 2018, 24(9): 1246-9. Jiang Y, Xuan W H, Ren T L. The effect and influence of vitamin D on sarcopenia[J]. Chin J Osteopor, 2018, 24(9): 1246-9. doi:10.3969/j.issn.1006-7108.2018.09.024 |