

高尿酸血症(hyperuricemia,HUA)是一种嘌呤代谢紊乱。当男、女血尿酸水平分别超过7 mg·dL-1及6 mg·dL-1时,可以临床诊断为高尿酸血症。中国高尿酸血症的发病率逐年上升,患者人数多,易发展为痛风[1-2]。现有的流行病学和实验分析表明,高尿酸血症不仅仅是痛风的直接致病因素,而且还与代谢综合征、高血压、肾损伤、脂质代谢紊乱、心血管疾病等有着密切联系,作为风险因素,高尿酸血症对这些疾病的病程发展产生重要作用[3-4]。人和禽类体内无尿酸酶,体内嘌呤代谢的终产物为尿酸,而啮齿类体内因有尿酸酶的存在,尿酸最终会被氧化成尿囊素排出体外[5]。治疗高尿酸血症药物的主要作用靶点是黄嘌呤氧化酶(xanthine oxidase, XOD),可以催化次黄嘌呤或黄嘌呤,生成尿酸的一种黄素钼蛋白,广泛分布于小鼠的各个脏器中[6]。抑制XOD的活性,可以直接降低体内尿酸生成量,减低体内的血尿酸水平。临床选择性XOD抑制剂包括别嘌呤醇(一种嘌呤类抑制剂)及非布索坦(一种非嘌呤类抑制剂)[7-8]。
目前,高尿酸血症模型动物主要为啮齿类和禽类[5]。根据尿酸的生成及排泄路径,造模方式主要包括增加尿酸前体物质的摄入、抑制啮齿类动物的尿酸酶、减少尿酸排泄。可采取单一因素诱导,或多种因素联合诱导形成高尿酸血症动物模型。本研究根据XOD性质,完善了体外XOD抑制剂筛选方法,建立了急性及慢性高尿酸血症模型等体内实验方法,为基于高尿酸血症的分子靶点XOD药物研发奠定了实验基础。
1 材料与方法 1.1 材料 1.1.1 药物与试剂牛奶来源XOD1(CAS 9002-17-9)、微生物来源XOD2(CAS 9002-17-9)、黄嘌呤(xanthine, XA,CAS 69-89-6)、次黄嘌呤(hypoxanthine,CAS 68-94-0),均购自Sigma公司;氧嗪酸钾(oteracil potassium,CAS 2207-75-2),购自美仑生物;非布索坦(febuxostat, FBX,CAS 144060-53-7),购自TCI公司;别嘌呤醇(allopurinol, ALP,CAS 315-30-0),购自Alfa Aesar公司;谷草转氨酶(aspartate aminotransferase, AST)、血尿酸(uric acid, UA)、谷丙转氨酶(alanine aminotransferase, ALT)、肌酐(creatinine, Cre)、尿素(Urea)测定试剂盒,均购自北京中生北控生物技术有限公司;XOD活性测定试剂盒,购自南京建成生物科技有限公司。
1.1.2 仪器酶标仪(美国BioTek公司);THZ-C型恒温振荡器(江苏太仓科教仪器厂);高速低温离心机(德国Heraeus公司);pH计(美国Fisher Scientific公司)。
1.1.3 实验动物ICR小鼠,♂,购于北京维通利华生物科技股份有限公司,许可证编号为SCXK(京)2016-0006。饲养于中国医学科学院药物研究所实验动物管理中心,饲养温度为(22~25) ℃,湿度为40%~60%,每天光照时间和黑暗时间各为12 h,进食及饮水自由。小鼠经过动物伦理委员会批准,动物使用许可证编号:SYXK(京)2014-0023。
1.2 方法 1.2.1 血清生化测定3 500 r·min-1离心小鼠全血4 min,取出上层血清,按照试剂盒说明书对UA、AST、ALT、Cre、Urea、XOD进行测定。
1.2.2 组织XOD活性测定取出组织,加入适量预冷的生理盐水,冰水浴条件下,机械匀浆,按试剂盒说明书测定组织XOD活性。
1.2.3 黄嘌呤氧化酶抑制剂体外筛选模型分别选用牛奶和微生物为酶来源的两种XOD作为筛选模型研究对象,分别探究反应体系中酶浓度、底物浓度、反应温度、反应pH值和反应时间的影响,根据终产物尿酸在293 nm处的吸光度,选出最适宜的反应条件,并分别测定阳性药非布索坦和别嘌呤醇的IC50值,选定最适宜的酶来源。
1.2.4 急性高尿酸血症小鼠模型单次灌胃次黄嘌呤500 mg·kg-1联合皮下注射氧嗪酸钾300 mg·kg-1。设正常小鼠为正常对照组(Control),灌胃给予纯水及皮下注射溶剂0.5% CMC-Na混悬液。将诱导小鼠随机分成模型对照组(Mod-A)和非布索坦组(Mod-A-FBX),分别灌胃给予纯水和非布索坦2 mg·kg-1。同时,造模前取血,测定全部小鼠血尿酸水平作为0 h点,之后分别于给药后1、2、4 h时取血,测定小鼠血尿酸水平。并于4 h取血之后脱颈处死小鼠,取血清测定AST、ALT、Cre、Urea和XOD活性,并迅速取出小鼠肝脏放置于液氮中速冻,然后置于-80 ℃冰箱保存,用于测定肝XOD活性。
1.2.5 慢性高尿酸血症小鼠模型多次皮下注射氧嗪酸钾300 mg·kg-1。诱导期间,分别于d 7、9、11、13、14,通过内眦取血测定血尿酸水平。设正常ICR小鼠为对照组(Control),取血尿酸值稳定且高于180 μmol·L-1的动物作为慢性高尿酸血症小鼠模型(Mod-C),内眦取血之后脱颈处死小鼠,测定血清AST、ALT、Cre、Urea;取小鼠肾脏和肝脏左外侧叶进行病理分析,苏木精-伊红(hematoxylin-eosin, HE)染色;并快速取肝中叶、心脏、脾、肺、肾和小肠等重要组织,置于液氮中速冻,然后置于-80 ℃冰箱保存,用于检测各组织中XOD的活性。将诱导小鼠随机分为模型对照组(Mod-C)和非布索坦组(Mod-C-FBX),分别灌胃给予纯水和非布索坦2 mg·kg-1,每天给药及造模1次,连续5 d,观测血尿酸水平、血清XOD活性、肝组织XOD活性的变化情况。
1.3 统计学处理数据用x ± s表示,应用GraphPad Prism 6统计软件,采用One-way ANOVA进行多组间比较。
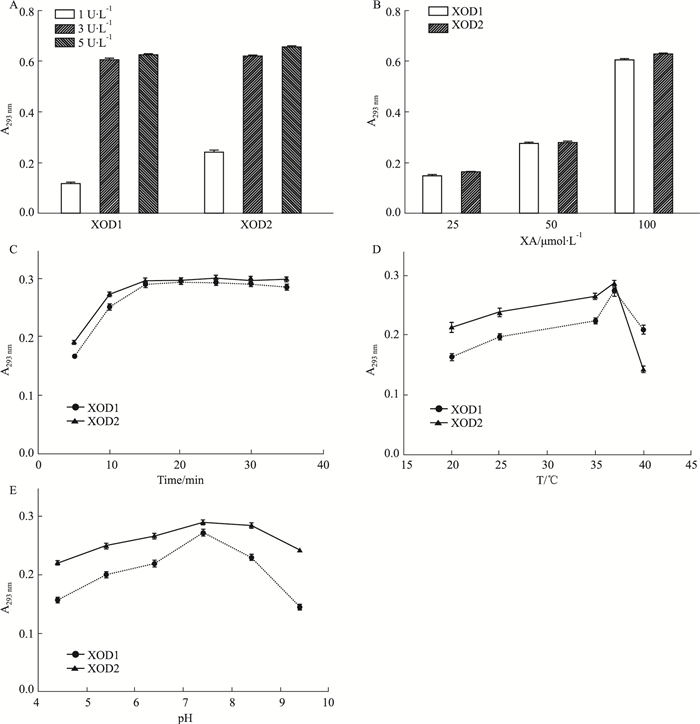
2 结果 2.1 XOD抑制剂体外筛选模型的建立常见的XOD分别为牛奶(XOD1)和微生物(XOD2)来源。室温下分别选择1、3、5 U·L-1的XOD1或XOD2,固定底物XA 100 μmol·L-1、反应时间30 min、pH 7.4的反应体系,观察不同浓度XOD的反应情况。Fig 1A结果显示,相同浓度的XOD1、XOD2反应效果相似;XOD1浓度为3、5 U·L-1的反应体系的OD值无明显差异,均明显高于其浓度为1 U·L-1的反应体系;XOD2的3种反应体系结果亦然。因此,选取3 U·L-1为XOD1或XOD2为最适反应浓度。
|
| Fig 1 Regulation of XOD activity (A), XA concentration (B), and reaction time (C), temperature (D), pH (E) on absorbance at wavelength 293 nm(x ± s, n=3) |
室温下,分别选择25、50、100 μmol·L-1的底物XA浓度,固定XOD1或XOD2 3 U·L-1、反应时间30 min、pH 7.4的反应体系,观察不同浓度底物XA的反应状态。Fig 1B结果显示,XOD1和XOD2反应体系基本一致,随着底物浓度的增加,其光吸收度逐渐增加。选择OD值范围较适宜的底物XA 50 μmol·L-1为最适的反应浓度。
室温下,固定XOD1或XOD2浓度为3 U·L-1、底物XA 50 μmol·L-1、pH 7.4的反应体系,观察不同作用时间对反应体系的影响。Fig 1C结果显示,XOD1和XOD2反应体系基本一致,选取进入反应平台期的20 min作为最适作用时间。
固定XOD1或XOD2 3U·L-1、底物XA 50 μmol·L-1、反应时间20 min、pH 7.4的反应体系,观察不同温度对反应体系的影响。Fig 1D结果显示,选取XOD酶活性最高点,则对于XOD1和XOD2反应体系的最适作用温度均为37 ℃。
37 ℃下分别选择pH为4.4、5.4、6.4、7.4、8.4、9.4的缓冲液,固定XOD1或XOD2 3 U·L-1、底物XA 50 μmol·L-1、反应时间20 min的反应体系,观察不同的缓冲液pH对反应体系的影响。Fig 1E结果显示,对于XOD1和XOD2酶活性最高点的反应体系均为pH 7.4。
目前已上市的选择性XOD抑制剂主要有ALP和FBX。分别应用XOD1或XOD2的反应体系,测定ALP、FBX抑制XOD的活性。Fig 2结果显示,ALP对XOD1和XOD2均具有明显的抑制作用,其IC50均可达到10-6 mol·L-1数量级;FBX对XOD1的抑制活性较强,其IC50可达到10-9 mol·L-1,但对XOD2则没有明显的抑制作用。

|
| Fig 2 Different activities of XOD1 and XOD2 in vitro (x ± s, n=3) A: ALP affecting XOD1; B: ALP affecting XOD2; C: FBX affecting XOD1; D: FBX affecting XOD2. |
上述结果提示,选择牛奶来源的XOD1 3 U·L-1、底物XA 50 μmol·L-1、反应时间为20 min、反应温度为37 ℃、pH为7.4的反应体系,FBX为阳性对照药,从而建立了XOD抑制剂的体外筛选模型。
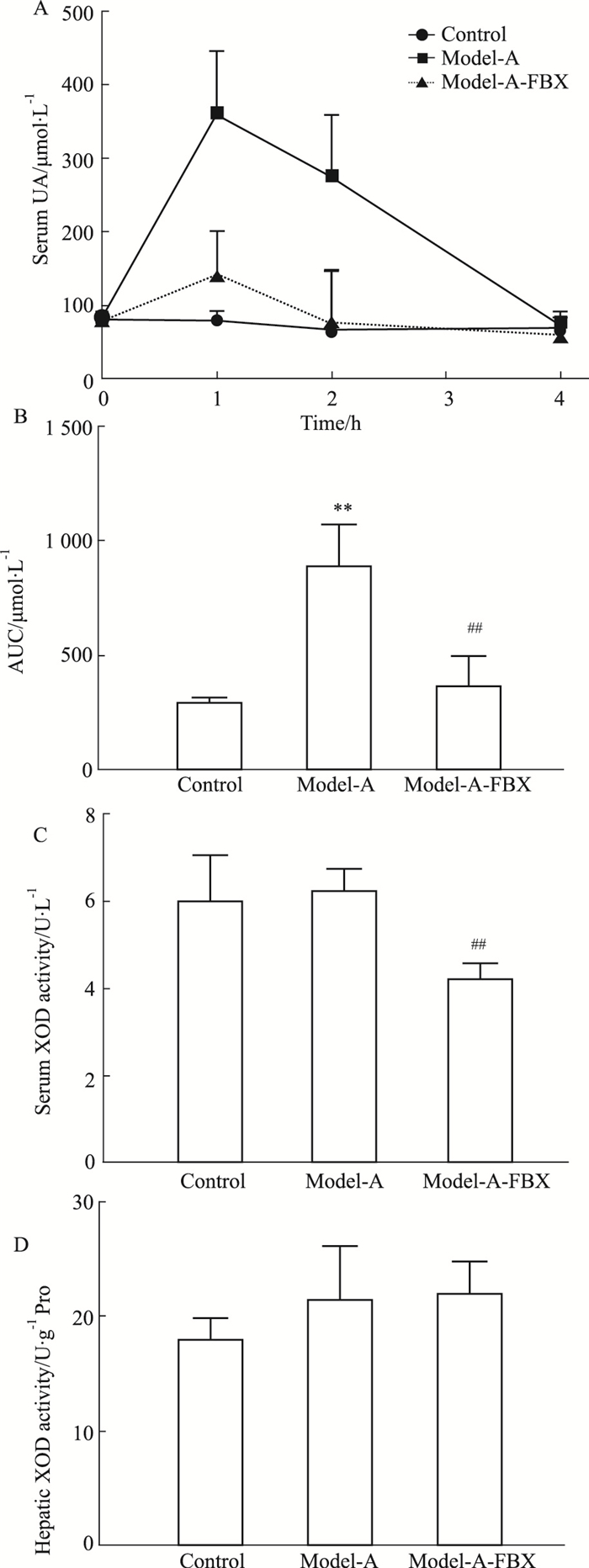
2.2 急性高尿酸血症小鼠模型的建立应用体质量为(24±2)g的♂ICR小鼠,单次灌胃给予次黄嘌呤500 mg·kg-1联合皮下注射氧嗪酸钾300 mg·kg-1,分别于给予阳性药FBX 2 mg·kg-1后0、1、2、4 h时,内眦取血测定小鼠血尿酸水平。以诱导剂溶剂代替诱导剂的动物作为正常对照Control组。Fig 3A结果显示,Mod-A组动物的血尿酸值与对照组相比明显上升,于给药后1 h时达到峰值,平均增长幅度达到348.2%;而后血尿酸值逐渐下降,于给药后4 h血尿酸值还原到基线程度;该血尿酸-时间曲线下面积(area under curve, AUC)上升了204.8%(Fig 3B)。灌胃给予阳性药FBX 2 mg·kg-1治疗后,Mod-A-FBX组动物的血尿酸值与Mod-A组相比明显降低,其血尿酸峰值及AUC值各下降了60.2%及59.6%,显示FBX具有明显改良小鼠急性高尿酸血症的功能。
|
| Fig 3 Changes of serum uric acid and XOD activity in acute hyperuricemia mice (x ± s, n=10) A: Changes of serum uric acid; B: Area under serum uric acid-time curve (AUC); C: Serum XOD activity; D: Hepatic XOD activity. Con: ICR mice; Mod-A: acute hyperuricemia mice induced with 500 mg·kg-1 hypoxanthine and 300 mg·kg-1 oteracil potassium; Mod-A-FBX: treatment with 2 mg·kg-1 febuxostat in acute hyperuricemia mice. **P < 0.01 vs Con; ##P < 0.01 vs Mod-A. |
在FBX给药后4 h内眦取血后,脱颈处死小鼠,迅速分离肝。分别测定血清XOD活性及肝组织XOD活性,结果显示(Fig 3C、3D),对照组、Mod-A组的血清XOD活性及肝组织XOD活性均未呈现明显差异;Mod-A-FBX组血清XOD活性与Mod-A组相比明显下降,肝组织XOD活性未见明显改变。
测定对照组和Mod-A组的肝肾功能血液指标,如AST、ALT、Cre和Urea。结果显示(Tab 1),对照组和Mod-A组均未见明显差异,提示急性高尿酸血症小鼠模型的肝肾功能未见明显损伤。
| Group | AST/U·L-1 | ALT/U·L-1 | Cre/μmol·L-1 | Urea/mmol·L-1 |
| Con | 21.29±9.8 | 5.18±3.2 | 80.32±11.05 | 8.08±1.52 |
| Mod-A | 17.97±9.0 | 5.87±4.9 | 70.41±9.32 | 9.39±3.91 |
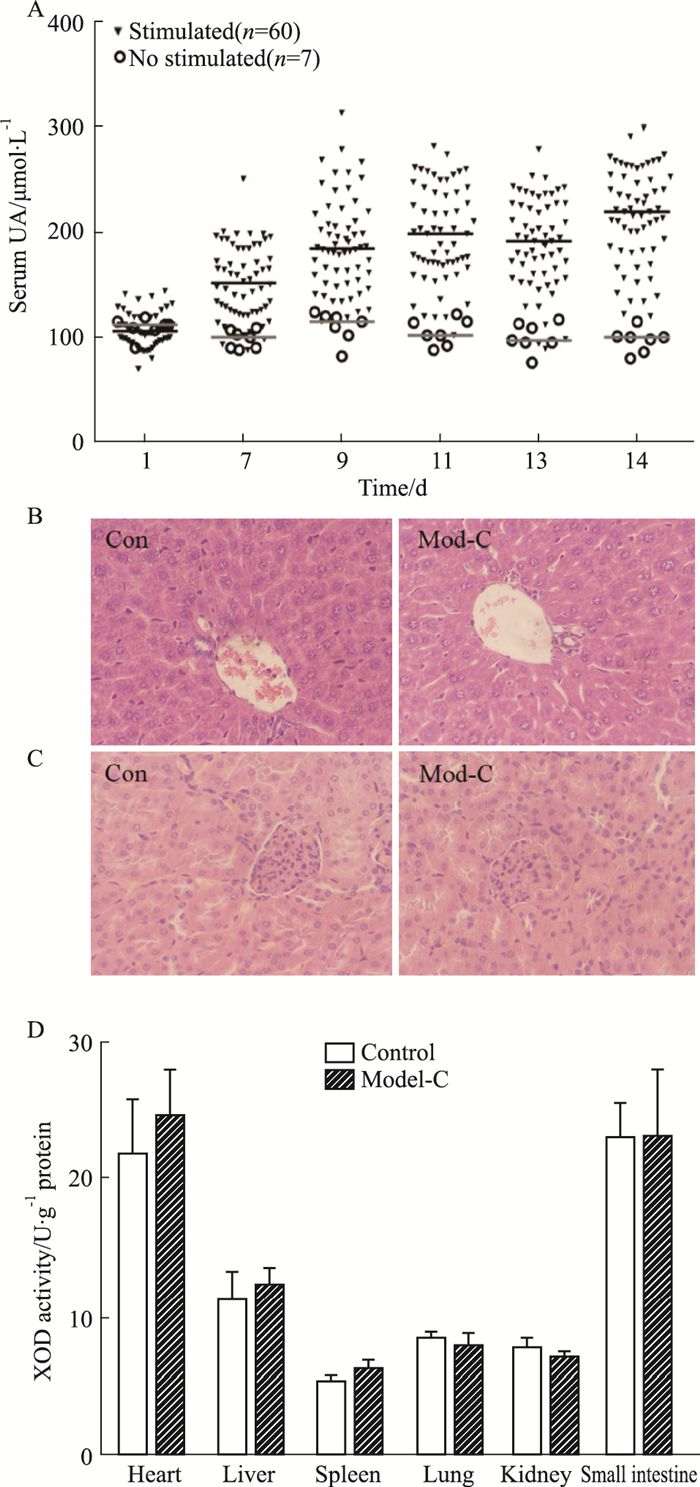
应用体质量(20±2)g的ICR ♂小鼠,采用连续多次皮下注射氧嗪酸钾300 mg·kg-1的诱导方式,每天1次。于诱导后d 7、9、11、13、14,内眦取血测定血尿酸水平。以诱导剂的溶剂代替诱导剂刺激的动物作为正常对照(No stimulated)组(n=7)。结果显示(Fig 4A),以氧嗪酸钾诱导的小鼠(Stimulated组,n=60)血尿酸水平逐渐升高,连续诱导2周后,与No stimulated组比较,Stimulated组的平均血尿酸水平升高了约2倍,约70%的动物血尿酸水平超过180 μmol·L-1。
|
| Fig 4 Characters of oteracil potassium-induced hyperuricemia mice (x ± s, n=10) A: Changes of serum uric acid level; B: Hepatic histopathological morphology(HE staining×200); C: Renal histopathological morphology(HE staining×200); D: XOD activity in tissues. |
慢性高尿酸血症模型小鼠(Mod-C)(n=10)与同批正常对照小鼠(n=10)比较,血液肝功能指标AST和ALT未见明显差异(Tab 2);肝脏HE染色(病理分析)未见明显差异,肝组织结构及细胞排列整齐,未见浊肿及坏死等受损现象(Fig 4B);血液肾功能指标Cre和Urea未见明显差异(Tab 2);肾脏HE染色(病理分析)未见明显差异,肾组织结构清晰,未见水肿及坏死等受损现象(Fig 4C)。说明采用此造模方式形成的慢性高尿酸血症小鼠模型未见明显肝肾损伤。
| Group | AST/U·L-1 | ALT/U·L-1 | Cre/μmol·L-1 | Urea/mmol·L-1 |
| Con | 29.85 ±19.7 | 9.47 ±3.8 | 74.29 ±12.78 | 11.84 ±1.43 |
| Mod-C | 21.81 ±12.8 | 8.80 ±4.1 | 83.61 ±14.64 | 11.49 ±2.08 |
检测动物主要脏器的XOD活性,结果显示(Fig 4D),对照组、Mod-C组各组织的XOD活性无明显差异;其各主要脏器XOD活性强弱顺序依次为小肠、心脏、肝脏、肺、肾及脾。
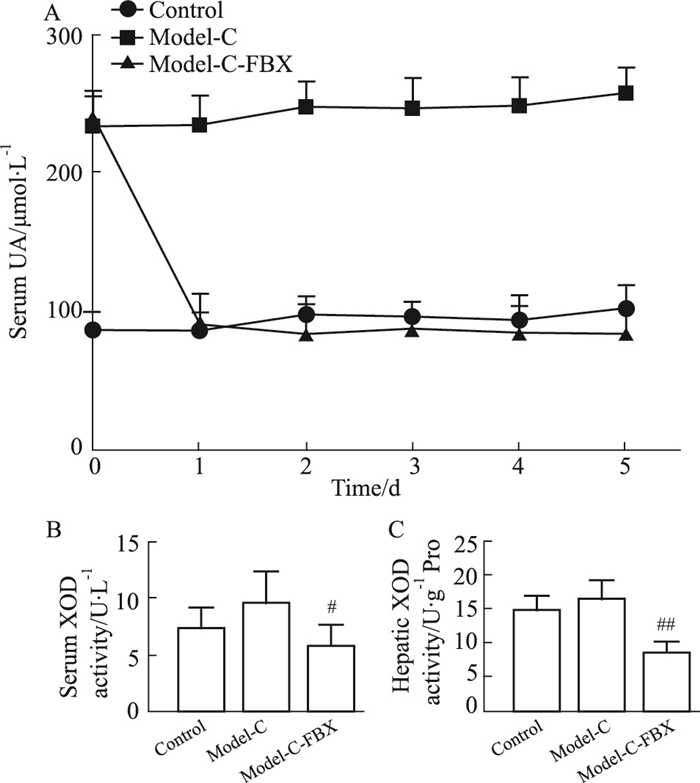
设正常小鼠作为对照组(Control,n=10)。把慢性高尿酸血症模型小鼠随机分为Mod-C组(n=10)和Mod-C-FBX组(n=10),分别持续灌胃水及阳性药FBX 2 mg·kg-1,持续治疗5 d,每天监测小鼠血尿酸水平变化情况。结果显示(Fig 5A),Mod-C组的平均血尿酸水平与对照组相比,上升了2.5倍。Mod-C-FBX组动物的血尿酸值与Mod-C组相比,降低大约60%,并保持稳定,连续给药5 d期间,Mod-C-FBX组动物的血尿酸值均保持与对照组相近的较低水平,显示FBX具有明显改善小鼠慢性高尿酸血症的作用。
|
| Fig 5 Effects of febuxostat on serum uric acid and XOD activity in chronic hyperuricemia mice (x ± s, n=7) A: Serum uric acid; B: Serum XOD activity; C: Hepatic XOD activity. Con: ICR mice; Model-C: chronic hyperuricemia mice induced with 300 mg·kg-1 oteracil potassium; Model-C-FBX: treatment with 2 mg·kg-1 febuxostat in chronic hyperuricemia mice. #P < 0.05, ##P < 0.01 vs Model-C. |
在给药d 5,测定血清XOD活性(Fig 5B)和肝组织XOD活性(Fig 5C),Mod-C组的血清XOD活性及肝组织XOD活性与对照组相比,各上升了31.3%及10.7%。Mod-C-FBX组的血清XOD活性及肝组织XOD活性与Mod-C组相比,分别下降了39.6%及49.0%。
3 讨论人类体内嘌呤代谢的终产物为尿酸。体内尿酸超过一定限度则称为高尿酸血症。随着现代人嘌呤类食物摄入增加,高尿酸血症及其相关疾病的发病率逐年升高[1]。XOD能催化黄嘌呤及次黄嘌呤产生尿酸,是体内合成尿酸的限速酶,为抗高尿酸血症药物的重要靶点[9-10]。
体外测定XOD活性的方法有多种,包括HPLC法[11-12],具有灵敏度高、样品易回收等优点,但单次分析样品数量少,不适用于同时分析大量样品;酶动力学法[13]具有反应时间较短的优点,但测定结果易受环境影响,不稳定;酶终点法可同时测定多种样品的抑制情况,受环境因素影响较小,结果重复性好,适用于测定样品对XOD活性的抑制情况。本研究中,根据适宜的反应终点OD值,选取最适XOD酶浓度和底物黄嘌呤浓度;动态观察反应状态,选取达到平台期的时间作为最适反应时间,反应效率最高的温度和pH作为最适反应体系,建立了体外XOD活性测定方法。分别应用已上市的XOD抑制剂别嘌呤醇和非布索坦,使用牛奶来源的XOD1测定其抑制XOD活性的IC50值分别为1.194 μmol·L-1和2.925 nmol·L-1。使用微生物来源的XOD2活性测定方法,嘌呤类经典药物别嘌呤醇抑制XOD活性的IC50值为1.150 μmol·L-1;非嘌呤类新型XOD特异性抑制剂非布索坦没有表现出明显的抑制作用,出现假阴性。因此,选用牛奶来源XOD1 3 U·L-1、底物XA 50 μmol·L-1、反应时间为20 min、反应温度为37 ℃、pH为7.4的反应体系,FBX为阳性对照药,建立了XOD抑制剂的体外筛选模型。
在全人类进化过程中,尿酸氧化酶基因序列发生突变,失去活性[14],尿酸为体内嘌呤代谢的终产物,致使体内血尿酸上升,使得人类较容易患高尿酸血症。小鼠的嘌呤代谢过程中,尿酸氧化酶可氧化尿酸生成尿囊素,后者是一种高度水溶性化合物,可高效排出,减少体内尿酸的积累。通过增加尿酸前体物质的摄入而增加尿酸的合成,抑制尿酸转运体减少尿酸的排泄和抑制尿酸氧化酶作用,均可导致小鼠的血尿酸升高,形成高尿酸血症模型。
本研究采取单次同时给予大剂量尿酸前体物质——次黄嘌呤及竞争性尿酸酶抑制剂——氧嗪酸钾[15]的方式,诱导ICR小鼠的血尿酸水平一过性上升,形成小鼠急性高尿酸血症模型。该小鼠模型在给予造模剂后血尿酸迅速上升,通常在诱导2 h后达到峰值;随后血尿酸水平逐渐下降,于造模剂诱导5 h后恢复到基线水平。与同批正常对照组比较,该模型小鼠Mod-A组的肝肾功能未见明显变化,表明此造模方法并不会对小鼠的肝肾功能造成明显损伤。此外,Mod-A组的血清XOD活性和肝组织XOD活性均未见明显变化。该模型类似于人类因饮食不节制,大量摄入嘌呤类食物后,血尿酸出现一过性升高,可通过动态监测血尿酸值变化情况和尿酸-时间曲线下面积AUC,评价受试药对急性高尿酸血症的治疗作用。
采取连续多次给予氧嗪酸钾的方法,使得小鼠血尿酸值逐渐升高,形成慢性高尿酸血症小鼠模型。该模型使用ICR小鼠,给予氧嗪酸钾连续刺激约2周后,与同批正常对照组比较,动物的血尿酸水平逐渐升高,发生高尿酸血症的动物数逐渐增多,血尿酸均值约为正常对照2倍。慢性高尿酸血症模型小鼠(Mod-C)血尿酸平稳升高。Mod-C组血清及肝组织XOD活性和正常对照组相比,均未见明显变化,肝、肾功能也无明显变化,肝组织和肾组织的病理检查(HE染色)亦未见明显损伤,说明此造模方法对小鼠的肝肾未见明显损伤。口服给予XOD抑制剂非布索坦治疗后,模型动物的血尿酸水平下降到与正常对照组相近的水平,并保持稳定。此慢性高尿酸血症小鼠模型类似于临床上高尿酸血症的情况,可以用于高尿酸血症药物的药效学评价及其作用机制的探究。
小鼠XOD组织分布相关报道较少。本研究结果显示,ICR小鼠主要脏器均存在XOD的表达,其XOD活性从高到低依次为小肠、心脏、肝脏、肺、肾、脾脏等组织。至于小肠、心脏高活性的XOD的生理功能,有待进一步探讨。此外,虽然由氧嗪酸钾诱导的慢性高尿酸血症模型小鼠各组织的XOD活性均未见明显变化,但是XOD抑制剂非布索坦可明显抑制该模型动物的血清和肝脏的XOD活性。
总之,本研究建立了包括检测样品对体外XOD抑制活性、对急性高尿酸血症小鼠一过性血尿酸水平上升的影响、对慢性高尿酸血症小鼠血尿酸水平“长”期平稳上升作用的XOD抑制剂筛选体系。该体系的3种体外、体内实验方法,各自独立又互相补充、相互验证受试样品的降血尿酸能力,为基于分子靶点XOD的抗高尿酸血症药物的研发和作用机制研究奠定了实验基础。
| [1] |
Dalbeth N, Merriman T R, Stamp L K. Gout[J]. Lancet, 2016, 388(10055): 2039-52. doi:10.1016/S0140-6736(16)00346-9 |
| [2] |
孙琳, 王桂侠, 郭蔚莹. 高尿酸血症研究进展[J]. 中国老年学杂志, 2017, 37(4): 1034-8. Sun L, Wang G X, Guo W Y. The progress of study on hyperuricemia[J]. Chin J Gerontol, 2017, 37(4): 1034-8. doi:10.3969/j.issn.1005-9202.2017.04.112 |
| [3] |
Chen D, Zhang H, Gao Y, et al. Cross-sectional and longitudinal associations between serum uric acid and metabolic syndrome: Results from fangchenggang area male health and examination survey in China[J]. Clin Chim Acta, 2015, 446: 226-30. doi:10.1016/j.cca.2015.04.019 |
| [4] |
Liu Z, Que S, Zhou L, Zheng S. Dose-response relationship of serum uric acid with metabolic syndrome and non-alcoholic fatty liver disease incidence: a Meta-analysis of prospective studies[J]. Sci Rep, 2015, 5: 14325. doi:10.1038/srep14325 |
| [5] |
林志健, 李凡, 张冰. 禽类动物高尿酸血症的研究进展[J]. 中国实验动物学报, 2017, 25(5): 572-6. Lin Z J, Li F, Zhang B. Advances in research on hyperuricemia in avians[J]. Acta Laboratorium Animalis Scientia Sin, 2017, 25(5): 572-6. doi:10.3969/j.issn.1005-4847.2017.05.019 |
| [6] |
Kurosaki M, Li Calzi M, Scanziani E, et al. Tissue-and cell-specific expression of mouse xanthine oxidoreductase gene in vivo: regulation by bacterial lipopolysaccharide[J]. Biochem J, 1995, 306(Pt 1): 225-34. |
| [7] |
Grewal H K, Martinez J R, Espinoza L R. Febuxostat: drug review and update[J]. Expert Opin Drug Metab Toxicol, 2014, 10(5): 747-58. doi:10.1517/17425255.2014.904285 |
| [8] |
Heimbach E J, Bowden R G, Griggs J O, et al. The effects of lowering uric acid levels using allopurinol on components of metabolic syndrome[J]. Cardiol Res, 2012, 3(2): 80-6. |
| [9] |
Maiuolo J, Oppedisano F, Gratteri S, et al. Regulation of uric acid metabolism and excretion[J]. Int J Cardiol, 2016, 213: 8-14. doi:10.1016/j.ijcard.2015.08.109 |
| [10] |
Ojha R, Singh J, Ojha A, et al. An updated patent review: xanthine oxidase inhibitors for the treatment of hyperuricemia and gout (2011-2015)[J]. Expert Opin Ther Pat, 2017, 27(3): 311-45. doi:10.1080/13543776.2017.1261111 |
| [11] |
Li L Z, Zhou G X, Li J, et al. Compounds containing trace element copper or zinc exhibit as potent hyperuricemia inhibitors via xanthine oxidase inactivation[J]. J Trace Elem Med Biol, 2018, 49: 72-8. doi:10.1016/j.jtemb.2018.04.019 |
| [12] |
Wan Y, Liang Y X, Zou B, et al. The possible mechanism of hydroxytyrosol on reducing uric acid levels[J]. J Functional Foods, 2018, 42: 319-26. doi:10.1016/j.jff.2018.01.009 |
| [13] |
Ao G Z, Zhou M Z, Li Y Y, et al. Discovery of novel curcumin derivatives targeting xanthine oxidase and urate transporter 1 as anti-hyperuricemic agents[J]. Bioorg Med Chem, 2017, 25(1): 166-74. doi:10.1016/j.bmc.2016.10.022 |
| [14] |
Wu X W, Muzny D M, Lee C C, Caskey C T. Two independent mutational events in the loss of urate oxidase during hominoid evolution[J]. J Mol Evol, 1992, 34(1): 78-84. doi:10.1007/BF00163854 |
| [15] |
陈刚, 谭明亮. 茶多酚对高尿酸血症小鼠尿酸产生与排泄的影响及机制研究[J]. 中国药理学通报, 2017, 33(2): 218-22. Chen G, Tan M L. Effect of green tea polyphenols on uric acid level in potassium oxonate-induced hyperuricemic mice and mechanism[J]. Chin Pharmacol Bull, 2017, 33(2): 218-22. doi:10.3969/j.issn.1001-1978.2017.02.015 |

