

鼠类肉瘤病毒癌基因(kirsten rat sarcoma viral oncogene,KRAS)的突变是许多肿瘤如结肠癌、胰腺癌、非小细胞肺癌等常见的生物学事件,也是很多肿瘤发病的主要机制之一。KRAS基因突变可导致机体失去GTP水解酶活性, 其致癌作用主要是影响细胞的生长和增殖。同时,KRAS突变遗传背景具有异质性, 对于KRAS基因突变治疗的药物研究迫在眉睫。本文就目前针对肿瘤KRAS基因突变的靶向治疗的研究进展进行综述,为KRAS突变肿瘤治疗提供最新线索。
1 KRAS基因RAS是人类基因中重要的原癌基因之一,被认为是控制细胞基本功能的鸟苷三磷酸酶(guanosine triphosphatase,GTPases)大型家族的创始成员,也是表皮生长因子受体(epidermal growth factor receptor,EGFR)信号通路上的重要靶点。其家族基因主要有3种,分别是KRAS、NRAS和HRAS。其中,KRAS基因突变对人类癌症的影响最为深刻,KRAS基因的突变在人类癌症中相当常见,占所有人类癌症的17%~25%[1]。自1982年KRAS作为一种致癌基因首次被发现以来,人们一直在努力开发针对KRAS突变肿瘤的靶向治疗。
KRAS基因编码的产物为一种被称为P21小G蛋白,具有GTP酶活性,在GTP和GDP结合转换之间发挥分子开关作用。RAS蛋白结合GDP通过鸟嘌呤核苷酸交换因子(guanine nucleotide exchange factor,GEFs)转换为GTP,从而使RAS激活[2]。KRAS蛋白控制细胞质信号网络,并调节多种细胞功能。热点突变的位置通常发生在第12和13位密码子上(Fig 1)。突变后的KRAS通过细胞表面受体影响细胞信号转导,使原本的GTP结合状态通过丧失内在的催化活性或者是通过GTPase丧失而最终激活蛋白,并启动复杂信号网络,持续激活下游RAS-RAF-MEK-MAPK细胞信号通路。此外,KRAS也是其他许多信号通路的关键激活因子,导致明显的生物学效应。例如,磷脂酰肌醇激酶(phosphate-3 kinase,PI3K)和Ral蛋白都是KRAS的下游效应物,在生物学功能上诱导细胞的过度繁殖、浸润、转移,以及血管生成和细胞凋亡等一系列肿瘤病理变化,从而促进肿瘤发生[3]。KRAS网络及其下游通路之间的相互作用的复杂性,使得KRAS基因突变蛋白难以通过传统手段抑制其活性,同时,KRAS对GDP和GTP酶的固有高亲和性以及蛋白质表面缺乏明确的药物位点[4],多年来在癌症基因组领域被称为“癌基因的珠穆朗玛峰”。

|
| Fig 1 KRAS hotspot mutation site |
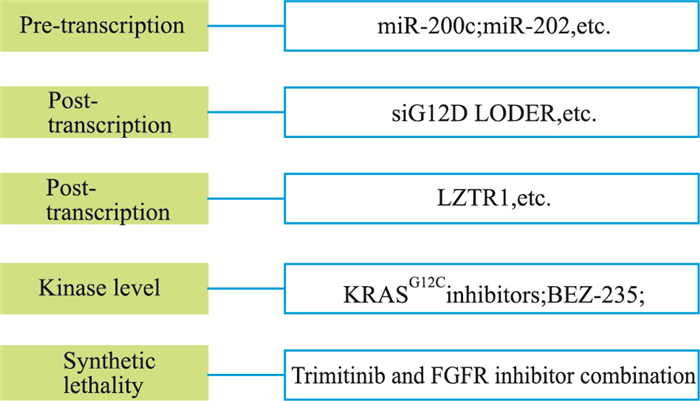
目前,大规模的临床研究发现,KRAS基因点突变在胰腺癌中发生频率最高,约有90%的胰腺癌患者具有至少1种KRAS基因的点突变;在结直肠癌发生的初始阶段,约有34.2%~52.7%的原发性结直肠癌患者中可以检测到突变型KRAS基因[5]。在非小细胞肺癌(non-small-cell lung cancer,NSCLC)的KRAS突变中,KRAS基因的突变率在东方人群和西方人种中具有较大差异,是西方人种最常见的突变基因,突变率接近30%[6]。KRAS突变肿瘤仍然是一种高度未被满足临床需要的疾病,三十多年来,对KRAS基因突变药物研究的步伐从未停滞。研究发现,靶向药物具有激活免疫反应的作用, 靶向治疗结合免疫治疗可以有效缩短免疫治疗响应周期, 而免疫治疗提高了机体内的抗肿瘤免疫反应, 也有利于靶向药物发挥作用[7]。研究者们主要从KRAS的基因水平、蛋白水平、功能水平的抑制,以及联合用药和协同致死等方面,进行多方面的深入研究(Fig 2)。
|
| Fig 2 Targeted strategies for inhibitingKRAS function in different stages |
KRAS的表达受多种微小RNA的直接调控。KRAS已知是miR-200c(一种小RNA抑制剂)的直接靶点,参与细胞外基质(extracellular matrix,ECM)重构的基因调控因子。过表达miR-200c可降低KRAS基因的表达。其下游的磷酸化Akt与ERK通路也发生了相应的下调,膀胱癌细胞的增殖能力也发生了明显的抑制[8]。Sun等[9]证明,miR-202能靶向非小细胞肺癌中的KRAS,过表达miR-202可以抑制RAS/MAPK通路活性水平,此外,miR-202表达水平的恢复可以提高非小细胞肺癌细胞对顺铂化疗的敏感性。
2.2 利用siRNA干扰技术干扰KRAS突变干扰KRAS已经被证明在控制胰腺癌细胞系增殖方面是有效的,目前Khvalevsky等[10]研发了一种传递系统LODER,使siRNA(siG12D LODER)能够干扰抵抗突变的KRAS。对siG12D LODER进行了体外和体内结构、释放和传递特性的评估。在原位小鼠模型中,评估了siG12D LODER对肿瘤生长的影响。进一步评估KRAS沉默对KRAS下游信号通路的影响。研究还发现,LODER包封的siRNA可在体内存活155 d,且稳定活跃。siG12D LODER处理胰腺癌细胞株后,KRAS表达水平明显下降,抑制了胰腺癌细胞的增殖和上皮间充质的转化。在体内,siG12D LODER可以抑制胰腺肿瘤细胞的生长。纳米颗粒载体作为有效siRNA传递的潜在候选载体具有以下优点:① siRNA不容易被降解; ② siRNA在肿瘤内局部缓慢释放,作用持续时间较长; ③ siG12D LODER具有治疗作用,不会导致任何局部或全身的副作用[11]。
2.3 基于反义寡核苷酸(antisense oligonucleotide,ASO)的抑制KRAS策略Ross等[12]使用基因疗法,描述了AZD4785的临床前评估,这是一种高亲和力约束的含乙基的反义寡核苷酸靶向KRAS mRNA。AZD4785细胞中KRAS的mRNA和蛋白高效地、有选择地耗尽,导致KRAS突变细胞下游效应通路的抑制和有选择地抗增殖作用。AZD4785介导的KRAS的缺失与MAPK通路的反馈激活无关,而RAS-MAPK通路则与此相关。全身给予AZD4785可有效地抑制KRAS在肿瘤中的表达和抗肿瘤活性,展示了一种反义寡核苷酸抑制KRAS的疗法。研究中使用的反义寡核苷酸经过化学修饰,允许通过皮下注射进行全身输送,避免使用专门的运载工具。Ross等[12]在多只非小细胞肺癌模型小鼠上测试了这种疗法的有效性,并评估了它在灵长类动物中的安全性,证明了它在人类的潜在适用性。
2.4 抑制KRAS基因突变体酶活性水平更多的研究者开始将他们的目光放在针对KRAS基因突变体蛋白靶向的小分子药物的研究中。如Ostrem等[13]发现了一种KRASG12C突变体特异性抑制剂,该抑制剂能有效抑制KRASG12C突变体和GTP结合,促进其与GDP的结合,阻止了后续下游信号的活化。Lim等[14]报道了另外一种KRASG12C抑制剂,在不影响正常KRAS的情况下,特异性结合突变的KRAS基因,共价抑制剂KRASp.G12C等位基因能够对突变的KRAS进行直接和特异性的抑制,使突变的KRAS失去活性。最近,一种针对KRASG12C变构开关Ⅱ口袋的新型细胞活性和突变特异性抑制剂,显示出更强的效率和选择性,进一步揭示了KRASG12C快速循环其核苷酸底物[15]。KRASG12C选择性抑制剂的开发开启了一个里程碑式的发现,它改变了RAS蛋白从不耐药到耐药的认知。最近在RAS与RAF和其他效应蛋白的结合中,发现了新的RAS模拟小分子药物Rigosertib,用于KRAS突变体的肿瘤的治疗[16-17]。
2.5 KRAS蛋白降解调节剂LZTR1是一个与人类疾病有关的新型RAS调节剂,关于RAS调节的替代机制将导致人们开发出治疗RAS驱动疾病的新型治疗方法。M. Steklov等[18]研究发现,内源性人LZTR1与主要RAS同种型结合。LZTR1介导的RAS在K170位点泛素化抑制了RAS-MAPK信号通路。该研究结果为LZTR1参与多种遗传性和获得性人类疾病提供了分子基础,LZTR1介导的RAS在K170上的泛素化调控RAS活性,而RAS活性的失调导致了人类疾病的发生。一项相关研究表明,LZTR1失调也会导致耐药性。了解这种非传统的RAS激活机制可能有助于确定哪些患者可能受益于RAS通路抑制剂,并为这些患者提供新的治疗方法。
2.6 阻断KARS下游的信号通路KRAS下游主要包括PI3K信号通路。PI3K是KRAS基因通路下游的一个重要的效应分子之一,PI3K信号通路以PI3K-Akt-mTOR通路为主,参与并调节细胞的增殖、凋亡、分化、葡萄糖转运等各种细胞过程。近年来,针对PI3K-mTOR双重靶向抑制剂,如BEZ-235(一种新型咪唑并喹啉衍生物)用于治疗晚期乳腺癌和实体瘤,临床上显示该药物治疗不仅可以大大降低耐药性,增强肿瘤细胞对顺铂、吉西他滨、长春新碱等细胞毒性药物的敏感性,还能维持糖代谢稳定[19]。
2.7 KRAS基因上游信号通路抑制剂KRAS是EGFR的下游效应物。传统观点认为,伴有KRAS突变的肿瘤对酪氨酸激酶抑制剂(tyrosine kinase inhibitor,TKI)具有耐药性,研究发现[20],由于KRAS基因的突变可以直接启动EGF通路下游的KRAS途径, 并间接启动了EGF信号通路中的PI3K途径,使得第1代酪氨酸激酶抑制剂埃罗替尼和吉非替尼对KRAS突变引起的非小细胞肺癌治疗无效。曲米替尼(Tram,GSK1120212)是一种新的MEK抑制剂,通过丝裂原活化蛋白激酶(MAPK)级联可有效抑制RAS信号通路。
2.8 联合用药与协同致死采用曲米替尼和EGFR抑制剂组合的协同作用于KRAS突变型肺癌和胰腺癌细胞,这些结果与单独使用MEK抑制剂曲米替尼后FRS2磷酸化增强密切相关,即抑制FGFR可增强曲米替尼的作用。同时也发现,靶向特定的RTK(如FGFR1)比靶向多效应因子(如AKT29)更容易耐受,并为进一步开发出更具特异性的FGFR1拮抗剂提供理论依据[21]。Dai等[22]发现,Tram治疗引起了RAS上游的反馈激活,诱导KRAS突变肿瘤中磷酸化MEK和磷酸化ERK的反弹。这种ERK持续抑制的失败导致了耐药性。唑来膦酸(ZA)是一种含氮双膦酸盐,通过抑制RAS基因的异戊二烯酰化,破坏RAS基因的生物活性。ZA通过甲戊酸钠通路增强了Tram的作用,可能代表一种治疗KRAS突变型癌症的新策略,从而克服了耐药性问题。瑞格非尼是一种口服多激酶抑制剂,其主要靶向抑制Ras/Raf/MEK/ERK通路中的RTKs,通过该联合用药可有效阻断Ras/Raf/MEK/ERK信号通路。对于转移性结直肠患者,采用瑞格非尼和福尔菲利联合应用,临床上取得了良好的疗效[23]。
KRAS突变基因的协同致死策略虽具有挑战性和艰难性,但仍是有希望的治疗方案。在26个结直肠癌和胰腺癌模型组中,证实了KRAS突变基因协同细胞周期蛋白依赖性激酶1(cyclin-dependent kinase 1,CDK1)合成致死适用于具有氨基酸位置12(p.G12V、pG12D、p.G12S)或氨基酸位置13(p.G13D)KRAS突变的肿瘤细胞。从机制上讲,CDK1抑制导致KRAS突变细胞的S期分数降低,这种作用的特点在于调节Rb,即G1/S检查点。总之,这些观察结果表明,KRAS/CDK1相互作用是一种强大的合成致死效应[24]。Sharaf等[25]发现,联合益生菌和塞来昔布同时使用治疗持续18周,结果发现这种组合方法可能降低肿瘤负担,减少肿瘤的多样性,降低抗凋亡Bcl-2、原癌基因KRAS的表达,上调促凋亡Bax和抑癌因子p53的表达。
3 总结与展望总的来说,KRAS靶向治疗药物的一个重要问题是,这些药物是否需要对KRAS的突变形式进行特异性的抑制,或者非选择性对KRAS的突变型和野生型的抑制是否具有预期的抗肿瘤活性和必要的安全性,是评价能否成为有价值的靶向抗癌药的指标。抑制RAS基因的最佳途径还有待确定,因为这些药物通过直接靶向RAS蛋白或RAS信号转导的方式在进入临床前还有很长的路要走。
| [1] |
Kranenburg O. The KRAS oncogene:past, present, and future[J]. Biochim Biophys Acta, 2005, 1756(2): 81-2. |
| [2] |
吕莹雪, 刘小玲. KRAS突变非小细胞肺癌的靶向治疗研究进展[J]. 中南药学, 2008, 16(4): 513-7. Lu Y X, Liu X L. Research progress of targeted therapy for non-small cell lung cancer with KRAS mutation[J]. Chin Med, 2008, 16(4): 513-7. |
| [3] |
Martin P, Leighl N B, Tsao M S, et al. KRAS mutations as prognostic and predictive markers in non-small cell lung cancer[J]. J Thorac Oncol, 2013, 8(5): 530-42. doi:10.1097/JTO.0b013e318283d958 |
| [4] |
Ostrem J M, Peters U, Sos M L, et al. K-Ras(G12C) inhibitors allosterically control GTP affinity and effector interactions[J]. Nature, 2013, 503(7477): 548-51. doi:10.1038/nature12796 |
| [5] |
Rui Y, Wang C, Zhou Z, et al. K-Ras mutation and prognosis of colorectal cancer: a meta-analysis[J]. Hepatogastroenterology, 2015, 62(137): 19-24. |
| [6] |
Kempf E, Rousseau B, Besse B, et al. KRAS oncogene in lung cancer: focus on molecularly driven clinical trials[J]. Eur Respir Rev, 2016, 25(139): 71-6. doi:10.1183/16000617.0071-2015 |
| [7] |
王伙刚, 洪波, 林文楚. 小细胞肺癌靶向治疗研究进展[J]. 中国药理学通报, 2017, 33(10): 1333-7. Wang H G, Hong B, Lin W C. Research progress of targeted therapy for small cell lung cancer[J]. Chin Pharmacol Bull, 2017, 33(10): 1333-7. doi:10.3969/j.issn.1001-1978.2017.10.001 |
| [8] |
Cao W, Sun J. MicroRNA-200c promotes tumor cell proliferation and migration by directly targeting dachshund family transcription factor 1 by the Wnt/β-catenin signaling pathway in nasopharyngeal carcinoma[J]. Anticancer Drugs, 2018, 30(3): 218-24. |
| [9] |
Sun W, Ping W. miR-202 enhances the anti-tumor effect of cisplatin on non-small cell lung cancer by targeting the Ras/MAPK pathway[J]. Cell Physiol Biochem, 2018, 51(5): 2160-71. doi:10.1159/000495835 |
| [10] |
Khvalevsky EZ, Gabai R, Rachmut IH, et al. Mutant KRAS is a druggable target for pancreatic cancer[J]. PNAS, 2013, 11(55): 20723-8. |
| [11] |
Ramot Y, Rotkopf S, Gabai R M, et al. Preclinical safety evaluation in rats of a polymeric matrix containing an siRNA drug used as a local and prolonged delivery system for pancreatic cancer therapy[J]. Toxicol Pathol, 2016, 44(6): 856-65. doi:10.1177/0192623316645860 |
| [12] |
Ross S J, Revenko A S, Hanson L L, et al. Targeting KRAS-dependent tumors with AZD4785, a high-affinity therapeutic antisense oligonucleotide inhibitor of KRAS[J]. Sci Transl Med, 2017, 9(394): pii: eaal5253. doi:10.1126/scitranslmed.aal5253 |
| [13] |
Ostrem J M, Peters U, Sos M L, et al. KRAS(G12C)inhibitors allosterically control GTP affinity and effector interactions[J]. Nature, 2013, 503(7477): 548-51. doi:10.1038/nature12796 |
| [14] |
Lim S M, Westover K D, Ficarro S B, et al. Therapeutic tar-geting of oncogenic KRAS by a covalent catalytic site in-hibitor[J]. Angew Chem Int Ed Engl, 2014, 53(1): 199-204. doi:10.1002/anie.201307387 |
| [15] |
Patricelli M P, Janes M R, Li L S, et al. Selective inhibition of oncogenic KRAS output with small molecules targeting the inactive state[J]. Cancer, 2016, 6(3): 316-29. |
| [16] |
Zimmermann G, Papke B, Ismail S, et al. Small molecule inhibition of the KRAS-PDEdelta interaction impairs oncogenic KRAS signaling[J]. Nature, 2013, 497(7451): 638-42. doi:10.1038/nature12205 |
| [17] |
Papke B, Murarka S, Vogel H A, et al. Development of pyridazinone chemotypes targeting the PDEδ prenyl binding site[J]. Chemistry, 2017, 23(25): 6083-93. doi:10.1002/chem.201603222 |
| [18] |
Steklov M, Pandolfi S, Baietti M F, et al. Mutations in LZTR1 drive human disease by dysregulating RAS ubiquitination[J]. Science, 2018, 362(6419): 1177-82. doi:10.1126/science.aap7607 |
| [19] |
Kim K W, Myers C J, Jung D K, et al. NVP-BEZ-235 enhances radiosensitization via blockade of the PI3K/mTOR pathway in cisplatin-resistant non-small cell lung carcinoma[J]. Cancer, 2014, 5(7-8): 293-302. |
| [20] |
张卉, 杨新杰, 秦娜, 等. 肺腺癌EGFR与KRAS基因突变状态分析[J]. 中国肺癌杂志, 2015, 18(11): 686-90. Zhang H, Yang X J, Qin N, et al. Mutation status analysis of EGFR and KRAS gene in lung adenocarcinoma[J]. Chin J Lung Cancer, 2015, 18(11): 686-90. doi:10.3779/j.issn.1009-3419.2015.11.05 |
| [21] |
Manchado E, Weissmueller S, Morris J P, et al. A combinatorial strategy for treating KRAS-mutant lung cancer[J]. Nature, 2016, 534(7609): 647-51. doi:10.1038/nature18600 |
| [22] |
Dai X, Xia H, Zhou S, et al. Zoledronic acid enhances the efficacy of the MEK inhibitor trametinib in KRAS mutant cancers[J]. Cancer Lett, 2019, 442: 202-12. doi:10.1016/j.canlet.2018.10.022 |
| [23] |
Stintzing S, Modest D P, Rossius L, et al. FOLFIRI plus cetuximab versus FOLFIRI plus bevacizumab as first-line treatment for patients with metastatic colorectal cancer(FIRE-3): a randomised, open-label, phase 3 trial[J]. Lancet Oncol, 2014, 15(10): 1065-75. doi:10.1016/S1470-2045(14)70330-4 |
| [24] |
Costa-Cabral S, Brough R, Konde A, et al.CDK1 Is a Synthetic Lethal Target for KRAS Mutant Tumours[J].2016, 11(2): e0149099.
|
| [25] |
Sharaf L K, Sharma M, Chandel D, et al. Prophylactic intervention of probiotics and celecoxib modulate Bax-mediated apoptosis.in.1, 2-dimethylhydrazine-induced experimental colon carcinogenesis[[J]. BMC Cancer, 2018, 18(1): 1111. doi:10.1186/s12885-018-4999-9 |

