

临床及基础研究表明,肠道慢性炎症的反复损伤、修复、增生,引起基因突变,从而引起细胞癌变。结肠炎相关性结肠癌(colitis-associated colorectal cancer,CAC)是结肠炎-癌病理过程的典型模型,其发病机制目前认为呈现“炎症-不典型增生-癌变”。炎症与肿瘤发生的机制是当前研究的热点之一[1-2]。
STAT3可通过介导炎症介质的细胞外信号,调控肿瘤细胞、免疫细胞等的生物学行为,是慢性炎症促进肿瘤发生及肿瘤相关性炎症形成过程中不可或缺的关键性分子。STAT3活化引起的炎症通路的激活,导致肠黏膜屏障破坏,是结肠炎发生、发展的重要因素[3]。溃疡性结肠炎患者中STAT3表达明显升高,IL-6/STAT3信号通路在溃疡性结肠炎向结肠癌转变过程中发挥重要作用[4-6]。同时,microRNAs是炎症和癌症的关键参与者,一些microRNAs可以作为炎症介质,另一些可以作为癌基因或肿瘤抑制因子。在此过程中,microRNAs与STAT3激活之间的关系尚不明确。黄芪白术汤由黄芪与白术组成,黄芪具有益气健脾、补气固表、利水退肿、托毒排脓、生肌等功效,为补中益气之良药; 白术具有补气健脾、燥湿利水、固表止汗等作用,主要用于治疗脾胃气虚证,脾虚泄泻,消化不良,胃肠疾病。二者配伍使用对结肠癌,脾胃虚弱,大肠阴津耗伤者具有独特疗效。因此,本课题组拟初步探讨差异表达的microRNA与STAT3在CAC进程中的作用及黄芪白术汤的干预机制。
1 材料与方法 1.1 药物黄芪(产地:内蒙古,生产批号:YPA7E0003),白术(产地:浙江,生产批号:YPA7E004),购自广州采芝林连锁药店。以黄芪:白术3 :1(黄芪210 g,白术70 g)混合后,在10倍的纯水中浸泡0.5 h,武火煮沸后,文火煎至(100~200) mL液体,纱布过滤,药渣再加入10倍体积纯水,煎至(100~200) mL。混合2次药液,在真空旋转蒸发器中浓缩到(100~150) mL,之后将液体置于冷冻干燥机中,直到液体完全干燥。制备好的冻干粉贮存于-20 ℃。使用时,将冻干粉与纯水混合成0.6 kg·L-1(黄芪白术低浓度,HBL)和1.2 kg·L-1(黄芪白术高浓度,HBH)用于小鼠灌胃给药。黄芪甲苷(UV≥98%,货号912A023),购自北京索莱宝生物科技有限公司; 白术内酯(UV≥98%,货号PA0808RA13),购自上海源叶生物科技有限公司。
1.2 实验动物与细胞株C57BL/6小鼠,SPF级,4~6周龄,体质量20 g左右,♀♂各半,购自广州中医药大学实验动物中心,动物质量合格证:SYXK(粤)2013-0001。小鼠单核巨噬细胞RAW264.7,购自吉妮欧公司。
1.3 试剂氧化偶氮甲烷(azoxymethane,AOM),购自Sigma-Aldirich公司; 葡聚糖硫酸钠(dextran sodium sulfate,DSS),购自MP; LipofectamineTM 2000、miR-31-5p precursor,均购自Life Technologies; GAPDH抗体,购自Abcam; STAT3抗体,购自Cell Signaling; IL-6Rα、p-STAT3抗体,购自Santa Cruz; miRNA提取试剂盒,购自康为世纪; miRNA逆转录试剂盒,购自TaKaRa公司; 引物由上海捷瑞生物工程有限公司合成。
1.4 仪器Mini-protean Tetra System电泳仪、Trans-Blot® SD Cell转印系统、ChemiDocTMXRS+成像仪、荧光定量PCR仪、Imark酶标仪(Bio-Rad公司); 超微量核酸蛋白检测仪(Thermo Scientific公司); FD系列冷冻干燥机(上海天丰); Axon GenePix4000B芯片扫描仪(Axon公司)。
1.5 方法 1.5.1 CAC小鼠模型的构建及样品采集C57BL/6小鼠喂养于广州中医药大学实验动物中心SPF动物室。小鼠适应性喂养3 d后,除正常组外,一次性腹腔注射AOM(12 mg·kg-1),然后正常喂养2 d。在d 3,给予3% DSS水自由饮用5 d,之后正常喂养16 d,此为DSS刺激第1个循环,重复DSS刺激3个循环。4周后,按HBL和HBH不同剂量开始灌胃给药,模型组和对照组给予纯水。所有动物实验过程均经广州中医药大学动物伦理学委员会批准。8周后常规处死动物,采用Swiss-roll方式、4%多聚甲醛固定结肠组织,用于病理观察。部分结肠组织液氮保存,用于microRNA测序,其他结肠组织-80 ℃保存备用。
1.5.2 RAW264.7细胞株转染RAW264.7对照组加LipofectamineTM 2000 10 μL到3 mL体系,miR-31-5p高表达组以LipofectamineTM 2000 10 μL+3 μL 50 μmol·L-1 miR-31-5p precursor加入3 mL体系,48 h后收集细胞。
1.5.3 ClariomTM D微阵列检测对照组和CAC小鼠中miRNA的差异表达TRIzol法提取RNA后,用RNasey Mini Kit纯化。RNA标记与芯片杂交根据Exiqon提供的方法进行。使用芯片扫描仪扫描芯片。
1.5.4 qPCR检测体外采用IL-6(50 mg·L-1)刺激RAW264.7 24 h后,加入白术内酯Ⅱ+黄芪甲苷复合物继续刺激24 h,收集细胞。小鼠结肠组织和RAW264.7细胞收集后,按照miRNA提取试剂盒说明书的步骤提取miRNA,进行逆转录。qPCR条件:95 ℃ 10 s,95 ℃ 5 s,60 ℃ 20 s,共40个循环,U6为内参。miR-31-5p引物序列:F:5′-CGGGCAGGCAAGATGCTGGC-3′,R:5′-CAGCCACAAAAGAGCACAAT-3′; U6引物序列:F:5′-CTCGCTTCGGCAGCACATATACT-3′,R:5′-ACGCTTCACGAATTTGCGTGTC-3′。
1.5.5 Western blot检测相关蛋白全蛋白提取试剂盒提取结肠组织和细胞中的蛋白后,BCA蛋白含量检测试剂盒测蛋白浓度。用10% SDS-PAGE凝胶分离蛋白样品,转移到PVDF膜上,一抗4 ℃孵育过夜。二抗在室温下孵育1.5 h,ECL显影后,扫描,Image Lab进行条带分析,目的蛋白灰度值/GAPDH灰度值为目的蛋白的相对表达量。
1.5.6 统计学方法采用SPSS 19.0分析,所有数据以x±s表示, 单向方差分析(方差分析)用于组间比较,两组间比较采用t检验。
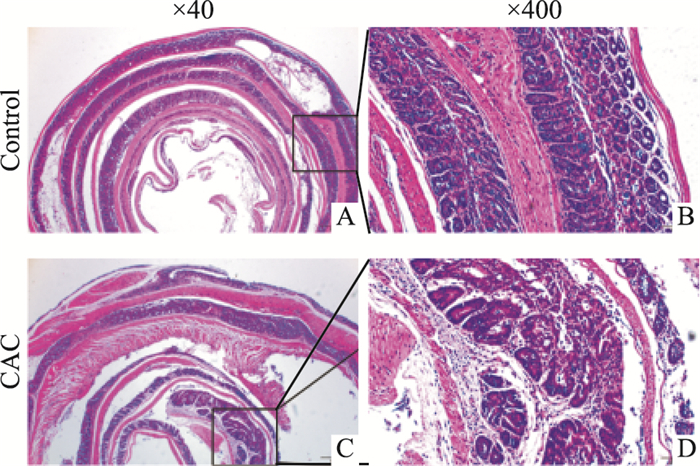
2 结果 2.1 CAC模型小鼠microRNA的差异表达CAC小鼠造模过程中出现精神萎靡不振、食量减少、身体消瘦、体质量减轻、便血、腹泻等症状。CAC模型8周小鼠结肠组织形态学观察显示(Fig 1),黏膜腺体排列紊乱,杯状细胞明显减少,黏膜及黏膜下层出现不同程度的炎细胞浸润,结肠远端黏膜出现中重度异型增生。microRNA测序结果显示,miR-31-5p、miR-132、miR-223等明显增高,经real-time PCR检测表明,miR-31-5p升高尤为明显(Fig 2)。提示miR-31-5p可能是结肠炎-癌发展过程中的病理诊断标志物,并调控可能的靶基因,参与结肠黏膜异型发生。
|
| Fig 1 Pathological changes of colon in CAC mice by HE staining A: Control group; B: control group; C: 8w CAC; D: 8w CAC |

|
| Fig 2 Differential expression of microRNA in CAC model mice A: Differential expression of microRNA in control and CAC mice by miRCURY LNATM microRNA microarray; B: Quantitative PCR was used to screen differential microRNAs(x±s, n=8).*P < 0.05, **P < 0.01 vs control. |
与对照组相比,CAC模型组小鼠结肠STAT3、p-STAT3蛋白表达明显升高; HBL及HBH干预后,均可降低STAT3、p-STAT3蛋白表达(Fig 3)。

|
| Fig 3 Expression of STAT3 and p-STAT3protein in mouse colonic mucosa(x±s, n=8) **P < 0.01 vs control; #P < 0.05 vs CAC |
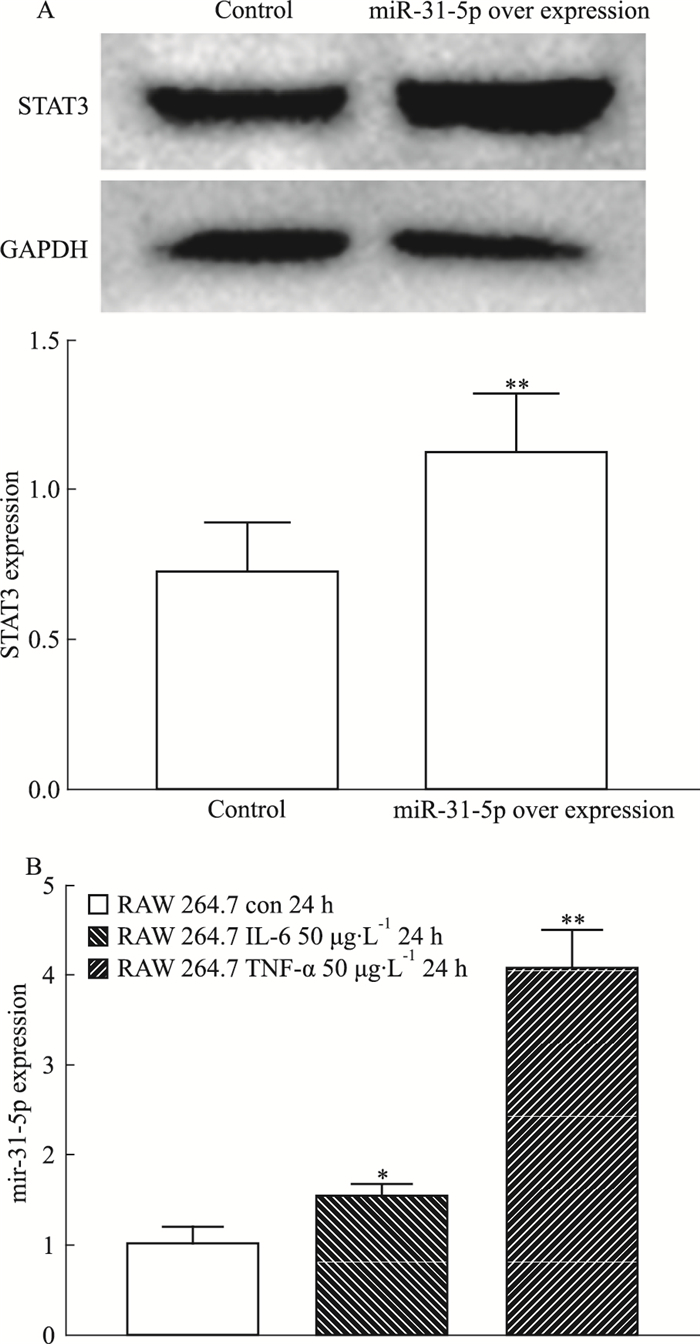
RAW264.7细胞转染miR-31-5p precursor使其高表达后,STAT3蛋白明显增高(Fig 4A)。采用炎症因子IL-6(50 μg·L-1)或TNF-α(50 μg·L-1)刺激RAW264.7细胞24 h后,miR-31-5p水平明显增高(Fig 4B)。以上结果提示,miR-31-5p与STAT3激活形成一个正相关的循环,可能参与结肠黏膜炎-癌病理进程。
|
| Fig 4 miR-31-5p with STAT3 formed apositive correlation(x±s, n=3) A:STAT3 protein expression significantly increased after RAW264.7 transfection with miR-31-5p precursor; B: After IL-6(50 μg·L-1), TNF-α(50 μg·L-1) stimulated RAW264.7 cells for 24 h, the expression level of miR-31-5p was significantly up-regulated.*P < 0.05, **P < 0.01 vs control. |
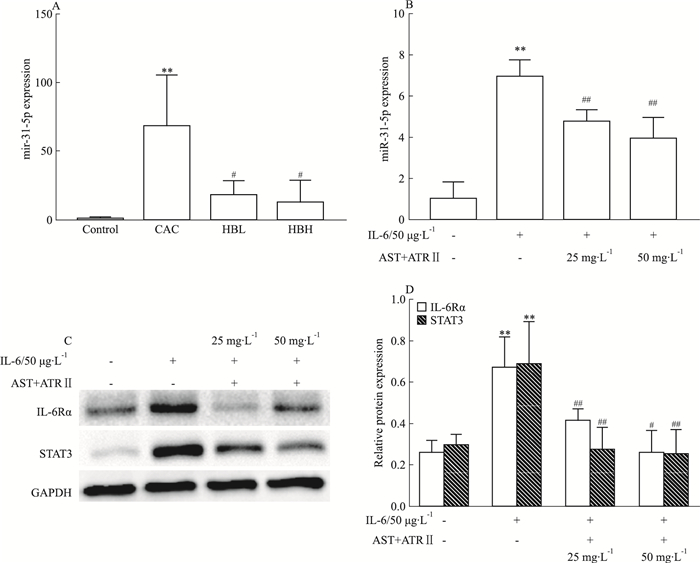
与CAC模型组相比,HBL与HBH组miR-31-5p表达下降(Fig 5A),同时降低STAT3、p-STAT3蛋白表达(Fig 3); 白术内酯Ⅱ和黄芪甲苷(atractylenolide Ⅱ and astragaloside,ATRII+AST)复合物不同浓度(25、50 mg·L-1)干预,可降低IL-6引起的miR-31-5p的表达水平增高(Fig 5B),同时,降低STAT3、IL-6Rα的表达(Fig 5C)。
|
| Fig 5 Intervention of Huangqi Baizhu decoction and monomer complex on miR-31-5p/STAT3 A: Huangqi Baizhu detection intervention on the expression level of miR-31-5p in CAC mice colon(x±s, n=8).**P < 0.01 vs control; #P < 0.05 vs CAC. B:Effect of ATR Ⅱ+AST(25, 50 mg·L-1) on miR-31-5p expression in RAW264.7 cells stimulated with IL-6(50 μg·L-1) for 24 h(x±s, n=3); C-D:Effect of ATR Ⅱ+AST(25, 50 mg·L-1) on STAT3 and IL-6Rα protein expression in RAW264.7 cells stimulated with IL-6(x±s, n=3).**P < 0.01 vs control; #P < 0.05, ##P < 0.01 vs IL-6. |
研究表明,局部炎症微环境促进肿瘤的形成机制包括:激活癌前细胞增殖和抗凋亡特性,同时导致细胞积累突变和遗传变异[7]。慢性肠道炎症通过促炎性细胞因子的产生、细胞增殖、免疫应答的改变,促进CAC的肿瘤发生[8-9]。CAC小鼠模型早期,IL-6大多是由髓样细胞产生的,其他细胞,如T细胞、肠上皮细胞也能产生IL-6。而骨髓来源的IL-6与潜在的慢性炎症密切相关,上皮细胞和肿瘤细胞产生的IL-6能促进新的肿瘤产生。与正常人活检对比,溃疡性结肠炎病人结肠上皮细胞中IL-6/STAT3被明显激活,而且STAT3显色阳性结果与炎症的严重程度相关[10]。
microRNA的异常表达和结肠癌之间密切相关,microRNA具有作为结肠直肠癌生物标志物和治疗靶点的潜力,目前认为可以作为早期检测的生物标记和预后的分类器[11]。microRNA参与结肠炎-癌病理发生机制尚不明晰。采用肿瘤细胞与免疫细胞共培养研究发现,IL-6与miR-21、miR-29b可以形成环路,进行免疫细胞与肿瘤细胞之间的“交流”,从而维持慢性炎症,并促进肿瘤细胞的侵袭特性。肿瘤微环境中的细胞交流可能为未来治疗措施提供思路[12]。本研究发现,miR-31-5p可能是结肠炎症和肿瘤发生的关键参与者,在小鼠CAC模型中miR-31-5p明显增高,且与IL6/STAT3信号通路的激活存在正向调控作用,miR-31-5p可能参与了肠道上皮细胞及免疫细胞之间的cross-talk,并且放大炎症信号,进而引起上皮细胞异型增生,乃至肿瘤的发生,其作用机制有待继续深入探讨。
目前,结直肠癌的治疗主要以外科治疗为主。采用放疗、化疗和靶向治疗,5年生存率仍徘徊在50%左右[13]。另外,定期电子肠镜检查是早期诊断CAC的重要手段(属于二级预防), 许多学者试图探索在治疗溃疡性结肠炎的同时,能够找到对CAC有预防作用的药物,期望这些药物能够逆转、抑制、预防CAC的发生与发展。中医药在缓解结肠炎症、修复肠道黏膜损伤等方面具有独特的疗效,且前期研究表明,益气健脾方药可通过调节IL-6/STAT3,干预溃疡性结肠炎的急慢性病理过程。中医理论认为,脾虚气滞是结肠炎相关性结肠癌的基础,补气健脾是其基本治疗方法[14]。黄芪白术汤源于金元医家刘完素《素问病机气宜保命集·泻痢论》,也是劳绍贤教授治疗脾虚气滞所致结肠炎和CAC的基础复方。前期研究表明,黄芪白术汤及其有效部位具有明显的抗炎作用,对溃疡性结肠炎和CAC的病理变化有抑制作用[15]。体外研究发现,黄芪甲苷及白术内酯Ⅰ、Ⅱ、Ⅲ对消化道肿瘤有较好的治疗作用[16-17]。本研究结果表明,黄芪白术汤及其单体复合物可通过抑制miR-31/STAT3的激活,阻滞CAC病理进程。本研究提示,miR-31-5p可作为CAC或相关结肠肿瘤的早期生物标记,并为临床以microRNA为治疗靶标提供了思路。
| [1] |
Candido J, Hagemann T. Cancer-related inflammation[J]. J Clin Immunol, 2013, 33(1): S79-84. |
| [2] |
Schetter A J, Heegaard N H, Harris C C. Inflammation and cancer: interweaving microRNA, free radical, cytokine and p53 pathways[J]. Carcinogenesis, 2010, 31(1): 37-49. doi:10.1093/carcin/bgp272 |
| [3] |
唐苗, 卢倩, 刘衡, 等. 溃疡性结肠炎相关信号通路的研究进展[J]. 中国药理学通报, 2018, 34(12): 1642-7. Tang M, Lu Q, Liu H, et al. Research progress of ulcerative colitis related signaling pathways[J]. Chin Pharmacol Bull, 2018, 34(12): 1642-7. doi:10.3969/j.issn.1001-1978.2018.12.004 |
| [4] |
Atreya R, Neurath M F. Involvement of IL-6 in the pathogenesis of inflammatory bowel disease and colon cancer[J]. Clin Rev Allergy Immunol, 2005, 28(3): 187-96. doi:10.1385/CRIAI:28:3:187 |
| [5] |
Musso A, Dentelli P, Carlino A, et al. Signal transducers and activators of transcription 3 signaling pathway: an essential mediator of inflammatory bowel disease and other forms of intestinal inflammation[J]. Inflamm Bowel Dis, 2005, 11(2): 91-8. doi:10.1097/00054725-200502000-00001 |
| [6] |
赵青春, 沈洪, 程海波, 等. 清肠化湿方对HT-29细胞IL-6/JAK2/STAT3的影响[J]. 中国药理学通报, 2015, 31(6): 883-5. Zhao Q C, Shen H, Cheng H B, et al. Effect of Qingchang Huashi Recipe on IL-6/JAK2/STAT3 pathway in HT-29 cells[J]. Chin Pharmacol Bull, 2015, 31(6): 883-5. doi:10.3969/j.issn.1001-1978.2015.06.029 |
| [7] |
Mantovani A, Allavena P, Sica A, et al. Cancer-related inflammation[J]. Nature, 2008, 454(7203): 436-44. doi:10.1038/nature07205 |
| [8] |
Siegel R L, Miller K D, Fedewa S A, et al. Colorectal cancer statistics, 2017[J]. CA Cancer J Clin, 2017, 67(3): 177-93. doi:10.3322/caac.21395 |
| [9] |
Jess T, Rungoe C, Peyrin-Biroulet L. Risk of colorectal cancer in patients with ulcerative colitis: a meta-analysis of population-based cohort studies[J]. Clin Gastroenterol Hepatol, 2012, 10(6): 639-45. doi:10.1016/j.cgh.2012.01.010 |
| [10] |
Grivennikov S, Karin E, Terzic J, et al. IL-6 and Stat3 are required for survival of intestinal epithelial cells and development of colitis-associated cancer[J]. Cancer Cell, 2009, 15(2): 103-13. |
| [11] |
Okayama H, Schetter A J, Harris C C. MicroRNAs and inflammation in the pathogenesis and progression of colon cancer[J]. Dig Dis, 2012, 30(2): 9-15. |
| [12] |
Patel S A, Gooderham N J. IL-6 mediates immune and colorectal cancer cell cross-talk via miR-21 and miR-29b[J]. Mol Cancer Res, 2015, 13(11): 1502-8. doi:10.1158/1541-7786.MCR-15-0147 |
| [13] |
Siegel R, Naishadham D, Jemal A. Cancer statistics, 2012[J]. CA Cancer J Clin, 2012, 62(1): 10-29. doi:10.3322/caac.20138 |
| [14] |
邵文琳, 谢斌, 姚亮亮, 等. 结肠炎相关性结肠癌前病变的研究进展[J]. 江西中医学院学报, 2010, 22(5): 87-91. Shao W L, Xie B, Yao L L, et al. Research progress of colitis-related precancerosis of colonic carcinoma[J]. J Jiangxi Univ TCM, 2010, 22(5): 87-91. doi:10.3969/j.issn.1005-9431.2010.05.034 |
| [15] |
石忠峰, 陈蔚文, 李茹柳, 等. 白术黄芪汤及其有效部位组方对小鼠溃疡性结肠炎的疗效观察[J]. 中药新药与临床药理, 2007, 18(2): 87-90. Shi Z F, Chen W W, Li R L, et al. Effects of Baizhu Huangqi detection and its effective-part prescription on mice ulcerative colitis[J]. Tradit Chin Drug Res Clin Pharmacol, 2007, 18(2): 87-90. doi:10.3321/j.issn:1003-9783.2007.02.001 |
| [16] |
庞歆桥, 赵鹏飞, 杨凡, 等. 黄芪甲苷联合西妥昔单抗对人结肠癌细胞系RKO自噬调节与增殖的抑制作用[J]. 实用医学杂志, 2016, 32(18): 2992-5. Pang X Q, Zhao P F, Yang F, et al. Astragaloside combine with cetuximab inhibits proliferation and regulates autophagy of human colon cancer cell RKO[J]. J Practical Med, 2016, 32(18): 2992-5. doi:10.3969/j.issn.1006-5725.2016.18.014 |
| [17] |
高小玲, 汪保英, 陈玉龙, 等. 白术内酯对小鼠结肠癌细胞增殖能力的影响[J]. 世界华人消化杂志, 2013, 21(26): 2690-3. Gao X L, Wang B Y, Chen Y L, et al. Atractylenolide Ⅱ significantly reduces proliferation of mouse colon cancer cells[J]. World Chin J Digestol, 2013, 21(26): 2690-3. |

