


2. 药用美洲大蠊四川省重点实验室,四川 成都 610000
巫秀美(1968-),女,博士,讲师,研究方向:医学统计学,通讯作者,E-mail:wxm6865@163.com
 ,
SUN Min-zhe1,
DU Wen-wen1,
LIU Heng1
,
SUN Min-zhe1,
DU Wen-wen1,
LIU Heng1
 ,
SHEN Yong-mei2,
WU Tao-qing2,
ZHAO Yu1,2,
WU Xiu-mei1
,
SHEN Yong-mei2,
WU Tao-qing2,
ZHAO Yu1,2,
WU Xiu-mei1

2. Sichuan Key Laboratory of Medical American Cockroach, Chengdu 610000, China
溃疡性结肠炎(ulcerative colitis,UC)是一种病因和发病机制尚不明确的炎症性肠病。该病通常反复发作,发病时主要临床表现为腹痛、腹泻、黏液脓血便、体质量减轻等[1]。临床以发作、缓解及复发交替为特点,是常见的消化系统疾病[2]。研究表明[3],UC的主要病理机制可能与免疫功能、细胞炎症因子调控网络失衡、肠道菌群失调等有关。目前,UC的治疗主要以5-氨基水杨酸类、糖皮质激素类或免疫抑制剂类药物为主[4],长期用药有一定的副作用,疗效降低。研究发现,中药复方保留灌肠治疗轻、中度UC具有明显的疗效[5]。
美洲大蠊(Periplaneta americana L.)是蜚蠊科中体积最大的昆虫,最早作为中药记录于神农本草经中,谓“性咸”、“味平”,归肝肾脾经,主血瘀,症坚,具有消积生肌,清热解毒等功效。临床常用于小儿疳积、咽喉肿痛、虫蛇咬伤、疮痈肿毒、消化道溃疡等[6]。美洲大蠊具有抗肿瘤、抗感染、提高机体免疫力、促进组织修复、抗炎镇痛等多方面药理作用[7]。研究发现,以美洲大蠊干燥虫体的提取物为有效成分的中成药康复新液,在临床上保留灌肠治疗UC具有明显的疗效[8]。因此,本实验在此研究基础上,将蜚蠊、蒲公英、薏苡仁、乌梅、陈皮按5 :2 :1 :1 :1组方配比,通过水提醇沉的方式获得复方蜚蠊提取物PB,采用灌肠给药的方法治疗异体抗原联合醋酸诱导的慢性UC大鼠,考察复方蜚蠊提取物PB对慢性UC的疗效及作用机制,为其用于慢性UC的治疗提供实验依据。
1 材料 1.1 实验动物健康SPF级2月龄SD大鼠86只,♀♂各半,体质量(200±10)g,购于湖南斯莱克景达实验动物有限公司,许可证号:SCXK(湘)2016-0004,饲养于大理大学IVC动物中心。适应性饲养健康家兔50只,♀♂不拘,体质量(3.0~3.5) kg,大理大学实验动物中心提供,许可证号:SCXK(滇)2008-0003。
1.2 药物与试剂复方蜚蠊提取物PB(包括蜚蠊、蒲公英、薏苡仁、乌梅、陈皮等混合提取物)(批号:20150724),由大理大学昆虫生物医药研究院张成桂副教授提供; 柳氮磺胺吡啶(sulfasalazine,SASP)(批号:09160503),上海信宜天平药业有限公司; 肠炎宁(批号:160303),江西天施康弋阳制药有限公司; 冰醋酸(批号:20130114),天津市瑞金特化学品有限公司; 完全弗氏佐剂(批号:SLBK1733),Sigma公司; 大鼠肿瘤坏死因子α(tumor necrosis factor α,TNF-α)ELISA试剂盒(批号:R160927-102a)、白细胞介素4(interleukin 4,IL-4)ELISA试剂盒(批号:R160927-002b)、IL-8 ELISA试剂盒(批号:R161025-008b)、干扰素γ(interferon γ,IFN-γ)试剂盒(批号R161025-101b),均购自于欣博盛QuantiCyto®生物科技有限公司; 大鼠C反应蛋白(C-reactive protein,CRP)试剂盒(批号:20151215)、免疫球蛋白G(immunoglobulin G,IgG)试剂盒(批号:20161101)、IL-17试剂盒(批号:20161228)、髓过氧化物酶(myeloperoxidase,MPO)试剂盒(批号:20161022)、表皮生长因子(epidermal growth factor,EGF)试剂盒(批号:20161228)、隐血试剂盒(批号:20160823),均购于南京建成生物科技有限公司。
1.3 仪器TL-16R台式高速冷冻离心机(上海离心机机械研究所); T6新世纪紫外-可见分光光度计(北京普析通用仪器有限责任公司); 2010酶标仪(奥地利安图斯公司)。
2 方法 2.1 异体抗原乳化剂的制备[9]取家兔新鲜结肠50根,刮取兔结肠黏膜,加入适量氯化钠溶液制成匀浆液,-20 ℃过夜,解冻后,4 000 r·min-1、4 ℃冷冻离心30 min,取上清液于-20 ℃过夜,解冻后,4 000 r·min-1、4 ℃离心30 min,再转移至-80 ℃过夜后冻干,制备成家兔结肠抗原冻干粉,-20 ℃放置备用。异体抗原乳化剂每次临用前配制,精密称取家兔结肠抗原冻干粉600 mg(每只8 mg),加入3.75 mL氯化钠溶液溶解,待完全溶解后,取3.75 mL完全弗氏佐剂,涡旋混匀制备成异体抗原乳化剂。
2.2 动物模型建立[9]于d 1、8、15、22、29,取异体抗原乳化剂(现配现用),分别在大鼠左侧足跖、右侧足趾、腹股沟、背部皮下、腹腔注射异体抗原乳化剂0.1 mL(每只含抗原8 mg,完全弗氏佐剂0.05 mL,末次注射不加佐剂),末次注射禁食不禁水24 h后,对大鼠用5%醋酸1 mL灌肠,留置15 s,用氯化钠溶液4 mL冲洗后,再用异体抗原乳化剂1 mL灌肠,留置30 min后,用4 mL氯化钠溶液洗净排出,造模完成。
2.3 分组及给药正常组大鼠不造模(10只),其余76只大鼠造模后,参考Hamamoto等[10]标准进行疾病活动指数(disease activity index,DAI)评分,按照大鼠DAI评分(0~3分为极轻度炎症,4~6分为轻度炎症,7~9分为中度炎症,10~12分为重度炎症),剔除极轻度炎症和重度炎症大鼠,剩余60只大鼠按炎症严重程度分层随机分组:模型组(Model)、柳氮磺胺吡啶组(SASP 300 mg·kg-1)、肠炎宁组(Changyanning 300 mg·kg-1)、复方蜚蠊提取物PB低、中、高剂量组(PB 50、100、200 mg·kg-1),每组10只,♀♂各半。除正常组、模型组灌肠0.9%氯化钠溶液外,其余各组灌肠给予相应的药物,每天1次,连续14 d。
2.4 观察指标及方法记录各组大鼠给药d 1、4、7、10、14的DAI评分。末次给药24 h后,用质量分数为10 g·L-1的水合氯醛麻醉大鼠,腹主动脉取血,4 ℃静置4 h,3 500 r·min-1离心10 min,取上层血清,按试剂盒说明检测IL-4、IL-8、IL-17、IFN-γ、CRP、IgG含量。解剖取出结肠,沿肠系膜缘剪开肠腔,氯化钠溶液冲洗粪便,观察肠壁,称量湿质量,采集结肠照片,参照标准[11]并进行结肠黏膜损伤指数(colonic mucosal damage index, CMDI)评分; 切取病变严重区域结肠0.15 g,按1 :9(W/V)氯化钠溶液匀浆,3 500 r·min-1离心10 min,取上清液,按试剂盒说明检测上清液中TNF-α、MPO、EGF含量。剩余结肠用40 g·L-1甲醛固定,制作病理切片,并参照Ekström[12]标准进行病理组织学评分(histopathological score,HS)。解剖取出肝脏、脾脏、胸腺等脏器,称量质量,计算脏器指数:脏器指数/%=各脏器质量/体质量×100%。
2.5 统计学方法计量资料以x±s表示,并用SPSS 20.0软件对各组数据进行统计分析,连续型资料采用单因素方差分析,组间比较采用LSD检验方法。根据数据处理结果,以GraphPad Prism 5制图。
3 结果 3.1 复方蜚蠊提取物PB对慢性UC大鼠DAI评分的影响异体抗原联合醋酸造模期间,除正常组以外,各组大鼠均出现不同程度的厌食、懒动、体质量下降、腹泻、血便等情况。Tab 1结果显示,实验期间,正常组大鼠DAI评分较小且基本不变; 根据给药d 1的DAI评分,模型组DAI评分与正常组DAI评分差异有显著性(P<0.01),提示模型建立成功; 复方蜚蠊提取物PB灌肠给药d 14,PB各剂量组DAI评分均较低,提示经复方蜚蠊提取物PB灌肠给药治疗后,大鼠的慢性UC症状在一定程度上得到缓解。与模型组比较,PB中剂量组DAI评分最低(P<0.01),接近正常组。
| Group | Does/mg·kg-1 | DAI score | ||||
| d 1 | d 4 | d 7 | d 11 | d 14 | ||
| Normal | - | 1.5±0.5 | 1.7±0.7 | 1.6±0.5 | 1.6±0.5 | 1.2±0.4 |
| Model | - | 9.6±0.8** | 9.8±0.9** | 7.2±1.3** | 4.3±1.0** | 3.1±0.9** |
| SASP | 300 | 9.5±0.8** | 8.3±1.3** | 4.8±1.4** | 2.9±1.0**## | 2.2±0.6* |
| Changyanning | 300 | 8.4±0.5** | 8.9±1.6** | 6.3±1.6** | 3.4±0.8** | 2.6±1.9** |
| PB | 50 | 8.5±0.5** | 9.6±0.8** | 6.2±1.7** | 4.5±1.8** | 2.3±1.1* |
| 100 | 8.2±0.9** | 8.6±0.8** | 5.3±1.1** | 2.6±1.4**## | 1.5±0.7## | |
| 200 | 8.4±0.5** | 9.1±0.7** | 6.2±2.0** | 3.9±0.3** | 2.6±1.0** | |
| *P<0.05, **P<0.01 vs normal; ##P<0.01 vs model | ||||||
正常组大鼠肠壁肉眼观察结肠黏膜无明显水肿、糜烂和溃疡形成; 模型组大鼠肠壁可见明显的充血与水肿。与正常组相比,模型组大鼠结肠长度变短,宽度变宽,CMDI评分最高(P<0.01)。与模型组比较,SASP组和肠炎宁组大鼠结肠长度变长,宽度变窄,CMDI评分降低,差异均具有统计学意义(P<0.01);复方蜚蠊提取物PB各剂量组大鼠结肠长度无显著性差异,结肠宽度明显变窄(P<0.01),CMDI明显降低(P<0.05,P<0.01)。与模型组比较,SASP组、肠炎宁组和PB中、高剂量组结肠指数明显降低(P<0.05,P<0.01)。见Tab 2。
| Group | Does/mg·kg-1 | Length/cm | Broad/cm | CMDI | Colon index/g·kg-1 |
| Normal | - | 20.52±2.17 | 0.77±0.11 | 0.70±0.5 | 3.71±0.94 |
| Model | - | 15.70±2.02** | 1.16±0.25** | 3.5±0.9** | 6.20±0.83** |
| SASP | 300 | 18.84±1.53*## | 0.82±0.13## | 1.8±0.9*## | 4.59±0.55## |
| Changyanning | 300 | 18.11±1.77 **## | 0.98±0.17**# | 2.5±1.0**# | 4.91±1.32*# |
| PB | 50 | 16.03±1.66**△△ | 0.92±0.15## | 2.6±1.2**# | 5.43±1.68** |
| 100 | 17.23±1.75** | 0.93±0.23*## | 2.0±1.3**## | 5.10±0.92**# | |
| 200 | 16.26±2.05**△△ | 0.92±0.16## | 2.2±0.8**## | 4.52±0.78**# | |
| *P<0.05, **P<0.01 vs normal; #P<0.05, ##P<0.01 vs model; △△P<0.01 vs SASP | |||||
Tab 3结果显示,与正常组比较,模型组小鼠肝脏、胸腺及脾脏指数均升高,但差异无显著性。复方蜚蠊提取物PB低剂量组的肝脏指数,以及PB中剂量组的胸腺指数均升高(P<0.05)。与模型组比较,PB低剂量组肝脏、脾脏指数以及PB中、高剂量组胸腺指数均升高,但差异无显著性。
| Group | Does/mg·kg-1 | Liver index/g·kg-1 | Spleen index/g·kg-1 | Thymus index/g·kg-1 |
| Normal | - | 23.82±5.46 | 1.95±0.42 | 0.50±.03 |
| Model | - | 26.27±5.62 | 2.02±0.70 | 0.73±0.26 |
| SASP | 300 | 24.36±2.11 | 1.71±0.46 | 0.65±0.36 |
| Changyanning | 300 | 25.47±1.91 | 1.80±0.54 | 0.67±0.29 |
| PB | 50 | 27.94±6.28* | 2.13±0.66 | 0.51±0.27 |
| 100 | 25.59±2.96 | 2.20±0.25 | 0.81±0.33* | |
| 200 | 25.28±1.60 | 1.93±0.25 | 0.73±0.31 | |
| *P<0.05 vs normal | ||||
如Tab 4所示,与正常组比较,模型组大鼠IL-8、IL-17、CRP、IFN-γ、IgG含量均明显升高(P<0.01),而IL-4含量明显降低(P<0.01);与模型组比较,SASP组、肠炎宁组、复方蜚蠊提取物PB各剂量组大鼠IL-8、IL-17、CRP、IFN-γ、IgG含量均明显降低(P<0.01);SASP组、肠炎宁组、PB高剂量组IL-4含量明显升高(P<0.01)。与SASP组比较,PB低剂量组大鼠IL-4、IL-8含量明显降低(P<0.01),IL-17、IFN-γ含量明显升高(P<0.05,P<0.01)。
| Group | Does/mg·kg-1 | IL-4/ng·L-1 | IFN-γ/ng·L-1 | IL-8/ng·L-1 | IL-17/ng·L-1 | CRP/ng·L-1 | IgG/ng·L-1 |
| Normal | - | 28.48±2.12 | 2.80±1.49 | 40.54±11.53 | 14.12±2.56 | 0.81±0.16 | 8.54±1.12 |
| Model | - | 20.29±2.73** | 14.1±2.81** | 77.78±9.66** | 22.95±3.29** | 4.12±0.74** | 14.84±3.14** |
| SASP | 300 | 26.59±5.71## | 4.65±1.98*## | 57.16±9.54**##▲▲ | 11.23±3.52## | 3.11±0.42**## | 7.70±1.17## |
| Changyanning | 300 | 28.93±6.69## | 7.81±1.17**##△ | 41.84±11.77## | 13.18±2.03## | 3.01±0.35**## | 8.77±0.93## |
| PB | 50 | 19.39±2.80**△△▲▲ | 6.45±1.18**##△ | 37.43±10.44##△△ | 16.02±2.99##△△ | 2.81±0.40**## | 9.01±1.65## |
| 100 | 22.80±2.98**▲▲ | 5.23±1.12**##▲▲ | 44.19±11.97##△ | 16.50±4.25##△△▲ | 2.85±0.33**## | 8.00±1.38## | |
| 200 | 25.78±3.86## | 5.76±1.88**##▲ | 49.44±9.24## | 15.26±2.25##△ | 2.79±0.53**## | 8.83±1.33## | |
| *P<0.05, **P<0.01 vs normal; ##P<0.01 vs model; △P<0.05, △△P<0.01 vs SASP; ▲P<0.05, ▲▲P<0.01 vs Changyanning | |||||||
如Tab 5所示,与正常组比较,模型组大鼠EGF含量明显降低,MPO、TNF-α含量均明显升高(P<0.01);与模型组相比,SASP组、肠炎宁组、复方蜚蠊提取物PB中剂量组大鼠结肠组织中TNF-α、MPO含量明显降低(P<0.01),SASP组、肠炎宁组大鼠结肠组织中EGF含量明显升高(P<0.01)。
| Group | Does/mg·kg-1 | TNF-α/ng·L-1 | MPO/kU·g-1 | EGF/ng·L-1 |
| Normal | - | 556.30±68.49 | 0.17±0.02 | 355.21±24.54 |
| Model | - | 878.81±43.03** | 0.62±0.07** | 197.49±8.21** |
| SASP | 300 | 667.40±51.48*## | 0.29±0.06**## | 298.51±62.78**## |
| Changyanning | 300 | 654.54±44.57*## | 0.34±0.09**## | 262.80±35.38**## |
| PB | 50 | 796.96±79.19**△△▲▲ | 0.33±0.07**## | 173.81±40.31**△△ |
| 100 | 745.54±11.28**## | 0.31±0.10**## | 224.45±32.03**△△ | |
| 200 | 712.95±170.15**## | 0.27±0.05*##▲ | 213.98±42.14**△△▲ | |
| *P<0.05, **P<0.01 vs normal; ##P<0.01 vs model; △△P<0.01 vs SASP; ▲P<0.05, ▲▲P<0.01 vs Changyanning | ||||
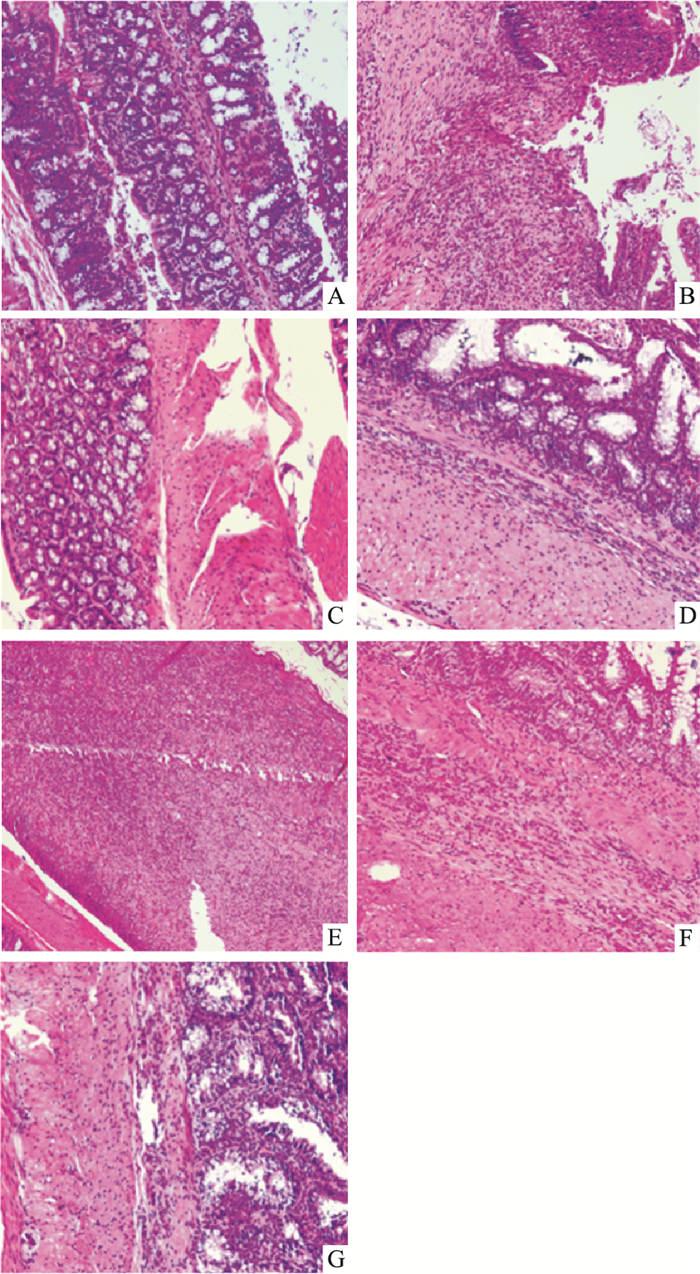
Tab 6、Fig 1结果显示,正常组大鼠结肠黏膜层、黏膜下层、肌层及浆膜层结构完整清晰,肠黏膜上皮细胞形态正常,腺体排列整齐,隐窝正常,无充血水肿、炎性细胞浸润现象; 模型组大鼠结肠黏膜不同程度的破损,杯状细胞和隐窝大量丢失,黏膜层和黏膜基层炎性细胞浸润,并伴有水肿。与正常组相比,模型组大鼠上皮细胞、炎性细胞及HS评分均明显升高(P<0.01);与模型组相比,SASP组、肠炎宁组及复方蜚蠊提取物PB低、中、高剂量组大鼠上皮细胞、炎性细胞及HS评分均明显降低(P<0.01);PB高剂量组与阳性药SASP组数值相当,PB低、中剂量组数值与阳性药肠炎宁组相当。
| Group | Does/mg·kg-1 | Epithelial cell/grade | Inflammatory cells/grade | HS/total points |
| Normal | - | 1.0±0.0 | 1.0±0.0 | 2.0±0.0 |
| Model | - | 3.3±0.5** | 3.4±0.5** | 6.7±0.8** |
| SASP | 300 | 1.0±0.0## | 1.0±0.0## | 2.0±0.0## |
| Changyanning | 300 | 1.8±0.8**##△△ | 1.8±0.8**##△△ | 3.6±1.6**##△△ |
| PB | 50 | 1.9±1.0**##△△ | 1.9±1.0**##△△ | 3.8±2.0**##△△ |
| 100 | 1.7±0.9*##△ | 1.8±0.9**##△△ | 3.5±1.8*##△ | |
| 200 | 1.3±0.5## | 1.6±0.7## | 2.9±1.1## | |
| *P<0.05, **P<0.01 vs normal; ##P<0.01 vs model; △P<0.05, △△P<0.01 vs SASP | ||||
|
| Fig 1 The pathological section of rat UC organization by clysis way (HE, ×200) A:Normal; B:Model; C:SASP; D:Changyanning; E:PB high dose; F:PB medium dose; G:PB low dose |
本研究采用异体抗原联合醋酸诱导大鼠慢性UC,大鼠在造模后出现腹泻、血便、体质量下降等症状,肉眼可见结肠黏膜糜烂和溃疡形成,镜下可见模型组大鼠结肠有大量炎性细胞浸润,血清中CRP含量明显升高。MPO是中性粒细胞产生的一种重要的过氧化物酶,其活性高低是判断中性粒细胞浸润程度的重要指标,也是结肠炎症严重程度的重要指标[13]。模型组HS评分、结肠黏膜MPO、TNF-α含量明显高于正常组; 与模型组比较,阳性药SASP组、肠炎宁组和复方蜚蠊提取物PB各剂量组HS评分、结肠黏膜MPO、TNF-α表达量均不同程度降低。结果提示,复方蜚蠊提取物PB可以降低中性粒细胞表达,促进黏膜修复,改善结肠病理组织变化。
目前研究认为,效应CD4+T细胞的异常活化可能是导致溃疡性结肠炎肠黏膜免疫和后续炎症反应的重要机制之一[14]。CD4+T细胞主要包括Th1、Th2、Th17和调节性T细胞,参与体内多种免疫应答和炎症反应。INF-γ、IL-8、TNF-α主要是Th1细胞分泌的促炎因子,在清除细胞内病原体中发挥重要作用; Th2细胞能分泌IL-4、TGF-β1等细胞因子,协助激活B细胞产生特异性抗体IgG,以清除细胞外病原体; Th17细胞是一类与Th1细胞和Th2细胞亚群不同分化机制和功能特性的新型CD4+T细胞亚群,主要分泌IL-17、IL-23等细胞因子。IL-17具有较强激活中性粒细胞的能力,可诱导炎症的发生和导致组织损伤。本实验中,模型组大鼠血清中IL-17、INF-γ、IL-8、IgG含量均明显升高,而IL-4含量明显降低,提示模型组大鼠结肠黏膜损伤,上皮细胞新陈代谢功能障碍,有大量炎症细胞浸润,Th1/Th2平衡失调且倾向于Th1。而慢性UC大鼠经过复方蜚蠊提取物灌肠治疗后,UC症状明显改善,大鼠体质量增加,精神逐渐恢复,血便、稀便等症状减轻,排便频数下降; 血清中IL-17、IL-8、IFN-γ、IgG含量明显降低,血清中IL-4的含量明显升高。提示复方蜚蠊提取物PB可以调节炎症因子的表达,减少炎症细胞浸润,减轻炎症反应,调节机体细胞免疫和体液免疫,使机体细胞免疫功能恢复平衡。
综上所述,复方蜚蠊提取物可以通过调节细胞免疫和体液免疫治疗UC,但是复方蜚蠊提取物PB治疗慢性UC并未出现明显的剂量依赖性,可能与中药复方制剂量效关系异常复杂有关。中药复方的量效关系不仅有化学药物的共同属性,同时又具有鲜明的中医药特色,中药复方在一系列复杂的化学反应后,每个单位被重新拆分和组合,形成了新的疗效物质成分[15]。由此可见,中药复方的量效关系复杂,如何确定中药复方剂量在临床上的疗效,仍然是中药科研者需要面临的问题之一。
( 致谢: 感谢大理大学昆虫生物医药研究院张俊、唐苗、余万鑫及大理大学动物实验中心吴定宇老师对本课题的支持!)
| [1] |
唐苗, 卢倩, 刘衡, 等. 溃疡性结肠炎相关信号通路的研究进展[J]. 中国药理学通报, 2018, 34(12): 1642-7. Tang M, Lu Q, Liu H, et al. Advances in the study of signaling pathways associated with ulcerative colitis[J]. Chin Pharmacol Bull, 2018, 34(12): 1642-7. doi:10.3969/j.issn.1001-1978.2018.12.004 |
| [2] |
张声生, 沈洪, 郑凯, 等. 溃疡性结肠炎中医诊疗专家共识意见(2017)[J]. 中华中医药杂志, 2017, 32(8): 3585-9. Zhang S S, Shen H, Zheng K, et al. Expert of diagnosis and treatment of ulcerative colitis of traditional Chinese medicine agrees opinion[J]. Chin J Tradit Chin Med Pharm, 2017, 32(8): 3585-9. |
| [3] |
Farrell R J, Peppercorn M A. Ulcerative colitis[J]. Lancet, 2002, 359(9303): 331-40. doi:10.1016/S0140-6736(02)07499-8 |
| [4] |
李军祥, 陈誩. 溃疡性结肠炎中西医结合诊疗共识意见(2017)[J]. 中国中西医结合消化杂志, 2018, 26(2): 105-11, 120. Li J X, Chen J. Expert of diagnosis and treatment of ulcerative colitis of traditional Chinese medicine agrees opinion[J]. Chin J Integr Trad West Med Dig, 2018, 26(2): 105-11, 120. |
| [5] |
陈冠儒, 张怡, 郑育卿, 等. 芪附理中灌肠方对溃疡性结肠炎大鼠血清IL-8、IL-10及肠黏膜ICAM-1表达的影响[J]. 中药药理与临床, 2017, 33(4): 122-5. Chen G R, Zhang Y, Zheng Y Q, et al. Effect of Qifulizhong Enema on expressions of IL-8, ICAM-1 of the rats with ulcerative colitis[J]. Pharmacol Clin Chin Mater Med, 2017, 33(4): 122-5. |
| [6] |
张俊, 魏永凯, 李玥, 等. 美洲大蠊提取物Ento-D对醋酸诱导的急性溃疡性结肠炎大鼠的作用及机制研究[J]. 中华中医药杂志, 2018, 33(1): 304-8. Zhang J, Wei Y K, Li Y, et al. Effects and mechanism of Periplaneta americana extracted Ento-D on aceticacid-induced ulcerative colitis in rats[J]. Chin J Tradit Chin Med Pharm, 2018, 33(1): 304-8. |
| [7] |
何正春, 彭芳, 宋丽艳, 等. 美洲大蠊化学成分及药理作用研究进展[J]. 中国中药杂志, 2007, 32(21): 2326-31. He Z C, Peng F, Song L Y, et al. Review on investigations related to chemical constituents and biological activities of Periplaneta Americana[J]. Chin J Chin Mater Med, 2007, 32(21): 2326-31. doi:10.3321/j.issn:1001-5302.2007.21.031 |
| [8] |
何元清, 何子彬, 张晗, 等. 美沙拉嗪联合康复新液保留灌肠治疗活动期溃疡性结肠炎的临床观察[J]. 中国药房, 2017, 28(29): 4133-6. He Y Q, He Z B, Zhang H, et al. Clinical observation of mesalazine combined with Kangfuxin solution retention enema in the treatment of active ulcerative colitis[J]. Chin Pharm, 2017, 28(29): 4133-6. doi:10.6039/j.issn.1001-0408.2017.29.28 |
| [9] |
张俊, 吴定宇, 戴莉萍, 等. 异体抗原联合醋酸诱导大鼠慢性溃疡性结肠炎模型的优化与评价[J]. 实验动物科学, 2017, 34(3): 43-8. Zhang J, Wu D Y, Dai L P, et al. Optimization and evaluation of allogeneic antigen combined with acetic acid in rats with chronic ulcerative colitis[J]. Lab Anim Sci, 2017, 34(3): 43-8. doi:10.3969/j.issn.1006-6179.2017.03.010 |
| [10] |
Hamamoto N, Maemura K, Hirata I, et al. Inhibition of dextransulphate sodium (DSS) -induced colitis in mice by intracolonically administered antibodies against adhesion molecules (endothelialleucocyte adhesion molecule-1 (ELAM-1) or intercellular adhe-sion molecule-1 (ICAM-1))[J]. Clin Exp Immunol, 1999, 117(3): 462-8. doi:10.1046/j.1365-2249.1999.00985.x |
| [11] |
Luk H H, Ko J K S, Fung H S, et al. Delineation of the protective action of zinc sulfate on ulcerative colitis in rats[J]. Eur J Pharmacol, 2002, 443: 197-204. doi:10.1016/S0014-2999(02)01592-3 |
| [12] |
Ekstrom G M. Oxazolone-induced colitis in rats: Effects of budesonide, cyclosporine A, and 5-aminosalicylic acid[J]. Scand J Gastroenterol, 1998, 33(2): 174-9. doi:10.1080/00365529850166914 |
| [13] |
张汉超, 王朋川, 刘衡, 等. 康复新液缓解三硝基苯磺酸致大鼠溃疡性结肠炎及其机制研究[J]. 中国药理学通报, 2018, 34(4): 496-501. Zhang H C, Wang P C, Liu H, et al. Effect of Kangfuxin on ulcerative colitis induced by trinitrobenzene sulfonic acid in rats[J]. Chin Pharmacol Bull, 2018, 34(4): 496-501. doi:10.3969/j.issn.1001-1978.2018.04.012 |
| [14] |
吴昊, 夏盛隆, 夏宣平, 等. 结肠组织中Th1/Th2和Th17细胞失衡与溃疡性结肠炎的关系[J]. 解放军医学杂志, 2017, 42(9): 793-8. Wu H, Xia S L, Xia X P, et al. Association of ulcerative colitis with the imbalance betwen Th1, Th2 and Th17 cells in the colonic tissues[J]. Med J Chin PLA, 2017, 42(9): 793-8. |
| [15] |
张斐, 杜武勋, 朱明丹, 等. 中药复方量效关系研究现状[J]. 中医杂志, 2013, 54(1): 74-7. Zhang F, Du W X, Zhu M D, et al. Research status of dose-effect relationship of traditional Chinese medicine compound[J]. J Tradit Chin Med, 2013, 54(1): 74-7. |