

2. 山西省中医药大学中药学院,山西 太原 030619
2. College of Traditional Chinese Medicine, Shanxi University of Traditional Chinese Medicine, Taiyuan 030619, China
党参是桔梗科植物Codonopsis pilosula(Franch.) Nannf.川党参Codonopsis tangshen Oliv.和素花党参Codonopsis pilosula Nannf var. modesta(Nannf.)L. T. Shen的干燥根[1]。具补中益气、健脾益肺的作用,是中医常用补气药。作为补益类中药材,党参在机体免疫调节方面的研究广泛而深入。张晓君等[2]发现,党参多糖对体液免疫有较强促进作用。张雅君等[3]的研究也发现,党参粗多糖提取液可促进小鼠脾脏B淋巴细胞的增殖,提高小鼠巨噬细胞的吞噬能力,进而调整机体免疫功能。
历代中医家对党参炮制也较为重视,通过辅料或不同炮制方法让党参的功效也各有不同。如米炒后的党参健脾的作用增强,蜜炙后的党参益气作用增强[4],酒炙和蜜炙可升高党参的多糖含量,米炒、麸炒可使党参多糖含量降低[5]。杨中林等[6]研究党参不同炮制品时发现:在提高小鼠巨噬细胞吞噬能力方面,蜜炙党参优于米炒党参和生党参,初步证明临床补气用传统的蜜炙法炮制品为佳。本文利用代谢组学技术,旨在进一步明确党参不同炮制品对环磷酰胺(cylophosphamide,CTX)所致免疫抑制大鼠的影响,并深入研究其作用机制。
1 材料 1.1 药物与试剂党参饮片(批号:20180104)、米炒党参饮片(批号:20180110)、蜜炙党参饮片(批号:20180101),由山西振东集团提供,均为潞党参及其炮制品。氯化钠注射液(杭州民生药业集团有限公司);CTX(江苏盛迪医药有限公司,批号:18022125);IL-2 ELISA试剂盒、免疫球蛋白G(IgG)ELISA试剂盒、分泌型免疫球蛋白A(sIgA)ELISA试剂盒,均购自美国ADL公司;氘代重水(D2O),购自美国Sigma-aldrich公司。
1.2 仪器KDC-2046高速冷冻离心机(科大创新股份有限公司);HEMAVET 950FS全自动血液分析仪(美国Drew Scientific公司);贝克曼流式细胞仪Cytomics FC 500(COULTER TQ-Prep工作站);Synergy H1酶标仪(BioTek公司);Bruker AVANCE Ⅲ 600超导高分辨核磁共振谱仪(德国Bruker公司)。
1.3 样品制备党参及其各炮制品饮片60 ℃烘干,加8倍水煎煮3次,每次1 h,过滤,滤液浓缩至一定浓度,60 ℃常压烘干,备用。
2 方法 2.1 动物分组及给药50只SPF级SD大鼠,♀♂各半,体质量(180±20)g,购自上海斯莱克实验动物有限责任公司,动物生产许可证号:SCXK(沪)2017-0005。适应性饲养7 d后,随机分为5组,每组10只,♀♂各半,即空白对照组(NS)、模型组(MS)、党参药材(Cp,3.75 g·kg-1生药)、蜜炙党参(HCp,3.75 g·kg-1生药)、米炒党参(RCp,3.75 g·kg-1生药)。各给药组按每只大鼠10 mL·kg-1剂量灌胃相应药物,空白对照组及模型组给予等体积生理盐水;连续14 d,每天1次。给药d 1起,除空白对照组外,各组均腹腔注射CTX(40 mg·kg-1·d-1),连续3 d,同时治疗给药。实验前禁食(不禁水)12 h。最后1 d给药1 h后,腹主动脉取血,一部分血置于抗凝管中;剩余血液置于EP管中,静置1 h左右,3 000 r·min-1、4 ℃离心15 min,取上清液,分装,-20 ℃冰箱保存,备用。摘取十二指肠、空肠和回肠(各约3 cm)置于平皿中,纵行剖开,刮取肠黏膜黏液,收集于同一离心管。内容物与生理盐水按1 :1(W/V)稀释,混匀后,3 000 r·min-1、4 ℃离心15 min,取上清液,-20 ℃冰箱保存备用。
2.2 指标检测部分外周血用动物血球计数仪计数外周血细胞;剩余部分外周血用流式细胞仪检测T细胞亚群CD4+、CD8+表达。采用ELISA法,分别检测血清中IL-2、IgG的含量,ELISA法检测肠道sIgA含量。
2.3 核磁样品制备与测试将400 μL解冻的血清加入311 μL D2O,涡旋30 s,4 ℃、13 000 r·min-1离心20 min,吸取上清液600 μL于5 mm核磁管中进行核磁测试。采用Bruker 600 MHz AVANCE Ⅲ NMR谱仪采集数据,CPMG序列压制水峰,扫描次数为64,谱宽12 345.7 Hz,图谱大小65 536数据点,脉冲宽度(PW)=30°(12.7 us),傅里叶变换LB=0.3 Hz,延迟时间为5.0 s。
2.4 1H NMR图谱处理与分析采用MestReNova核磁图谱处理软件(version 8.0.1)对所有1H NMR图谱进行手动相位和基线调整。所有图谱以肌酸(δ 3.04)为标准进行化学位移、相位与基线校正,对δ 0.60~9.00区域的谱图进行0.01等宽度分割积分,切除水峰δ 4.50~5.00。剩余积分数据归一化后,运用SIMCA-P 13.0(Umetrics,瑞典)软件进行多元统计分析。主成分分析(principal component analysis,PCA)反映的是样本内部固有的差异性和相似性,以显示数据的原始分类状态,进一步进行偏最小二乘判别分析(partial least squares discriminant analysis,PLS-DA)和正交偏最小二乘判别分析(orthogonal PLS-DA,OPLS-DA),用排列实验(permutation tests,200次)来验证PLS-DA的有效性。结合OPLS-DA的VIP值和相应的s-plot图,寻找组间的差异代谢产物。
2.5 统计学分析应用SPSS 13.0统计软件,计量资料以x±s表示,多组间比较采用one-way ANOVA分析。采用GraphPad Prism(version 6.0)软件对差异代谢物进行柱状图分析。
3 结果 3.1 免疫细胞结果Tab 1结果表明,与对照组相比,模型组白细胞总数、B淋巴细胞数及T细胞CD4+/CD8+值明显降低(P < 0.01),说明免疫低下模型复制成功;给药后,党参组(P < 0.01)、蜜炙组(P < 0.01)和米炒组(P < 0.05)均有明显升高,说明3组炮制品均可明显提高机体免疫细胞水平。
| Group | White blood cell count/×109 | Lymphocyte count/×109 | CD4+/CD8+ |
| NS | 8.502±2.229 | 6.549±1.629 | 1.767±0.394 |
| MS | 3.040±1.053** | 1.271±0.431** | 1.239±0.218** |
| RCp | 4.088±0.669# | 1.789±0.502# | 1.522±0.355# |
| HCp | 4.483±1.052## | 2.615±0.846## | 1.575±0.382## |
| Cp | 4.992±0.771## | 2.589±0.562## | 1.611±0.478## |
| **P < 0.01 vs NS; #P < 0.05, ##P < 0.01 vs MS | |||
Tab 2结果显示,与对照组相比,模型组各免疫因子含量明显降低(P < 0.01);给药后,党参组(P < 0.05)、米炒党参组(P < 0.01)、蜜炙党参组(P < 0.01)对IL-2均有明显回调作用;党参组对IgG有升高作用(P < 0.01),米炒党参组和蜜炙党参组则没有变化;对于sIgA,只有蜜炙组对其有回调作用(P < 0.05),米炒组和党参组没有变化。
| Group | IL-2 | IgG | sIgA |
| NS | 0.389±0.046 | 0.139±0.045 | 1.144±0.484 |
| MS | 0.263±0.064** | 0.093±0.007** | 0.873±0.238* |
| Cp | 0.329±0.083# | 0.147±0.095## | 0.617±0.157 |
| RCp | 0.380±0.135## | 0.097±0.032 | 0.848±0.276 |
| HCp | 0.365±0.073## | 0.091±0.024 | 0.924±0.154# |
| *P < 0.05, **P < 0.01 vs NS; #P < 0.05, ##P < 0.01 vs MS | |||
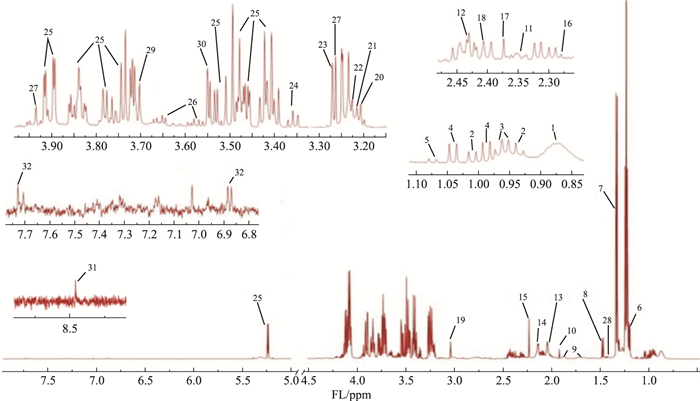
大鼠血清的核磁图谱见Fig 1。根据化学位移、峰形、偶合常数,结合BMRB(Biological Magnetic Resonance Data Bank, http://www.bmrb.wisc.edu/)数据库,以及文献[7-9]中数据对图谱进行指认,在大鼠血清中共指认出32种代谢产物,包含大量的氨基酸、碳水化合物、有机酸等,结果见Tab 3(Fig 1中标号与Tab 3相对应)。
|
| Fig 1 Typical 1H NMR spectrum of serum from rats |
| No. | Metabolites | δH |
| 1 | Lipid fragments | 0.88(m), 1.28(m), |
| 2 | Isoleucine | 0.94(t, J=7.2 Hz), 1.01(d, J=7.2 Hz) |
| 3 | Leucine | 0.96(t, J=6.6 Hz) |
| 4 | Valine | 0.99(d, J=7.2 Hz), 1.04 (d, J=7.2 Hz) |
| 5 | 2-Ketone isovalerate | 1.08(d, J=7.2 Hz), 3.0(m) |
| 6 | 3-Hydroxybutyrate | 1.20(d, J=6.6 Hz) |
| 7 | Lactate | 1.33(d, J=7.2 Hz), 4.12(q, J=7.2 Hz) |
| 8 | Alanine | 1.48(d, J=7.8 Hz) |
| 9 | Lysine | 1.70(m), 1.88(m), 1.56(m) |
| 10 | Acetate | 1.92(s) |
| 11 | Glutamate | 2.05(m), 2.35(m) |
| 12 | Glutamine | 2.15(m), 2.44(m) |
| 13 | N-acetylglycoprotein | 2.05(s) |
| 14 | O-acetylglycoprotein | 2.14(s) |
| 15 | Acetone | 2.23(s) |
| 16 | Acetoacetate | 2.28(s) |
| 17 | Pyruvate | 2.37(s) |
| 18 | Succinate | 2.41(s) |
| 19 | Creatine | 3.04(s), 3.94(s) |
| 20 | Choline | 3.20(s) |
| 21 | PC | 3.21(s) |
| 22 | GPC | 3.22(s) |
| 23 | TMAO | 3.27(s) |
| 24 | Scyllitol | 3.35(t) |
| 25 | Glucose | 3.45(m), 3.74(m), 3.82(m), 3.90(dd, J=1.8, 12 Hz), 5.24(d, J=3.6 Hz) |
| 26 | Glycerol | 3.57(dd, J=4.8, 11.4 Hz), 3.66(dd, J=4.2, 12 Hz) |
| 27 | Betaine | 3.26(s), 3.93(s) |
| 28 | Threonine | 1.31(d, J=6.5 Hz), 4.22(m) |
| 29 | Dimethylglycine | 3.71(s) |
| 30 | Glycine | 3.55(s) |
| 31 | Formate | 8.46(s) |
| 32 | L-tyrosine | 6.87(d, J=8.4 Hz), 7.19(d, J=7.2 Hz) |
| PC: Phosphatidylcholine; GPC: Glycerophosphocholine; TMAO: Trimethylamine oxide; m: multiple peaks; s: single peak; d: double peaks; t: triple peaks; J: coupling constant. | ||
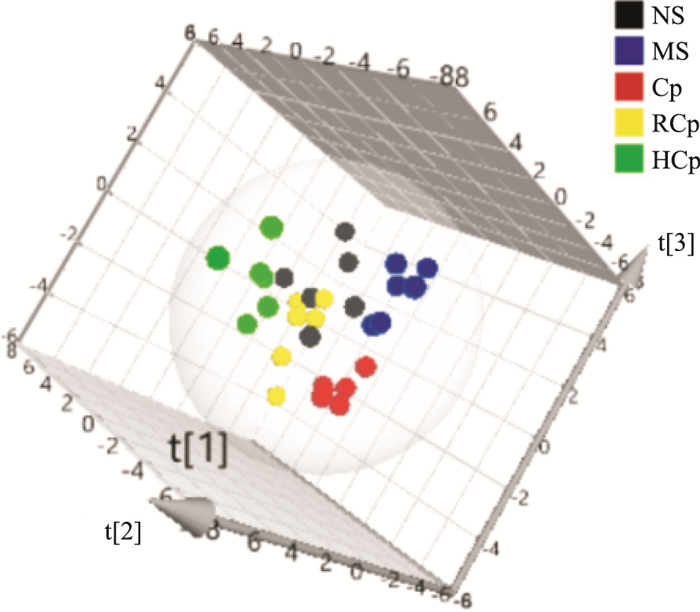
由于NMR图谱反映的信息较多,很难直观地反映出各组之间的差异,因此借助多元统计分析做进一步的分析。采用PCA 3D散点图对所有样本进行分析, 以显示数据的原始分类状态(Fig 2),可以看出对照组与模型组明显分离,表明模型复制成功;党参组在三维空间里更接近于模型组,而蜜炙党参组和米炒组与模型组明显分开,说明蜜炙党参组和米炒组与模型组差异较大;其中蜜炙党参组与模型组相距最远,提示蜜炙党参组具有明显回调作用。
|
| Fig 2 PCA 3D score plot of rat serum among all groups |
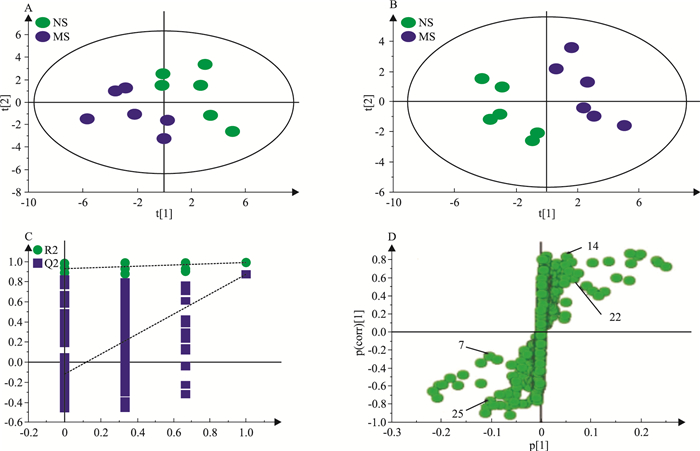
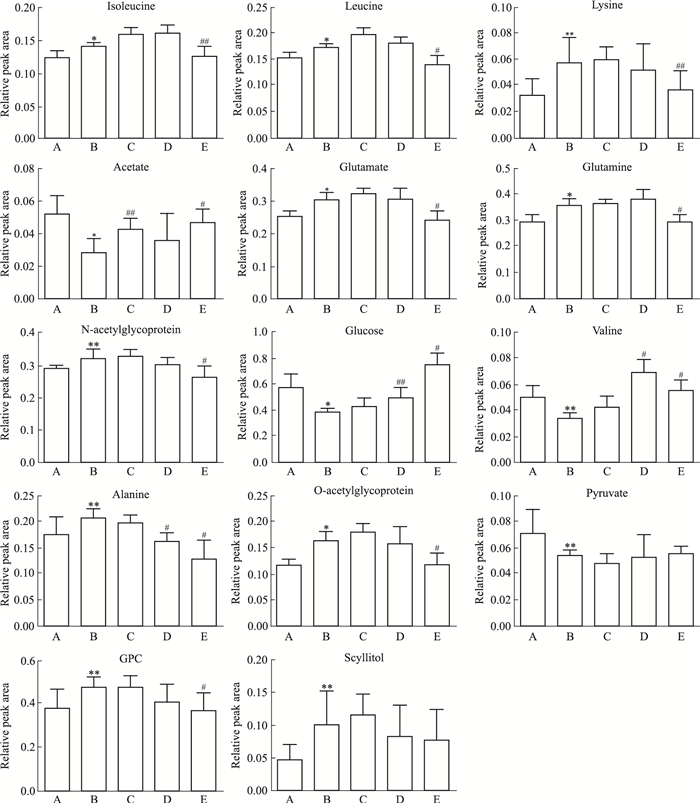
为了进一步分析模型组与空白组之间的差异,首先采用PCA散点图(Fig 3A)观察两组样本的分离趋势,可以看出模型组与空白组明显分离;进一步采用PLS-DA分析(Fig 3B),并在PLS-DA模型成立的基础上,对原始数据建立排列实验,表明随机变量Y变量产生的R2、Q2均小于原始值(Fig 3C,R2=缬氨酸、醋酸、葡萄糖、丙酮酸含量降低;异亮氨酸、亮氨酸、丙氨酸、赖氨酸、谷氨酸、谷氨酰胺、N-乙酰0.995,Q2=0.875),证明模型有效可靠。通过S-plot(Fig 3D)结合VIP值,进行独立样本t检验(P < 0.05)寻找差异代谢物,得到14个具有显著性差异的内源性代谢产物。与空白对照组相比,模型组中糖蛋白、O-乙酰糖蛋白、甘油磷酰胆碱(GPC)、鲨肌醇含量升高。所有差异代谢物在各组中的含量分布见Fig 4,结果表明,蜜炙党参组基本对所有差异代谢物均有明显回调作用,党参组和米炒党参组对个别代谢物有明显回调作用。
|
| Fig 3 PCA score plot(A), PLS-DA score plot(B), corresponding validation(C), and S-plot(D) from serum of rat between control and model groups |
|
| Fig 4 Comparison of relative peak areas of potential biomarkers from 1H NMR spectra of serum(x±s, n=6) A:NS; B:MS; C:Cp; D:RCp; E:HCp.*P < 0.05, **P < 0.01 vs NS group; #P < 0.05, ##P < 0.01 vs MS group. |
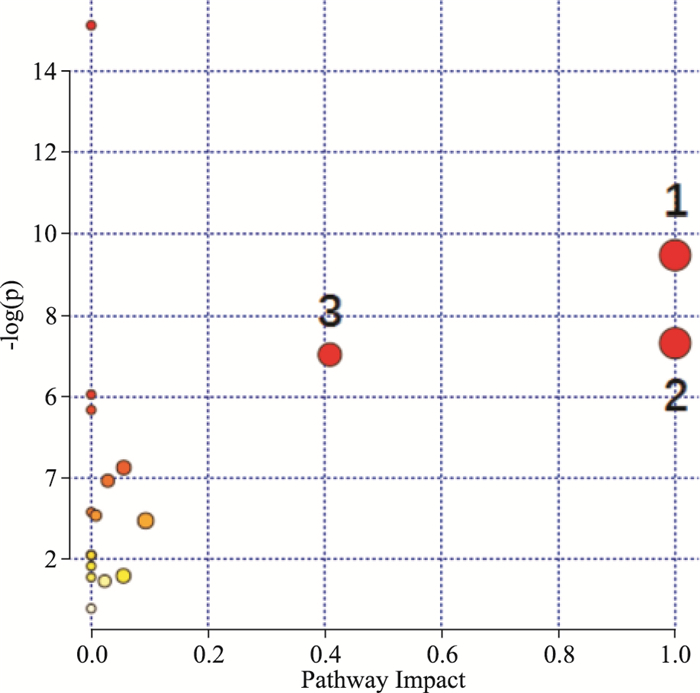
将找到的差异代谢物输入www.metaboanalyst.cn进行Met PA分析,将Pathway Impact>0.1的代谢途径列为最重要的代谢途径,得到与免疫低下模型相关的代谢通路如Fig 5所示。
|
| Fig 5 MetPA analysis of metabolic pathway 1:Valine, leucine, isoleucine metabolism; 2: Glutamate, glutamine metabolism; 3: Alanine, asparticacid, glutamicate metabolism. |
白细胞是体内防御系统的重要组成部分,其数量的减少代表着机体免疫功能低下[10]。B淋巴细胞是体液和细胞免疫的重要组成部分,能够通过多种调控方式发挥正向免疫调节作用。T细胞在免疫应答过程中发挥中枢的作用,CD4+ T细胞具有辅助细胞免疫和体液免疫应答的作用,CD8+ T细胞则是重要的效应细胞,两者的比值可以反映机体免疫功能水平。给药后,党参组及各炮制品组均可明显升高模型大鼠白细胞、B淋巴细胞及T细胞CD4+/CD8+值水平。与米炒党参相比,党参组和蜜炙党参组在改善CTX引起的白细胞及淋巴细胞数减少方面效果更好。各给药组在提高T细胞CD4+/CD8+值方面效果相当。
4.2 免疫因子结果分析sIgA是构成肠道黏膜免疫的重要组成成分,也是维持其稳态的第一道防线。IL-2是重要的免疫调控因子,可直接增强T细胞介导的细胞免疫功能,能促进T细胞生长、增殖、分化及抗体形成[11]等。IL-2也可直接活化B细胞,使其生长并刺激抗体产生,故也是一种B细胞生长因子,促进B细胞介导的体液免疫[12]。IgG是免疫系统重要的组成部分,其含量一定程度上反映了机体免疫功能的强弱。给药后,党参可明显提高IL-2、IgG水平;蜜炙党参明显改善免疫抑制引起的IL-2、sIgG含量降低;米炒党参升高模型大鼠IgG水平明显。
4.3 代谢通路分析亮氨酸、异亮氨酸,是蛋白质和葡萄糖代谢的调节器[13],也是维持淋巴细胞敏感性与免疫细胞功能所必需的功能物质。缬氨酸属生糖氨基酸,可促进糖异生,还能通过影响免疫球蛋白的合成来影响免疫功能[14]。本实验中,米炒组、蜜炙组缬氨酸含量升高,说明给予其可促进机体葡萄糖的生成,产生更多能量,同时合成免疫球蛋白,提高机体免疫力;蜜炙党参组亮氨酸、异亮氨酸含量降低,说明蜜炙组促进其代谢,维持机体各免疫细胞的功能,从而增强机体免疫力。
谷氨酸、谷氨酰胺是淋巴细胞和中性粒细胞等快速分裂的主要能源物质,在其代谢过程中起氮的载体和供体作用,可间接提高白细胞与淋巴细胞的增殖,改善机体免疫作用[15]。给药后,谷氨酸、谷氨酰胺含量降低,推测谷氨酸、谷氨酰胺不断快速代谢,从而加速淋巴细胞增殖,提高机体免疫力,这一变化与免疫细胞结果相一致。
丙氨酸和谷氨酸是体内重要氨基酸,通过氨基转移酶在体内相互转化。丙氨酸是肝脏合成葡萄糖的主要底物,影响白细胞的合成,进而影响机体免疫功能。有研究表明,在B淋巴细胞杂交瘤中添加2 mmol·L-1的丙氨酸可以防止细胞凋亡、促进细胞生长以及刺激抗体的产生[16]。模型组大鼠血清丙氨酸及谷氨酸含量升高,表明CTX引起机体丙氨酸和谷氨酸的蓄积,利用率明显降低,从而造成免疫抑制。党参各炮制品治疗后,丙氨酸和谷氨酸水平均有向对照组回调的趋势,其中以蜜炙党参组效果最明显,表明党参可以促进丙氨酸和谷氨酸的代谢,从而修复机体免疫功能缺陷。
葡萄糖、丙酮酸是糖代谢中重要能源物质,机体进行有氧代谢时,葡萄糖生成丙酮酸后,进入三羧酸循环,保证机体正常供能。本实验中,蜜炙党参组葡萄糖和丙酮酸含量高于模型组,说明免疫低下模型大鼠的糖代谢以无氧代谢为主,而党参组以有氧代谢为主,从而提高机体供能水平。
GPC参与细胞膜对蛋白质的识别和信号转导,可调节细胞膜的流动性,属脂质代谢的中间体。本实验中,蜜炙党参组GPC含量降低,说明蜜炙党参可以改善CTX诱导的细胞膜的损伤,维持免疫细胞的结构和功能。
乙酰糖蛋白作为炎症反应的急性期反应蛋白[17],在机体受到刺激发生炎症反应后含量升高[18]。本研究中,蜜炙党参组O-乙酰糖蛋白、N-乙酰糖蛋白含量低于模型组,表明CTX诱导免疫低下大鼠的炎症反应发生,蜜炙党参可促使机体免疫反应恢复,免疫力趋于正常。
本研究基于1H NMR代谢组学技术,对比了党参及其不同炮制品(米炒党参、蜜炙党参)对免疫抑制大鼠的影响。结果表明,对于CTX所致的免疫低下大鼠,蜜炙党参改善效果优于党参和米炒党参,表现在明显提高大鼠血清中白细胞、淋巴细胞及CD4+/CD8+值、IL-2、sIgA的含量,明显回调血清中12个内源性代谢物的水平,主要通过缬氨酸、亮氨酸、异亮氨酸代谢,谷氨酸、谷氨酰胺代谢以及丙氨酸、天冬氨酸、谷氨酸代谢3条通路,以及其他物质(如葡萄糖、丙酮酸、GPC以及乙酰糖蛋白)的代谢来发挥免疫作用。该研究结果为党参药效物质基础研究及其不同炮制品的临床精准化使用提供了理论依据。
| [1] |
中国药典委员会[S].中华人民共和国药典. 2015年版一部.北京: 中国医学科学出版社, 2015: 281-2. Chinese Pharmacopoeia Commission. Pharmacopoeia of the People's Republic of China[S]. 2015 ed. Part 1. Beijing: China Medical Science Press, 2015: 281-2. |
| [2] |
张晓君, 祝晨蔯, 胡黎, 等. 党参多糖对小鼠免疫和造血功能的影响[J]. 中药新药与临床药理, 2003, 14(3): 174-6. Zhang X J, Zhu C C, Hu L, et al. Effects of Codonopsis pilosula polysaccharides on immunity and hematopoietic function in mice[J]. Tradit Chin Drug Res Pharmacol, 2003, 14(3): 174-6. doi:10.3321/j.issn:1003-9783.2003.03.012 |
| [3] |
张雅君, 梁忠岩, 张丽霞. 党参粗多糖的组成及其免疫活性研究[J]. 西北农林科技大学学报(自然科学版), 2012, 40(7): 199-202, 208. Zhang Y J, Liang Z Y, Zhang L X. Composition and immunological activity of crude polysaccharide from Dang Shen[J]. J Nort A&F Univ(Natur Sci), 2012, 40(7): 199-202, 208. |
| [4] |
吴尚英, 范圣此, 关扎根, 琚斌峰. 影响党参药材品质的因素分析[J]. 安徽农业科学, 2011, 39(30): 18528-30. Wu S Y, Fan S C, Guan Z G, Ju B F. Anaiysis of factors influencing the quality of Dang Shen medicinal materials[J]. J Anhui Agric Sci, 2011, 39(30): 18528-30. doi:10.3969/j.issn.0517-6611.2011.30.056 |
| [5] |
邹利, 邱炳勋, 刘珂, 等. 党参米炒前后党参多糖与5-羟甲基糠醛的变化及其对胃肠平滑肌运动的影响[J]. 中草药, 2017, 48(1): 149-54. Zhou L, Qiu B X, Liu K, et al. Changes of 5-hydroxymethyl furfural of Codonopsis pilosula polysaccharides before and after stir-frying and its effect on gastrointestinal smooth muscle movement[J]. Chin Tradit Herb Drug, 2017, 48(1): 149-54. |
| [6] |
杨中林, 刘海臣, 林蔚. 党参的炮制研究[J]. 中药材, 1990, 23(4): 25-6. Yang Z L, Liu H C, Lin W. Study on processing of Codonopsis pilosula[J]. Chin Med Mat, 1990, 23(4): 25-6. |
| [7] |
斯皮热古丽·阿布都卡地, 阿里木·帕塔尔, 古孜力克孜·阿布都克热木. 基于NMR的免疫抑制小鼠模型血清代谢组学研究[J]. 中国药理学通报, 2016, 32(6): 853-7. Sipireguli·Abudoukadi, Alimu·Pataer, Guzilikezi·Abudoukeremu. Metabolic analysis of immune suppression mice based on NMR[J]. Chin Pharmacol Bull, 2016, 32(6): 853-7. doi:10.3969/j.issn.1001-1978.2016.06.022 |
| [8] |
刘成鹏, 殷晓芹, 李玉琴, 等. 基于核磁共振的益母草碱抗急性心肌缺血的代谢组学研究[J]. 中国药理学通报, 2017, 33(9): 1235-42. Liu C P, Yin X Q, Li Y Q, et al. 1H NMR-based metabolomics study of intervention effects of leonurine on acute myocardial ischemia in rats[J]. Chin Pharmacol Bull, 2017, 33(9): 1235-42. doi:10.3969/j.issn.1001-1978.2017.09.011 |
| [9] |
龚梦鹃, 巫圣乾, 岳贺, 等. 基于1H-NMR护肝片抗大鼠急性肝损伤的代谢组学研究[J]. 中国药理学通报, 2017, 33(12): 1766-70. Gong M J, Wu S Q, Yue H, et al. Metabonomic analysis of Hugan Tablets on CCl4-induced acute hepatic injury in rats based on 1H-NMR[J]. Chin Pharmacol Bull, 2017, 33(12): 1766-70. doi:10.3969/j.issn.1001-1978.2017.12.027 |
| [10] |
Lämmermann T, Germain R N. The multiple faces of leukocyte interstitial migration[J]. Semin Immunopathol, 2014, 36(2): 227-51. doi:10.1007/s00281-014-0418-8 |
| [11] |
Cho J H, Boyman O, Kim H O, et al. An intense form of homeostatic proliferation of naive CD8+ cells driven by IL-2[J]. J Exp Med, 2007, 204(8): 1787-801. doi:10.1084/jem.20070740 |
| [12] |
罗治彬. 肠道黏膜SIgA免疫系统的研究进展[J]. 细胞与分子免疫学杂志, 1997, 13(S2): 40-3. Luo Z B. Progress of sIgA immune system in intestinal mucosa[J]. J Cell Mol Immunol, 1997, 13(S2): 40-3. |
| [13] |
Les I, Doval E, García-Martínez R. Effects of branched-chain amino acids supplementation in patients with cirrhosis and a previous episode of hepatic encephalopathy: a randomized study[J]. Am J Gastroenterol, 2011, 106(6): 1081-8. doi:10.1038/ajg.2011.9 |
| [14] |
Zhao L, Li Y, Li Z, et al. Effect of the valine-to-lysine ratio on the performance of sows and piglets in a hot, humid environment[J]. J Therm Biol, 2019, 81: 89-97. doi:10.1016/j.jtherbio.2019.02.021 |
| [15] |
毕晓林, 何伟东. 谷氨酰胺对病毒性脑炎小鼠免疫功能的影响[J]. 南京医科大学学报(自然科学版), 2007(9): 1029-30. BI X L, HE W D. Effects of glutamine on immune function in mice with viral encephalitis[J]. Acta Acad Med Nanjing(Natur Sci), 2007(9): 1029-30. |
| [16] |
Duval D, Demangel C, Munier-Jolain K, et al. Factors controlling cell proliferation and antibody production in mouse hybridoma cells: Ⅰ. Influence of the amino acid supply[J]. Biotechnol Bioeng, 1991, 38(6): 561-70. doi:10.1002/bit.260380602 |
| [17] |
Deja S, Porebska I, Kowal A, et al. Metabolomics provide new insights on lung cancer staging and discrimination from chronic obstructive pulmonary disease[J]. J Pharm Biomed Anal, 2014, 100: 369-80. doi:10.1016/j.jpba.2014.08.020 |
| [18] |
de Graaff D R, Felz S, Neu T R, et al. Sialic acids in the extracellular polymeric substances of seawater-adapted aerobic granular sludge[J]. Water Res, 2019, 155: 343-51. doi:10.1016/j.watres.2019.02.040 |

