


2. 湖北科技学院药学院,湖北 咸宁 437100;
3. 贵州医科大学公共卫生学院,贵州 贵阳 550025
2. School of Pharmacy, Hubei University of Science and Technology, Xianning, Hubei 437100, China;
3. School of Public Health, Guizhou Medical University, Guiyang 550025, China
神经母细胞瘤是小儿最常见的颅外恶性实体肿瘤,据统计,约40%进展期神经母细胞瘤有MYCN扩增[1]。MYCN扩增神经母细胞瘤恶性程度高,对常规化疗药物高度耐药,常因多重治疗出现严重毒性反应[2]。因此,寻找新的治疗方法提高治愈率,减少毒性反应意义重大。二甲双胍(metformin)是治疗2型糖尿病的一线口服药物。体外研究显示,二甲双胍可抑制多种癌细胞的生长,包括乳腺癌、结肠癌、前列腺癌、卵巢癌、胶质瘤等[3-4]。但是二甲双胍在调节细胞代谢时,诱导乳酸堆积,引起肿瘤周围微环境酸化,从而降低二甲双胍的抗癌效应[5]。若能有效克服该副作用,无疑有助于增强二甲双胍的抗癌效果。近年来研究发现,用于治疗人类遗传性线粒体代谢疾病和乳酸酸中毒的廉价药二氯乙酸盐(dichloroacetate,DCA)可杀死多种癌细胞,如卵巢癌、脑癌细胞等,但对正常细胞无损害,并可改善肿瘤细胞对多种化疗药物的获得性耐药[6-7]。有文献报道,DCA可减少乳酸堆积,破坏肿瘤细胞赖以生存的微环境,抑制肿瘤细胞的生存[8]。因此推测,二甲双胍和DCA对MYCN扩增神经母细胞瘤可能具有协同抑制作用。本文旨在研究二甲双胍和DCA对MYCN扩增神经母细胞瘤细胞增殖的影响,并探讨其机制,为MYCN扩增神经母细胞瘤的治疗提供实验依据。
1 材料与方法 1.1 材料 1.1.1 细胞株MYCN扩增神经母细胞瘤细胞株BE-2C细胞,购自中科院上海生命科学研究院细胞资源中心。
1.1.2 药物与试剂二甲双胍盐酸盐、DCA,均购自Sigma公司(使用前均用培养基配制成所需浓度);RPMI 1640培养基,购自美国Hyclone公司;胎牛血清、胰酶、青霉素、链霉素,均购自美国Gibco公司;CCK-8试剂盒、细胞凋亡检测试剂盒,购自于碧云天生物技术有限公司;葡萄糖测试盒、乳酸测定试剂盒,均购自南京建成生物工程研究所;一抗Bax、Bcl-2,p-Akt、Akt、p-S6K、S6K、cleaved caspase-3及β-actin,均购自于美国Cell Signaling公司;ECL发光液,购自美国Thermo公司。
1.1.3 仪器细胞培养箱、生物安全柜(Thermo公司);倒置显微镜(德国徕卡公司);多功能酶标仪(美国Bio-Tek公司);流式细胞仪(美国BD公司);化学发光成像系统(美国Bio-Rad公司);超净工作台(苏州净化设备厂)。
1.2 方法 1.2.1 细胞培养BE-2C细胞常规培养于37 ℃、5%二氧化碳,含10%胎牛血清、100 kU·L-1青霉素和100 kU·L-1链霉素的RPMI 1640培养基中,0.25%胰酶消化传代。
1.2.2 CCK-8法检测细胞增殖活性与联合指数的计算取对数生长期的BE-2C细胞,用0.25%胰酶消化成单细胞悬液,按每孔8 000个细胞接种于96孔板中,培养24 h后分组进行处理,分为空白对照组、二甲双胍单独用药组(1.25、2.5、5、10、20 mmol·L-1)、DCA单独用药组(2.5、5、10、20、40、80 mmol·L-1)、二甲双胍与DCA联合用药组(摩尔比1 :2),以1.25、2.5、5、10、20 mmol·L-1的浓度为基准,以上每组设置5个复孔。药物作用24 h后,每孔加入10 μL的CCK-8溶液,37 ℃避光孵育30 min后,用酶标仪在450 nm处测量96孔板的吸光度值(OD值),计算细胞生长抑制率:细胞生长抑制率/%=[1-(实验组OD值-调零组OD值)/(空白对照组OD值-调零组OD值)]×100%。使用Graph Pad Prism5.0软件计算药物半数抑制质量浓度IC50,同时应用CalcuSyn1软件,计算两药联用的联合指数(combination index,CI),判断两药联用效果。
1.2.3 培养基中葡萄糖含量和乳酸生成量的测定取对数生长期的BE-2C细胞,以2×105每孔的密度接种于6孔板中。细胞贴壁生长24 h后,更换含药物的培养基。以培养基为对照组,以单用二甲双胍10 mmol·L-1、DCA 20 mmol·L-1及其联用组为实验组。药物作用24 h后,收集培养基上清于EP管中,采用葡萄糖测试盒和乳酸测定试剂盒,检测培养基中葡萄糖含量和乳酸生成量。
1.2.4 流式细胞技术检测细胞凋亡取对数生长期的BE-2C细胞,以2×105每孔的密度接种于T25细胞培养瓶中,待细胞贴壁生长24 h后,更换含药物的培养基。以培养基为阴性对照组,单用二甲双胍10 mmol·L-1、DCA 20 mmol·L-1及其联用组为实验组。药物作用24 h后,用不含EDTA的胰酶消化细胞,接着用预冷的PBS洗1次,再加入binding buffer 0.5 mL轻柔吹打混匀,吸取细胞至流式管,避光加入5 μL PI与5 μL Annexin-V FITC溶液孵育5 min,此外需设置空白管,于1 h内用流式细胞仪检测细胞凋亡情况。
1.2.5 Western blot检测凋亡相关蛋白Bax、Bcl-2,cleaved caspase-3的表达取对数生长期的BE-2C细胞,以2×105每孔的密度接种于6孔板中。待细胞贴壁生长24 h后,更换含药物的培养基。以生理盐水为阴性对照组,单用二甲双胍10 mmol·L-1、DCA 20 mmol·L-1及其联用组为实验组。药物作用24 h后,于冰上裂解收集蛋白,采用BCA检测蛋白含量,取40 μg蛋白上样,进行SDS-PAGE电泳,用湿转法将蛋白转至PVDF膜,5%脱脂牛奶室温封闭1 h,4 ℃孵育一抗过夜,洗膜,室温孵育二抗1 h,洗膜,ECL发光液显影,通过ImageJ软件分析各样品目的蛋白的灰度值,用β-actin作为内参。
1.2.6 统计学处理数据以x±s表示,应用SPSS 18.0软件进行统计学分析,多组间比较用方差分析,两组间比较采用t检验。
2 结果 2.1 二甲双胍与DCA联用对BE-2C细胞增殖的抑制具有协同作用不同浓度的二甲双胍或DCA处理BE-2C细胞24 h,采用CCK-8法检测其细胞毒性。结果显示,二甲双胍或DCA对BE-2C细胞的抑制率随浓度的增加而增高,具有浓度依赖性(Fig 1A、1B)。通过Graph Pad Prism5.0软件,计算二甲双胍的IC50值为(23.1±0.1)mmol·L-1,DCA的IC50值为(46.1±0.1)mmol·L-1,确定二甲双胍与DCA联用的摩尔比为1 :2。继而通过CCK-8法,测定药物联用对细胞毒性的大小,并采用CalcuSyn1软件计算两药联用的CI。结果显示,两药联用在不同效应(即联用时细胞生长抑制率)时的CI均小于1,表明二甲双胍和DCA联用呈现协同效应(Fig 1C)。倒置显微镜下观察到单独应用二甲双胍或DCA组的细胞数量减少,但未见明显的脱落细胞,而联用组细胞数量明显减少,细胞皱缩明显,并可见大量漂浮的死亡细胞(Fig 1D)。
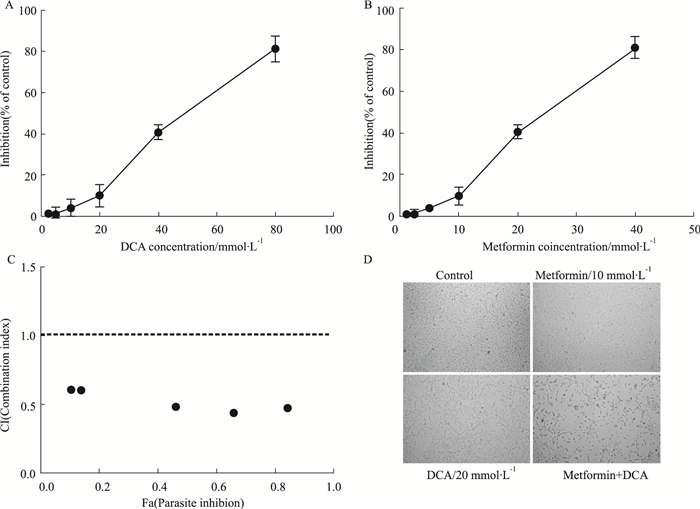
|
| Fig 1 Synergistic inhibition of proliferation of BE-2C cells by metformin plus DCA (x±s, n=5) A: Metformin inhibited the viability of BE-2C cells in a dose-dependent manner; B: DCA showed a dose-dependent cytotoxicity in BE-2C cells; C: Combination index (CI) values of combined effect of metformin and DCA on BE-2C cells; D: The effects of metformin and DCA combination on morphology of BE-2C cells (×400). |
分别单独或联合应用10 mmol·L-1的二甲双胍或20 mmol·L-1的DCA处理BE-2C细胞24 h,检测培养基中葡萄糖和乳酸的含量。Fig 2结果显示,与对照组相比,二甲双胍组的葡萄糖消耗和乳酸的产生量明显增加(P < 0.05),而DCA组的葡萄糖消耗和乳酸的产生量明显减少(P < 0.01);与二甲双胍组相比,两药联用组的葡萄糖消耗和乳酸的产生量明显减少(P < 0.05),表明DCA可减少二甲双胍引起的乳酸的堆积。

|
| Fig 2 Effects of metformin and/or DCA on glucose uptake and lactic acid production in BE-2C cells(x±s, n=5) *P < 0.05, **P < 0.01 vs control group; #P < 0.05, ##P < 0.01 vs metformin group |
为了证实二甲双胍与DCA联用产生协同作用与凋亡相关,采用流式细胞术检测二甲双胍和DCA单独或联合应用所引起的细胞凋亡变化。Fig 3结果表明,与对照组相比,二甲双胍或DCA单独用药组细胞凋亡比例明显增高(P < 0.05);与二甲双胍或DCA单独用药组相比,两药联用组细胞凋亡比例明显增高(P < 0.05),提示二甲双胍与DCA联用可诱导BE-2C细胞凋亡增加。
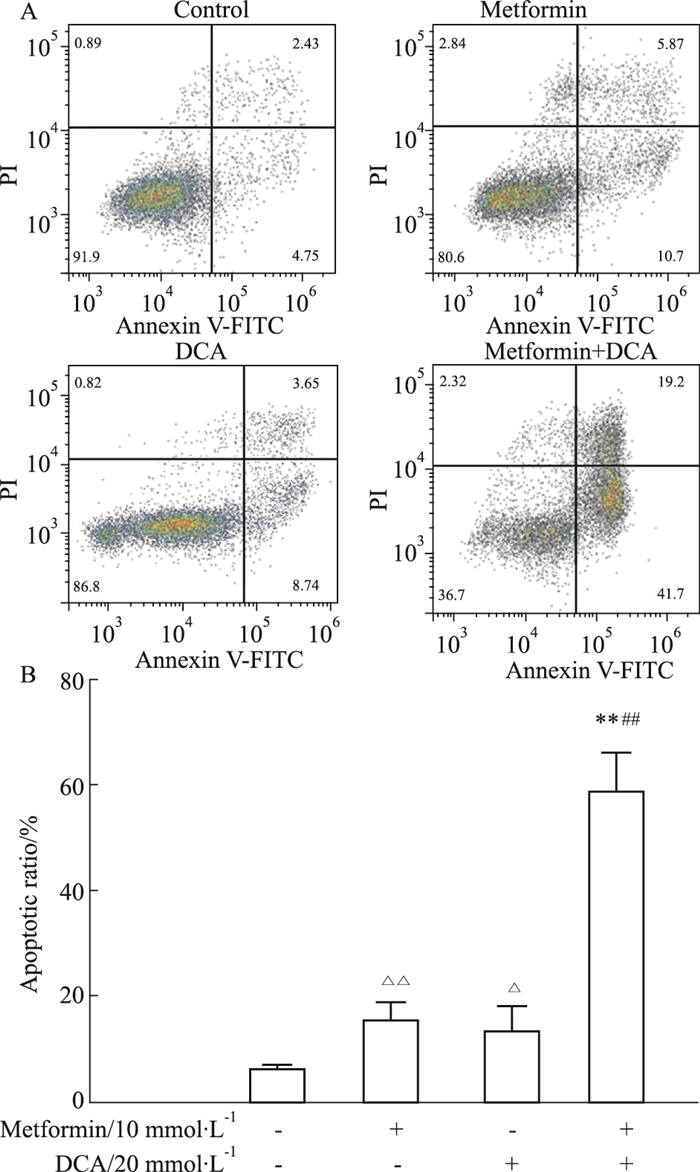
|
| Fig 3 Effects of metformin and/or DCA on apoptosis of BE-2C cells(x±s, n=3) A: Representative PI-Annexin V staining plots of BE-2C cells treated with control or 10 mmol·L-1 metformin and/or 20 mmol·L-1DCA; B: Apoptotic rate detected by Annexin V-FITC /PI flow cytometry. △P < 0.05, △△P < 0.01 vs control group; **P < 0.01 vs metformin group; ##P < 0.01 vs DCA group. |
为了进一步研究两药联用诱导细胞凋亡是否与凋亡相关蛋白表达增加有关,采用Western blot检测二甲双胍与DCA单用及联用对细胞凋亡相关蛋白表达的影响。如Fig 4所示,与对照组相比,二甲双胍与DCA单用组细胞的Bax、cleaved caspase-3蛋白表达水平均升高,而Bcl-2蛋白表达水平下降(P < 0.05);与二甲双胍或DCA单独用药组相比,联用组细胞的Bax、cleaved caspase-3蛋白表达水平均较单用组增加,而Bcl-2蛋白表达水平均较单用组明显降低(P < 0.01)。表明二甲双胍与DCA联用诱导BE-2C细胞凋亡增加,可能与下调Bcl-2蛋白表达、上调Bax蛋白表达、增强caspase-3活性有关。
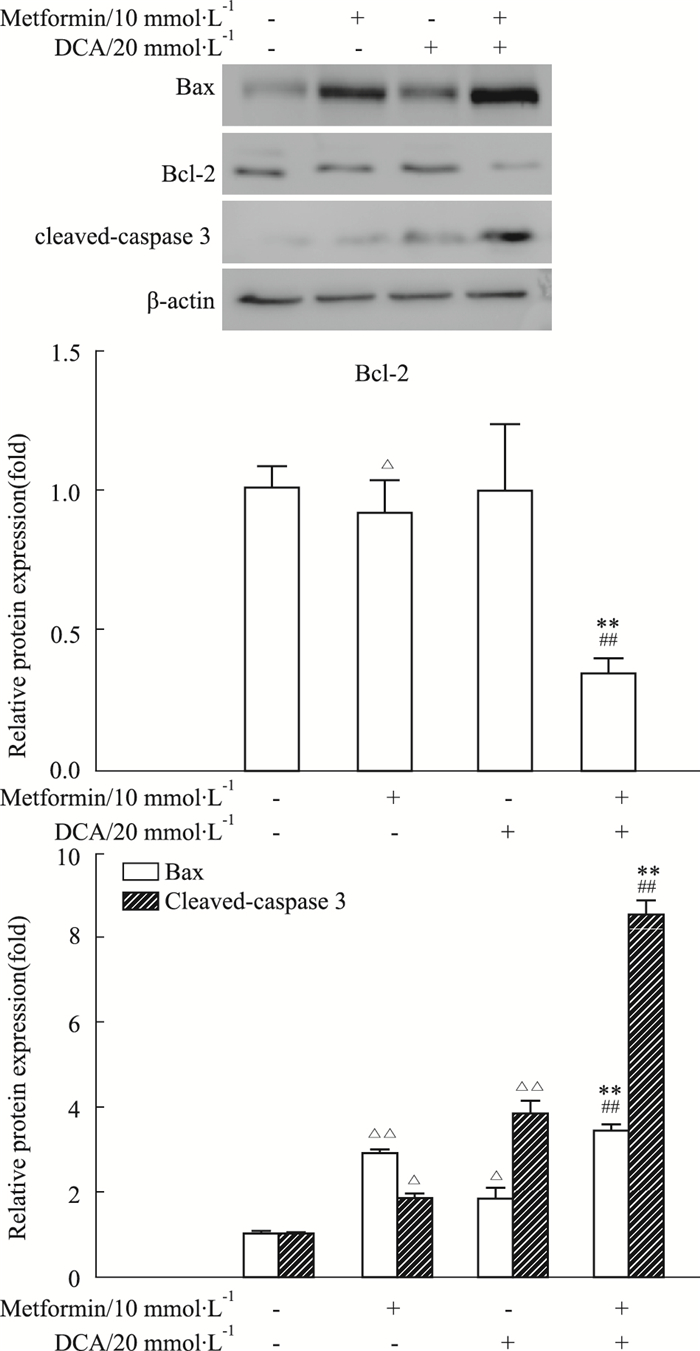
|
| Fig 4 Effects of metformin and/or DCA on protein levels of apoptosis-related proteins in BE-2C cells(x±s, n=3) △P < 0.05, △△P < 0.01 vs control group; **P < 0.01 vs metformin group; ##P < 0.01 vs DCA group |
近年来研究发现,肿瘤是一种代谢异常性疾病[9]。肿瘤细胞由于线粒体呼吸链出现不可逆损伤,造成其在正常氧浓度条件下仍然倾向于糖酵解,这种现象称为Warburg效应[10]。由于肿瘤细胞对糖酵解的依赖和高水平的葡萄糖摄取利用率,因此,抑制糖酵解和葡萄糖代谢可成为肿瘤治疗的潜在目标。在诸多通过调节代谢而抗肿瘤的药物中,DCA与二甲双胍显示出良好的抗肿瘤前景。
本研究结果显示,二甲双胍和DCA单独应用可明显抑制MYCN扩增神经母细胞瘤BE-2C细胞的生长,具有浓度依赖性,其IC50值分别为23.1 mmol·L-1和46.1 mmol·L-1,这些发现与先前报道的二甲双胍与DCA降低神经母细胞瘤细胞的生长和存活的结果一致[11-12]。而当二甲双胍与DCA以1 :2摩尔比联用时,其联用指数均小于1,显微镜下观察,联用后其细胞数量明显减少,有大量漂浮的死亡细胞,表明两药联用具有协同作用。
但是二甲双胍可抑制细胞内线粒体电子传递链复合物I,进而抑制葡萄糖代谢,造成肿瘤细胞的糖剥夺,诱导了乳酸堆积,引起肿瘤周围微环境酸化,从而降低二甲双胍的抗癌效应[5]。我们在研究两药对葡萄糖的消耗和糖酵解代谢产物乳酸生成能力的影响中发现,DCA可明显减少二甲双胍促进葡萄糖的消耗而导致乳酸堆积的副作用,这表明二甲双胍与DCA协同抑瘤作用可能与DCA抑制糖酵解有关。
细胞凋亡在生物体的进化、内环境的稳定以及多个系统的发育中起着重要作用,肿瘤细胞会逃避凋亡,这与肿瘤的发展形成及耐药性有着密不可分的关系。目前已发现,二甲双胍可激活AMP激活的蛋白激酶(AMP-activated protein kinase,AMPK),进而抑制mTORC1信号转导,促进癌细胞凋亡[13]。DCA可增强有氧氧化作用,释放大量活性氧簇,造成线粒体膜去极化,激活Kv通道等[14],从而逆转肿瘤细胞中线粒体的功能紊乱,激活线粒体依赖的细胞凋亡,杀伤肿瘤细胞。我们检测两药联用后其凋亡的变化,结果显示,二甲双胍与DCA均可诱导BE-2C细胞发生凋亡,且联用后细胞凋亡明显增加,与单用组相比,差异有统计学意义。凋亡是多基因严格控制的过程,如Bcl-2家族、caspase家族、癌基因如c-Myc、抑癌基因p53等。Bcl-2家族成员可分为两类,一类为细胞凋亡的抑制基因,主要有Bcl-2、Bcl-xL、Bcl-W等,在caspase级联放大与线粒体之间扮演着“桥梁”的作用;另一类是促进细胞死亡,主要包括Bax、Bak、Bid等,可调节凋亡进程,释放细胞色素C,启动caspase级联反应,最终导致凋亡的发生[15]。本研究结果显示,二甲双胍与DCA联用可明显抑制Bcl-2的表达,上调Bax的表达,说明两药联用可能通过改变Bcl-2与Bax的比例,增加了细胞凋亡。有活性的caspase-3是细胞凋亡过程中最主要的终末剪切酶,把DNA降解为特异片段,从而诱导凋亡的发生[15]。本实验结果显示,二甲双胍与DCA联用可增加cleaved caspase-3的表达,这些结果说明二甲双胍与DCA联用发生的协同机制可能是通过上调Bax、cleaved caspase-3蛋白表达,下调Bcl-2蛋白表达,从而诱导细胞凋亡的发生。
综上所述,二甲双胍与DCA联用产生协同作用可能与DCA抑制糖酵解,减弱二甲双胍诱导的乳酸产生,增强二甲双胍的抗癌效应,也可能与调节凋亡相关蛋白表达,提高细胞凋亡率有关。本研究为二甲双胍与DCA联用治疗MYCN扩增神经母细胞瘤提供了良好的实验依据。
( 致谢: 本实验在湖北科技学院任平教授实验室完成,谨此致谢。)
| [1] |
Maris J M. Recent advances in neuroblastoma[J]. N Engl J Med, 2010, 362(23): 2202-11. doi:10.1056/NEJMra0804577 |
| [2] |
Huang M, Weiss W A. Neuroblastoma and MYCN[J]. Cold Spring Harb Perspect Med, 2013, 3(10): a014415. |
| [3] |
Zakikhani M, Dowling R, Fantus I G, et al. Metformin is an AMP kinase-dependent growth inhibitor for breast cancer cells[J]. Cancer Res, 2006, 66(21): 10269-73. doi:10.1158/0008-5472.CAN-06-1500 |
| [4] |
Isakovic A, Harhaji L, Stevanovic D, et al. Dual antiglioma action of metformin: cell cycle arrest and mitochondria-dependent apoptosis[J]. Cell Mol Life Sci, 2007, 64(10): 1290-302. doi:10.1007/s00018-007-7080-4 |
| [5] |
Ben Sahra I, Laurent K, Loubat A, et al. The antidiabetic drug metformin exerts an antitumoral effect in vitro and in vivo through a decrease of cyclin D1 level[J]. Oncogene, 2008, 27(25): 3576-86. doi:10.1038/sj.onc.1211024 |
| [6] |
Saed G M, Fletcher N M, Jang Z L, et al. Dichloroacetate induces apoptosis of epithelial ovarian cancer cells through a mechanism involving modulation of oxidative stress[J]. Reprod Sci, 2011, 18(12): 1253-61. doi:10.1177/1933719111411731 |
| [7] |
Michelakis E D, Sutendra G, Dromparis P, et al. Metabolic modulation of glioblastoma with dichloroacetate[J]. Sci Transl Med, 2010, 2(31): 31ra34. |
| [8] |
Ohashi T, Akazawa T, Aoki M, et al. Dichloroacetate improves immune dysfunction caused by tumor-secreted lactic acid and increases antitumor immunoreactivity[J]. Int J Cancer, 2013, 133(5): 1107-18. doi:10.1002/ijc.28114 |
| [9] |
DeBerardinis R J, Lum J J, Hatzivassiliou G, et al. The biology of cancer: metabolic reprogramming fuels cell growth and proliferation[J]. Cell Metab, 2008, 7(1): 11-20. doi:10.1016/j.cmet.2007.10.002 |
| [10] |
Hanahan D, Weinberg R A. Hallmarks of cancer: the next generation[J]. Cell, 2011, 144(5): 646-74. doi:10.1016/j.cell.2011.02.013 |
| [11] |
Costa D, Gigoni A, Würth R, et al. Metformin inhibition of neuroblastoma cell proliferation is differently modulated by cell differentiation induced by retinoic acid or overexpression of NDM29 non-coding RNA[J]. Cancer Cell Int, 2014, 14: 59. doi:10.1186/1475-2867-14-59 |
| [12] |
Niewisch M R, Kuçi Z, Bruchelt G, et al. Influence of dichloroacetate (DCA) on lactate production and oxygen consumption in neuroblastoma cells: is DCA a suitable drug for neuroblastoma therapy?[J]. Cell Physiol Biochem, 2012, 29(3-4): 373-80. doi:10.1159/000338492 |
| [13] |
Sarbassov D D, Ali S M, Sabatini D M. Growing roles for the mTOR pathway[J]. Curr Opin Cell Biol, 2005, 17(6): 596-603. doi:10.1016/j.ceb.2005.09.009 |
| [14] |
Zhuang Y, Miskimins W K. Cell cycle arrest in metformin treated breast cancer cells involves activation of AMPK, downregulation of cyclin D1, and requires p27Kip1 or p21Cip1[J]. J Mol Signal, 2008, 3: 18. doi:10.1186/1750-2187-3-18 |
| [15] |
李锋, 裴世锋, 石贤爱. 海蛾活性部位抑制人宫颈癌HeLa细胞增殖及诱导凋亡作用研究[J]. 中国药理学通报, 2017, 33(11): 1546-52. Li F, Pei S F, Shi X A. Effects of active fraction from Pegasus laternarius Cuvier on proliferation and apoptosis of human cervical cancer HeLa cells[J]. Chin Pharmacol Bull, 2017, 33(11): 1546-52. doi:10.3969/j.issn.1001-1978.2017.11.014 |

