

2. 延边大学医学院病理学教研室,吉林 延吉 133002;
3. 延边大学吉林省科技厅重点实验室,吉林 延吉 133002;
4. 大连医科大学附属第一医院病理科,辽宁 大连 116011;
5. 延边大学附属医院神经内科,吉林 延吉 133000
2. Dept of Pathology, Medical College, Yanbian University, Yanji Jilin 133002, China;
3. Key Lab of the Science and Technology Dept of Jilin Province, Yanbian University, Yanji Jilin 133002, China;
4. Dept of Pathology, the First Affiliated Hospital of Dalian Medical University, Dalian Liaoning 116011, China;
5. Dept of Neurology, Affiliated Hospital of Yanbian University, Yanji Jilin 133000, China
我国是原发性肝癌(hepatocellular carcinoma,HCC)大国,全球每年约一半新发病例出现在我国。近几年,虽然分子靶向治疗肝癌取得了一定的效果,但局部扩散和远端转移仍是肝癌患者死亡的主要原因。因此,寻找可以有效抑制肝癌细胞转移的分子靶向药物刻不容缓。上皮-间质转化(epithelial-mesenchymal transition,EMT)是肿瘤转移的重要机制。而PI3K/Akt/mTOR通路是细胞重要的信号转导通路之一,与肿瘤的蛋白合成、生长代谢、迁移浸润以及血管生成密切相关。研究显示,PI3K/Akt/mTOR通路可通过直接诱导、上调核转录因子表达等方式,诱导EMT的发生。同时,Six1作为Ezrin的上游调节因子,可激活TGF-β信号通路,从而促进EMT相关基因的表达。
NVP-BEZ235(以下简称为BEZ235,结构见Fig 1A)是PI3K和mTOR的双重靶点抑制剂,可抑制乳腺癌[1]、前列腺癌[2]、胃癌[3]、结直肠癌[4]、神经母细胞瘤[5]等多种肿瘤的恶性进展。目前,虽有文献报道BEZ235可抑制肝癌的增殖和侵袭,但其作用机制仍不清楚[6]。因此,本研究旨在检测BEZ235对肝癌细胞HepG2增殖和迁移的影响,并探讨其可能的分子机制。
1 材料与方法 1.1 材料 1.1.1 细胞株人肝癌细胞株HepG2,购自美国模式培养物保藏所(American Type Culture Collection)。
1.1.2 试剂胎牛血清、DMEM培养基、青霉素/链霉素、胰蛋白酶等试剂,均购自美国Gibco公司; 磷酸盐缓冲溶液(phosphate buffer saline,PBS),购自北京中杉金桥生物技术有限公司; 二甲基亚砜(dimethyl sulfoxide,DMSO)、Hoechst 33342荧光染料、MTT,均购自北京索莱宝生物科技有限公司; RIPA裂解液、BCA蛋白定量试剂盒,均购自北京康为世纪生物科技有限公司; BEZ235购自美国Sigma Aldrich公司; p-mTORSer2448、mTOR、p-AktSer473、Akt、p-S6Thr389、S6、p-4E-BP1Thr37/46、4E-BP1、E-cadherin、Vimentin、Snail、Six1、p-EzrinTyr353、Ezrin等抗体,均购自美国Cell Signaling Techology公司; β-actin、HRP标记的二抗,均购自北京中杉金桥生物技术有限公司; 荧光二抗Alexa Fluor® 488、Alexa Fluor® 568,均购自美国Thermo Fisher Scientific公司。
1.1.3 仪器CO2恒温培养箱(新加坡ESCO公司); 全波长多功能酶标仪(瑞士Tecan公司); 光学倒置显微镜(日本Olympus公司); 台式高速离心机(美国Thermo公司); ChemiDoc成像系统(美国Bio-Rad公司); 共聚焦显微镜(德国Leica公司)。
1.2 方法 1.2.1 细胞培养将HepG2细胞置于含10%胎牛血清、1%青霉素/链霉素的DMEM培养基中,在37 ℃、5% CO2的培养箱中培养。
1.2.2 MTT实验将HepG2细胞以每孔100 μL(5×103个细胞)接种于96孔板。次日,加入BEZ235(0、25、50、100、250、500 nmol·L-1)继续培养48 h,每个浓度设5个平行复孔。每孔加入5 g·L-1 MTT溶液20 μL,继续培养4 h后,弃上清,加入DMSO,震荡,用全波长酶标仪于490 nm波长测定吸光值。根据公式计算细胞生存率:细胞生存率=用药组吸光值/对照组吸光值×100%。
1.2.3 细胞形态学观察通过倒置显微镜观察BEZ235对HepG2细胞形态学的影响。
1.2.4 Hoechst 33342染色在6孔板中放置预先灭菌处理好的盖玻片并接种细胞,各组细胞BEZ235处理48 h后,用10 mg·L-1 Hoechst 33342染液于培养箱内避光孵育15 min,经固定、洗涤、封片后,在荧光显微镜下拍照。
1.2.5 划痕愈合实验将细胞等量接种于6孔板中,待细胞的融合度达到90%时,用200 μL枪头划痕。加入BEZ235/DMEM培养基,分别处理0、24、48 h后观察、拍照。测量划痕间距,根据公式计算划痕愈合率:划痕愈合率/%=(0 h划痕宽度-24/48 h划痕宽度)/0 h划痕宽度×100%。
1.2.6 Transwell迁移实验将HepG2细胞消化、离心,并以100 μL(5×104个细胞)接种于Transwell上室。细胞贴壁后,上室分别加入BEZ235/DMEM培养基(无血清),下室加入含10%血清的DMEM培养基。于37 ℃、5% CO2的培养箱中培养24 h后终止培养,依次进行固定、结晶紫染色、脱色、擦去上室细胞、取膜、封片后,于显微镜下观察、拍照。
1.2.7 Western blot检测HepG2经不同浓度BEZ235处理48 h后,收集各组细胞,用RIPA裂解液提取总蛋白,BCA蛋白定量试剂盒测定蛋白浓度。取40 μg蛋白依次进行SDS-PAGE凝胶电泳、转膜、5%脱脂牛奶封闭后,一抗(1 :1 000)4 ℃孵育过夜。次日,洗膜,二抗(1 :3 000)室温孵育2 h后,ECL法显影、曝光。以β-actin为内参,评价各目的蛋白的相对表达水平。
1.2.8 免疫荧光染色在6孔板中放置灭菌处理好的盖玻片并接种细胞,各组细胞经BEZ235处理48 h后,依次进行多聚甲醛固定、Triton X-100透化、牛血清封闭后,一抗(1 :500)4 ℃孵育过夜。次日,洗涤,荧光二抗(1 :400)室温避光孵育2 h。洗涤后,DAPI染色,封片,于荧光显微镜下拍照。
1.2.9 GeneMANIA数据库分析登陆GeneMANIA在线数据库(http://www.genemania.org),选择人类种属Homo Sapiens,输入Six1、Ezrin以及PI3K/Akt/mTOR信号通路的相关基因,确认信息后即可显示分析结果。
1.2.10 统计学分析采用SPSS 17.0统计软件进行数据分析,实验数据以x±s表示,组间比较采用单因素方差分析。每组实验均重复3次以上。
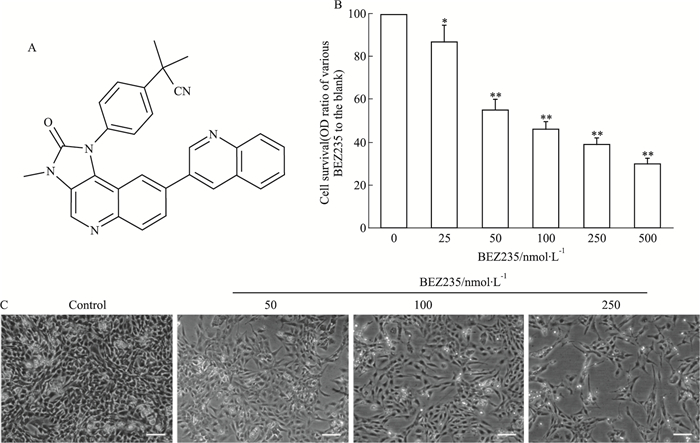
2 结果 2.1 BEZ235抑制HepG2细胞增殖Fig 1B的MTT结果显示,BEZ235(0、25、50、100、250、500 nmol·L-1)处理HepG2细胞48 h后,细胞的增殖活性随着用药浓度的升高逐渐降低,且呈浓度依赖性(P<0.05)。根据MTT结果,BEZ235(0、50、100、250 nmol·L-1)作为后续实验的用药浓度。通过倒置显微镜观察细胞形态发现(Fig 1C),对照组细胞增殖旺盛、单个细胞胞体饱满且呈密集分布; 而梯度用药组随着BEZ235浓度的升高,其细胞密度逐渐降低、细胞间隙逐渐增大、核内颗粒也逐渐增多,进一步表明BEZ235明显抑制HepG2细胞的增殖。
|
| Fig 1 Effect of BEZ235 treatment on proliferation of HepG2 cell in vitro A: The molecular structure of BEZ235; B:Cell viability of HepG2 cells treated by BEZ235 was measured by MTT assay(x±s, n=3); C: Phase-contrast photomicrographs displayed the morphology of BEZ235-treated HepG2 cells(×200).*P < 0.05, **P < 0.01 vs control group. |
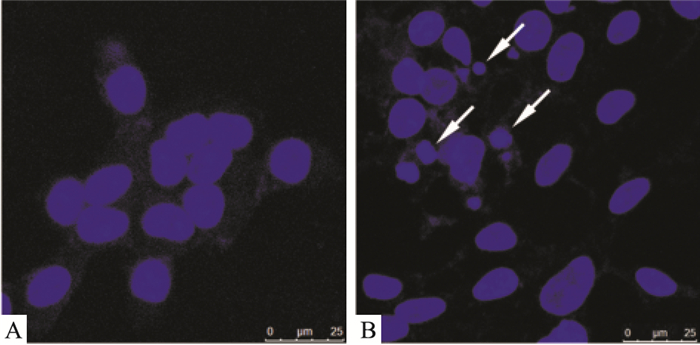
Hoechst 33342染色发现(Fig 2),与对照组相比,BEZ235组细胞出现了明显的核固缩和亮蓝染色的凋亡小体,提示BEZ235可诱导HepG2细胞发生凋亡。
|
| Fig 2 Apoptosis of HepG2 cells exacerbatedby BEZ235 by Hoechst 33342 staining(×400) White arrowhead identifies apoptotic nuclei. A:Control group; B:BEZ235(100 nmol·L-1)-treated group. |
Fig 3的划痕愈合实验和Transwell迁移实验结果显示,与对照组相比,用药组细胞的横向和纵向迁移能力明显受到抑制,且差异具有统计学意义(P<0.01),提示BEZ235可抑制肝癌细胞的横向和纵向迁移能力。

|
| Fig 3 Influence of BEZ235 on migration of HepG2 cells determined by scratch wound-healing assay and Transwell assay(x±s, n=3) A: Scratch wound-healing assay(×100); B: Quantification of results; C: Transwell assay(×200); D: Quantification of results.*P < 0.05, **P < 0.01 vs control group. |
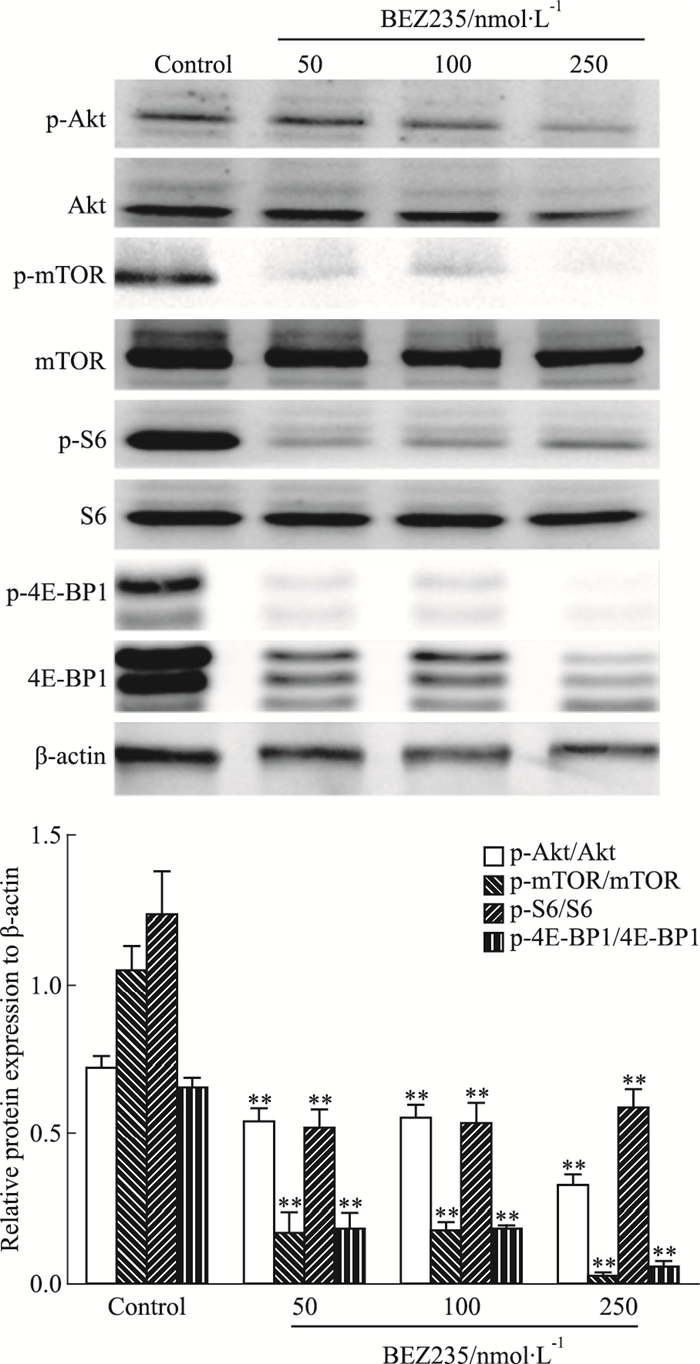
Fig 4的Western blot结果显示,与对照组相比,用药组p-AktSer473、p-S6Thr389和p-4E-BP1Thr37/46的蛋白表达水平随着药物浓度的升高明显下调(P<0.01)。提示BEZ235抑制HepG2细胞的增殖、迁移与Akt、S6以及4E-BP1的磷酸化水平降低有关。
|
| Fig 4 Activation of PI3K/mTOR pathway inhibitedby BEZ235 in HepG2 cells(x±s, n=3) **P < 0.01 vs control group |
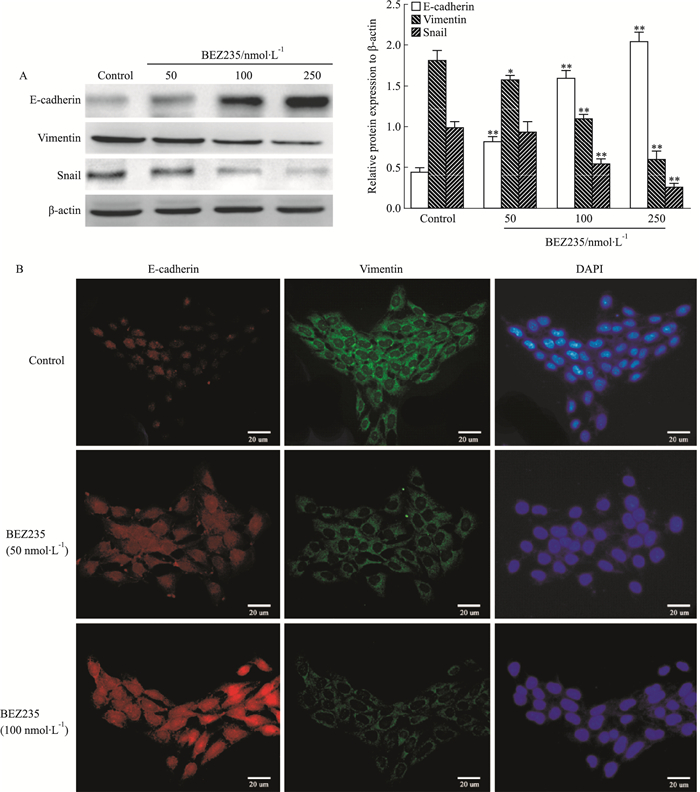
为了检测BEZ235对EMT进程的影响,Western blot检测EMT相关蛋白的表达水平。结果显示(Fig 5A),与对照组相比,BEZ235组上皮标志物E-cadherin表达上调,间质标志物Vimentin、Snail表达下调,且呈浓度依赖性(P<0.05)。免疫荧光结果显示(Fig 5B),BEZ235可上调E-cadherin的表达,下调Vimentin的表达,提示BEZ235可明显抑制肝癌细胞的EMT进程。
|
| Fig 5 EMT progression of HepG2 cells suppressed by BEZ235 A: Expression of E-cadherin, Vimentin and Snail was detected in BEZ235-treated HepG2 cells by Western blot(x±s, n=3); B: Expression of E-cadherin and Vimentin in BEZ235-treated-HepG2 cells was detected by immunofluorescence staining(×400).*P < 0.05, **P < 0.01 vs control group. |
GeneMANIA数据库分析结果显示(Fig 6A),PI3K/Akt/mTOR信号通路与Six1和Ezrin具有相关性。同时,本课题组前期研究发现,Six1和Ezrin在肝癌患者中过表达,且与患者的TNM分期和转移密切相关[7]。因此,进一步通过Western blot实验检测BEZ235是否对Six1和Ezrin产生影响。结果显示(Fig 6B),与对照组相比,BEZ235组Six1和p-EzrinTyr353的蛋白表达水平明显下调,且呈浓度依赖性(P<0.05),提示Six1/Ezrin信号轴参与了BEZ235对HepG2细胞增殖和迁移的调控。

|
| Fig 6 Six1 and p-Ezrin protein expression of HepG2 cells suppressed by BEZ235 A: Network of PI3K/Akt/mTOR-Six1/Ezrin interactions; B: Expression of Six1, p-Ezrin and Ezrin was detected in BEZ235-treated HepG2 cells by Western blot(x±s, n=3).*P < 0.05, **P < 0.01 vs control group. |
研究显示,单纯针对PI3K的抑制剂,如LY294002,虽可抑制肿瘤细胞增殖、诱导凋亡的发生,但存在药物疗效差、潜在毒性强等缺点; 而单纯针对mTOR的抑制剂,如RAD001,则可负反馈激活PI3K,导致细胞出现耐药性[8-9]。本研究中使用的BEZ235是PI3K/mTOR的双靶点抑制剂,可竞争性结合ATP,影响PI3K/mTOR通路的下游分子[10],从而抑制肿瘤的发生、发展。
在实验中,我们通过MTT实验检测BEZ235对HepG2肝癌细胞增殖活性的影响。结果显示,BEZ235可以明显抑制HepG2细胞的增殖活性,且呈现浓度依赖性。进一步的形态学观察结果显示,BEZ235可明显减少HepG2细胞的增殖数量,提示BEZ235可以从细胞活性和细胞数量两个方面对HepG2细胞的增殖产生抑制作用。这一结果与李良庆等[3]的研究结果相一致。Chang等[11]研究显示,BEZ235可通过诱导凋亡而抑制肝癌细胞Hep3B的增殖。在本研究中,Hoechst 33342染色结果提示,BEZ235可诱导HepG2细胞凋亡,从而抑制细胞增殖。在迁移方面,划痕愈合实验和Transwell迁移实验结果显示,BEZ235可明显抑制HepG2细胞的迁移。这一结果与魏娟等[6]的研究结果一致。
大量研究显示,PI3K的下游分子Akt的磷酸化水平可调控肿瘤细胞的凋亡,而mTOR的下游分子S6和4E-BP1的磷酸化水平可影响肿瘤细胞的增殖和迁移[12]。我们的结果显示,BEZ235组p-AktSer473、p-S6Thr389和p-4E-BP1Thr37/46的蛋白表达水平均受到明显抑制,提示BEZ235可通过抑制Akt、S6和4E-BP1的磷酸化,调控HepG2细胞的凋亡、增殖和迁移。EMT在肿瘤细胞的迁移和浸润过程中发挥重要作用。在EMT的进程中,上皮标志物(如E-cadherin、ZO-1等)表达下调,间质标志物(如Vimentin、N-cadherin、Snail、Slug、Twist等)表达上调,可诱导细胞骨架重构,使原先紧密连接的细胞变得松散、黏附力下降,更易于从原发部位脱落,从而增强肿瘤细胞的运动和侵袭性。本课题组前期的研究结果显示,BEZ235可通过上调E-cadherin、ZO-1的表达,下调Vimentin、Twist的表达,逆转非小细胞肺癌的EMT进程[13]。本实验采用Western blot和免疫荧光实验,检测了BEZ235对HepG2细胞EMT相关标志物的影响。结果显示,与对照组相比,BEZ235组E-cadherin表达明显上调,Vimentin和Snail表达明显下调,提示BEZ235可通过逆转EMT进程,抑制HepG2细胞的迁移。Yu等[14]研究显示,Six1/Ezrin在肿瘤的转移中发挥着重要的作用。本课题组前期的研究证实,Six1和Ezrin在肝癌患者中过表达,且与患者的TNM分期和转移密切相关[7]。通过GeneMANIA数据库发现,Six1/Ezrin与PI3K/Akt/mTOR信号通路存在交互关系。Gautreau等[15]的研究也显示,p-EzrinTyr353可直接作用于p85,进而激活PI3K/Akt信号通路,调控肿瘤细胞的增殖和转移。因此,我们采用Western blot检测了BEZ235对Six1/Ezrin表达的影响。结果显示,BEZ235可下调Six1和p-EzrinTyr353的蛋白表达。提示Six1/Ezrin信号轴参与了BEZ235对HepG2细胞增殖和迁移的调控。
综上所述,NVP-BEZ235可有效抑制HepG2细胞的增殖和迁移,其机制可能与NVP-BEZ235降低p-AktSer473、p-S6Thr389、p-4E-BP1Thr37/46的表达,抑制Six1/Ezrin信号轴以及逆转EMT的进程有关。
( 致谢: 本实验是在吉林省科技厅重点实验室、延边大学肿瘤研究中心分子病理实验室完成,感谢实验室各位老师的指导与帮助。)
| [1] |
周宪春, 张松男, 林贞花, 等. BEZ235体内外抑制人乳腺癌细胞系增殖[J]. 基础医学与临床, 2016, 36(3): 311-4. Zhou X C, Zhang S N, Lin Z H, et al. BEZ235 inhibits the proliferation of breast cancer cells in vitro and in vivo[J]. Basic Clin Med, 2016, 36(3): 311-4. |
| [2] |
侯国军, 阙慧琳, 孙洁, 等. BEZ235对体外前列腺癌细胞的抑制作用[J]. 中南大学学报(医学版), 2017, 42(8): 869-73. Hou G J, Que H L, Sun J, et al. Inhibitory effect of BEZ235 on human prostate carcinoma in vitro[J]. J Centr South Univ(Med Sci), 2017, 42(8): 869-73. |
| [3] |
李良庆, 郑雪兰, 潘敦, 等. NVP-BEZ235对人胃癌AGS细胞抑制作用的研究[J]. 中华普通外科杂志, 2018, 33(5): 431-2. Li L Q, Zheng X L, Pan D, et al. Inhibitory effect of BEZ235 on human gastric cancer cell AGS[J]. Chin J Gen Surg, 2018, 33(5): 431-2. doi:10.3760/cma.j.issn.1007-631X.2018.05.020 |
| [4] |
Yu Y, Yu X, Ma J, et al. Effects of NVP-BEZ235 on the proliferation, migration, apoptosis and autophagy in HT-29 human colorectal adenocarcinoma cells[J]. Int J Oncol, 2016, 49(1): 285-93. doi:10.3892/ijo.2016.3507 |
| [5] |
Liu S L, Liu Z, Zhang L D, et al. GSK3β-dependent cyclin D1 and cyclin E1 degradation is indispensable for NVP-BEZ235 induced G0/G1 arrest in neuroblastoma cells[J]. Cell Cycle, 2017, 16(24): 2386-95. doi:10.1080/15384101.2017.1383577 |
| [6] |
魏娟, 祁继平, 郑勤. NVP-BEZ235对肝癌HepG2细胞增殖、凋亡及侵袭转移的影响[J]. 临床肿瘤学杂志, 2014, 19(7): 594-8. Wei J, Qi J P, Zheng Q. Effect of NVP-BEZ235 on proliferation, apoptosis, invasion and metastasis of HepG2 cells[J]. Chin Clin Oncol, 2014, 19(7): 594-8. |
| [7] |
孔界男, 周宪春, 韩龙哲, 等. 甲胎蛋白阴性肝细胞癌中埃兹蛋白(ezrin)和SIX1蛋白表达水平的临床病理意义[J]. 细胞与分子免疫学杂志, 2016, 32(2): 236-9. Kong J N, Zhou X C, Han L Z, et al. Clinicopathological significance of ezrin and SIX1 protein expression in alpha fetoprotein-negative hepatocellular carcinoma[J]. Chin J Cell Mol Immunol, 2016, 32(2): 236-9. |
| [8] |
Passacantilli I, Capurso G, Archibugi L, et al. Combined therapy with RAD001 e BEZ235 overcomes resistance of PET immortalized cell lines to mTOR inhibition[J]. Oncotarget, 2014, 5(14): 5381-91. |
| [9] |
张铮铮, 刘筱, 徐浩, 等. 骨化三醇、雷帕霉素及其联合使用对人子宫内膜癌Ishikawa细胞株的作用及机制研究[J]. 中国药理学通报, 2018, 34(10): 1444-9. Zhang Z Z, Liu X, Xu H, et al. Effect of calcitriol, rapamycin and their combination on human endometrial carcinoma Ishikawa cells in vitro and its mechanism[J]. Chin Pharmacol Bull, 2018, 34(10): 1444-9. doi:10.3969/j.issn.1001-1978.2018.10.023 |
| [10] |
Chen D, Lin X, Zhang C, et al. Dual PI3K/mTOR inhibitor BEZ235 as a promising therapeutic strategy against paclitaxel-resistant gastric cancer via targeting PI3K/Akt/mTOR pathway[J]. Cell Death Dis, 2018, 9(2): 123. doi:10.1038/s41419-017-0132-2 |
| [11] |
Chang Z, Shi G, Jin J, et al. Dual PI3K/mTOR inhibitor NVP-BEZ235-induced apoptosis of hepatocellular carcinoma cell lines is enhanced by inhibitors of autophagy[J]. Int J Mol Med, 2013, 31(6): 1449-56. doi:10.3892/ijmm.2013.1351 |
| [12] |
Pei Y F, Zhang Y J, Lei Y, et al. Hypermethylation of the CHRDL1 promoter induces proliferation and metastasis by activating Akt and Erk in gastric cancer[J]. Oncotarget, 2017, 8(14): 23155-66. |
| [13] |
Piao J, Chen L, Quan T, et al. Superior efficacy of co-treatment with the dual PI3K/mTOR inhibitor BEZ235 and histone deacetylase inhibitor Trichostatin A against NSCLC[J]. Oncotarget, 2016, 7(37): 60169-80. |
| [14] |
Yu Y, Khan J, Khanna C, et al. Expression profiling identifies the cytoskeletal organizer ezrin and the developmental homeoprotein Six-1 as key metastatic regulators[J]. Nat Med, 2004, 10(2): 175-81. doi:10.1038/nm966 |
| [15] |
Gautreau A, Poullet P, Louvard D, et al. Ezrin, a plasma membrane-microfilament linker, signals cell survival through the phosphatidylinositol 3-kinase/Akt pathway[J]. Proc Natl Acad Sci USA, 1999, 96(13): 7300-5. doi:10.1073/pnas.96.13.7300 |

