

感染和炎症过程中诱发炎性细胞因子白细胞介素-1β(interleukin 1β,IL-1β)和肿瘤坏死因子α(tumor necrosis factor α,TNF-α)高表达,介导细胞色素P450(cytochrome P450,CYP450)的下调[1]。炎症细胞因子在全身或局部炎症后,由多种细胞产生,包括单核细胞、巨噬细胞、Kupffer细胞和内皮细胞。卡介苗(Bacillus Calmette-Guérin,BCG)免疫性肝损伤过程中亦可刺激单核细胞和Kupffer细胞产生大量TNF-α和IL-1β。此外,TNF-α抗体消除Kupffer细胞可有效减少体内肝损伤,提示Kupffer细胞分泌的TNF-α可能在肝损伤中起主要作用[2]。本课题组以往的研究主要集中在免疫性肝损伤过程中,NF-κB被诱导并产生氧化应激作用,抑制NF-κB的激活,可以阻止NF-κB向核内移位,减少下游细胞因子的表达[3]。而在免疫性肝损伤过程中,NF-κB活化后IL-1β、TNF-α高表达与代谢酶CYP2E1的代谢活力、蛋白表达之间的关系尚不清楚。本研究在以往研究基础上,探讨细胞因子IL-1β、TNF-α在免疫性肝损伤过程中对代谢酶CYP2E1下调的作用机制,为免疫介导的肝损伤的药物治疗提供新的靶点和思路。
1 材料与方法 1.1 实验动物与试剂清洁级♂ SD大鼠,内蒙古大学动物实验中心提供,体质量(220±20)g,动物许可证号:SCXK(蒙)2005-0001。BCG冻干粉(每支60 mg,1 g·L-1),购自中国食品药品检定研究院,批号:2013-01;氯唑沙宗标准品(批号:100364-201302),中国食品药品检定研究院; 氯唑沙宗对照品(批号:L1B0Q15),北京百灵威科技有限公司; NF-κB的特异性抑制剂吡咯烷二硫氨基甲酸(ammonium pyrrolidinedithiocarbamate,PDTC)(批号:851002),美国Sigma公司; 乙酸乙酯(色谱纯,批号:20180301)、无水甲醇(分析纯,批号:20150503),天津市大茂化学试剂厂; 磷酸二氢钠(批号:20140417),天津市北辰骅跃化学试剂厂; 超敏ECL化学发光即用型底物(批号:13D17B70),BCA蛋白定量试剂盒(批号:12C17B46),购自博士德生物工程有限公司。
1.2 仪器Water2998高效液相色谱仪(美国Waters公司; TGL-16C离心机(上海安亭科学仪器厂); AUW120D分析天平(岛津企业管理有限公司); Multiskan FC酶标仪(赛默飞世尔上海仪器有限公司); DYY-6D电泳仪电源(北京六一生物科技有限公司); OmegaLum C凝胶成像仪(环亚生物科技)。
1.3 动物分组及免疫性肝损伤模型的制备SD大鼠50只,适应性饲养2周,随机分为5组,分别为Control、BCG、BCG+PDTC低、中、高剂量组(25、50、100 mg·kg-1),每组10只。除Control组外,其他4组尾静脉注射BCG(125 mg·kg-1)制备免疫性肝损伤大鼠模型,Control组尾静脉注射等体积生理盐水。用工具药PDTC分别对BCG+PDTC低、中、高剂量组进行干预(d 11、12、13的16时各注射1次,低、中、高剂量分别为25、50、100 mg·kg-1)。d 14眼眶静脉丛取血,用于HPLC法测定CYP2E1代谢活性实验,随后将大鼠断头处死,迅速剖取肝脏,称重。称取部分肝脏组织用于ELISA及蛋白定量检测; 另称取部分肝脏组织冻存,用于Western blot检测。
1.4 HPLC法测定CYP2E1代谢活性将5组大鼠单次静脉注射氯唑沙宗20 mg·kg-1,分别于给药后5、10、20、30、60、90、120、240 min,从眼内眦静脉丛取血20滴(约1 mL)于肝素化试管中,3500 r·min-1离心10 min,取血浆,保存在-20 ℃的冰箱待测[4]。根据文献方法[5],测定血浆中CYP2E1探针药物氯唑沙宗浓度的血药浓度经时变化。用药物代谢动力学软件DAS 3.0对血药浓度数据进行拟合,得出AUC、Cmax、t1/2、Ke、V、CL等各项药代动力学参数。通过测定血浆中探针药物氯唑沙宗药-时曲线及药代动力学参数的变化,检测CYP2E1代谢活性。色谱条件:采用Waters C18色谱柱(4.6 mm ×250 mm, 5 μm), 序号为201763619313813,柱温37 ℃。色谱工作站:Breeze2;检测波长:287 nm。流动相:甲醇:0.001%磷酸二氢钠(70 :30,V/V),流速:1 mL·min-1,进样量25 μL,pH 5.0[4]。
1.5 ELISA法检测大鼠肝脏IL-1β、TNF-α水平将预先提取的蛋白稀释到合适浓度,与预先配好的标准溶液加入到酶标板中,并增加一孔作为TMB空白显色孔,其余样本放入-80 ℃冰箱保存。用酶标仪在450 nm测定IL-1β、TNF-α的水平。
1.6 Western blot检测肝组织CYP2E1表达取大鼠肝脏,精确称取0.1 g,IP细胞裂解液提取组织总蛋白。BCA法蛋白定量,在10% SDS-聚丙烯酰胺凝胶上电泳,转膜,封闭,孵育一抗及二抗,显影。
1.7 统计学处理实验结果用x±s表示,采用SPSS 19.0统计软件,多组比较采用单因素方差分析进行组间比较,相关分析采用两变量相关分析。
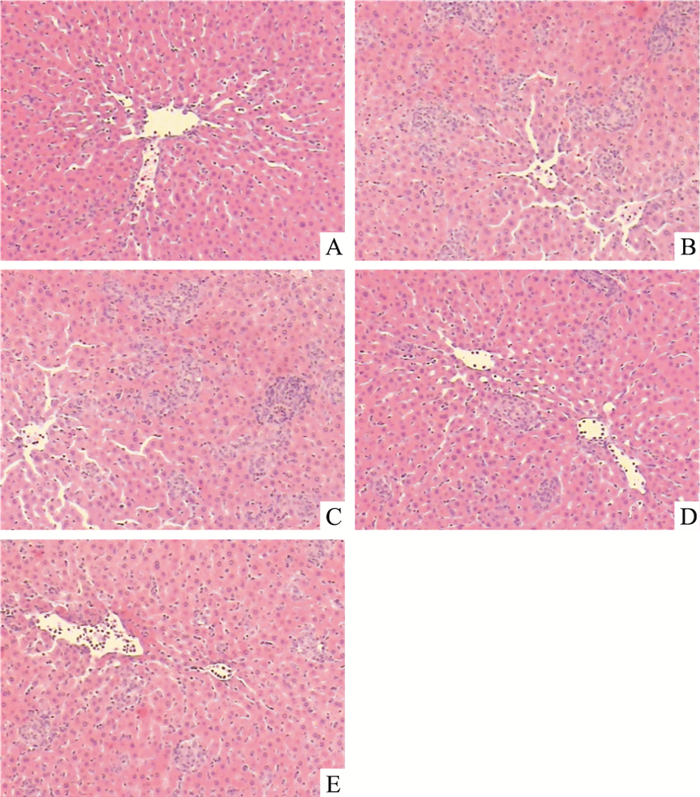
2 结果 2.1 BCG诱导的免疫性肝损伤大鼠肝脏病理组织学的变化如Fig 1所示,大鼠注射BCG 14 d后,光镜下观察到肝实质及汇管区周围有大量单核细胞及淋巴细胞浸润,形成大小不等且弥漫性分布的大量肉芽肿团块,为特征的免疫性肝损伤; 给予PDTC进行干预,可见炎性细胞浸润情况有所减轻。
|
| Fig 1 Pathological features in liver (HE×200) A: Control group; B: BCG group; C:BCG+PDTC (25 mg·kg-1); D:BCG+PDTC (50 mg·kg-1); E:BCG+PDTC (100 mg·kg-1). |
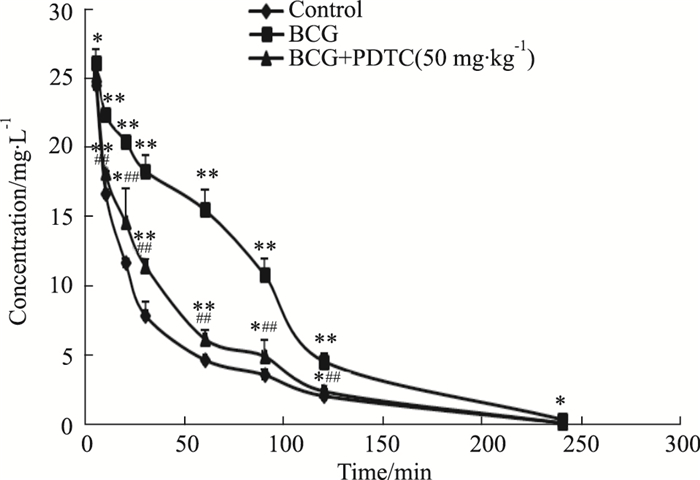
大鼠注射BCG 14 d后,HPLC法测定各组大鼠血药浓度经时变化。如Fig 2所示,BCG组各个时间点血药浓度均高于Control组,在给予工具药PDTC干预后,BCG+PDTC组在20、90 min时间点的血药浓度低于BCG组(P<0.01)。经DAS 3.0药代动力学软件计算各组药代动力学参数,Tab 1结果显示,BCG组Ke、CL均小于Control组,V、Cmax、AUC、t1/2均高于Control组(P<0.05)。BCG+PDTC组Ke、CL高于BCG组,Cmax、AUC均低于BCG组(P<0.05)。
|
| Fig 2 Plasma chlorzoxazone levels in all groups (x±s, n=10) *P < 0.05, **P < 0.01 vs control group; #P < 0.05, ##P < 0.01 vs BCG group |
| Group | Control | BCG | BCG+PDTC (50 mg·kg-1) |
| AUC0-t/mg·L-1·min-1 | 1 073.66±7.79 | 2 099.16±3.22** | 1 354.62±70.15**## |
| Cmax/mg·L-1 | 24.53±0.80 | 26.10±0.30** | 25.20±0.62# |
| t1/2/min | 28.40±1.18 | 47.46±0.54** | 33.99±2.90**## |
| Ke/min-1 | 0.02±0.01 | 0.01±0.02* | 0.02±0.01# |
| V/L·kg-1 | 89.34±4.22 | 120.74±3.94** | 96.11±10.74## |
| CL/L·min-1·kg-1 | 2.18±0.01 | 1.76±0.04** | 1.95±0.05**## |
| *P<0.05, **P<0.01 vs control; #P<0.05, ##P<0.01 vs BCG | |||
Fig 3的Western blot结果显示,内参GAPDH各条带密度均一,提示蛋白定量基本准确,各组蛋白上样量基本一致。Control组肝脏组织中有CYP2E1的基础表达,BCG组中CYP2E1表达明显减少(P<0.05),给予PDTC干预,随着剂量的增加,CYP2E1表达逐渐恢复。

|
| Fig 3 CYP2E1 expression in all groups (x±s, n=6) **P < 0.01 vs control group; #P < 0.05 vs BCG group |
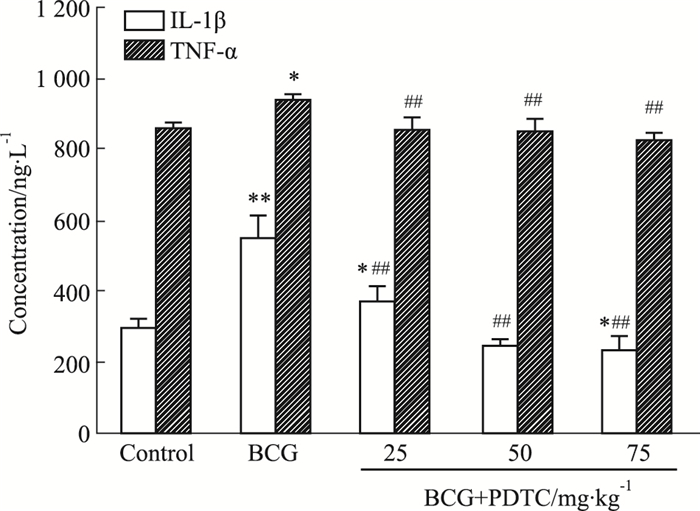
如Fig 4所示,大鼠注射BCG 14 d后,肝脏组织中IL-1β、TNF-α含量增加(P<0.05),给予工具药PDTC干预后,随着PDTC剂量的增大,大鼠肝脏组织中TNF-α、IL-1β含量逐渐降低。
|
| Fig 4 Changes of inflammatory cytokine IL-1β and TNF-α in all groups (x±s, n=6) *P < 0.05, **P < 0.01 vs control group; ##P < 0.01 vs BCG group |
药代动力学参数AUC与IL-1β(r=0.871,P=0.000)以及TNF-α(r=0.788,P=0.000)呈明显正相关。CYP2E1蛋白表达与IL-1β(r=-0.222,P=0.027)呈负相关。
3 讨论本实验以尾静脉注射BCG冻干粉复制大鼠免疫性肝损伤模型,由于大鼠不能感染人类的肝炎病毒[6],转染人类肝炎病毒的转基因鼠由于造价昂贵,又存在着转基因鉴定等问题,难以实现较大样本量的研究。采用尾静脉注射BCG方法造模,能够较好地模拟人类的免疫性肝损伤。大鼠注射BCG 14 d后,观察到肝实质及汇管区周围大量炎性细胞浸润、肝脾肿大及肝功能受损[7],根据本室以往研究表明大鼠免疫性肝损伤模型建立成功。
大鼠注射BCG 2周后,给予NF-κB的特异性抑制剂PDTC干预,根据大鼠氯唑沙宗的血药浓度经时变化曲线和各组大鼠的血浆氯唑沙宗药代动力学参数,推测NF-κB的激活会使CYP2E1的代谢活力下调,钝化NF-κB的激活可以减缓这种下调。本实验进一步研究表明,在免疫性肝损伤过程中,BCG组CYP2E1的蛋白表达含量减少,给予NF-κB抑制剂PDTC后,可使CYP2E1蛋白表达含量逐渐恢复,推测CYP2E1蛋白表达的下调可能与NF-κB的激活有关。为了进一步验证NF-κB的活化与肝脏组织中IL-1β、TNF-α表达的关系,本实验还检测了大鼠肝脏组织中的炎性细胞因子IL-1β、TNF-α,发现NF-κB被激活后,IL-1β、TNF-α高表达,给予工具药PDTC干预后,肝脏组织中的炎性细胞因子恢复到与Control组相近的正常水平。推测免疫性损伤过程中,NF-κB激活,调控大量下游炎性细胞因子,参与损伤过程。而PDTC可以通过抑制NF-κB的作用,减少IL-1β、TNF-α的表达。根据相关性分析,药代动力学参数AUC与IL-1β、TNF-α的含量呈明显正相关,蛋白含量与IL-1β含量呈负相关,推测炎性细胞因子IL-1β、TNF-α的高表达可能使CYP2E1代谢活力和蛋白表达下调。许多先前的研究表明,IL-1、TNF-α是免疫介导肝炎的关键因素[1-2]。根据本室以往研究,NF-κB信号传导途径是经典的炎症信号传导途径。NF-κB调节多种基因在炎症反应的表达,并且可以通过大量的细胞外刺激因子激活核转录因子[8]。肝脏的常驻巨噬细胞Kupffer细胞产生TNF-α和IL-1β,NF-κB的激活引发炎性细胞因子的释放,在免疫性肝损伤中起重要作用。NF-κB一旦受到刺激就会转移到细胞核,并触发促炎性介质如TNF-α和IL-1β的释放。通过研究我们还发现,IL-1β、TNF-α的高表达会使NF-κB表达增加,进而会使CYP2E1的表达下调[9]。
综上所述,本研究推测炎性细胞因子IL-1β、TNF-α在免疫性肝损伤过程中可以激活NF-κB,使代谢酶CYP2E1代谢活力和蛋白表达下调。用NF-κB的特异性抑制剂PDTC干预后,可以钝化NF-κB的激活,缓解下游IL-1β、TNF-α的高表达,减缓CYP2E1代谢活力和蛋白表达的下调。
| [1] |
Nyagode B A, Jahangardi R, Morgan E T, et al. Selective effects of a therapeutic protein targeting tumor necrosis factor-alpha on cytochrome P450 regulation during infectious colitis: implications for disease-dependent drug-drug interactions[J]. Pharmacol Res Perspect, 2014, 2(1): e00027. doi:10.1002/prp2.27 |
| [2] |
Yao J, Du X, Feng G, et al. Rv2346c enhances mycobacterial survival within macrophages by inhibiting TNF-α and IL-6 production via the p38/miRNA/NF-κB pathway[J]. Emerg Microbes Infect, 2018, 7(1): 158. |
| [3] |
贾金雪, 秦金东, 李学峰, 等. 钝化NF-κB的活化对免疫性肝损伤大鼠CYP2E1的影响[J]. 中国药理学通报, 2015, 31(8): 1076-80. Jia J X, Qin J D, Li X F, et al. Effect of blunting NF-kappa B activation on CYP2E1 in immunological liver injury rats[J]. Chin Pharmacol Bull, 2015, 31(8): 1076-80. doi:10.3969/j.issn.1001-1978.2015.08.010 |
| [4] |
李玲, 张远. 氯唑沙宗及其代谢物的HPLC测定方法和药代动力学研究[J]. 药学学报, 1998, 33(10): 12-7. Li L, Zhang Y. HPLC determination and pharmacokinetics of chlorzoxazone and its metabolites[J]. Acta Pharm Sin, 1998, 33(10): 12-7. |
| [5] |
林琴, 贾金雪, 王涛, 等. 抑制NF-κB的活化对免疫性肝损伤大鼠CYP1A2的影响[J]. 中国药理学通报, 2018, 34(11): 1605-9. Lin Q, Jia J X, Wang T, et al. Inhibition of NF-κB activation on CYP1A2 in rats with immune liver injury[J]. Chin Pharmacol Bull, 2018, 34(11): 1605-9. doi:10.3969/j.issn.1001-1978.2018.11.025 |
| [6] |
谭建扬, 宋梦楠, 丁虹, 李晓斐. 甘露糖对免疫性肝损伤小鼠的保护作用[J]. 食品工业科技, 2016, 37(20): 341-4. Tan J Y, Song M N, Ding H, Li X F. Protective effects of mannose on mice with immune liver injury[J]. Sci Technol Food Ind, 2016, 37(20): 341-4. |
| [7] |
李学峰, 郭海军, 张小谦, 等. 抑制NF-κB的活化对免疫性肝损伤小鼠CYP3A代谢活力的影响[J]. 中国药理学通报, 2017, 33(5): 733-5. Li X F, Guo H J, Zhang X Q, et al. Effects of inhibition of NF-κB activation on CYP3A metabolism in mice with immune liver injury[J]. Chin Pharmacol Bull, 2017, 33(5): 733-5. doi:10.3969/j.issn.1001-1978.2017.05.027 |
| [8] |
Nawaz R, Zahid S, Idrees M, et al. HCV-induced regulatory alterations of IL-1β, IL-6, TNF-α, and IFN-γ operative, leading liver en-route to non-alcoholic steatohepatitis[J]. Inflamm Res, 2017, 66(6): 477-86. doi:10.1007/s00011-017-1029-3 |
| [9] |
Xu L, Yu Y, Sang R, et al. Protective effects of taraxasterol against ethanol-induced liver injury by regulating CYP2E1/Nrf2/HO-1 and NF-κB signaling pathways in mice[J]. Oxid Med Cell Longev, 2018, 2018: 8284107. |

