


2. 延边大学附属医院皮肤科,吉林 延吉 133000
 ,
JIANG Jing-zhi1,
LI Jun-feng1,
ZHU Lian-hua2,
JIN Shan2,
JIN Zhe-hu2,
XU Chang1,
YAN Guang-hai1
,
JIANG Jing-zhi1,
LI Jun-feng1,
ZHU Lian-hua2,
JIN Shan2,
JIN Zhe-hu2,
XU Chang1,
YAN Guang-hai1

2. Dept of Dermatology, Hospital of Yanbian University, Yanji Jilin 133000, China
哮喘是一种较为常见的过敏源引起的气道炎症性疾病,发病初期主要由气道炎症细胞与其释放的炎症细胞因子黏附于气道管壁,引发气道高反应性(airway hyper reactivity,AHR),使气道形成不可逆性重塑,并导致肺功能下降[1]。气道炎症与气道重塑被认为是相互作用、相辅相成,最终导致了哮喘[2]。目前除激素外,尚无特效药物可有效治疗过敏性气道炎症。因此,研究哮喘气道炎症的发病机制具有十分重要的意义。
肿瘤坏死因子样凋亡弱诱导因子(TNF-related weak inducer of apoptosis,TWEAK)是一种可以表达于多种细胞的Ⅱ型跨膜蛋白[3]。TWEAK通过成纤维细胞生长诱导因子14(fibroblast growth factor-inducible 14,Fn14)发挥对其他细胞的调节作用,包括促进炎症细胞的活性、调节细胞生长、血管生成。据报道,TWEAK/Fn14/NF-κB通路在哮喘气道炎症中发挥重要作用[4]。转化生长因子β1 (transforming growth factor β1,TGF-β1)为TGF家族的成员,在细胞增殖、分化等过程中发挥作用[5-6]。TGF-β1依靠其下游的Smads家族转导信号,其中以Smad3蛋白与TGF-β家族关系最为密切,Smad3可以认为是TGF-β1的直接底物[7]。有报道指出,TGF-β1/Smads和VEGF信号通路协同参与肺部纤维化以及炎症的调控[8]。本实验旨在研究TWEAK/Fn14和TGF-β1/Smads信号通路交互作用对支气管哮喘气道炎症的影响。
丹参是治疗过敏性疾病的中药。隐丹参酮(cryptotanshinone,CTS)作为丹参中主要的脂溶性成分,具有抗炎、抗氧化等多种药理作用。另外,Tang等[9]研究发现,CTS能够缓解脂多糖引起的急性肺损伤; Suh等[10]报道,CTS能够抑制TNF-α诱导的基质金属蛋白酶-9(matrix metalloproteinase-9,MMP-9)的产生,以及人气道平滑肌细胞的迁移。本研究旨在阐明CTS是否通过TWEAK/Fn14和TGF-β1/Smads信号通路,缓解哮喘模型小鼠气道炎症,为临床寻找新的开发药物,提供实验依据。
1 材料与方法 1.1 材料 1.1.1 实验动物♀清洁级BALB/c小鼠40只,体质量(20±2)g,购自延边大学实验动物中心,合格证号为SCXK(吉)2017-0003。本研究已获得延边大学医学院伦理委员会的批准,整个实验进程中遵守《实验动物管理条例》。
1.1.2 药物与试剂CTS,购自德国Merck Millipore公司; 卵清蛋白(ovalbumin,OVA)、氢氧化铝粉、地塞米松(dexamethasone,DEX),均购自美国Sigma公司; DAB、免疫组化试剂盒、炎症细胞因子ELISA试剂盒,均购自北京中杉金桥公司; 抗TWEAK、Fn14抗体,均购自美国Abcam公司; 抗TGF-β1(货号:3711)、Smad2/3(货号:12747)、Smad4(货号:38454)、β-actin (货号:4970)抗体,均购自美国Cell Signaling公司。
1.1.3 仪器雾化器(大连医疗器械厂U219);2135型轮转式切片机(德国徕卡公司); 酶标仪EPOCH、细胞成像微孔板检测系统(美国Beckman公司); 15K高速冷冻台式离心机(美国Sigma公司); Western blot转膜仪(Bio-Rad公司); TXD3细胞涂片离心机(广州泸瑞明仪器有限司)。
1.2 方法 1.2.1 实验动物分组将40只♀ BALB/c小鼠随机分为5组,每组8只,分别为正常组(control)、OVA慢性气道炎症模型组(OVA)、CTS低、高剂量治疗组(CTS-L、CTS-H)、地塞米松阳性对照组(DEX)。
1.2.2 小鼠气道重塑模型的制备所有小鼠饲养1周,随后d 1、7、14,正常组小鼠每只腹腔注射200 μL生理盐水,其它4组小鼠均每只腹腔注射200 μL OVA 10 μg与氢氧化铝1 mg的混合溶液致敏。从d 14开始,正常组和OVA组每天腹腔注射二甲基亚砜(dimethyl sulfoxide,DMSO)200 μL,CTS-L、CTS-H组分别腹腔注射稀释于DMSO的CTS(20、40 mg·kg-1)200 μL,地塞米松组腹腔注射地塞米松(1 mg·kg-1)200 μL。于d 21,在每日给药1 h后,给予正常组生理盐水雾化,给予除正常组外其它4组3% OVA 10 mL雾化吸入激发哮喘的发生,每日30 min,连续激发7 d。
1.2.3 标本收集实验小鼠在最后一次给药激发24 h后,采用过量乙醚吸入法,使小鼠麻醉至死,将小鼠固定后并用酒精消毒需手术部位,使用手术剪刀剪开小鼠颈部皮肤,小心剥离小鼠颈部肌肉并暴露气管,在气管上剪一开口置入软管,并将1 mL冷生理盐水缓慢注入气管内,在按摩小鼠肺部的同时缓慢回抽液体,将回抽的液体即肺泡灌洗液离心提纯后,置-80 ℃冻存。提纯后剩余的沉淀用于细胞涂片,再将小鼠双侧肺组织剥离,置4%甲醛中固定。
1.2.4 支气管肺泡灌洗液(bronchoalveolar lavage fluid,BALF)炎症细胞分类及计数BALF经高速离心后的细胞沉淀中加入生理盐水,至600 μL,混匀后,取200 μL置入细胞涂片离心机,以1 500 r·min-1离心5 min制备细胞涂片。经Diff-Quick染色,在光学显微镜下进行炎症细胞分类及计数。
1.2.5 BALF中细胞因子含量的检测根据ELISA试剂盒说明书的步骤,依次检测BALF中TNF-α、IL-1β、IL-4、IL-5、IL-13的含量。通过标准曲线计算其浓度。
1.2.6 肺组织学检查将固定后的左肺依次进行脱水、浸蜡、包埋等步骤,并分别进行HE、PAS染色。
1.2.7 免疫组织化学检测将切片置于60 ℃烤箱内熔蜡,然后进行脱蜡、脱水,并置于100 ℃的抗体修复液中修复30 min,然后分别用TWEAK和TGF-β1一抗和相对应的二抗进行孵育。DAB显色、苏木精复染,最后封片观察。
1.2.8 Western blot检测将所需检测的蛋白裂解后,BCA试剂盒测定样品蛋白浓度。每个泳道加等量的蛋白质样品分离后,转移到硝化纤维素膜中,5% BSA室温封闭2 h,并加入稀释的一抗(TWEAK、Fn14、TGF-β1、Smad2/3、Smad4、β-actin)4 ℃过夜。洗膜,并用相应的二抗孵育2 h。洗膜后加入ECL发光试剂,利用Amersham Imager 600采集图像。
1.3 统计学处理数据采用SPSS 17.0统计分析,实验数据以x±s表示,所有柱状图均使用GraphPad Prism 7.0绘制,各组实验指标均采用随机设计的单因素方差分析。
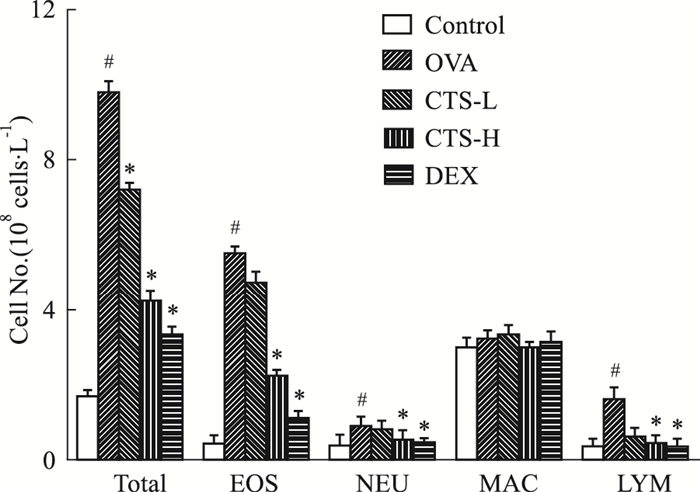
2 结果 2.1 CTS抑制OVA诱导的过敏性哮喘小鼠各炎症细胞的渗出如Fig 1所示,OVA组BALF中总细胞数与嗜酸性粒细胞(eosinophil,EOS)、中性粒细胞(neutrophil,NEU)、淋巴细胞(lymphocyte,LYM)的细胞数较正常组明显升高(P<0.05)。与OVA组相比,CTS-L组中总细胞数与EOS的细胞数均减少(P<0.05),且CTS-H组的总细胞数与EOS、NEU、LYM均明显减少(P<0.05),DEX作为阳性对照组减少更为明显(P<0.05)。而巨噬细胞(macrophage,MAC)的细胞数在各组之间无明显差异。
|
| Fig 1 Number of total and differential cellular components of BALF(x±s, n=8) EOS:Eosinophil; NEU:Neutrophil; MAC:Macrophage; LYM:Lymphocyte. #P < 0.05 vs control; *P < 0.05 vs OVA. |
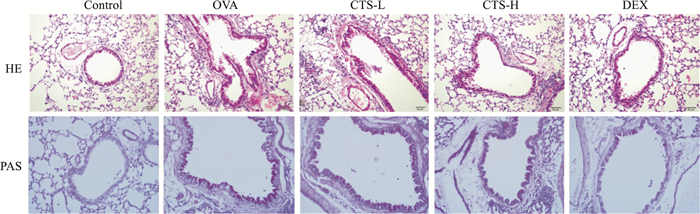
Fig 2的HE染色结果显示,OVA组较正常组炎症细胞浸润明显增多,且发现在血管及细支气管周围浸润明显,而CTS治疗组炎症细胞的浸润明显减少,且CTS高剂量组较低剂量组炎症减轻明显,DEX组减少最明显。相对于正常组的PAS染色,OVA组出现明显的杯状细胞增生与黏液分泌,而CTS-L与CTS-H组PAS染色以上表现明显减轻。由此得出,CTS可明显减少炎症细胞渗出和杯状细胞增生。
|
| Fig 2 Effect of cryptonshinone on pathologic changes of lung tissues(×200) |
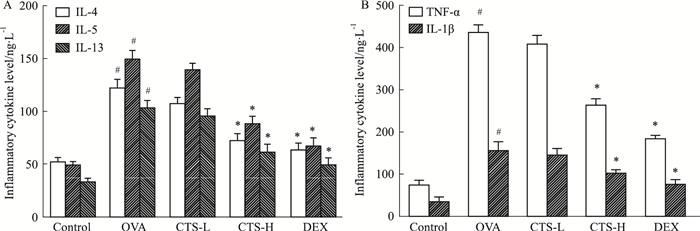
如Fig 3所示,经OVA吸入后,白细胞浸润明显增加,BALF中的炎症细胞因子水平明显升高(P<0.05)。CTS和DEX治疗组中,以上炎症细胞因子水平明显减弱。提示CTS能够明显降低OVA诱导的哮喘小鼠BALF中炎症细胞因子的水平。
|
| Fig 3 Levels of IL-4, IL-5, IL-13(A) and TNF-α, IL-1β (B) quantified by ELISA(x±s, n=8) #P < 0.05 vs control; *P < 0.05 vs OVA |
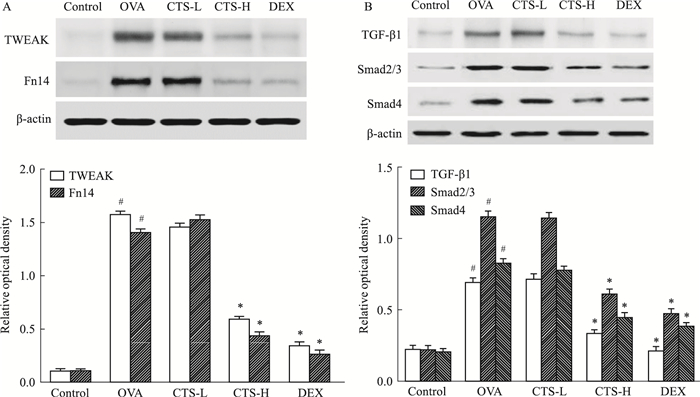
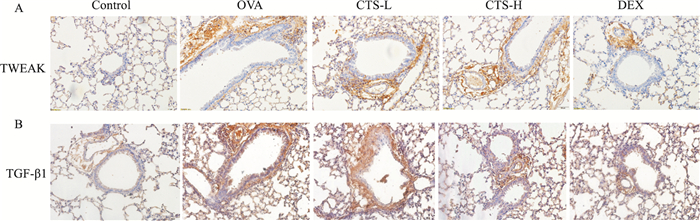
Fig 4A的Western blot结果显示,OVA诱导哮喘小鼠肺组织中TWEAK和Fn14的蛋白表达明显高于正常组(P<0.05),CTS-H与DEX组TWEAK、Fn14蛋白表达较OVA组明显下降(P<0.05),而CTS-L组虽然TWEAK蛋白较OVA组有下降的趋势,但差异无统计意义,且CTS-L组Fn14蛋白较OVA组非但没有减少,反而高于OVA组,表明CTS在一定剂量下可以抑制TWEAK和Fn14的蛋白表达。Fig 5A免疫组织化学染色可见,OVA组较正常组气道周围TWEAK蛋白聚集明显,而CTS-L组与CTS-H组较OVA组TWEAK蛋白水平均有不同程度的减弱。由此可见,CTS减弱OVA诱导小鼠的过敏气道炎症可能与TWEAK/Fn14通路有关。
|
| Fig 4 Detection of TWEAK, Fn14(A) and TGF-β1, Smads (B) protein by Western blot #P < 0.05 vs control; *P < 0.05 vs OVA |
|
| Fig 5 Distribution of TWEAK and TGF-β1 assessed by immunohistochemical staining(×200) |
Fig 4B结果表明,OVA组中TGF-β1蛋白表达较正常组明显增加(P<0.05),CTS-L组中的TGF-β1蛋白表达与OVA组无明显差异,但CTS-H组TGF-β1的表达却明显减少(P<0.05)。与正常组相比,OVA组小鼠肺组织中Smad2/3和Smad4的蛋白含量明显升高(P<0.05),而CTS-L组中这两种蛋白的表达较OVA组有下降趋势,但无统计学意义,CTS-H组中Smad2/3和Smad4蛋白的表达较OVA组明显减少(P<0.05)。结果提示,CTS缓解过敏性哮喘小鼠气道炎症可能与TGF-β1/Smads通路有关。Fig 5B免疫组织化学染色可见,OVA组较正常组气道周围TGF-β1蛋白聚集明显,而CTS-L组与CTS-H组较OVA组TGF-β1蛋白水平减弱。表明CTS对OVA诱导的小鼠哮喘的抑制作用可能与TGF-β1/Smads通路有关。
3 讨论目前,全世界患过敏性疾病的人数急剧上升,其中支气管哮喘不仅发病率高,且难以有效治愈,其最有效的治疗方式仍是使用类固醇等激素类药物。除了提倡吸烟者戒烟,体弱者多做运动,保持健康饮食等预防措施外,似乎没有其他有效办法[11]。因此,迫切需要更有效的治疗方法来提高支气管哮喘疾病治疗的效果。CTS是一种从丹参中纯化的化合物,有报道指出,CTS在体外和体内对肺损伤均有保护作用[9, 12]。本研究证实,CTS能够明显减轻OVA诱导的哮喘小鼠炎症,表明CTS可能是支气管哮喘疾病潜在的治疗药物。
本研究发现,OVA诱导的小鼠气道灌洗液中增加了大量炎症细胞,包括淋巴细胞、嗜酸性粒细胞、中性粒细胞、肥大细胞等。同时,OVA诱导的小鼠BALF中促炎细胞因子(TNF-α、IL-1β)、Th2细胞因子(IL-4、IL-5和IL-13)的水平也明显升高,说明OVA的诱导能够打破Th1与Th2的平衡,小鼠过敏性哮喘模型成功。HE染色、PAS染色结果显示,OVA诱导的小鼠杯状细胞明显增生,向周围分泌大量黏液,炎症细胞浸润,渗出明显; CTS可明显降低气道灌洗液中总细胞、中性粒细胞和嗜酸性粒细胞的数量。同时ELISA结果证明,CTS能够降低OVA诱导的哮喘小鼠促炎细胞因子及Th2细胞因子的含量,且HE染色、PAS染色结果显示,CTS可以减少OVA诱导的小鼠杯状细胞增生,降低黏液分泌,缓解血管和支气管周围的炎症细胞浸润和渗出。以上结果表明,CTS对OVA诱导的哮喘模型小鼠气道炎症有明显的抑制作用。
研究发现,TWEAK可以在多种器官、组织、细胞上表达,但尤以炎症细胞中TWEAK的表达最高,包括被激活的T细胞、分化的白细胞、巨噬细胞等。在正常的组织细胞中Fn14通常呈低表达状态,却高表达于组织损伤或慢性炎症,这也证实了TWEAK/Fn14相互作用参与某些炎症反应[13]。TGF-β1同样是气道炎症中的一个关键因素,它能够与下游蛋白形成异聚复合体,共同调控其下游信号通路,将其协同转运到细胞核内,诱导靶基因转录[14]。Smads蛋白家族已被证实为TGF-β1受体的关键底物之一,是TGF-β1受体复合物的下游信号调节蛋白,在诱导TGF-β1信号从细胞表面转入到细胞核的过程中起到重要作用[15]。本研究Western blot结果表明,CTS可有效抑制TWEAK和Fn14的蛋白表达,且与OVA组相比,CTS高剂量组可明显降低TGF-β1、Smad2/3、Smad4的蛋白表达。免疫组织化学染色结果同样证明,CTS可以降低OVA诱导的小鼠肺部组织TWEAK和TGF-β1的含量。以上结果说明,CTS可能通过TWEAK/Fn14和TGF-β1/Smads双通路来改善过敏性哮喘气道炎症。
综上所述,CTS通过减少肺组织中杯状细胞的增生、炎症细胞浸润和抑制炎症细胞因子,并降低TWEAK和TGF-β1蛋白的生成,起到改善气道炎症的作用,且其作用机制可能与TWEAK/Fn14和TGF-β1/Smads通路密切相关。
( 致谢: 本实验在吉林省过敏性疾病重点实验室完成,感谢各位老师和同学们给予的指导和帮助。)
| [1] |
Ni Y, Hao J, Hou X, et al. Dephosphorylated polymerase I and transcript release factor prevents allergic asthma exacerbations by limiting IL-33 release[J]. Front Immunol, 2018, 9: 1422. doi:10.3389/fimmu.2018.01422 |
| [2] |
赵雨喆, 姜京植, 叶晶, 等. 虎杖苷通过p38 MAPK/Nrf2/HO-1通路减轻小鼠哮喘模型气道炎症[J]. 中国药理学通报, 2018, 34(6): 851-6. Zhao Y Z, Jiang J Z, Ye J, et al. Polydatin attenuates airway inflammation in asthmatic mouse model via p38 MAPK/Nrf 2 /HO-1 pathway[J]. Chin Pharmacol Bull, 2018, 34(6): 851-6. doi:10.3969/j.issn.1001-1978.2018.06.022 |
| [3] |
Kim S Y, Kim J D, Sol I S, et al. Sputum TWEAK expression correlates with severity and degree of control in non-eosinophilic childhood asthma[J]. Pediatr Allergy Immunol, 2018, 29(1): 42-9. doi:10.1111/pai.12827 |
| [4] |
Zhu C, Zhang L, Liu Z, et al. TWEAK/Fn14 interaction induces proliferation and migration in human airway smooth muscle cells via activating the NF-kappaB pathway[J]. J Cell Biochem, 2018, 119(4): 3528-36. doi:10.1002/jcb.26525 |
| [5] |
Macias M J, Martin-Malpartida P, Massagué J. Structural determinants of Smad function in TGF-β signaling[J]. Trends Biochem Sci, 2015, 40(6): 296-308. doi:10.1016/j.tibs.2015.03.012 |
| [6] |
Bruna A, Darken R S, Rojo F, et al. High TGFbeta-Smad activity confers poor prognosis in glioma patients and promotes cell proliferation depending on the methylation of the PDGF-B gene[J]. Cancer Cell, 2007, 11(2): 147-60. |
| [7] |
Shi Y, Massagué J. Mechanisms of TGF-beta signaling from cell membrane to the nucleus[J]. Cell, 2003, 113(6): 685-700. doi:10.1016/S0092-8674(03)00432-X |
| [8] |
Shin I S, Jeon W Y, Shin H K, et al. Effects of montelukast on subepithelial/peribronchial fibrosis in a murine model of ovalbumin induced chronic asthma[J]. Int Immunopharmacol, 2013, 17(3): 867-73. doi:10.1016/j.intimp.2013.09.017 |
| [9] |
Tang Y, Chen Y, Chu Z, et al. Protective effect of cryptotanshinone on lipopolysaccharide-induced acute lung injury in mice[J]. Eur J Pharmacol, 2014, 723: 494-500. doi:10.1016/j.ejphar.2013.10.019 |
| [10] |
Suh S J, Jin U H, Choi H J, et al. Cryptotanshinone from Salvia miltiorrhiza BUNGE has an inhibitory effect on TNF-alpha-induced matrix metalloproteinase-9 production and HASMC migration via dwmn-regulated NF-kappaB and AP-1[J]. Biochem Pharmacol, 2006, 72(12): 1680-9. doi:10.1016/j.bcp.2006.08.013 |
| [11] |
李良昌, 朴红梅, 延光海, 等. 芝麻素抗哮喘炎症作用研究[J]. 中国药理学通报, 2015, 31(3): 411-5. Li L C, Piao H M, Yan G H, et al. Sesamin attenuates inflammation response in a murine model of asthma[J]. Chin Pharmacol Bull, 2015, 31(3): 411-5. doi:10.3969/j.issn.1001-1978.2015.03.023 |
| [12] |
Jiang Y, You F, Zhu J, et al. Cryptotanshinone Ameliorates Radiation-Induced Lung Injury in Rats[J]. Evid Based Complement Alternat Med, 2019, 2019, 2019: 1908416. doi:10.1155/2019/1908416 |
| [13] |
Liu Q, Xiao S, Xia Y. TWEAK/Fn14 activation participates in skin inflammation[J]. Mediators Inflamm, 2017, 2017: 6746870. |
| [14] |
Wang Y, Wu C, Zhang C, et al. TGF-beta-induced STAT3 overexpression promotes human head and neck squamous cell carcinoma invasion and metastasis through malat1/miR-30a interactions[J]. Cancer Lett, 2018, 436: 52-62. doi:10.1016/j.canlet.2018.08.009 |
| [15] |
Shin D S, Kim H N, Shin K D, et al. Cryptotanshinone inhibits constitutive signal transducer and activator of transcription 3 function through blocking the dimerization in DU145 prostate cancer cells[J]. Cancer Res, 2009, 69(1): 193-202. doi:10.1158/0008-5472.CAN-08-2575 |