

2. 上海市第十人民医院中心实验室,上海 200072;
3. 上海市第十人民医院药学部,上海 200072;
4. 上海市第十人民医院崇明分院药剂科,上海 202157
2. Central Lab, Shanghai Tenth People′s Hospital, Shanghai 200072, China;
3. Dept of Pharmacy, Shanghai Tenth People′s Hospital, Shanghai 200072, China;
4. Dept of Pharmacy, Chongming Branch of Shanghai Tenth People′s Hospital, Shanghai 202157, China
胶质母细胞瘤(glioblastoma multiforme,GBM)是最具侵袭性的恶性原发性脑肿瘤,占原发性脑肿瘤的16%[1]。目前,GBM的标准治疗是手术配合放化疗,由于肿瘤所在位置及高侵袭性,手术难以完全切除[2]。替莫唑胺(temozolomide,TMZ)是GBM化疗的一线药物,主要通过使DNA甲基化而导致DNA错配修复系统失效,并最终导致肿瘤细胞死亡[3]。目前,GBM的治疗方法预后并不好,患者中位生存期只有15个月,仅有少部分存活达2.5年,5年生存率不到5%[1]。因此,GBM的治疗需要更加有效的方案。近来研究表明,胶质瘤细胞中多伴有磷脂酰肌醇-3-激酶(phosphatidylinositol 3-kinase,PI3K)/Akt通路过度活化,该通路的激活促进了胶质瘤细胞的侵袭、转移及耐药的产生[4]。PI3K抑制剂BKM120可通过下调PI3K/Akt通路表达,恢复GBM细胞对TMZ的敏感性,增强其疗效[5],提示该通路可作为GBM治疗的手段。
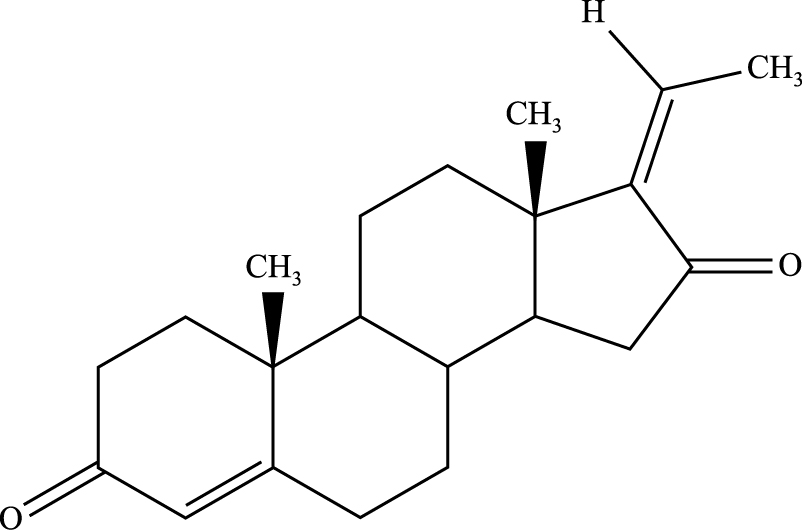
没药为橄榄科植物没药树的油胶树脂,没药甾酮(guggulsterone,GS)是没药中的主要活性成分,包含Z和E两种同分异构体[6]。目前研究表明,GS可通过抑制PI3K p85及Akt(Ser473)和(Thr308)位点磷酸化,抑制头颈癌细胞SCC4增殖,并诱导其凋亡[7]。但是GS对胶质瘤PI3K/Akt通路的调控作用,至今未有报道。我们前期研究发现,GS能增强化疗药物阿霉素对白血病细胞K562和乳腺癌细胞MCF-7的增殖抑制和凋亡诱导作用[8]。本文拟探讨Z-没药甾酮(Z-GS, 化学结构见Fig 1)能否通过下调PI3K/Akt通路,增强TMZ对人脑胶质瘤细胞的增殖抑制和凋亡诱导作用,为寻找新的GBM化疗方案提供理论依据。
|
| Fig 1 Chemical structure of Z-guggulsterone |
Z-没药甾酮(Z-GS), 购自美国Sigma公司,溶于DMSO,配成母液16 003 μmol·L-1;TMZ购自美国Sigma公司,溶于DMSO,配成母液51 506 μmol·L-1;CCK-8,购自日本同仁化学研究所;Hoechst 33342染料,购自上海碧云天生物技术公司;凋亡试剂盒,购自美国Invitrogen公司;PI3K、p-PI3K、Akt、p-Akt(Ser473)、p-Akt(Thr308)、Bcl-2、Bax、β-actin抗体,购自美国Cell Signaling Technology公司。
1.2 仪器Synergy2多功能酶标仪(美国BioTek公司);DMI 6000B倒置显微镜(德国Leica公司);FACSCanto Ⅱ流式细胞仪(美国BD公司);Odyssey双色红外激光成像系统(美国LI-COR公司)。
2 方法 2.1 细胞培养与药物处理人胶质瘤细胞U251,购自中国科学院上海细胞库。用含有10%胎牛血清、100 μmol·L-1青霉素和链霉素的DMEM培养液(美国Gibco公司),在5% CO2、37 ℃条件下培养。当细胞长至培养皿底部80%时,用胰酶消化并接种至孔板中,待细胞长至孔板底部80%时,弃去旧培养液,分组加入含不同浓度药物的完全培养液。
2.2 CCK-8法检测细胞增殖取对数生长期细胞接种于96孔板中,每孔细胞量为1×104,每孔液体量为100 μL。Z-GS和TMZ单药处理的药物浓度梯度均为1、3、10、30、100、200、400 μmol·L-1;Z-GS与TMZ联合使用中,TMZ(1、3、10、30、100、200、400 μmol·L-1)分别与30 μmol·L-1 Z-GS联合使用,每个浓度3个复孔。细胞经药物处理12、24、48 h后,加入10% CCK-8试剂,于培养箱中反应2 h,用酶标仪测450 nm处OD值。每组实验重复4次。使用公式:存活率/%=OD实验组平均值/OD对照组平均值×100%,计算细胞存活率。
2.3 合用指数(combination index, CI)计算使用Excel 2016软件,得到GS和TMZ单药的拟合量效曲线及函数方程。使用公式CI=DA, x/DB, x+ICx, A/ICx, B计算CI,其中DA, x和DB, x为两药联用达到x效应时两药的浓度,ICx, A和ICx, B为两药单独使用时达到x效应所需的浓度。CI < 1表示两药协同,CI=1表示两药相加,CI> 1表示两药拮抗[9]。
2.4 Hoechst 33342染色取对数生长期细胞接种于6孔板中,每孔细胞量为3×105,每孔液体量为2 mL。用Z-GS(30 μmol·L-1)和TMZ(400 μmol·L-1)单药及两药联合处理细胞24 h。弃培养液,每孔加Hoechst 33342试剂1 mL,置于培养箱中30 min,弃染料,PBS洗3遍,使用倒置荧光相差显微图像系统观察并采集图像。
2.5 流式细胞术检测细胞凋亡取对数生长期细胞接种于6孔板中,每孔细胞量为3×105,每孔液体量为2 mL。用Z-GS(30 μmol·L-1)和TMZ(400 μmol·L-1)单药及两药联合处理细胞。药物处理细胞24 h后分别收集细胞和上清液,PBS洗2次,胰酶消化,与之前收集的上清液混合,细胞悬液1 000 r·min-1离心5 min,弃上清,PBS重悬,1 000 r·min-1离心5 min,弃上清,加入1×binding buffer 50 μL重悬,再加入Annexin V-FITC 5 μL,避光反应15 min,加入PI 5 μL,5 min后加入1×binding buffer 300 μL混匀,使用流式细胞仪检测,使用FACSDIVA软件分析。实验重复3次。
2.6 Western blot检测蛋白表达取对数生长期细胞接种于6孔板中,每孔细胞量为3×105,每孔液体量为3 mL。用Z-GS单药(30 μmol·L-1)、TMZ单药(400 μmol·L-1)及两药联合处理细胞,24 h后提取蛋白。BCA法测定样品蛋白浓度,上样量为50 μg。样品经SDS-PAGE电泳分离,之后转移至NC膜上,用5% BSA室温下在摇床上封闭1 h,用封闭液稀释抗体(β-actin抗体按1 :5 000稀释,其余一抗按1 :1 000稀释),一抗4 ℃过夜孵育,之后用PBST洗膜3次,每次10 min,二抗室温下避光孵育1 h,PBST洗膜3次,每次10 min,用Odyssey红外激光成像系统采集图片,用Odyssey软件分析图像。实验重复3次。
2.7 统计学分析使用SPSS 17.0软件进行数据分析。组间均数比较采用两独立样本t检验。
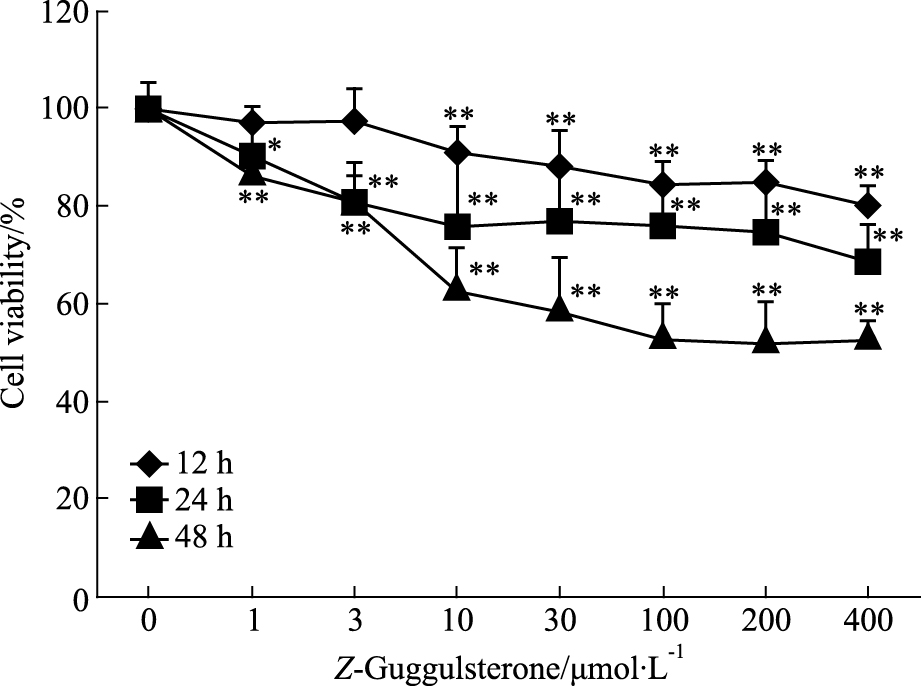
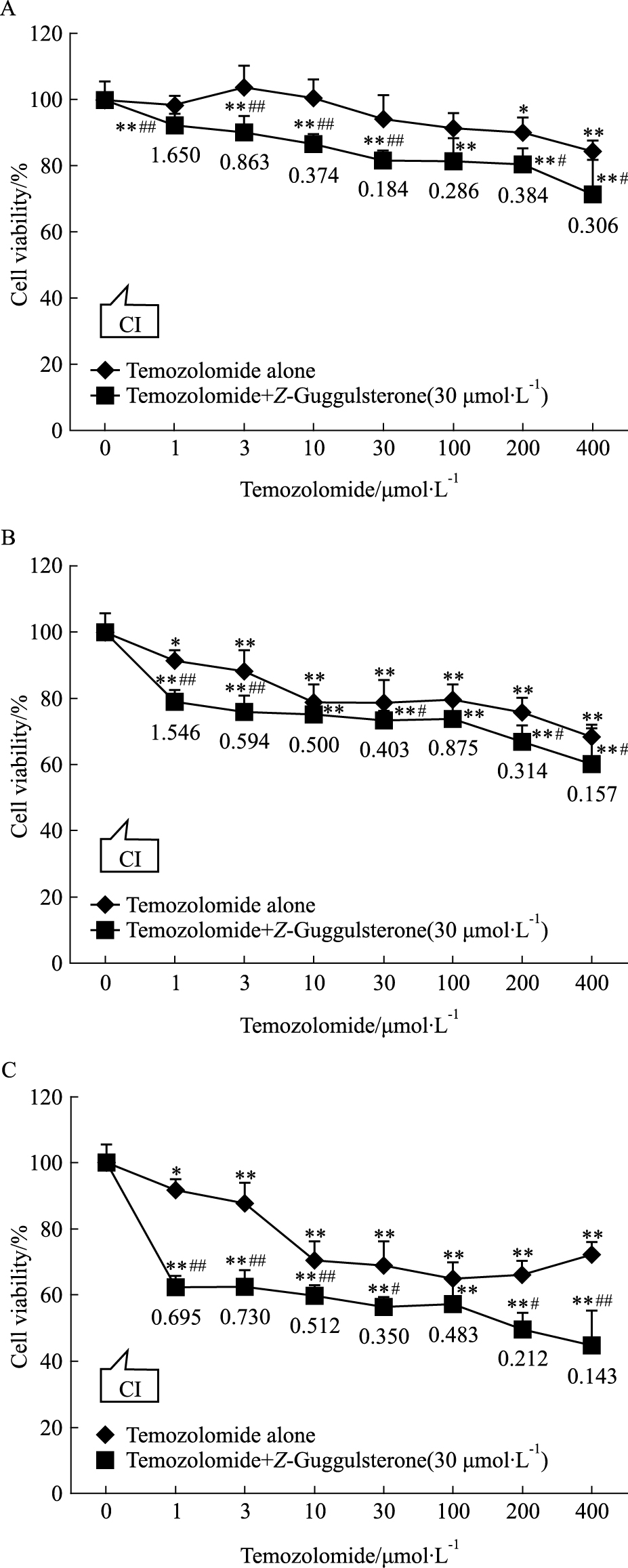
3 结果 3.1 Z-GS、TMZ及两药联合对U251细胞增殖的影响Fig 2、3结果显示,Z-GS和TMZ对U251细胞的增殖抑制作用呈时间及浓度依赖性。与TMZ单药组相比,GS联合TMZ能明显增强对U251细胞的增殖抑制作用。
|
| Fig 2 Effects of Z-guggulsterone on proliferation in U251 cells(x±s,n=4) U251 cells were treated with Z-guggulsterone(1~400 μmol·L-1) for 12 h, 24 h or 48 h as determined by CCK-8.*P<0.05, **P<0.01 vs control. |
|
| Fig 3 Effects of temozolomide or temozolomide combined with Z-guggulsterone on proliferation of U251 cells(x±s,n=4) U251 cells were treated with temozolomide(1~400 μmol·L-1) alone or in combination with Z-guggulsterone(30 μmol·L-1) for 12 h(A), 24 h(B) or 48 h(C) as determined by CCK-8.*P<0.05, **P<0.01 vs control; #P<0.05, ##P<0.01 vs TMZ alone at the same concentration. |
Fig 4结果显示,与对照组相比,Z-GS单独给药组细胞凋亡率为(5.3±1.0)%,TMZ单独给药组细胞凋亡率为(12.7±1.7)%;与TMZ单独给药组相比,联合给药能明显增强对U251细胞凋亡诱导作用,凋亡率上调至(29.5±4.3)%(P<0.01)。

|
| Fig 4 Z-Guggulsterone increased temozolomide-induced apoptosis in U251 cells(x±s,n=4) U251 cells were treated with Z-guggulsterone(30 μmol·L-1) and temozolomide(400 μmol·L-1) alone or in combination for 24 h. A:Nuclear morphology of U251 cells stained with Hoechst 33342; B: Flow cytometric analyses of Annexin V-FITC/PI double staining; C: Apoptosis rate from flow cytometer analysis.**P<0.01 vs control; ##P<0.01 vs TMZ. |
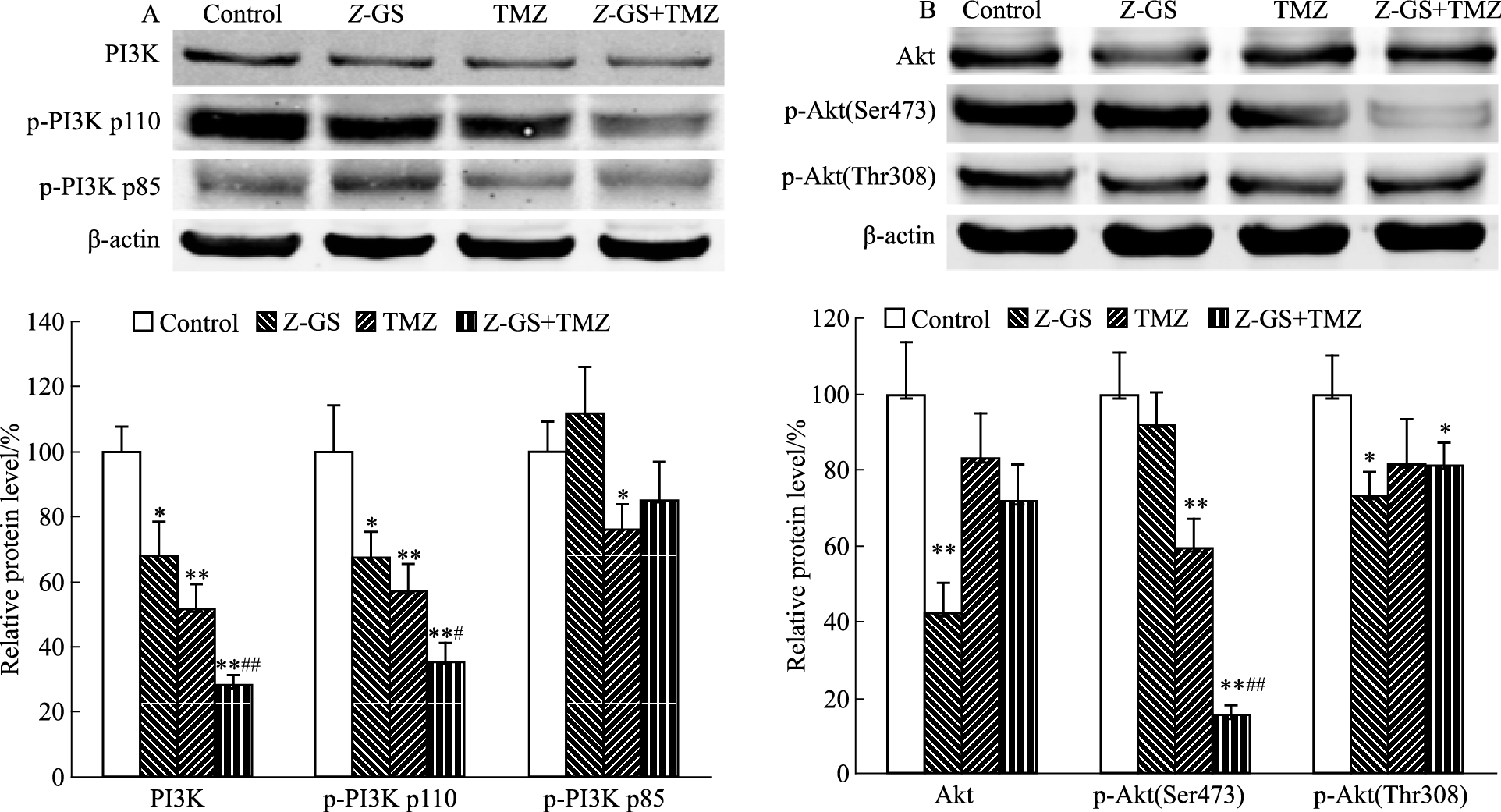
Fig 5结果显示,与对照组相比,Z-GS单独给药组明显下调了PI3K、p-PI3K p110、Akt和p-Akt(Thr308)表达,TMZ单独给药组明显下调了PI3K、p-PI3K p110、p-PI3K p85和p-Akt(Ser473)表达;与TMZ单独给药组相比,联合给药明显下调了PI3K、p-PI3K p110和p-Akt(Ser473)表达。
|
| Fig 5 Effects of Z-GS and TMZ on expression of PI3K, p-PI3K p110, p-PI3K p85(A) and Akt, p-Akt(Ser473), p-Akt(Thr308)(B) in U251 cells(x±s,n=3) U251 cells were treated with Z-GS(30 μmol·L-1) and TMZ(400 μmol·L-1) alone or in combination for 24 h.*P<0.05, **P<0.01 vs control, #P<0.05, ##P<0.01 vs TMZ. |
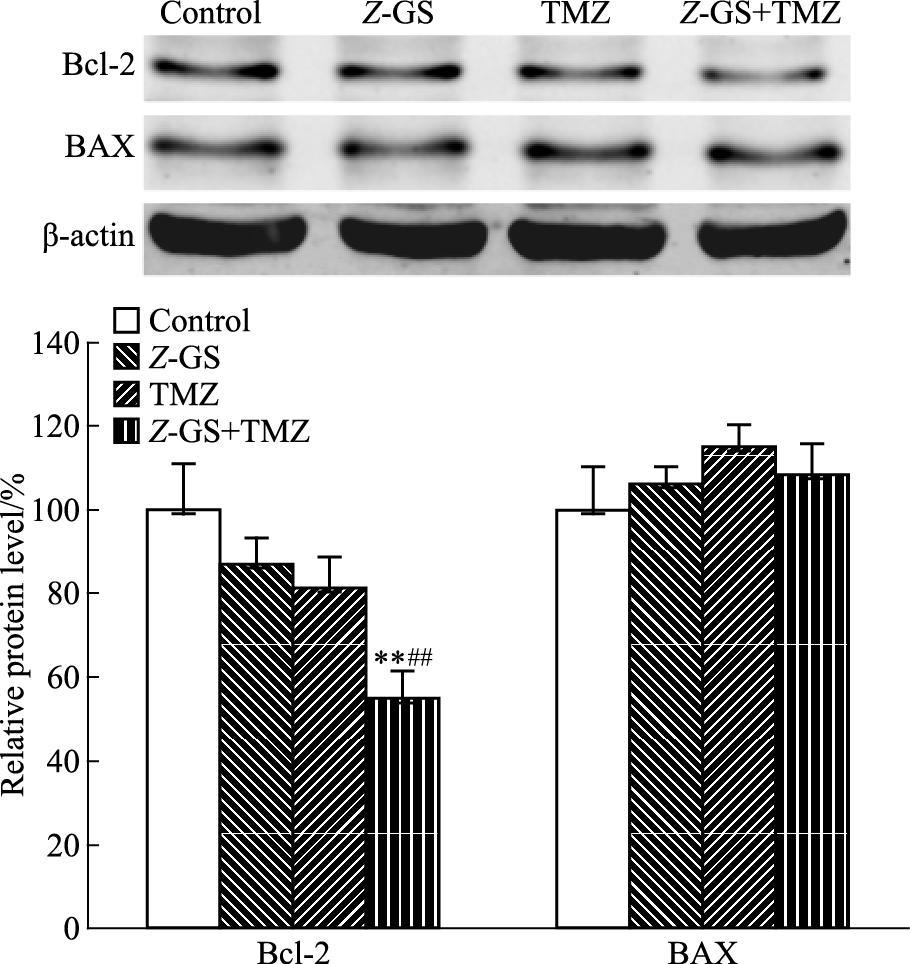
Fig 6结果显示,与对照组相比,两药单独给药对Bcl-2和Bax表达影响均无统计学差异(P>0.05);与TMZ单独给药组相比,联合用药明显下调了Bcl-2表达(P<0.01)。
|
| Fig 6 Effects of Z-GS and TMZ on expressions of Bcl-2 and Bax in U251 cells(x±s,n=3) U251 cells were treated with Z-GS(30 μmol·L-1) and TMZ(400 μmol·L-1) alone or in combination for 24 h.**P<0.01 vs control, ##P<0.01 vs TMZ. |
本实验结果显示,与TMZ单独给药相比,Z-GS能增强TMZ对U251细胞的增殖抑制和凋亡诱导作用。进一步研究显示,与TMZ单独给药相比,GS能明显下调PI3K、p-PI3K p110、p-Akt(Ser473)和Bcl-2的表达。研究结果表明,没药甾酮可通过下调PI3K/Akt通路,增强替莫唑胺对人脑胶质瘤细胞U251的增殖抑制作用。
PI3K由催化亚基p110和调节亚基p85组成,p85与效应物结合后释放出p110,p110将磷脂酰肌醇二磷酸(phosphatidy-linositol-3, 4-bisphosphate,PIP2)磷酸化为磷脂酰肌醇三磷酸(phosphatidy-linositol-3, 4, 5-bisphosphate,PIP3),PIP3招募Akt,并使其Thr308和Ser473位点磷酸化[10]。其中,Thr308残基位于Akt的核心,其磷酸化为Akt活化所必需,Ser473残基的磷酸化能稳定Thr308磷酸化和Akt活化状态,使Akt活性最大化[11]。Akt可以激活下游的目的蛋白,如核转录因子κB(nuclear factor-kappa B,NF-κB)、mTOR等,从而促进细胞增殖[12]。Chen等[13]研究发现,PI3K抑制剂LY294002能抑制脑胶质瘤U87细胞中PI3K和p-Akt水平,与TMZ联用,增强其对U87细胞的增殖抑制作用。Mao等[5]研究发现,PI3K抑制剂BKM120也能通过下调PI3K、p-Akt,恢复胶质瘤细胞C6对TMZ的敏感性。还有研究表明,通过抑制Akt下游的NF-κB,也可促进胶质瘤细胞凋亡[14]。本研究发现,Z-GS通过下调PI3K、p-PI3K p110和p-Akt(Ser473)表达,增强TMZ对U251细胞的增殖抑制和凋亡诱导作用。
磷酸化的Akt可通过磷酸化BAD,释放出Bcl-2,抑制细胞凋亡[15]。Chen等[13]研究发现,与单独使用TMZ相比,PI3K抑制剂LY294002联合TMZ可明显下调脑胶质瘤U87细胞中Bcl-2的表达,同时上调Bax表达。Mao等[5]研究发现,与单独使用TMZ相比,PI3K抑制剂BKM120联合TMZ可明显上调脑胶质瘤C6细胞中Bax表达。本研究发现,与单独使用TMZ相比,Z-GS联合TMZ可明显下调脑胶质瘤U251细胞中Bcl-2的表达。
TMZ作为GBM的一线化疗药物,其单独使用的疗效并不令人满意,本实验结果表明,Z-GS有望改善TMZ的疗效,具有与TMZ联合用于GBM治疗的应用前景。但Z-GS对胶质瘤PI3K/Akt通路影响及联合作用机制,仍需要进一步的研究,今后还将开展体内实验,为Z-GS用于GBM治疗提供依据。
( 致谢: 本实验在上海市第十人民医院中心实验室完成,感谢各位老师的帮助。)
| [1] |
Vleeschouwer S D. Epidemiology and outcome of glioblastoma[M]//Tamimi A F, Juweid M. GLIOBLASTOMA. Brisbane: Codon Publications, 2017: 143-53.
|
| [2] |
Paolillo M, Boselli C, Schinelli S. Glioblastoma under Siege: an overview of current therapeutic strategies[J]. Brain Sci, 2018, 8(1): 8010015. |
| [3] |
Ohba S, Hirose Y. Current and future drug treatments for glioblastomas[J]. Curr Med Chem, 2016, 23(38): 4309-16. doi:10.2174/0929867323666161014132907 |
| [4] |
Ji C, Guo H, Zhang P, et al. AnnexinA5 promote glioma cell invasion and migration via the PI3K/Akt/NF-κB signaling pathway[J]. J Neuro-oncology, 2018, 138(3): 469-78. doi:10.1007/s11060-018-2818-4 |
| [5] |
Mao L, Ruo F L, Xiang W, et al. BKM120 sensitizes C6 glioma cells to temozolomide via suppression of the PI3K/Akt/NF-κB/MGMT signaling pathway[J]. Oncol Lett, 2017, 14(6): 6597-603. |
| [6] |
Yamada T, Sugimoto K. Guggulsterone and its role in chronic diseases[J]. Adv Exp Med Biol, 2016, 929: 329-61. |
| [7] |
Macha M A, Matta A, Chauhan S S, et al. Guggulsterone targets smokeless tobacco induced PI3K/Akt pathway in head and neck cancer cells[J]. PLoS One, 2011, 6(2): e14728. doi:10.1371/journal.pone.0014728 |
| [8] |
Xu H B, Xu L Z, Li L, et al. Reversion of P-glycoprotein-mediated multidrug resistance by guggulsterone in multidrug-resistant human cancer cell lines[J]. Eur J Pharmacol, 2012, 694(1): 39-44. |
| [9] |
Zhao L, Au J L, Wientjes M G, et al. Comparison of methods for evaluating drug-drug interaction[J]. Front Biosci, 2010, 2(1): 241-9. |
| [10] |
Li X, Wu C, Chen N, et al. PI3K/Akt/mTOR signaling pathway and targeted therapy for glioblastoma[J]. Oncotarget, 2016, 7(22): 33440-50. |
| [11] |
Manning B D, Toker A. AKT/PKB signaling: navigating the network[J]. Cell, 2017, 169(3): 381-405. doi:10.1016/j.cell.2017.04.001 |
| [12] |
Caporali S, Levati L, Graziani G, et al. NF-κB is activated in response to temozolomide in an AKT-dependent manner and confers protection against the growth suppressive effect of the drug[J]. J Transl Med, 2012, 10(1): 252. doi:10.1186/1479-5876-10-252 |
| [13] |
Chen L, Han L, Shi Z, et al. LY294002 enhances cytotoxicity of temozolomide in glioma by down-regulation of the PI3K/Akt pathway[J]. Mol Med Rep, 2011, 5(2): 575-9. |
| [14] |
杨秀伟, 谢靖, 钟凤, 等. 左卡尼汀抑制NF-κB敏化TRAIL诱导神经胶质瘤细胞凋亡[J]. 中国药理学通报, 2016, 32(5): 664-70. Yang X W, Xie J, Zhong F, et al. L-carnitine sensitizes human glioblastoma cells to TRAIL-induced apoptosis[J]. Chin Pharmacol Bull, 2016, 32(5): 664-70. |
| [15] |
Abeyrathna P, Su Y. The critical role of Akt in cardiovascular function[J]. Vascul Pharmacol, 2015, 74: 38-48. doi:10.1016/j.vph.2015.05.008 |

