

2. 广州中医药大学第二临床医学院 珠海医院药剂科,广东 广州 510120
2. Pharmacy Dept of Zhuhai Hospital, Second Clinical Medical College Affiliated to Guangzhou University of Chinese Medicine, Guangzhou 510120, China
士的宁(strychnine,STR)和马钱子碱(brucine,BRU)作为中药马钱子的主要药效生物碱成分,具有明显的镇痛[1-2]、抗炎[3-4]、抗肿瘤[5-7]、中枢神经系统兴奋[8-9]等多种药理活性。研究表明,其代谢产物士的宁氮氧化物(strychnine N-oxide,SNO)和马钱子碱氮氧化物(brucine N-oxide,BNO)的毒性比原型物大大降低,且具有较好的生物活性。目前,关于4种成分的组织测定方法主要包括高效液相色谱法(HPLC),但存在分析时间长、灵敏度较低、专属性和特异性不强等缺点[10-11]。本研究旨在建立快速、灵敏、准确的液相色谱-质谱联用法(LC-MS/MS),同时测定大鼠组织中STR、BRU、SNO和BNO的含量,比较正常和毒性剂量马钱子总碱给药后,4种成分的组织分布情况,为其在生物体内的代谢动力学研究提供测定方法,并为其毒性机制和药理作用研究等提供更准确、可靠的科学依据。
1 材料 1.1 药品与试剂士的宁对照品(批号131030)、马钱子碱对照品(批号131040),成都普菲德生物技术有限公司;士的宁氮氧化物对照品(批号S450162)、马钱子碱氮氧化物对照品(批号S450142),Sigma-Aldrich公司;盐酸麻黄碱对照品(批号0714-9402),中国药品生物制品检定所,对照品纯度均>98%。乙醇为分析纯;甲酸、乙酸铵、甲醇,均为HPLC色谱纯;水为Milli-Q超纯水;马钱子总碱由南京中医药大学药剂实验室馈赠,其中士的宁占33.33%,马钱子碱占21.28%。
1.2 仪器SHIMADZULC-20A高效液相色谱(日本岛津公司);API4000+型液相色谱-三重四级杆质谱联用仪(LC-MS/MS),配备Turbo Ionspray离子源(ESI)及Analyst 1.6数据处理系统(美国AB Sciex公司);Thermo SPD121P P1真空离心浓缩仪(美国Thermo Fisher公司);BF2000-30A氮气吹干仪(北京八方世纪科技有限公司);Microfuge 16台式微量离心机(美国Beckman Coulter公司)。
1.3 实验动物SPF级SD大鼠,♂,体质量(225±25)g,购于广东省医学实验动物中心,合格证号:(粤)44007200008985。实验前禁食12 h以上,自由饮水。
2 方法 2.1 色谱与质谱条件色谱条件:色谱柱为ZORBAX Eclipse XDB-C18柱(2.1 mm×150 mm,3.5 μm);流动相A为10 mmol·L-1乙酸铵(用甲酸调pH 4.0),流动相B为甲醇,梯度洗脱:B相0~1 min,5%;1~6.5 min, 5%~70%;6.5~7.5 min,70%;7.5~7.6 min,70%~5%;7.6~11 min,5%,流速0.2 mL·min-1;柱温30 ℃,进样量5 μL。
质谱条件:电喷雾ESI离子源,检测方式为正离子多离子反应检测(MRM);喷雾电压为5500 V;雾化温度为350 ℃。其他质谱参数设置分别为:碰撞气(CAD)12 psi;雾化气(GAS1)20 psi;帘气(CUR)40 psi;用于定量分析的离子对分别为m/z 335.3→184.1(士的宁),395.3→324.3(马钱子碱), 351.4→334.1(士的宁氮氧化物),411.2→394.2 (马钱子碱氮氧化物),166.2→148.3(内标盐酸麻黄碱)。
2.2 溶液的制备分别精密称取STR、BRU、SNO和BNO 1.05 mg、1.17 mg、1.06 mg和1.17 mg,甲醇溶解,配成浓度分别为105、117、106、117 mg·L-1的储备液。精密称取盐酸麻黄碱(IS)1.39 mg,甲醇溶解,得到终浓度为139 μg·L-1的内标工作液。精密称取适量马钱子总碱,PBS :乙醇=80 :20溶解,配成浓度0.3 g·L-1的溶液。以上溶液均于4 ℃冷藏备用。
2.3 组织匀浆样本处理各组织样品称重,以质量体积比1 :3的比例加入超纯水,匀浆。精密移取内标工作液(139 μg·L-1)20 μL,常温真空浓缩后加入组织匀浆200 μL,震荡涡旋30 s混匀,加入40 μL氨水碱化,涡旋30 s,加入4 mL氯仿,充分涡旋2 min,3 750 r·min-1离心10 min,取下层有机相于35 ℃下N2吹干,使用200 μL流动相[甲醇:10 mmol·L-1乙酸铵(用甲酸调pH 4.0)=40 :60]复溶,涡旋2 min,14 000 r·min-1离心15 min,过滤,取上清液进行分析,进样量5 μL。
2.4 给药与组织样品采集SD大鼠随机分为正常和毒性剂量组,每组25只。每组大鼠按时间点随机分成5组,每个时间点5只。正常和毒性剂量组分别灌胃马钱子总碱溶液1.2 mg·kg-1(STR 0.4 mg·kg-1,BRU 0.2554 mg·kg-1)和3.0 mg·kg-1(STR 1 mg·kg-1,BRU 0.6385 mg·kg-1),分别于给药后5、15、30、60、120 min麻醉,分离心、肝、脾、肺、肾和脑,脏器用超纯水洗净,滤纸吸干,于-80 ℃保存。
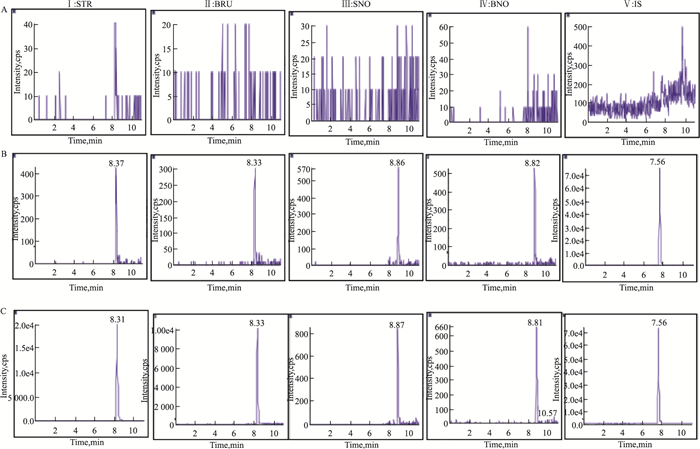
3 结果 3.1 专属性分别取来自6只大鼠的空白肾组织匀浆(以肾组织为代表),空白肾组织匀浆加4种待测物和内标,以及大鼠灌胃给药后的肾组织匀浆样品,按照“2.3”项下操作,在选定的检测条件下考察5种分析成分。Fig 1结果显示,STR、BRU、SNO、BNO和内标的保留时间分别为8.31、8.33、8.86、8.82、7.56 min,组织中内源性物质不会对待测成分产生干扰,峰形良好。
|
| Fig 1 Representative MRM chromatograms A: Blank kidney homogenate; B: Blank kidney homogenate spiked with analytes and IS; C: Kidney homogenate obtained from a rat after intragastric administration of Semen Strychni total alkaloids. |
分别精密吸取适量STR、BRU、SNO和BNO储备液,用甲醇逐级稀释成系列标样,精密吸取200 μL标样,真空浓缩,分别加入到200 μL空白大鼠组织匀浆中,按“2.3”项下操作,分别以STR、BRU、SNO和BNO与内标盐酸麻黄碱的峰面积比值对各自相应的浓度进行加权(1/X2)线性回归。定量下限(LLOQ)为标准曲线的最低浓度。所得回归方程及定量下限见Tab 1,各成分在测定范围内线性关系良好。
| Tissue | Analyte | Calibration curve | r | Linear range/μg·L-1 | LLOQ/μg·L-1 |
| Kidney | STR | Y=3.12×10-3X+3.77×10-4 | 0.9960 | 1.02-450 | 1.02 |
| BRU | Y=2.63×10-3X+1.81×10-3 | 0.9945 | 1.02-451 | 1.02 | |
| SNO | Y=3.83×10-3X+7.97×10-4 | 0.9990 | 0.307-135 | 0.306 | |
| BNO | Y=1.42×10-2X+1.39×10-3 | 0.9977 | 0.307-135 | 0.306 | |
| Liver | STR | Y=5.88×10-3X+1.65×10-3 | 0.9942 | 1.02-450 | 1.02 |
| BRU | Y=2.94×10-3X+2.36×10-3 | 0.9959 | 1.02-451 | 1.02 | |
| SNO | Y=1.3×10-3X+1.13×10-3 | 0.9969 | 0.307-135 | 0.306 | |
| BNO | Y=6.78×10-3X+1.99×10-3 | 0.9968 | 0.307-135 | 0.306 | |
| Heart | STR | Y=2.76×10-3X+1.15×10-3 | 0.9974 | 1.02-450 | 1.02 |
| BRU | Y=1.26×10-3X+1.03×10-3 | 0.9986 | 1.02-451 | 1.02 | |
| SNO | Y=2.9×10-3X+5.61×10-4 | 0.9986 | 0.307-135 | 0.306 | |
| BNO | Y=1.23×10-2X+2.18×10-3 | 0.9990 | 0.307-135 | 0.306 | |
| Lung | STR | Y=3.16×10-3X+1.68×10-3 | 0.9985 | 1.02-450 | 1.02 |
| BRU | Y=1.42×10-3X+1.02×10-3 | 0.9948 | 1.02-451 | 1.02 | |
| SNO | Y=3.44×10-3X+1.12×10-3 | 0.9940 | 0.307-135 | 0.306 | |
| BNO | Y=1.25×10-2X+4.6×10-4 | 0.9994 | 0.307-135 | 0.306 | |
| Spleen | STR | Y=3.15×10-3X+9.76×10-4 | 0.9968 | 1.02-450 | 1.02 |
| BRU | Y=1.38×10-3X+1.21×10-3 | 0.9966 | 1.02-451 | 1.02 | |
| SNO | Y=3.19×10-3X+4.59×10-4 | 0.9990 | 0.307-135 | 0.306 | |
| BNO | Y=1.33×10-2X+1.44×10-3 | 0.9987 | 0.307-135 | 0.306 | |
| Brain | STR | Y=3.19×10-3X+2.44×10-3 | 0.9996 | 1.02-450 | 1.02 |
| BRU | Y=1.46×10-3X+1.61×10-3 | 0.9939 | 1.02-451 | 1.02 | |
| SNO | Y=3.49×10-3X+1.13×10-3 | 0.9987 | 0.307-135 | 0.306 | |
| BNO | Y=1.45×10-2X+3.71×10-3 | 0.9975 | 0.307-135 | 0.306 |
分别配制低、中、高浓度的质控样品:STR 3.00、30.03、390.39 μg·L-1,BRU 3.01、30.10、390.90 μg·L-1,SNO 0.901、9.01、117.13 μg·L-1,BNO 0.901、9.01、117.12 μg·L-1,按“2.3”项下操作,每个质量浓度平行5份,连续测定3 d,以当天随行的标准曲线测定质控样品浓度。结果显示,心、肝、脾、肺、肾、脑组织中的相对回收率和日内、日间精密度分别为STR:(87.66±1.01)%~(112.51±3.40)%、2.13%~9.31%、1.29%~14.70%;BRU:(87.16±1.07)%~(110.49±1.74)%、2.83%~9.36%、1.34%~14.13%;SNO:(86.84±1.71)%~(113.77±5.19)%、2.14%~10.02%、0.34%~14.90%;BNO:(85.94±1.43)%~(113.29±5.46)%、2.05%~9.31%、0.90%~14.30%。均符合生物样品分析的方法学要求。
3.4 提取回收率及基质效应按“3.3”项下操作,配制低、中、高3个浓度水平的STR、BRU、SNO、BNO组织质控样品(以肾组织为代表),每个浓度平行操作5份,按“2.3”所述操作,进样考察,峰面积记作A1;取空白组织匀浆同样操作,N2吹干后残渣分别加入相应低、中、高浓度的对照品溶液复溶,进样考察,峰面积记作A2,以A1/A2×100%为提取回收率(Tab 2)。分别配制含有低、中、高浓度STR、BRU、SNO、BNO的混合标准品溶液,直接进样,峰面积记作A3,以A2/A3×100%为基质效应,见Tab 2。
| Analyte | Added concentration/μg·L-1 | Recovery/% | RSD/% | Matrix effect/% | RSD/% |
| STR | 3 | 98.80±11.29 | 11.40 | 110.00±10.29 | 9.39 |
| 30 | 95.80±11.94 | 12.50 | 99.80±4.27 | 4.27 | |
| 390 | 110.00±6.48 | 5.88 | 93.70±4.51 | 4.81 | |
| BRU | 3.01 | 96.50±7.83 | 8.11 | 105.00±7.54 | 7.21 |
| 30.1 | 93.70±9.17 | 9.79 | 102.00±3.34 | 3.28 | |
| 391 | 105.00±9.85 | 9.40 | 98.40±7.94 | 8.07 | |
| SNO | 0.9 | 81.60±4.03 | 4.94 | 98.80±7.83 | 7.93 |
| 9 | 79.20±8.54 | 10.80 | 98.00±6.74 | 6.88 | |
| 117 | 79.80±8.04 | 10.10 | 94.20±4.84 | 5.14 | |
| BNO | 0.9 | 86.50±6.43 | 7.43 | 98.70±1.16 | 1.18 |
| 9 | 84.90±6.13 | 7.23 | 103.00±4.12 | 4.02 | |
| 117 | 85.50±7.79 | 9.11 | 98.70±5.86 | 5.94 |
按“3.3”项下操作,配制低、中、高3个浓度STR、BRU、SNO、BNO的质控样品(以肾组织为代表),每个浓度5个样本,分别考察样品在室温放置4 h,反复冻融3次,以及制备好的待测液4 ℃放置12 h条件下的稳定性。Tab 3结果表明,4种成分在上述条件下均较为稳定。
| Analyte | Added concentration/μg·L-1 | Accuracy/% | ||
| Short-term stability(4 h) | Three freeze-thaw cycles stability | Autosampler stability(4 ℃,12 h) | ||
| STR | 3 | 99.67±8.86 | 95.57±6.64 | 102.00±3.88 |
| 30 | 109.21±2.22 | 106.10±2.36 | 110.60±2.77 | |
| 390 | 98.67±3.39 | 98.67±0.61 | 90.93±1.80 | |
| BRU | 3.01 | 90.76±10.51 | 92.06±7.27 | 108.47±7.17 |
| 30.1 | 111.11±2.05 | 106.24±2.59 | 108.49±2.26 | |
| 391 | 98.16±3.15 | 99.63±1.54 | 91.35±2.09 | |
| SNO | 0.9 | 109.88±6.11 | 106.66±7.74 | 106.88±2.02 |
| 9 | 103.28±1.77 | 103.27±3.41 | 110.18±3.23 | |
| 117 | 92.45±3.25 | 97.88±1.93 | 96.75±3.17 | |
| BNO | 0.9 | 110.08±6.38 | 110.81±3.86 | 108.89±7.03 |
| 9 | 101.45±2.52 | 100.58±2.15 | 108.80±3.28 | |
| 117 | 89.13±2.19 | 93.22±0.81 | 95.89±1.66 | |
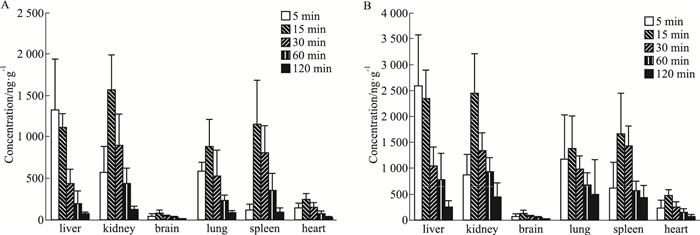
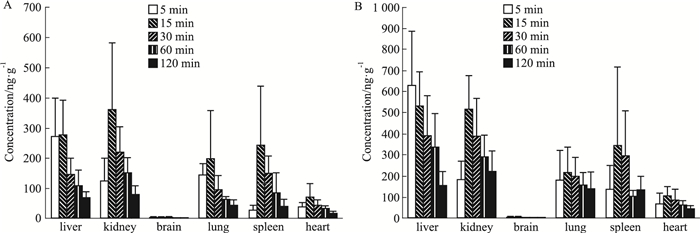
大鼠单次灌胃马钱子总碱溶液正常和中毒剂量后,正常剂量组STR在各组织中含量排列顺序为:肾>脾>肝>肺>心>脑(Fig 2A),毒性剂量组的顺序依次为:肾>肝>肺>脾>心>脑(Fig 2B);正常剂量组BRU含量依次为(Fig 3A):肾>肝>脾>肺>心>脑,毒性剂量组的含量依次为:肝>肾>脾>肺>心>脑(Fig 3B);正常剂量和毒性剂量组SNO含量依次为:脾>肝>肾>肺(Fig 4)。代谢产物BNO浓度低于定量限。
|
| Fig 2 Tissue distribution of strychnine in rats following single intragastric administration of total alkaloids from Semen Strychni(x±s, n=5) A:Normal dose; B: Toxic dose. |
|
| Fig 3 Tissue distribution of brucine in rats following single intragastric administration of total alkaloids from Semen Strychni(x±s, n=5) A: Normal dose; B: Toxic dose. |

|
| Fig 4 Tissue distribution of strychnine N-oxide in rats following single intragastric administration of total alkaloids from Semen Strychni(x±s, n=5) A: Normal dose; B: Toxic dose. |
本文建立了LC-MS/MS同时测定大鼠心、肝、脾、肺、肾、脑组织中马钱子碱、士的宁及其氮氧化物含量的分析方法,以10 mmol·L-1乙酸铵(用甲酸调pH=4.0)-甲醇为流动相进行梯度洗脱,内源性杂质干扰小,峰形对称,分离度好;采用正离子多离子反应检测,质谱响应及灵敏度高。在样品前处理条件优化过程中,比较了不同处理方法(甲醇沉淀法、氯仿液液萃取法),并进一步考察了氯仿多步和一步液液萃取,及氯仿体积(3、4 mL)对4种待测物提取回收率的影响。另外,由于马钱子碱和士的宁均为碱性药物成分,因此,采用氨水碱化生物样品[12],提高提取效率。
组织分布结果显示,正常和毒性马钱子总碱剂量下,STR和BRU在大鼠主要脏器中分布相似,其中以肝脏和肾脏最高,脾脏浓度也较高,脑中的分布量最少。提示STR和BRU可能存在肝脏的代谢或胆汁排泄;肾脏很可能是其主要的排泄途径;脾脏浓度较高,推测这与其具有免疫调节的作用可能有关;STR和BRU均能透过血脑屏障,但透过能力有限。
两种剂量给药后,SNO在主要脏器中均能检出(脑、心除外),但是浓度较低,远低于STR原型物,说明在体内STR确实可转化成SNO,但STR可能不是以SNO的形式在体内蓄积。BRU在体内可代谢成BNO[13-14],本实验仅在毒性剂量给药后的个别肝脏样品中测到,但测得的BNO浓度低于定量下限。
综上所述,本研究建立了灵敏、快速和准确的LC-MS/MS法测定STR、BRU、SNO和BNO,基于该法比较了正常和毒性剂量马钱子总碱给药后,4种成分在大鼠组织中的分布特征,为其在生物体内的代谢动力学研究奠定了基础,并对阐明其药理毒理机制有重要意义。
| [1] |
李阿荣, 刘若轩, 邓志军, 等. 人尿苷二磷酸葡糖醛酸转移酶参与马钱子碱和士的宁体外代谢研究[J]. 中药新药与临床药理, 2018, 29(6): 780-4. Li A R, Liu R X, Deng Z J, et al. Identification of UDP-glucuronosyltransferase isoforms responsible for strychnine and brucine metabolism in vitro[J]. Tradit Clin Drug Res Clin Pharmacol, 2018, 29(6): 780-4. |
| [2] |
唐敏, 伍冠一, 朱婵, 等. 马钱子碱镇痛研究进展[J]. 中草药, 2014, 45(12): 1791-5. Tang M, Wu G Y, Zhu C, et al. Research progress on analgesic properties of brucine[J]. Chin Tradit Herb Drugs, 2014, 45(12): 1791-5. doi:10.7501/j.issn.0253-2670.2014.12.027 |
| [3] |
邓向涛, 阮晓东, 郝海军. 马钱子碱固体脂质纳米粒凝胶骨架缓释片的研制[J]. 中草药, 2018, 49(22): 5298-304. Deng X T, Ruan X D, Hao H j. Study on matrix sustained release tablets of brucine solid lipid nanoparticles[J]. Chin Tradit Herb Drugs, 2018, 49(22): 5298-304. doi:10.7501/j.issn.0253-2670.2018.22.012 |
| [4] |
管庆霞, 张悦, 邹淑君, 等. 马钱子碱及其纳米结构脂质载体在大鼠体内的药动学比较研究[J]. 中国药房, 2018, 29(20): 2777-81. Guan Q X, Zhang Y, Zou S J, et al. Comparative study on pharmacokinetics of brucine and its nanostructure lipid carrier in rats[J]. Chin Pharm, 2018, 29(20): 2777-81. doi:10.6039/j.issn.1001-0408.2018.20.09 |
| [5] |
邓旭坤, 蔡宝昌, 殷武, 等. Brucine对Heps荷瘤小鼠的抗肿瘤作用和毒性的研究[J]. 中国药理学通报, 2006, 22(1): 35-9. Deng X K, Cai B C, Yin W, et al. Anti-tumor activity and toxicity of brucine on mice with transplanted Heps[J]. Clin Pharmacol Bull, 2006, 22(1): 35-9. doi:10.3321/j.issn:1001-1978.2006.01.010 |
| [6] |
索明珠, 李平, 张梅, 等. 马钱子碱抑制乳腺癌细胞体外血管生成拟态的形成及其可能机制研究[J]. 中国癌症杂志, 2018, 28(4): 241-7. Suo M Z, Li P, Zhang M, et al. Brucine inhibits vasculogenic mimicry of breast cancer cell lines in vitro and the related mechanism[J]. China Oncol, 2018, 28(4): 241-7. |
| [7] |
Agrawal S S, Saraswati S, Mathur R, et al. Cytotoxic and antitumor effects of brucine on Ehrlich ascites tumor and human cancer cell line[J]. Life Sci, 2011, 89(5-6): 147-58. doi:10.1016/j.lfs.2011.05.020 |
| [8] |
吴小娟, 马凤森, 郑高利, 等. 马钱子吲哚类生物碱毒性研究进展[J]. 中药药理与临床, 2016, 32(6): 231-5. Wu X J, Ma F S, Zheng G L, et al. Toxicity research progress on indole alkaloids of strychni semen[J]. Pharmacol Clin Chin Mater Med, 2016, 32(6): 231-5. |
| [9] |
解宝仙, 唐文照, 王晓静. 马钱子的化学成分和药理作用研究进展[J]. 药学研究, 2014, 33(10): 603-6. Xie B X, Tang W Z, Wang X J. Research progress on chemical constituents and pharmacological effects of Strychnos nux-vomica[J]. J Pharm Res, 2014, 33(10): 603-6. |
| [10] |
蔡宝昌, 徐晓月, 潘扬, 等. 马钱子生物碱在大鼠体内的组织分布[J]. 中国药理学通报, 2004, 20(4): 421-4. Cai B C, Xu X Y, Pan Y, et al. Tissue distribution of strychnos nux-vomica alkaloids in rats[J]. Clin Pharmacol Bull, 2004, 20(4): 421-4. doi:10.3321/j.issn:1001-1978.2004.04.015 |
| [11] |
Li J, Chen J, Cai B C, et al. Preparation, characterization and tissue distribution of brucine stealth liposomes with different lipid composition[J]. Pharm Dev Technol, 2013, 18(4): 772-8. doi:10.3109/10837450.2011.598165 |
| [12] |
高颖, 陈军, 蔡宝昌, 等. HPLC法测定大鼠血浆中马钱子碱的浓度[J]. 药物分析杂志, 2008, 28(12): 2036-9. Gao Y, Chen J, Cai B C, et al. HPLC determination of brucine in rat plasma[J]. J Pharm Anal, 2008, 28(12): 2036-9. |
| [13] |
Tian J X, Peng C, Xu L, et al. In vitro metabolism study of Strychnos alkaloids using high-performance liquid chromatography combined with hybrid ion trap/time-of-flight mass spectrometry[J]. Biomed Chromatogr, 2013, 27(6): 775-83. doi:10.1002/bmc.v27.6 |
| [14] |
Chen X, Lai Y, Cai Z. Simultaneous analysis of strychnine and brucine and their major metabolites by liquid chromatography-electrospray ion trap mass spectrometry[J]. J Anal Toxicol, 2012, 36(3): 171-6. doi:10.1093/jat/bks004 |

